帕博利珠单抗联合靶动脉灌注化疗治疗晚期NSCLC的效果及安全性分析
卢保华,张军伟,张俊杰
(周口市中医院1外一科,2胸外科,河南 周口 466000)
肺癌是全球发病率第二、死亡率第一的恶性肿瘤,其中非小细胞肺癌(NSCLC)约占85%[1]。NSCLC早期症状隐匿,且缺乏有效的早期筛查方案,故约70%的患者确诊时已处于中晚期。化疗为治疗晚期NSCLC的一线方案,但对机体损伤较大。与静脉化疗相比,靶动脉灌注化疗可直接将药物送达病灶,增强疗效,减轻药物不良反应[2]。研究[3]表明,以免疫检查点抑制剂为代表药物的肿瘤免疫治疗NSCLC效果较好。作为免疫治疗的代表性药物,帕博利珠单抗是一种免疫球蛋白G4单抗,可通过与PD-1结合,激活机体T细胞的免疫反应,进而激活宿主免疫系统增强对肿瘤细胞的识别、杀伤作用。本研究探讨帕博利珠单抗联合靶动脉灌注化疗治疗晚期NSCLC的效果及安全性,现报道如下。
1 资料与方法
1.1 一般资料选取2019年1月至2021年1月我院收治的60例晚期NSCLC患者,随机分为观察组与对照组各30例。观察组男性20例,女性10例;年龄52~88岁,平均(70.16±4.62)岁;平均病程(1.23±1.02)年。对照组男性19例,女性11例;年龄54~86岁,平均(70.62±4.69)岁;平均病程(1.16±0.96)年。两组的一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经我院伦理委员会批准。
1.2 入选标准纳入标准:①病理分期Ⅲb~Ⅳ期;②EGFR、ALK、ROS-1基因阴性;③预计生存时间>3个月;④对本研究内容知情同意。排除标准:①参与其他研究;②对本研究药物过敏;③患有自身免疫性疾病;④其他不能配合治疗的情况。
1.3 方法对照组采用靶动脉灌注治疗,包括多西他赛(浙江海正药业股份有限公司,国药准字H20093092)75 mg/m2、顺铂(齐鲁制药有限公司,国药准字H37021358)80 mg/m2,20~30 min内灌注完毕。灌注前后给予患者地塞米松、昂丹司琼预防性抗过敏、止吐处理。每3周介入治疗1次,连续治疗4个周期。观察组在对照组基础上采用帕博利珠单抗 [MSD Ireland(Carlow),注册证号S20180019]200 mg/次,每3周静脉滴注1次,连续治疗4个周期。
1.4 观察指标疗效评价:完全缓解(CR):症状、肿瘤病灶完全消失,持续4周以上;部分缓解(PR):症状明显缓解,肿瘤直径较基线缩小>30%且持续4周以上;稳定(SD):肿瘤直径较基线缩小≤30%或增加≤20%;进展(PD):肿瘤直径较基线增加>20%或出现新病灶。疾病控制率(DCR)=(CR例数+PR例数+SD例数)/总例数×100%;客观缓解率(ORR)=(CR例数+PR例数)/总例数×100%。采集患者血液样本离心处理,采用全自动生化分析仪检测癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE),采用全自动化学发光免疫分析仪检测T淋巴细胞亚群。统计两组毒副作用发生率。
1.5 统计学方法采用SPSS 21.0统计软件处理数据。计数资料行χ2检验,计量资料行t检验,P<0.05为差异有统计学意义。
2 结果
2.1 疗效观察组的DCR、ORR高于对照组(P<0.05)。见表1。

表1 两组的疗效比较[n(%)]
2.2 血清肿瘤标志物治疗后,两组的CEA、NSE水平降低,且观察组的CEA、NSE水平低于对照组(P<0.05)。见表2。
表2 两组的血清肿瘤标志物比较(±s,ng/mL)
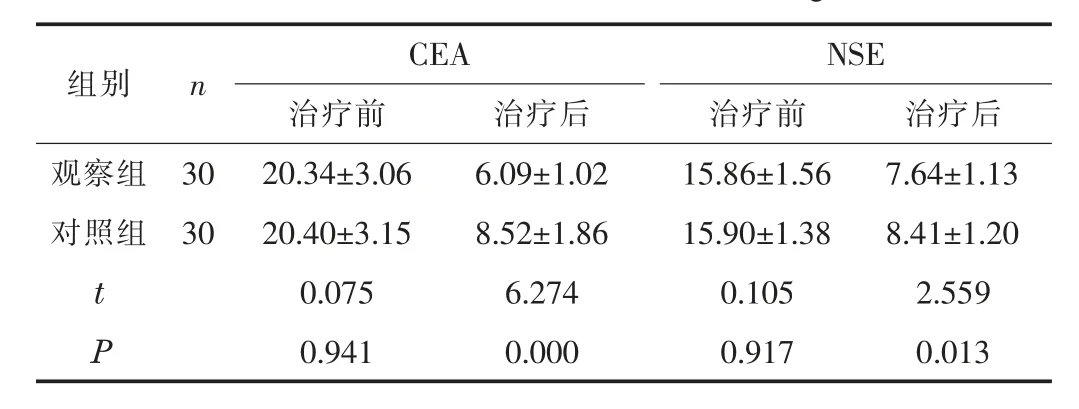
表2 两组的血清肿瘤标志物比较(±s,ng/mL)
组别 n CEA NSE治疗前 治疗后 治疗前 治疗后观察组 30 20.34±3.06 6.09±1.02 15.86±1.56 7.64±1.13对照组 30 20.40±3.15 8.52±1.86 15.90±1.38 8.41±1.20 t 0.075 6.274 0.105 2.559 P 0.941 0.000 0.917 0.013
2.3 T淋巴细胞亚群治疗后,两组的CD4+、CD8+、CD4+/CD8+水平均降低,且观察组的CD4+、CD8+、CD4+/CD8+低于对照组(P<0.05)。见表3。
表3 两组的T淋巴细胞亚群比较(±s,ng/mL)

表3 两组的T淋巴细胞亚群比较(±s,ng/mL)
组别 n CD4+ CD8+ CD4+/CD8+治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 30 35.61±1.12 25.81±1.11 22.21±1.07 15.24±1.05 1.64±0.18 1.50±0.10对照组 30 35.30±1.17 28.12±1.14 22.27±1.04 18.14±1.09 1.63±0.16 1.57±0.12 t 1.048 7.952 0.220 10.495 0.227 2.455 P 0.299 0.000 0.827 0.000 0.821 0.017
2.4 毒副作用两组的毒副作用发生率比较无明显差异(P>0.05)。见表4。

表4 两组的毒副作用发生率比较[n(%)]
3 讨论
NSCLC早期症状无特异性,确诊时已处于中晚期。晚期NSCLC患者丧失根治性切除的机会,只能接受免疫治疗、靶向治疗、放化疗等保守方式。其中化疗为临床治疗晚期NSCLC的一线方案,但单纯化疗方案可因耐药问题及毒副作用等影响治疗效果。靶动脉灌注化疗可通过供血动脉将药物注入肿瘤局部,提升局部药物浓度;此外可在局部去瘤负荷作用下,提升肿瘤病灶对药物的敏感性,增强治疗效果,且减轻了传统静脉化疗药物对全身各器官的影响,患者接受程度较高[4]。随着医疗技术的发展,肿瘤治疗方法不断增加,晚期NSCLC的治疗可供选择的药物种类与方案也在逐渐增多。
近年来,以免疫治疗为基础的单药或联合用药方案与传统化疗相比具有明显优势,有研究[5]表明免疫与化疗联合方案的MPR可达83%。帕博利珠单抗是免疫治疗的代表性药物,已被证实其治疗NSCLC的效果较好[6]。本研究结果显示,治疗后,两组的肿瘤标记物、T淋巴细胞亚群水平均降低,且观察组肿瘤标志物、T淋巴细胞亚群水平低于对照组,提示帕博利珠单抗联合靶动脉灌注化疗治疗晚期NSCLC的效果较好,可抑制肿瘤标志物表达,减轻对患者免疫功能的影响,其原因可能为帕博利珠单抗可增强宿主免疫系统对肿瘤细胞的监视及杀伤作用,并调节免疫抑制肿瘤微环境[7]。本研究结果还显示,观察组的DCR、ORR高于对照组,而两组的毒副作用发生率无明显差异,表明帕博利珠单抗联合靶动脉灌注化疗治疗晚期NSCLC的效果理想,且毒副作用发生率较低。
综上所述,帕博利珠单抗联合靶动脉灌注化疗治疗晚期NSCLC的效果较好,可改善机体免疫状态,安全性较高。

