恶性高血压肾损害1 例报道并文献复习
陈淑园,许筠,丁文君,张丽,张茹
(1.甘肃中医药大学中西医结合学院,甘肃 兰州 730000;2.兰州市第一人民医院,甘肃 兰州 730000;3.甘肃省中医院,甘肃 兰州 730000)
1 病历摘要
1.1 一般资料
患者钟某,男,28 岁,2021 年5 月12 日以“发现血压升高3 年余,间断性头晕1 月。”入院。患者2018年4 月体检时发现血压升高(BP 170/110mmHg),未予重视,2020 年5 月体检BPmax 230/140mmHg,近1月头晕明显,遂至兰州某三甲医院急诊科就诊,测BP 220/150mmHg,查血常规:NEUT%74.00%,LYMPH%15.70%,MONO% 8.10%,RPC 6.64×1012/L,Hb 176g/L,急诊以“高血压急症”收至心血管科。入院症见:患者神清,精神差,头晕,伴恶心,胸闷、气短,偶有咳嗽、咳痰。食纳差,夜寐差,大小便正常。有高血压家族遗传病史(父亲罹患高血压病史16 年),否认其他遗传病史。
1.2 查体
T 36.8℃,P 103 次/分,R 20 次/分,BP 227/157mmHg,BMI 24.07 kg/m2;双肺呼吸音粗,可闻及散在的湿罗音;心率103 次/分, 律齐,各瓣膜听诊区未闻及病理性杂音。肝脾胁下未触及,移动性浊音(-)。双肾叩击痛(+-),双下肢中度凹陷性水肿。生理反射存在、病理反射未引出。舌质红,苔薄黄,脉弦数。
1.3 实验室检查
入 院 后 查 血 常 规:NEUT% 74.00%,LYPH%15.70%,MONO% 8.10%,PBC 5.64×1012/L,PLT116×109/L; 生 化:CREA 292μmol/L,UA 497μmol/L,EGFR 22mL/(min·1.73m2),TP 51.3g/L,ALB 31.30g/L,LDH 336U/L,HCY 25μmol/L,K+3.12mmol/L,Ca2+2.04mmol/L;感 染三项:CRP 13.77mg/L;心梗 组合:MYO 224.80ng/mL, TnT-T 0.06ng/mL,NT-proBNP 6236.0pg/mL;免疫五项:IgM 0.3g/L,IgG 6.6g/L,C4 0.51g/L;凝血系列:FIB 4.35g/L;SLE 六项:抗核抗体ANA+,抗Sm 抗体+-,抗RNP 抗体+-;肾素/醛固酮检测(立位):renin 350.6pg/mL,ALD 763.18pg/mL;肾素/醛固酮检测(卧位):renin 284.16pg/mL,ALD 641.706pg/mL。尿常规:尿蛋白++;24h 尿蛋白总量:3091mg/24h;24 小时尿电解质:P 10.99mmol/24h,Zn 22.04μmol/L/24h,Na57.7mmol/24h,K 40.0mmol/24h,Cl 54.8mmol/24h,Ca 1.8mmol/24h;血清蛋白电泳:白蛋白a1b 64.30%,未发现M 蛋白;血沉、肿瘤系列、病毒系列、甲状腺五项、糖化血红蛋白、结核涂片、痰培养未见明显异常。眼底镜检查:血管痉挛,动脉硬化反光增强,视网膜表面可见少量棉絮斑及硬性渗出物,考虑高血压视网膜病变(Ⅲ级)。双肾+腹部、泌尿系彩超:①双肾大小形态正常,双肾动脉峰值血流速度减低;②右肾囊肿;③脾大,脾静脉增宽;④肝、胆、胰、输尿管声像图未见明显异常。心脏彩超:①左心、右房增大、左室肥厚;主动脉瓣关闭不全(轻度),二尖瓣关闭不全(轻度);②心包积液(少量);③左心功能正常底限(LVEF 约56%),左心室收缩功能大致正常,舒张功能减低(Ⅱ级)。颅脑CT 平扫:①双侧脑室前后角旁、双侧放射冠多发低密度灶,多考虑梗塞可能;②右侧大脑中动脉M1 段高密度影,建议MRI 进一步排查除外梗塞。胸部CT 平扫:①双肺多发感染,双下肺为著;②双侧胸腔及右侧叶间裂积液,心包积液。肾上腺CT 平扫:双侧肾上腺未见明显异常。颅脑(MPI平扫+DWI):①脑干、双侧侧脑室颞角、后角旁白质异常,多考虑可逆性后白质脑病;②双侧额顶颞叶、放射冠及脑干多发异常信号,考虑缺血灶;③右侧颞叶急性脑梗塞灶。
1.4 诊断与治疗
①高血压急症,原发性高血压3级 极高危组,高血压脑病,高血压视网膜病变(Ⅲ级);②高血压心脏病,心功能不全(二级),心包积液;③慢性肾脏病4 期;④肺部感染;⑤急性脑梗死;⑥电解质紊乱 低钾血症;⑦继发性醛固酮增多症;⑧肾囊肿(右侧)。入院后给予重症监护,氧气吸入,静脉滴注硝普钠50mg 扩张血管以降压,托拉塞米注射液10mg 以利尿、降低心脏负荷,头孢唑肟钠2g Q12H 静滴以抗感染,硫酸镁注射液2.5g+氯化钾注射液0.7g 以纠正电解质紊乱;雾化吸入异丙托溴铵溶液 1 支+乙酰半胱氨酸溶液1 支 BID 促进排痰;肝素钠注射液 1.25 万IU ST 以抗凝治疗;口服苯磺酸氨氯地平片 5mg QM、珀酸美托洛尔缓释片47.5mg QM、螺内酯片20mg TID 以联合利尿、降压;枸橼酸钾颗粒4g BID 以辅助补钾;尿毒清颗粒1包 QID 护肾排毒,复方a 酮酸片2.52g TID 以降氮补充必需氨基酸。入院8 天,患者不适症状明显减轻,双下肢无明显水肿,小便量1580-2250mL/24h,测BP132/96mmHg,复查指标较前好转,血常规:WBC 3.48×109/L,CPR 6.14mg/L,NEUT% 61%,Hb 151g/L,PLT 175×109/L;心 酶 组 合:LDH 221U/L;生化:K+3.69mmol/L,UREA 11.7mmol/L,CREA 263umol/L,eGFR 28mL/(min·1.73m2);尿常规:尿蛋白+;24h 尿蛋白总量:1885mg/24h。
鉴于患者肾损伤病因不明,且病情复杂,与患者及家属充分沟通病情并征得同意后拟行肾脏穿刺活检术以明确诊断及指导治疗。2021 年5 月25日我院在B 超引导下行肾脏穿刺活检术,活检组织外送至广州某三甲医院,病理回报:电镜描述:肾小球:2 个缺血皱缩,内皮细胞明显空泡变性及增生,毛细血管襻开放;肾小囊:壁层细胞空泡变性;基底膜:节段性增厚,厚度约为230-740nm,节段性皱缩;脏层上皮细胞:上皮细胞肿胀,足突大部分融合;系膜区:系膜细胞和基质增生,未见确切电子致密物沉积;肾小管-间质:肾小管萎缩,肾间质炎症细胞浸润伴胶原纤维增生。电镜诊断:电镜下肾小球基底膜节段性增厚,足突大部分融合,未见确切电子致密物沉积,请结合临床及常规病理检查(见图1)。光镜描述:肾小动脉病变较重,小动脉内皮细胞增生肿胀,内膜显著增厚,粘液变性,呈“洋葱皮”样改变,官腔明显狭窄,甚至闭塞,细动脉管壁透明变性,管腔狭窄,冰冻切片中见2 个肾小球,未见球形硬化及节段硬化;石蜡组织行HE、PAS、PASM 及Masson 染色,切片中见40 个肾小球,其中10 个球性硬化,1 处节段硬化;余肾小球系膜细胞及基质节段轻度增生,内皮细胞肿胀,伴袢腔内炎症细胞浸润;毛细血管袢显著缺血皱缩,少数球囊粘连,少数肾小球球囊周围纤维化(见图2)。免疫荧光:2 个肾小球,IgG、IgM、IgA、C3、C1q、IgG1、IgG2、IgG4、PLA2R 均为阴性。病理诊断:血栓性微血管病性肾损伤,考虑为恶性高血压肾损伤。
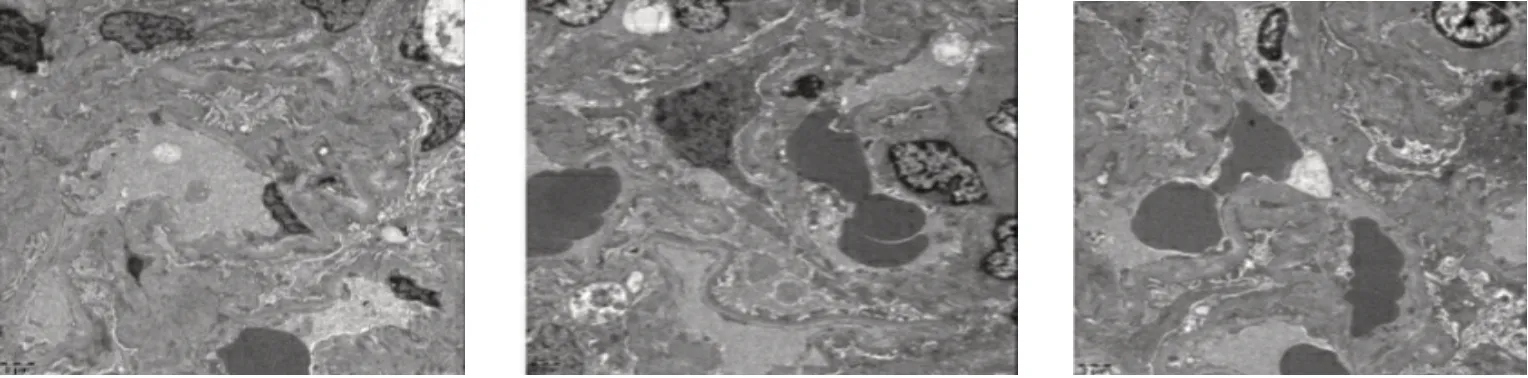
图1 肾小球基底膜节段性增厚,足突大部分融合(光镜×2000)
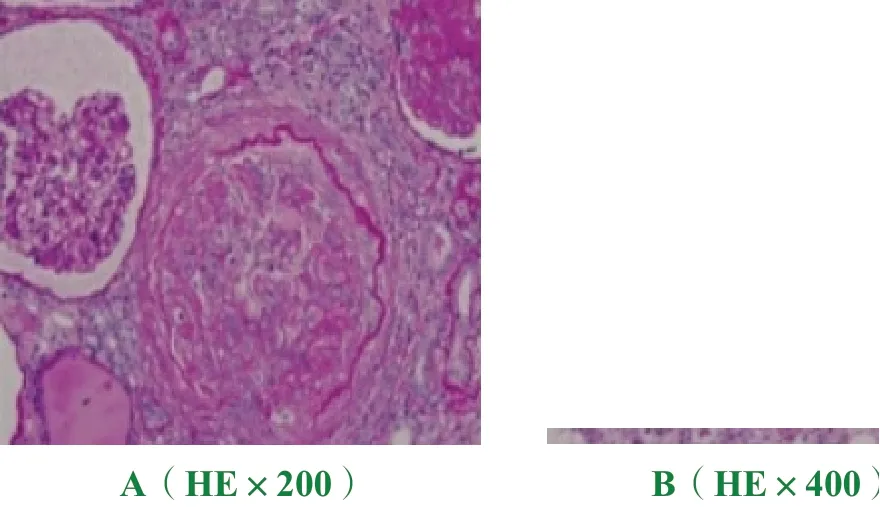
图2 肾小动脉内膜呈“洋葱皮样”改变
结合患者临床症状、体征、辅助检查、病理等,明确诊断为:恶性高血压(malignant hypertension,MHT),恶性高血压肾损害。诊断明确后,调整治疗方案,在此前降压药物的治疗基础上,给予沙库巴曲缬沙坦钠片50mg QM 以联合降压、保护心肾、降低尿蛋白。治疗期间,监测血压波动在BP110-120/88-95mmHg,病情好转出院。出院后维持上述治疗方案,定期门诊复查,随访半年,血压控制良好,肾功能无进行性恶化。
2 讨论
恶性高血压(malignant hypertension,MHT)指血压短期内显著升高,舒张压≥130 mmHg(1 mmHg=0.133 kPa),同时有眼底Ⅲ级和(或)Ⅳ级病变,或舒张压未达到130mmHg 但出现急性肾功能损害伴眼底改变(Ⅲ级以上),亦累及心、脑等多个器官的一组临床综合征[1,2]。MHT 病情危急,是动脉高血压最严重的表现形式,归属于高血压急症,20%-40%的高血压可以发展为MHT,我国MHT 患者中37%由原发性高血压发展而来。MHT 在中青年人群中多见,且发病率逐渐年轻化[3],常表现为剧烈的头痛、眩晕、恶心呕吐、意识模糊、视力减退,出现渗出性视网膜脱离和脉络病变[2],常累及肾脏出现少尿、蛋白尿、血尿、氮质血症等肾功能受损的临床表现,如血压未得到积极有效的控制,则会发展为终末期肾脏病(Endstage renal disease ,ESRD)甚至死亡,也可累及心脑出现急性左心衰或高血压脑病等。
MHT 是由大血管和微血管内皮细胞损伤引起的多器官损害,特别是脑、眼底及肾脏的损伤,Mishima、Funayama 等在《高血压研究》杂志上也论证了恶性高血压与脑、眼、肾的密切关系[4]。MHT 与肾脏关系尤为密切,约63%-90%的MHT易致肾脏损害,且发展至ESRD 及替代治疗的比率逐年呈上升趋势,肾脏损害的严重程度决定了MHT 的预后。恶性高血压肾损害又可分为原发性和以IgAN 为主肾实质性肾损害,有研究发现[5],贫血、尿酸、血浆白蛋白是MHT 发生肾功能受损的危险因素,也有研究[6]通过对照恶性高血压与良性高血压肾损害患者体内的Elabela 水平,发现收缩压是体内Elabela 水平降低的危险因素,也是恶性高血压发生肾损害的独立危险因素。恶性高血压肾损害的发病机制主要为肾小球高压、肾素-血管紧张素-醛固酮系统(RAAS)的过度活化、氧化应激、内皮功能的紊乱以及遗传因素导致的基因易感性等[7,8],其中最主要的是血压急剧升高损伤入球小动脉,引起RAAS 系统极度兴奋,RAAS 系统兴奋又会反射性引起肾血管收缩,血压进一步升高,形成恶性循环,最终导致多个靶器官严重受损并影响患者的预后及生存率。
本病例中,患者入院测BP 220/150mmHg,明显头晕,胸闷、气短,双下肢水肿,考虑高血压急症,静脉给予硝普钠50mg、托拉塞米注射液 10mg QD,口服苯磺酸氨氯地平片 5mg QM、琥珀酸美托洛尔缓释片 47.5mg QM、吲达帕胺片 2.5mg QM、螺内酯片 20mg TID、盐酸特拉唑嗪片 2mg BID 以降压治疗。因患者肾损伤病因不明,且病情复杂,与患者及家属充分沟通,待血压控制平稳后,进一步做肾穿刺活检以明确诊断。肾穿结果示电镜下肾小球基底膜节段性增厚,光镜下肾小动脉病变较重,小动脉内皮细胞增生肿胀,内膜显著增厚,粘液变性,呈“洋葱皮”样改变,官腔明显狭窄,甚至闭塞,为血栓性微血管病性肾损伤,考虑恶性高血压肾损害。有研究发现,恶性高血压伴原发性肾脏损害比不伴原发性肾脏损害的病理更严重,预后更差[9]。因此调整治疗方案,首选RAAS 抑制剂,患者醛固酮及肾素明显升高,伴血钾偏低,提示RAAS 系统过度活化,导致RBF、GFR 下降,组织重构、肾脏纤维化、肾小球硬化等临床表现,故加用沙库巴曲缬沙坦钠片50mg QM 以抑制RAAS 系统过度激活而降压,同时能够改善心室重构,具有心肾双重获益的功效。因患者CREA 292μmol/L、GFR 22mL/(min·1.73m2),故停用螺内酯片以避免肾脏进一步受损。但需注意的是,降压不宜迅猛,以免重要器官缺血而致病情恶化,在治疗过程中,严密监测肝肾功能、血压、电解质,及时调整药物。治疗后,患者血压逐渐趋于平稳,病情好转。因此,尽早的评估和诊断至关重要,明确诊断MHT 肾损害后,应首选RAAS 抑制剂,其不良反应较少,临床疗效良好,在降压的同时保护肾功能,延缓病情的进一步恶化。
高血压视网膜病变在非糖尿病人群中的患病率为3%-14%,与缺血性卒中的风险增加相关,也可预测冠心病、心衰事件的倍增[10]。患者虽然眼部无明显不适症状,但会诊查眼底时考虑高血压性视网膜病变,在平稳降压的基础上给予血栓通胶囊2 粒 TID、甲钴胺胶囊 0.5mg TID 以活血化瘀、改善微循环,延缓视网膜病变的进展。这提醒我们,应提高并重视视网膜病变相关的恶性高血压,在患者就诊时尽早地行眼底镜的筛查是评估高血压患者终末器官损害的基础部分。
综上,恶性高血压肾损害临床上并不常见,早期快速诊断和合理降压是预防高血压急性及严重并发症的关键,这就需要临床医生掌握诊疗知识,避免误诊、漏诊,如诊断治疗不及时,则会加速病情的发展,导致多器官损害乃至死亡。因此,临床医生也应做好宣教工作,嘱咐患者重视高血压、改善生活方式,加强血压监测、眼科检查,预防MHT 的发生和多器官损害,改善临床预后和提高生存率。

