电絮凝活化过单硫酸盐降解磺胺甲唑
刘晓艳,詹 焕,叶中伟,谢世伟,王松林
(1.武汉科技大学城市建设学院,湖北武汉 430065;2.武汉市致远市政建设有限公司,湖北武汉 430050;3.华中科技大学环境科学与工程学院,湖北武汉 430074)
近年来,基于硫酸根自由基(SO4·-)的过硫酸盐高级氧化技术〔5-6〕已经在水环境污染治理领域得到广泛的应用,与传统Fenton 氧化的主导活性物质羟基自由基(·OH,E0=1.8~2.7 V)相比,SO4·-(E0=2.5~3.1 V)有更强的氧化性〔7-8〕,且其半衰期(30~40 μs)远大于·OH 的半衰期(10-3μs),有较好稳定性〔9〕。除此之外,SO4·-还可以在较宽的pH 范围(2~8)下应用,而以·OH 为基础的高级氧化的最佳pH 范围为2~5〔10-11〕,SO4·-对pH 的适应性更广泛。本研究以SMX 为目标污染物,在电絮凝(EC)/过单硫酸盐(PMS)体系中考察了电流、PMS 浓度、初始pH、SMX 初始质量浓度等因素对SMX 降解过程的影响,并基于猝灭实验对体系中产生的自由基的分析,对电絮凝活化过硫酸盐机理进行了探究,以期为电絮凝活化PMS 技术的应用和推广提供参考。
1 材料与方法
1.1 实验材料
磺胺甲 唑(C10H11N3O3S,质量分数≥98%)与过硫酸氢钾(PMS),均为分析纯,购于Aladdin 公司;氢氧化钠、硫酸、甲酸、叔丁醇,均为分析纯,购于国药集团化学试剂有限公司;甲醇,HPLC 级,购于美国Fisher 公司;电极材质为纯铁片(铁质量分数>99.5%),尺寸为8 cm × 1.5 cm;实验用水均为电阻率18.25 MΩ·cm 的超纯水。
1.2 实验仪器
高效液相色谱仪(FL2200,浙江福立分析仪器股份有限公司),配套C18 色谱柱(4.6 mm×250 mm×5 μm,岛津技迩商贸有限公司);多功能水质分析仪(XLD-Multi-350i,德 国WTW 集 团);超 纯 水 机(ZWM,湖南中沃水务环保科技有限公司);电子天平(AL204,瑞 士Mettler Toledo 集团);直 流 电 源(GPS-2303C,台湾固纬电子有限公司);电流表(F15B+,美国Fluke 公司);超声波清洁仪器(PS-30AD,深圳市洁康洗净电器有限公司)。
1.3 实验方法
实验装置如图1 所示,采用550 mL 的圆柱形玻璃反应器进行实验,内装有500 mL 电解液,置有2 片纯铁电极(8 cm×1.5 cm),极板间距为2 cm。选择10 mmol/L Na2SO4溶液为电解液,电解过程中采用磁力搅拌器使溶液保持完全混合;稳压直流电源供电,采用电流表对电流进行监测。
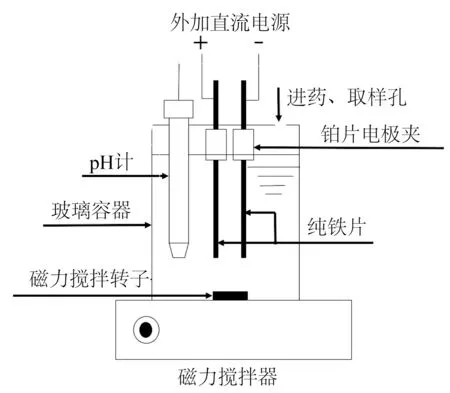
图1 实验装置示意Fig.1 Schematic diagram of the experimental device
具体实验步骤如下:将500 mL 超纯水置于550 mL 的玻璃容器中,加入一定量SMX 和Na2SO4,通 过0.1 mol/L 的H2SO4和0.1 mol/L 的NaOH 调 节 初始pH 至一定值,加入PMS 并通电后开始计时。分别在0、0.5、1、2、4、6、8 min 取样,并将样品用0.22 μm 滤膜过滤,取1 mL 过滤液,加入过量的甲醇猝灭,分析其中SMX 的浓度。所有实验至少重复2 次及以上。实验中所配SMX 反应液初始pH 为7。下文若未特殊说明,反应基本条件均控制为:SMX 初始质量浓度为1 mg/L,初始pH 为7,电解质Na2SO4浓度为10 mmol/L,电流为10 mA,极板间距为2 cm。
1.4 分析方法
SMX 质量浓度采用高效液相色谱(FL2200)测定。色谱柱条件:柱温20 ℃,流动相采用体积比为35∶65 的甲醇和0.1%甲酸溶液,流速为1 mL/min,进样量为20 μL,检测波长270 nm。
2 结果与讨论
2.1 不同反应体系对SMX 的降解效率
考察单独EC、单独投加Fe2+(37 μmol/L)、单独投加PMS(20 μmol/L)、PMS(20 μmol/L)/Fe2+(37 μmol/L)和EC/PMS(20 μmol/L)共计5 种不同体系降解SMX 的效率,实验结果见图2。

图2 不同体系下SMX 的降解效率Fig.2 Degradation efficiency of SMX in different systems
由图2 可以看出,6 min 内EC、Fe2+、PMS 体系对SMX 的降解极少,说明这3 种体系基本上对SMX 不降解。PMS/Fe2+体系在1 min 内对SMX 的降解率为72.3%,6 min 时降解率为74.2%,说明直接投加Fe2+能够快速活化PMS。EC/PMS 体系随反应时间延长,降解率逐渐增加,在6 min 时对SMX 的降解率可达到97.8%,这说明,与直接投加Fe2+的PMS/Fe2+体系相比,通过铁电絮凝缓慢地释放出Fe2+更有利于对SMX 的降解,这是因为PMS/Fe2+体系在短时间内Fe2+活化PMS 产生的大量SO4•-会发生猝灭而被消耗,如式(1)和(2)所示。综上所述,相比于其他体系,EC/PMS 体系对SMX 具有较好的降解效果。
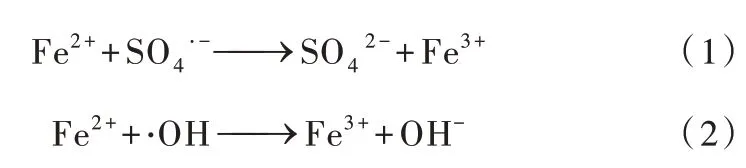
2.2 电流对SMX 降解的影响
根据法拉第电解定律,EC/PMS 体系电解过程中产生的Fe2+的量与电流、通电时间成正比。为了研究电流对PMS/EC 体系降解SMX 的影响,考察了反应时间6 min 时不同电流对PMS/EC 体系降解SMX的影响,实验结果见图3。
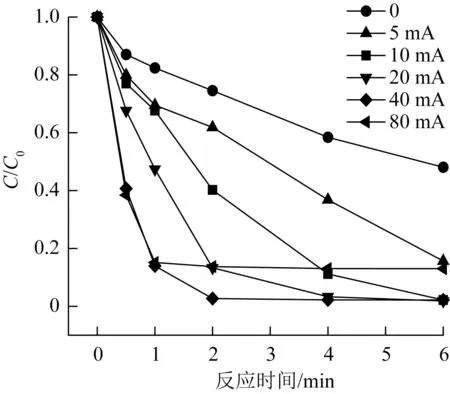
图3 电流对EC/PMS 体系降解SMX 的影响Fig.3 The effect of current on the degradation of SMX in EC/PMS system
由图3 可知,当电流为0 时,铁片在水中因被腐蚀而产生Fe2+,从而活化PMS 产生SO4·-降解SMX,SMX 的降解率为52.9%;当电流为5 mA 时,SMX 的降解率为84.4%;电流从10 mA 增加到40 mA 时,不同电流条件下,SMX 的降解率均能达到97.8%及以上;而当电流继续增加至80 mA 时,反应在2 min 内就结束了,但对SMX 的降解率却仅有87.1%。这是因为,在一定范围内,提高电流会增加Fe2+的产生量,加快活化PMS 的速率,生成·OH 和SO4·-的量随之增加,从而提高了SMX 的降解率,但当电流过大时,相同时间内产生的Fe2+就会过量,短时间内PMS 大量分解产生·OH 和SO4·-会加快SMX 的降解速率,然而生成的·OH 和SO4·-会与Fe2+发生反应造成消耗〔式(1)、式(2)〕,同时自由基之间也会产生自我消耗〔12〕,导 致·OH 和SO4·-利用率降低,从而降低了SMX 的降解率。
电化学反应的能耗常用单位电能(EEO)来进行评价〔13〕,其被定义为将1 m³水中的污染物浓度降低1 个数量级(即90%)所需的电能〔14〕,计算方法见式(3)。
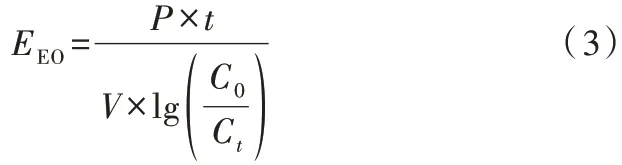
式中:EEO——单位电能,kW·h/m³;
P——功率,kW;
t——电解时间,h;
V——处理体积,m³;
C0——初始时刻SMX 的质量浓度,mg/L;
Ct——t 时刻SMX 的质量浓度,mg/L。
当水中SMX 初始质量浓度为1 mg/L,电流分别为10 mA 和40 mA 时,降解率基本持平时能耗如表1所示,显然二者在6 min 反应时间内均能取得较好的降解效果,但电流为10 mA 时能耗更低,而电流为40 mA 时反应更快。考虑到电流为40 mA 条件下短时间内体系中就会产生大量Fe2+,反应迅速,不利于考察其他反应因素对该实验的影响,故该实验选用电流10 mA 为基本反应条件,以便于研究的开展。

表1 10 mA 和40 mA 电流下降解率基本持平时能耗比较Table 1 Comparison of energy consumption when the degradation rate was basically the same under the current of 10 mA and 40 mA
2.3 PMS 浓度对SMX 降解的影响
为确定EC/PMS 反应体系中最佳PMS 浓度,本研究设置了PMS 浓度分别为0、10、20、40、80 μmol/L的5 组实验进行考察,实验结果见图4。
由图4可知,当PMS浓度从0增加到20 μmol/L,反应时间为6 min 时SMX 的降解率可由0 提高到97.8%,这是因为体系Fe2+充足情况下,PMS 浓度增加会产生更多的活性物质,从而使SMX 的降解率提高。但是当PMS 浓度从20 μmol/L 增加到80 μmol/L 时,6 min 内SMX 降解率反而下降到88.5%,这主要是因为:(1)过量的PMS 产生大量的活性自由基,从而发生自由基的自我消耗〔15〕;(2)PMS 中过量的HSO5-会 与·OH 和SO4·-反应生成氧化性较低的SO5·-,反应如式(4)、式(5)所示〔16〕。
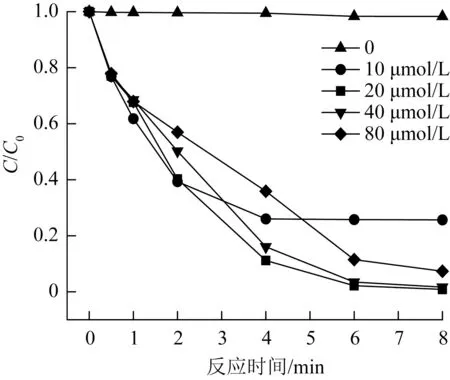
图4 PMS 浓度对EC/PMS 体系降解SMX 的影响Fig.4 The effect of PMS concentration on the degradation of SMX in the EC/PMS system
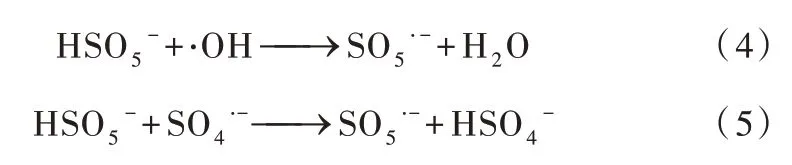
2.4 初始pH 对SMX 降解的影响
溶液pH 会影响Fe2+的存在形态和PMS 的活化效果,因此本研究设置了pH 为3、5、7(原液)、9、11的5 组实验,以探究溶液初始pH 对EC/PMS 反应体系的影响,实验结果见图5。
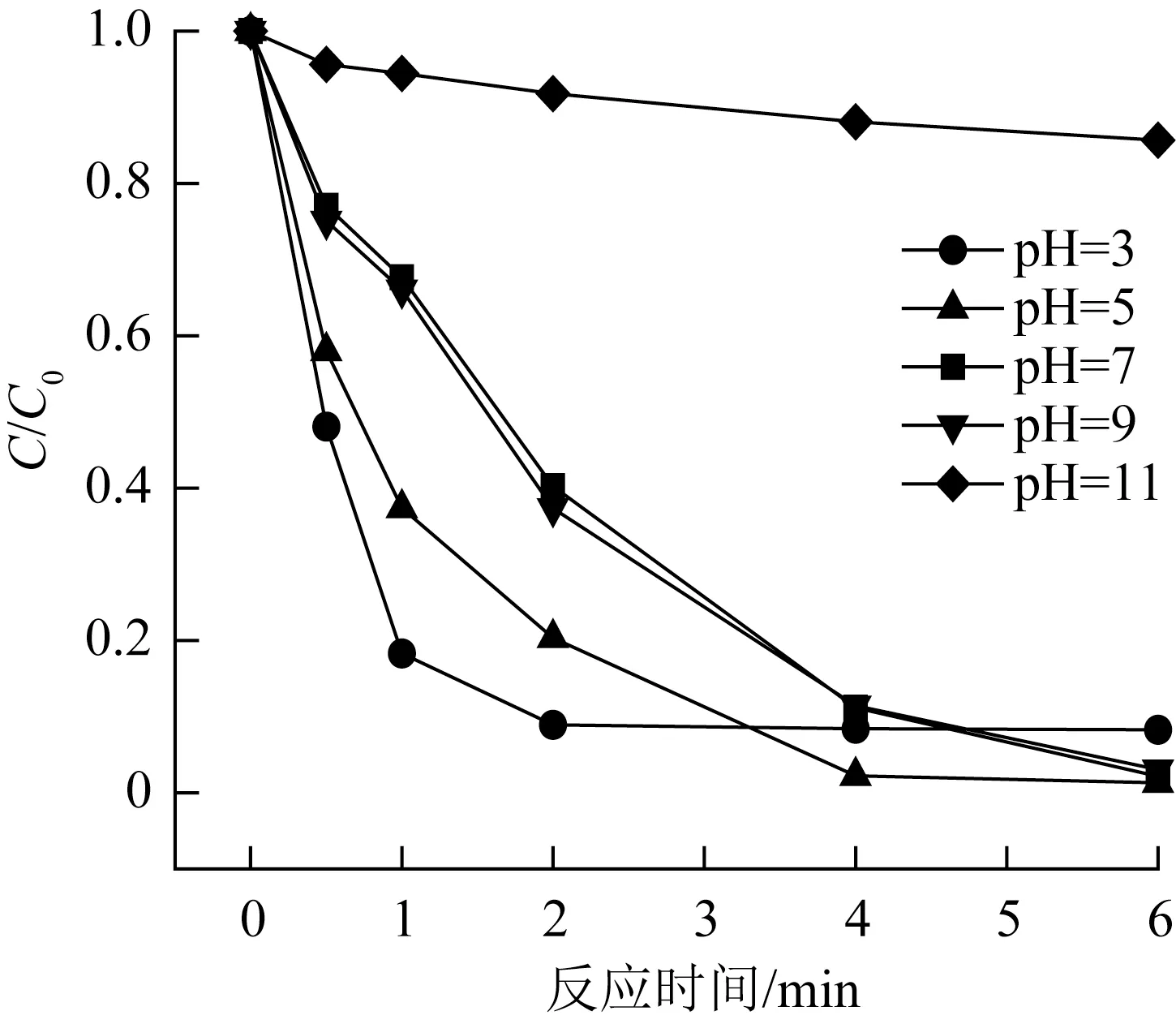
图5 初始pH 对EC/PMS 体系降解SMX 的影响Fig.5 The effect of initial pH on the degradation of SMX in the EC/PMS system
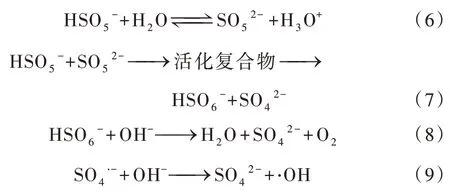
由图5可以看出,初始pH为3时,EC/PMS体系2 min内即可完成对SMX 的降解,降解率为91.7%。这是因为铁片在强酸性条件下更易被腐蚀,能短时间内产生大量的Fe2+来活化PMS,加快了反应速率,但过量的Fe2+会消耗一定的自由基,从而一定程度上抑制了对SMX的降解,致使最终降解率不够理想。当初始pH 为5、7、9 时,SMX 降解速率随着pH 的提高有所降低,最终降解率分别为98.7%、97.8%、97.0%,相较于pH=3 时最终降解率有所提高。当pH 为11 时,SMX 降解速率和降解率均明显下降,这是因为在强碱性条件下,溶液中的大部分Fe2+形成氢氧化物沉淀,使得Fe2+减少,从而抑制了对SMX 的降解;另外,在强碱性条件下,PMS 中HSO5-会发生如式(6)~(9)的反应〔17〕,HSO5-被消耗,SMX的降解率下降。
2.5 初始SMX 质量浓度对SMX 降解的影响
目标污染物的浓度对体系的降解效果有着直接影响。实验设置了SMX 初始质量浓度为0.5、1、2、4 mg/L共计4组实验,以探究不同SMX初始质量浓度对EC/PMS体系降解SMX 的影响,实验结果见图6 及表2。
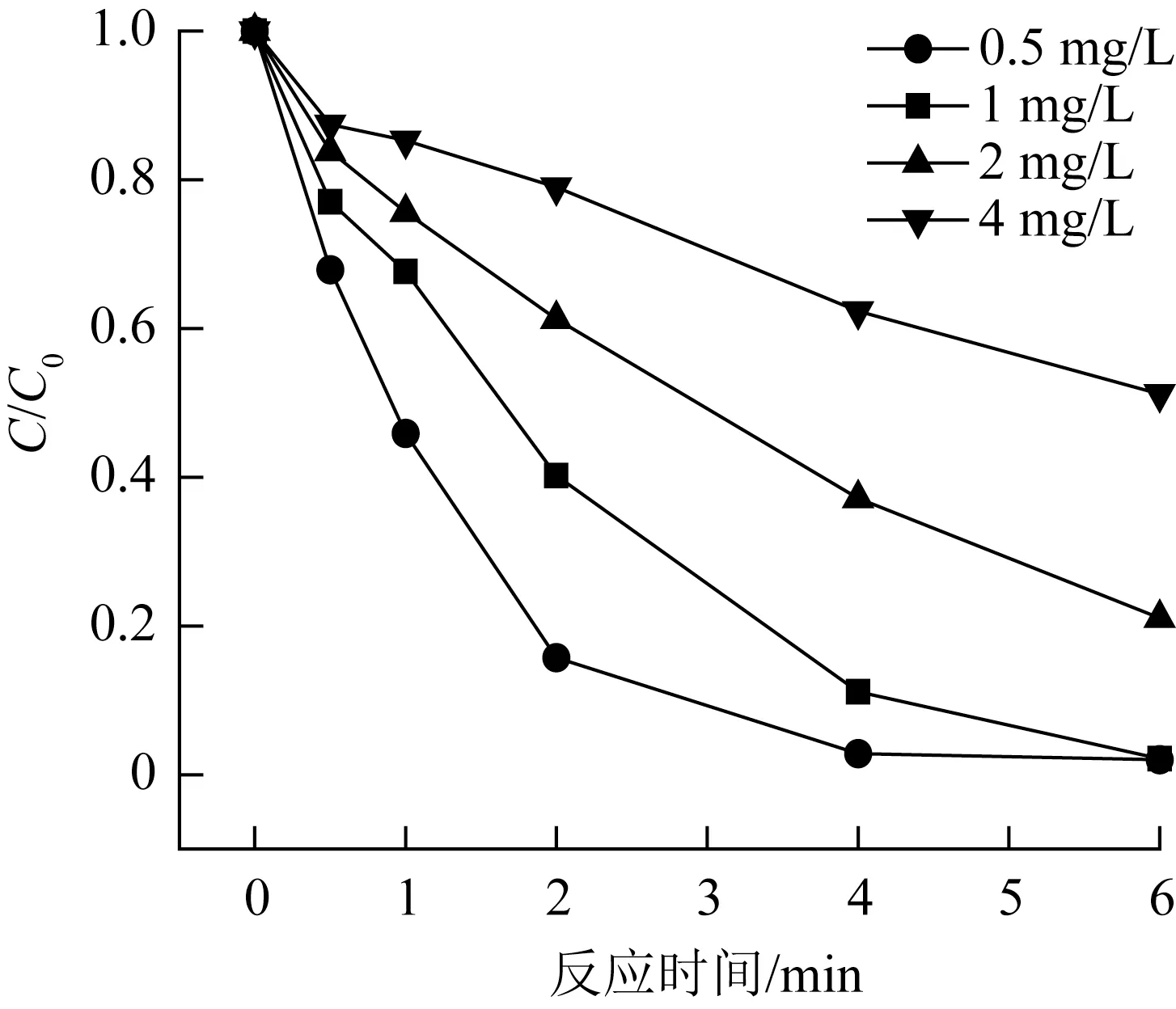
图6 初始SMX 质量浓度对EC/PMS 体系降解SMX 的影响Fig.6 The effect of initial SMX mass concentration on the degradation of SMX in the EC/PMS system

表2 不同SMX 质量浓度下SMX 的降解总量Table 2 Total degradation of SMX under different SMX mass concentrations
由图6 可知,SMX 初始质量浓度为0.5 mg/L 时,在6 min 内SMX 的降解率为98%,当SMX 初始质量浓度超 过1 mg/L 时,6 min 内EC/PMS 体系对SMX 的降解率随着SMX 浓度的增加而下降,SMX 的初始质量浓度从1 mg/L 增加至4 mg/L 时,降解率从97.8%减少到48.8%。由表2 知,SMX 的降解率虽然有所降低,但SMX 降解总量却是上升的。这是因为在电流和PMS 的量一定的条件下,当SMX 浓度较低时,反应中产生的·OH 和SO4·-的量足够降解SMX,反应迅速;当SMX 浓度增加时,由于·OH 和SO4·-在 体 系中浓度相对减少会降低SMX 降解率,但是一定量的·OH 和SO4·-与SMX 反应几率增加,即自由基利用更加充分,导致SMX 被降解的总量增加〔18〕。
2.6 自由基的鉴定及反应机理分析
甲醇与·OH和SO4·-反应非常快,其反应速率常数分别为(1.2~2.8)×109L/(mol·s)和(1.6~7.8)×107L/(mol·s)〔19〕,对二者均有很好的猝灭效果。叔丁醇与·OH能快速反应,其反应速率常数为(3.8~7.6)×108L/(mol·s),而叔丁醇与SO4·-的反应速率常数仅为(4.0~9.1)×105L/(mol·s)〔20〕。利用甲醇和叔丁醇与不同自由基反应存在的反应速率常数的差异可以鉴别出反应中的主要自由基。实验设定SMX 初始质量浓度为1 mg/L,初始pH 为7,电解质Na2SO4浓度为10 mmol/L,PMS浓度为20 μmol/L,电流为10 mA,极板间距为2 cm,此条件下采用甲醇和叔丁醇作为猝灭剂进行自由基猝灭实验,并与空白组进行对照,以探究EC/PMS体系产生的主要自由基,结果见图7。

图7 猝灭剂对SMX 降解的影响Fig.7 The effect of quencher on the degradation of SMX
由图7可知,随着甲醇浓度从0逐渐上升到25 mmol/L,SMX的降解受到的抑制作用也越来越强烈,SMX 降解率从最初的97.8%降低至15%。而叔丁醇浓度从0~25 mmol/L 变化时,其对SMX 降解的抑制作用相对甲醇较小,SMX降解率从97.8%降低至78.2%。因此,可以初步认为EC/PMS体系降解SMX过程中主要自由基为·OH 和SO4·-,且SO4·-在反应中贡献率较大。据此,对EC/PMS体系降解SMX 的机理进行推测,结果如图8 所示。在外加电源的作用下,通过电解铁阳极产生Fe2+,同时阴极电解水产生H2,且Fe2+被空气氧化所形成的Fe3+可能在阴极又被还原为Fe2+,利用这些Fe2+活化PMS 可生成活性自由基·OH 和SO4·-,从而直接降解目标污染物。
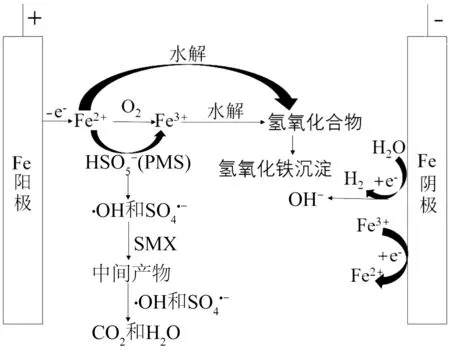
图8 EC/PMS 体系降解SMX 的机理示意Fig.8 Schematic diagram of the mechanism of degradation of SMX in EC/PMS system
3 结论
(1)在SMX 初始质量浓度为1 mg/L、初始pH=7、PMS 浓度为20 μmol/L、电流为10 mA 的条件下,通过电絮凝缓慢地释放Fe2+,EC/PMS 体系在6 min 内对SMX 降解率可达97.8%;
(2)增加电流和PMS 浓度能提高SMX 的降解效率,但是电流超过40 mA 或PMS浓度超过20 μmmol/L均会抑制SMX 的 降 解;体 系 初 始pH 为5~9 时,对SMX 都能有很好的降解效果,而初始pH 为3 时SMX的降解率会稍有降低,但初始pH 为11 时SMX 的降解会受到严重抑制。
(3)EC/PMS 体系产生的主要活性自由基为·OH和SO4·-,其中SO4·-所占比例较大。