NiO-FeS纳米复合材料的电沉积与电催化水分解性能
范厚强, 李来胜, 李旭凯, 王 静
(华南师范大学环境学院/环境化学教育部重点实验室, 广州 510006)
随着工业化的迅猛发展,全球正面临着日益严峻的能源危机和环境污染问题。氢能是一种高效、清洁的新能源,可被广泛用于氢能发电、氢动力汽车和氢燃料电池等领域[1]。电催化分解水作为一种可持续地利用丰富水资源制氢的方法备受关注[2-4],通常包含2个半反应:阴极的析氢反应(HER)和阳极的析氧反应(OER),其中OER涉及四电子转移,从而制约了电催化分解水制氢的效率[5-6]。Ir和Ru化合物已被证明具有优秀的OER性能,然而这些贵金属催化剂储量稀少,价格昂贵,无法大规模制备和应用[7-8]。因此,利用非贵金属催化剂取代贵金属催化剂是研究者追求的目标。金属硫化物具有较高的电导率、优良的电化学稳定性和丰富的活性位点,已被广泛用作OER催化剂,例如Fe-Ni3S2/NF[9]。金属硫化物一般通过水热或溶剂热法、湿化学法和化学气相沉积法等方法合成[10-11],不可避免地需要高温或高压等苛刻条件,同时伴有H2S等有害气体的释放。
本研究采用电沉积技术在镍网(NF)上原位制备氧化镍-硫化铁(NiO-FeS)复合材料,研究电催化分解水的产氢效率[12-14]。电沉积法具有操作简单、可控性强等特点[15-17]。采用两步电沉积法制备的NiO-FeS@NF呈现独特的二维纳米片状结构,极大提升了电催化OER性能。
1 实验部分
1.1 试剂及仪器
试剂:硫脲(CH4N2S)、硫酸镍(NiSO4·6H2O)、硫酸亚铁(FeSO4·7H2O)、盐酸(HCl)和氢氧化钾(KOH),所有试剂均为分析纯。
仪器:扫描电镜(SEM,Sigma 300,德国Zeiss)、透射电镜(TEM,Talos F200X,美国FEI)、能量色散X射线谱(EDS,X-Max 50,英国Oxford)、X射线光电子能谱(XPS,Lab220i-XL,美国Thermo Fisher)、电化学工作站(CHI660E,上海辰华)。
1.2 NiO-FeS@NF的合成
用盐酸、乙醇和去离子水依次超声清洗镍网(NF,1 cm×0.5 cm)约20 min,干燥待用;以NF为工作电极、Ag/AgCl电极为参比电极、铂线为对电极进行电沉积,电解质为0.1 mol/L FeSO4·7H2O和0.1 mol/L CH4N2S的混合溶液,沉积电位为-0.85 V vs Ag/AgCl,沉积时间为15 min,沉积完成后用去离子水清洗并干燥;采用FeS@NF为工作电极,电解质是0.1 mol/L NiSO4·6H2O水溶液,沉积电位为-1 V vs Ag/AgCl,沉积时间为15 min;将沉积产物用去离子水清洗并干燥,得到NiO-FeS@NF复合材料。
1.3 电化学测试方法
采用电沉积法使NiO-FeS在NF表面原位生长,保证了复合材料和基底之间的电子传递,因此NiO-FeS@NF可以直接用作电催化水解的工作电极。在1 mol/L KOH电解质中测试NiO-FeS@NF复合材料的线性扫描伏安(LSV)曲线。泡沫镍在电催化过程中易被氧化,出现较强的氧化还原峰。为了准确测试材料的电催化OER性能,避免镍的氧化还原反应,LSV的扫描电位采用从高电位到低电位的方式,即从0.8 V到0 V,扫描速率为5 mV/s。
在 10-2~105Hz的频率、0.45 V vs Ag/AgCl下测试材料的电化学阻抗谱(EIS),测试电解质为1 mol/L的KOH溶液。
依据LSV曲线,利用塔菲尔公式分析过电位。塔菲尔公式:
η=blgj+a,
(1)
其中,b是Tafel斜率,j是电流密度,η是过电位。
③通过响应面试验设计统计分析得到可靠性较高的二次响应面回归模型,并预测最佳工艺参数:对于固态发酵551H,发酵时间27 h,固态培养基组成/固液比值2.125,发酵温度25℃,接种量10%;对于固态发酵552H,发酵时间48 h,固态培养基组成/固液比值1.5,发酵温度30℃,接种量3%,验证试验证明该参数可行。
在25 ℃下,可逆氢电极(RHE)与Ag/AgCl电极电位的换算关系:
VRHE=VAg/AgCl+0.059 pH+0.197。
(2)
2 结果与讨论
2.1 NiO-FeS@NF复合材料的表征结果
2.1.1 NiO-FeS@NF的表面形貌 分别对FeS@NF、NiO@NF以及NiO-FeS@NF复合材料的形貌采用SEM形貌观察(图1),FeS@NF为错落交织的二维片状结构,NiO@NF为堆积的片状结构,而NiO-FeS@NF复合材料兼具这两种形貌,主要由二维纳米片形成的团簇组成,表明FeS与NiO已成功复合。

图1 不同纳米复合材料的SEM图及NiO-FeS@NF的TEM图
复合材料的TEM和HRTEM表征结果(图1D)表明:NiO-FeS@NF呈现明显的二维纳米片结构,且高度透明,说明所得材料具有超薄的特点。超薄二维片状材料具有大的比表面积和丰富的暴露活性位点[18],有利于催化效率的提高[19-20]。从图1E中可以清晰观察到晶格间距为0.210、0.217 nm的2种晶格条纹,分别对应于NiO的(200)晶面和FeS的(202)晶面[21],证实NiO-FeS@NF具有良好的结晶度,同时也表明FeS与NiO形成了较好的异质结[22]。一方面这种异质结具有特殊的电荷转移特性,另一方面可以保证相邻组分的良好接触,进而实现有效的界面电荷传输,提升电催化性能[23-25]。
2.1.2 NiO-FeS@NF的化学成分 对NiO-FeS@NF复合材料进行XPS分析(图2),在Ni 2p谱(图2A)中,结合能为855.6 eV和873.7 eV处的主峰分别代表Ni 2p3/2和Ni 2p1/2,对应于Ni—O键中的Ni2+[26-27]。类似地,Fe 2p谱(图2B)中结合能为711.5 eV和725.4 eV处的主峰分别对应于Fe 2p1/2和Fe 2p3/2,表明复合材料中存在Fe2+和Fe3+,其中Fe3+可能来自于材料表面的氧化[5,28]。O 1s谱(图2C)中结合能为530.6、531.6、533.1 eV处的谱峰分别代表Ni—O、O—H以及吸附的水或氧,从而证实了NiO的存在。S 2p谱(图2D)中结合能为160.0、167.9 eV处的峰证明存在金属硫化物(S2-),材料表面少部分已被氧化成SOx[16,28-30]。采用两步电沉积法成功制备出具有二维片状结构的NiO-FeS@NF复合材料。

图2 NiO-FeS@NF的高分辨率XPS谱
2.1.3 NiO-FeS@NF的生长机理 根据前述对NiO-FeS@NF表面形貌和化学成分的XPS分析,提出NiO-FeS@NF复合材料在两步电沉积法制备过程的生长机理(图3)。电沉积法是一种“自下而上”的自组装过程[7]。在第一步沉积过程中,电解液中的Fe2+和S2-在电场作用下发生迁移并在NF基底表面富集,2种离子发生反应生成FeS核。随着沉积时间的延长,FeS核逐渐定向生长,最后形成二维片状结构。在第二步沉积过程中,电解液中的Ni2+也迁移到FeS表面并逐渐富集,最终形成NiO-FeS二维复合材料。
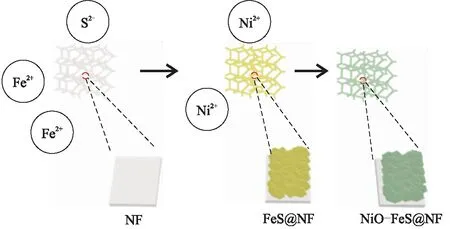
图3 两步电沉积法制备NiO-FeS@NF复合材料的示意图
2.2 NiO-FeS@NF电化学性能
2.2.1 不同沉积条件的优化结果 电催化性能与电催化材料的物理、化学和电子特性等相关,往往可以通过制备过程中的参数进行调控。因此,考察电沉积过程所用不同电解液中硫酸镍的浓度、沉积电位和沉淀时间等对NiO-FeS@NF复合材料OER性能的影响。

图4 不同条件下沉积NiO-FeS@NF材料的LSV曲线
改变操作参数考察沉积电位和沉积时间对OER性能的影响(图4B)。采用3种沉积电位(-0.9、-1.0、-1.1 V vs Ag/AgCl),沉积15 min,c(Ni2+)为0.10 mol/L。当沉积电位为-1.0 V时,NiO-FeS@NF的OER过电位最低(263.8 mV)。一般外加电位的大小能够改变离子的迁移速度,过大或过小都会影响材料的均匀生长,因此本研究最佳的沉积电位选用-1.0 V vs Ag/AgCl。
考察3种沉积时间(10、15、20 min)对材料OER性能的影响(图4C),沉积电位为-1.0 V vs Ag/AgCl,c(Ni2+)为0.1 mol/L。当沉积15 min时,材料的OER过电位最低。我们认为沉积时间较短时,NiO不足以形成良好的超薄片状结构,而沉积时间较长时,所得纳米片结构可能太厚、太密集,进而影响活性位点的数量。因此,采用的最佳沉积时间为15 min。
综合以上实验可确定最佳沉积条件:电解液中硫酸镍的浓度为0.1 mol/L,沉积电位为-1.0 V vs Ag/AgCl,沉积时间为15 min。在该条件下,FeS和NiO界面的电子传输性能最好,并且镍铁双金属的协同效应最佳,使得复合材料的OER性能最优。
2.2.2 不同材料的OER性能 对比NiO-FeS@NF复合材料和单独FeS@NF、单独NiO@NF的OER性能(图5A)结果表明:NiO的加入使FeS@NF的氧化还原峰的峰电流变大,反应进行速率加快;NiO-FeS@NF仅需263.8 mV的过电位即可达到电流密度10 mA/cm2,过电位低于FeS@NF的282.2 mV和NiO@NF的319.2 mV;NiO-FeS@NF的过电位降低说明NiO-FeS@NF复合材料的OER性能得到了提升。
通过塔菲尔曲线(图5B)进一步考察电催化剂的OER动力学,塔菲尔曲线的线性部分能够反映较简单的电子传递过程。通过计算得到NiO-FeS@NF的塔菲尔斜率仅为23.7 mV/dec,远远低于FeS@NF的55.1 mV/dec和NiO@NF的114.7 mV/dec[8,27,31-32]。塔菲尔斜率越小,表明在相同动力学电流密度下该催化过程的过电位越低,进一步说明NiO-FeS@NF复合材料的OER动力学性能得到了大幅提升。
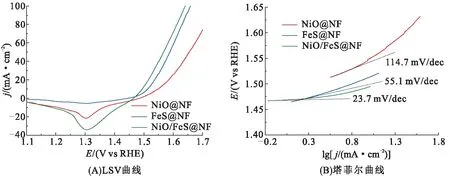
图5 NiO-FeS@NF、FeS@NF和NiO@NF的LSV和塔菲尔曲线
2.2.3 复合材料OER稳定性测试 对NiO-FeS@NF电催化稳定性进行研究,采用i-t法测试材料在1 mol/L KOH溶液中的电流曲线(图6)。在1.494 V vs RHE的恒电位下,NiO-FeS@NF的电流密度在10 h内一直保持在 10 mA/cm2,未发现明显的衰竭现象,表明电极优异的稳定性。首先,NiO-FeS@NF复合材料独特的二维片状结构能够快速释放产生的O2,材料在连续OER反应过程中未出现严重变形;其次,NiO-FeS在NF基底表面原位生长,不需要使用任何粘合剂,因此材料能够与基底紧密连接,不易脱落。

图6 NiO-FeS@NF复合材料在1.494 V vs RHE下的i-t曲线
2.3 NiO-FeS@NF的OER机理探讨
电催化剂的催化性能往往与电极表面的电荷转移电阻有关。Nyquist图可以反映表面电荷的转移过程,通过拟合电化学阻抗谱(EIS)可以评价电极的电导率,进而揭示OER反应机理。在相同电位(0.45 V vs Ag/AgCl)下,在10-2~105Hz频率范围测试了几种材料的EIS谱Nyquist图(图7)。单独NiO@NF和单独FeS@NF电极具有较大的半圆直径,说明它们的电阻较大,而NiO-FeS@NF复合材料的电阻仅为7 Ω,表明其导电性最好。在复合材料中,FeS和NiO形成了良好的异质结,同时存在镍铁双金属协同效应,使两者界面处的电子转移速率加快,从而OER电催化性能最好[12,16,33]。

图7 不同材料的Nyquist图
一般认为,在碱性电解液中OER反应主要分为4个步骤[34-35]:
M+OH-→M—OH+e-,
(3)
M—OH+OH-→M—O+H2O+e-,
(4)
M—O+OH-→M—OOH+e-,
(5)
M—OOH+OH-→M+O2+H2O+e-。
(6)
OER是一种四电子-质子耦合反应,涉及M—OH,M—O和M—OOH中间体的形成。这种间接途径导致电催化反应需要更高的能量和过电位,使OER动力学过程变得极为缓慢,主要取决于第三步(式(5)),因此调控M—O的结合能对OER性能的提升至关重要。制备的NiO-FeS@NF复合材料具有二维超薄结构,能够为电催化反应提供较大的比表面积和更多暴露的活性位点,同时异质结的存在促进了界面电子转移过程,降低了M—O的结合能,进而降低了OER反应中的动力学势能垒,使NiO-FeS@NF复合材料的OER性能得到提升。
3 结论
通过简易的电沉积法制备了二维复合材料NiO-FeS@NF,将其应用于电解水OER反应。SEM、TEM和XPS等表征结果表明:NiO-FeS@NF复合材料具有二维超薄片状结构,FeS和NiO能够形成良好的异质结。由于电沉积法的原位合成,NiO-FeS材料和NF基底之间存在较好的电子转移,因此可直接用作电催化OER电极。通过调节电沉积参数确定了最佳沉积条件:电解液中硫酸镍的浓度为0.1 mol/L,沉积电位为-1.0 V vs Ag/AgCl,沉积时间为15 min。在1 mol/L KOH碱性电解液中,NiO-FeS@NF电极展现出优异的OER性能,当电流密度为10 mA/cm2时,OER过电位为263.8 mV,塔菲尔斜率为23.7 mV/dec,优于单独的NiO@NF和FeS@NF电极。通过EIS谱分析发现NiO-FeS@NF电阻仅为7 Ω,在所有样品中最小,说明其电子转移速度最快。一方面,二维超薄结构为电催化OER提供更多的活性位点;另一方面,FeS和NiO形成的异质结以及镍铁双金属协同效应能够增强界面电子传递,促进OER动力学过程。这种简单的电沉积法有利于制备高效的催化剂材料,有望在能源和环境等领域得到广泛应用。

