工艺条件对甲烷催化裂解制氢及碳纳米管的性能影响研究
裴婷,张淑侠,王姗姗,张华,张妮娜
(陕西延长石油(集团)有限责任公司研究院,陕西 西安 710075)
随着人类生活中各种燃料的日益枯竭,开发洁净与廉价的燃料已成为各国研究的热点[1],氢气是较理想的清洁燃料[2],燃烧后的产物只有水,对环境并无大的污染,同时还具有高效、易制备、能再生等优点,已被广泛的应用于化工、航天、电子与冶金行业。制备氢气方法以催化裂解制氢法[3]、重整制氢法[4]和电解水法[5]等为主。而这些方法中,用碳氢化合物甲烷催化裂解制氢是学者研究的热点,原因是碳氢化合物甲烷催化裂解制氢合成反应后产物主要有碳纳米管[6]、碳纤维[6]和无定形碳[7]。其中,碳纳米管是以其特殊的纳米管状结构和突出的物理化学特性在高强度复合材料、高效导热复合材料、催化材料等方面得到欢迎。
甲烷催化裂解制氢碳纳米管是以天然气为原料,在高温催化的条件下,把天然气资源转化成氢气及碳纳米管这两种高附加值的产品。同时产物中无温室气体的排放,原子转化率较高,成本较低,获得的碳纳米管产品经济价值高,在天然气清洁转化的领域拥有很好的发展前景。本文利用自主研发的催化剂,在配备有产物在线色谱检测的固定床反应装置上,考察了不同工艺条件对甲烷催化裂解制氢及碳纳米管研究的性能影响。
1 实验部分
1.1 试剂与仪器
Ni(NO3)2、Al2O3均为分析纯;去离子水,实验室自制;CH4(≥99.999%);N2(≥99.999%)。
HZK-FA110电热鼓风干燥箱;KBF11Q-Ⅲ气氛式箱式马弗炉;KQ-300E超声波清洗器;GC-2014岛津气相色谱。
1.2 催化剂制备
常温下,将5.0 g Al2O3催化剂载体超声分散于100 mL去离子水中。搅拌下,加入3.61 g Ni(NO3)2,磁力搅拌10 h,室温下静置1 h。鼓风干燥箱中 110 ℃烘干10 h,研磨成粉末,过筛,收集40~60目的催化剂样品,于马弗炉中550 ℃煅烧4 h,冷却至室温后,制得催化剂。
1.3 甲烷催化裂解制备CNTs
0.200 0 g催化剂均匀分散在石英反应管(内径10 mm)中央,在石英反应管两端放少量石棉,把反应管放于催化剂评价装置裂解炉恒温区,在N2气氛中程序升温(N2流速为20 mL/min),当温度升到 700 ℃,停止通N2气体,通入CH4气体(CH4流速为20 mL/min),同时色谱开始进样,反应4 h时,停止通入CH4气体,切换N2气体(N2流速为 20 mL/min),使系统在N2气氛下自然降温,关闭色谱,取出石英反应管,称取反应生成的CNTs量。
2 结果与讨论
2.1 催化剂用量的影响
催化剂用量对CNTs生成量的影响见图1,每克催化剂生成每克CNTs的结果见图2。
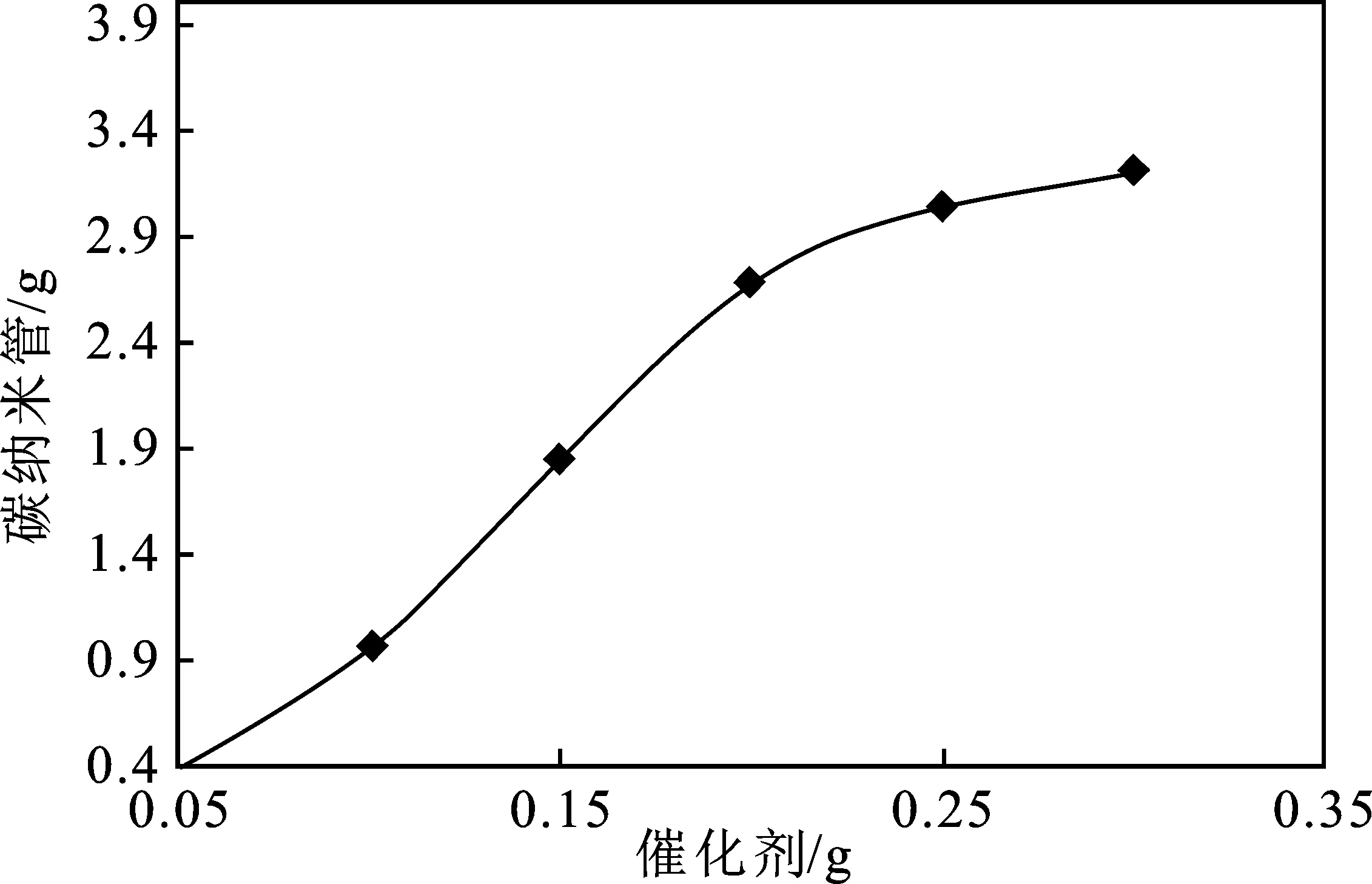
图1 催化剂用量对CNTs的影响Fig.1 Effect of catalyst amount on CNTs

图2 每克催化剂生成每克CNTs的关系Fig.2 Relationship of CNTs per gram of catalyst
由图可知,当催化剂用量为0.200 0 g时,生成CNTs量达到较大值,这时每克催化剂生成每克CNTs的比值达到最大。在一定内径的石英反应管内,并不是催化剂的量越大得到的CNTs量就越大,在CH4流速为20 mL/min的情况下,0.200 0 g的催化剂量能达到较好的反应状态。
2.2 反应管内径的影响
石英反应管内径为10 mm和20 mm(DCNTS10和DCNTS20)生成CNTs量见图3,每克催化剂生成每克CNTs的结果见图4。

图3 催化剂用量对CNTs的影响Fig.3 Effect of catalyst amount on CNTs
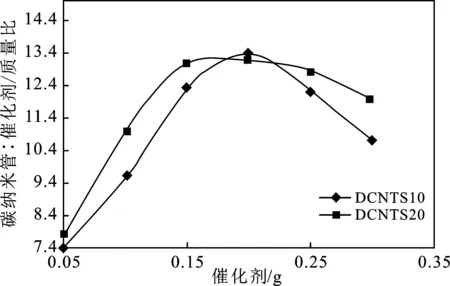
图4 每克催化剂生成每克CNTs的关系Fig.4 Relationship of CNTs per gram of catalyst
由图可知,石英反应管内径对反应结果的影响并不是很大。在内径为10 mm的石英反应管中,催化剂、催化剂量与反应气CH4气体已达到一个较合适的状态,也就是说反应管的体积会和催化剂用量有一个饱和状态。
2.3 反应温度的影响[8]
称取催化剂0.200 0 g,均匀分散于石英反应管(内径10 mm)的中央,反应温度对CNTs生成量的影响见图5。

图5 反应温度对CNTs的影响Fig.5 Effect of reaction temperature on CNTs
由图5可知,反应温度对CNTs有较大影响,因为甲烷裂解是吸热反应,较高的温度有利于甲烷催化裂解反应,能够得到更高与更好的转化率。另外,甲烷催化裂解反应中,催化剂需要较合适的温度,以便能够达到催化剂反应的寿命与活性的最佳状态,使得催化剂能够高效与稳定地催化甲烷的裂解。当反应温度较低时,反应缓和,获得的转化率也会较低,当反应温度较高时,CH4分解会较快[9],催化剂也能够获得一定的稳定性和一定的活性。温度到700 ℃时,催化剂具有了良好的催化活性,因此温度升高并非能提高CNTs量,反而会有下降的趋势,所以反应温度选择为700 ℃。
2.4 甲烷流速的影响[10]
称取催化剂0.200 0 g均匀分散于石英反应管(内径10 mm)中央,反应温度700 ℃,反应4 h,CH4气体流速对CNTs生成量的影响见图6,空速对CNTs的影响见图7。
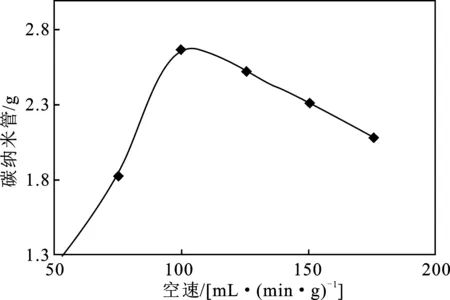
图7 空速对CNTs的影响Fig.7 Effect of airspeed on CNTs
由图6、图7可知,甲烷流速对CNTs量生成有较大影响,对一定的反应装置而言,当进料量一定,空速增大时,表示单位时间内通过催化剂的原料气多,原料气在催化剂上停留时间短,反应深度变浅,同理,空速小表示反应时间长,利于提高反应的转化率。20 mL/min 甲烷流速较为合适,能得到较多的CNTs。
2.5 反应时间的影响[11]
称取催化剂样品0.200 0 g,均匀分散于石英反应管(内径10 mm)中央,反应温度700 ℃,CH4气体流速为20 mL/min,反应时间对CNTs生成量的影响见图8。
由图8可知,反应4 h时,能得到较多CNTs量。反应初期,催化剂活性位点比较多,因此甲烷转化率高,随着 CNTs 在催化剂表面上渐渐生长,催化剂活性位被渐渐覆盖住,活性随之降低,但覆盖有CNTs催化剂的粒子仍然会有一定的催化裂解反应活性。反应时间超过4 h时,将会被大量CNTs覆盖,催化剂的粒子渐渐失去了催化裂解的能力,活性随之降低,从而影响反应的进行。
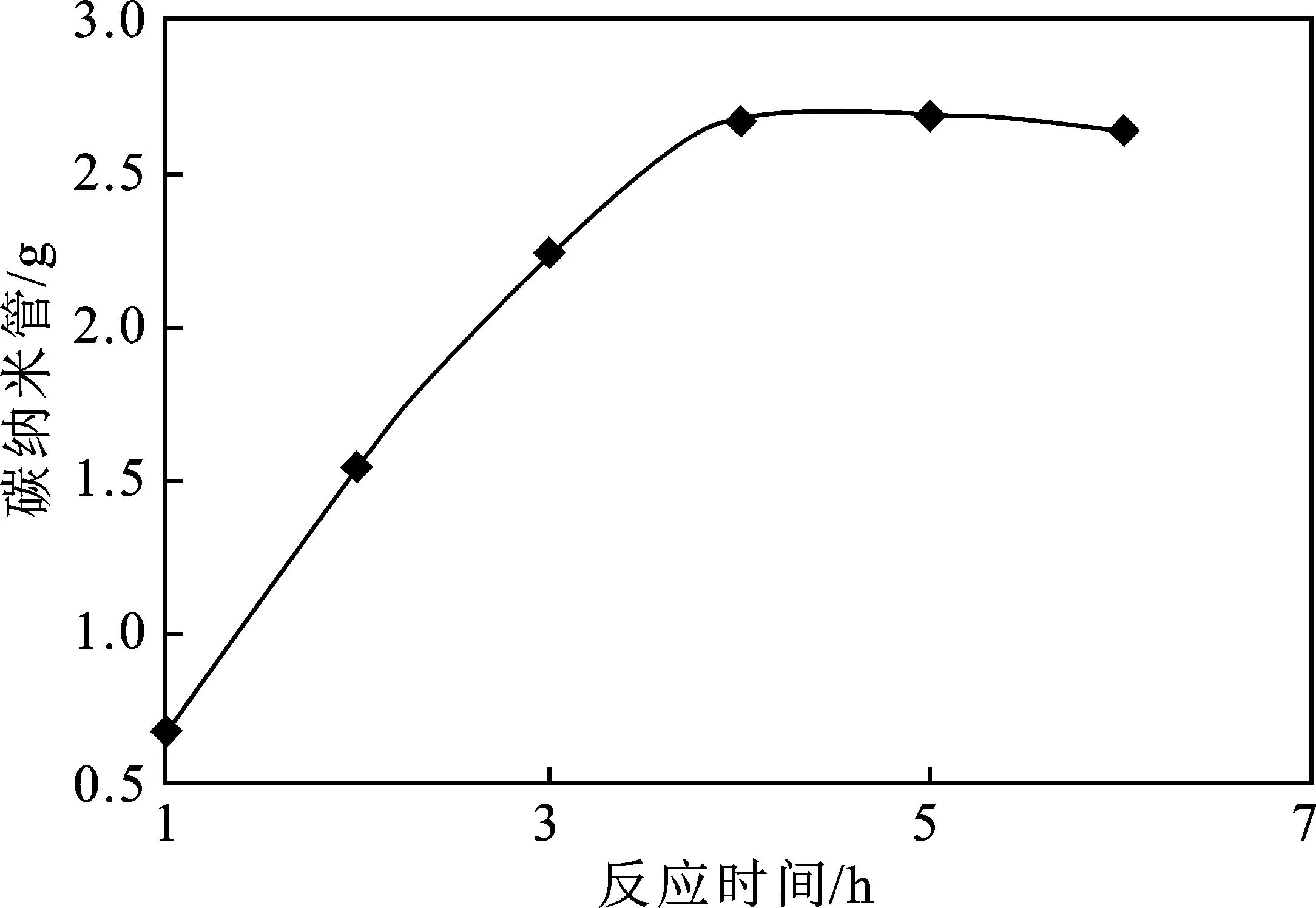
图8 反应时间对CNTs的影响Fig.8 Effect of reaction time on CNTs
2.6 催化剂评价结果
常温下,称取催化剂0.200 0 g均匀分散于石英反应管(内径10 mm)中央,反应温度700 ℃,CH4流速为20 mL/min,反应4 h,获得产物CNTs 2.67 g,反应生成碳氢化合物用气相色谱(GC-2014型)在线分析,计算甲烷的转化率是18.9%。图9为甲烷催化裂解反应后生成CNTs的SEM图。

图9 甲烷催化裂解反应后生成CNTs的SEM图Fig.9 SEM of CNTs generated after catalytic cracking of methane
由图9可知,CNTs 产品大部分都呈现不规则分布的柱状,管径较为均匀,具有中空结构的管状,形状呈现卷曲状,无规则地团聚或缠绕在一块。有些CNTs颗粒端有一些白色的亮点,可能是一些未反应的催化剂粒子。
3 结论
常温下,称取催化剂0.200 0 g均匀分散于石英反应管(内径10 mm)中央,在石英反应管两端放入少量石英棉,把反应管放于催化剂评价装置裂解炉的恒温区,在N2气氛中程序升温(N2流速为 20 mL/min),当温度升到700 ℃,停止通N2气体,通入CH4气体(CH4流速为20 mL/min),同时色谱开始进样,待反应到4 h,停止通入CH4气体,切换N2气体(N2流速为20 mL/min),使系统在N2气氛下自然降温,关闭色谱,获得呈不规则分布的柱状、管径较为均匀的CNTs 2.67 g,CH4转化率18.9%。

