中性脂肪沉积症伴肌病患者的外周血细胞形态特点并文献复习
邢莹,普程伟,尚柯,屈晨雪
中性脂肪 沉 积 症(neutral lipid storage disease,NLsD)是一种罕见的常染色体隐性遗传病,主要由脂肪代谢途径中的酶或辅基缺陷导致三酰甘油(triglyceride,TG)在不同组织细胞内异常沉积引起。依据临床表现和突变基因不同可将NLsD 分为中性脂肪沉积症伴肌病(neutral lipid storage disease with myopathy,NLsDM)和中性脂肪沉积症伴鱼鳞病(neutral lipid storage disease with ichthyosis,NLsDI)[1]。 前 者 是 由于 patatin样磷酸酯酶结构域蛋白 2(patatin-like phospholipase domain-containing protein 2,PNPLA2)基因发生突变导致,主要临床表现为骨骼肌或心肌损害症状[2];后者的致病基因是比较基因识别 -58(comparative gene identification-58,CGI-58),又称含α/β水解酶结构域蛋白5(α/βhydrolase domain-containing protein 5,ABHD5),主要临床表现为鱼鳞病,又称为Dorfman-chanarin综合征[3]。NLsD发病率低、临床表现缺乏特异性、患者可就诊于多个不同科室,部分患者伴有实验室检查结果异常如高脂血症、高肌酸激酶(creatinine kinase,CK)、肝功能异常等,肌肉病理检查可见肌纤维内大量脂肪沉积。但是以上检查均不具有特异性,明确诊断仍有赖于基因检测,很多患者因没有及时进行基因检测而延误了诊断和治疗。NLsD患者外周血涂片可见中性粒细胞胞质中存在大量空泡(瑞-姬氏染色),经油红O染色证实为脂肪沉积有较高的诊断价值,但油红O染色操作复杂,不适合常规实验室开展。因此,本研究将3例NLsDM患者的外周血涂片采用多种方法进行染色,旨在找到更为便捷的染色方法,为NLsDM的及时诊断提供参考依据。
1 病例简介
病例1,女性,36岁。因肌肉无力于2021年6月就诊于北京大学第一医院神经内科。患者双上肢肌无力2年余,右侧为著,双上肢肌肉萎缩;无听力下降及心功能下降;家族史:父母无近亲结婚史,父母和弟弟均无类似症状;祖籍武汉;实验室检查:血清CK及TG水平升高;肌电图(EMG):双上肢肌源性损害;肌肉活检:可见脂质沉积;基因检测:患者PNPLA2基因纯合变异(c.757+1G>T),家人未做基因检测。患者诊断为NLsDM,建议服用非诺贝特降低血脂以及中链脂肪酸饮食。
病例2,男性,27岁。8年前出现四肢无力,双下肢近、远端肌肉萎缩,且逐渐加重,目前行动困难;无听力下降及心功能下降;未做肌电图及肌肉活检;于2021年7月就诊于北京大学第一医院神经内科。家族史:父母无近亲结婚史、无类似症状,姐姐存在肌无力症状和听力下降。实验室检查:血清TG和CK水平均增高。基因检测:父母均存在PNPLA2基因杂合变异(c.757+1G>T),患者和姐姐该位点存在纯合变异,诊断为NLsDM,治疗方案同病例1。
病例3,男性,38岁。5年前感觉双腿易疲劳,上楼时无力,天冷时明显;2年前出现双耳听力下降,双腿无力加重,目前无法上楼;于2021年8月就诊于北京大学第一医院神经内科。家族史:父母近亲结婚(奶奶和姥姥是亲姐妹),无类似症状;哥哥患强直性脊柱炎,无听力问题。实验室检查:血清TG和CK水平均增高。基因检测:患者父母均存在PNPLA2基因杂合变异(c.703C>T),患者该位点存在纯合变异,诊断为NLsDM,治疗方案同病例1。
本文价值:
(1)本文首次提出外周血细胞形态学检查在及时诊断中性脂肪沉积症伴肌病(NLsDM)中的重要价值,以往的研究多集中于肌肉活检、基因检测等,但肌肉活检为有创检查,患者依从性差,而基因检测尚没有在临床广泛开展。外周血细胞形态学检查操作方便,简单易行,不需要额外检测设备,在基层医院均可开展,可作为筛查NLsDM的常规方法。(2)由于NLsDM非常罕见,本研究纳入病例数较少,需要在今后的工作中继续积累。
2 NLSDM患者外周血细胞形态特点
采用瑞-姬氏染色观察患者外周血白细胞形态发现:中性粒细胞、嗜酸粒细胞、嗜碱粒细胞及单核细胞胞质中均可见数个大小不一的圆形空泡(图1)。
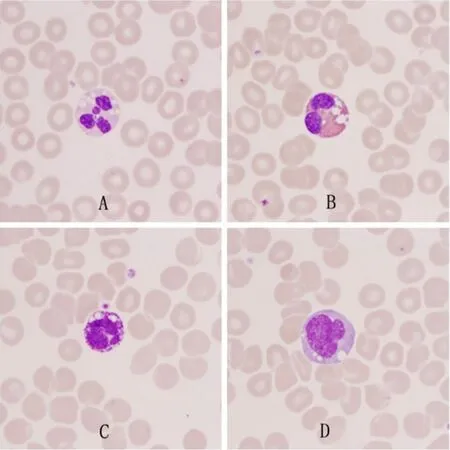
图1 NLsDM患者外周血白细胞形态(瑞-姬氏染色,×1 000)Figure 1 Morphology of peripheral blood leukocytes in NLsDM patients(Wright-Giemsa staining)
当人体存在细菌感染时,中性粒细胞胞质中亦可见空泡变性(图2)。为了更好地与感染相鉴别,本研究进行了中性粒细胞碱性磷酸酶染色(NAP)、髓过氧化物酶染色(MPO)和糖原染色(PAs)。NAP(图3):根据中性粒细胞胞质中有无阳性颗粒及多少和分布情况分为(-)、(+)、(++)、(+++)和(++++),分别对应0~4分,100个细胞中阳性细胞总数为阳性率,阳性细胞积分之和为积分值[4]。NLsDM患者的中性粒细胞胞质中呈阴性反应,与正常人和感染患者差异明显,感染患者阳性率和积分值均明显增高;MPO(图4):NLsDM患者的中性粒细胞胞质中呈阳性反应,与正常人的中性粒细胞阳性程度接近,但弱于感染患者(阳性颗粒粗大覆盖在细胞核上,导致细胞核结构不清);PAs(图5):NLsDM患者、正常人及感染患者的中性粒细胞阳性反应程度均未见明显差异。提示NAP可作为鉴别NLsDM与感染患者最佳的染色方法。

图2 感染患者外周血白细胞形态(瑞-姬氏染色,×1 000)Figure 2 Morphology of peripheral blood leukocytes in infected patients(Wright-Giemsa staining)
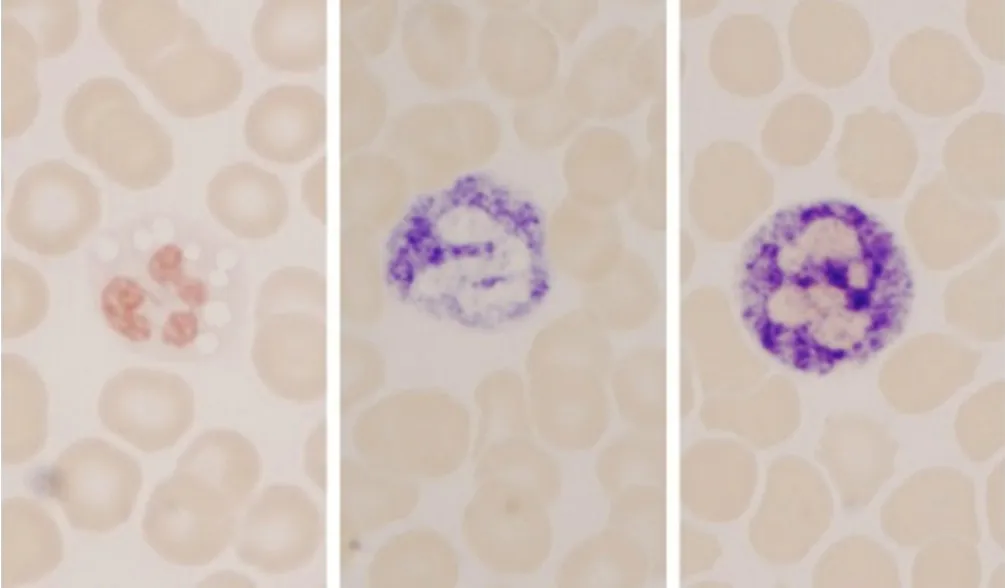
图3 NLsDM患者、正常人和感染患者的中性粒细胞(NAP,×1 000)(从左到右)Figure 3 Neutrophil of NLsDM patients,healthy individualsand infected patients(NAP staining)(from left to right)
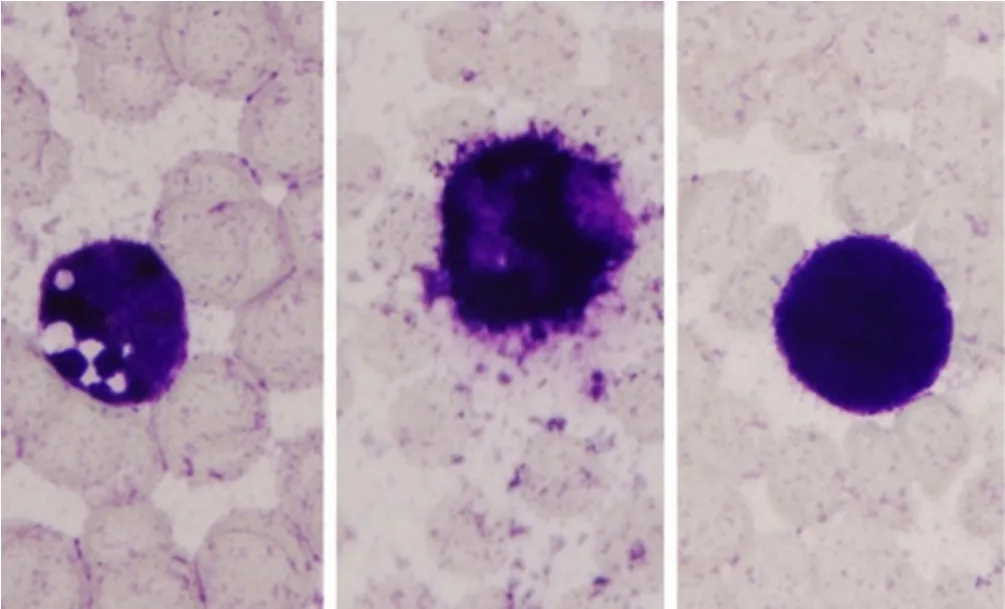
图4 NLsDM患者、正常人和感染患者的中性粒细胞(MPO,×1 000)(从左到右)Figure 4 Neutrophil of NLsDM patients,healthy individuals and infected patients(MPO staining)(from left to right)
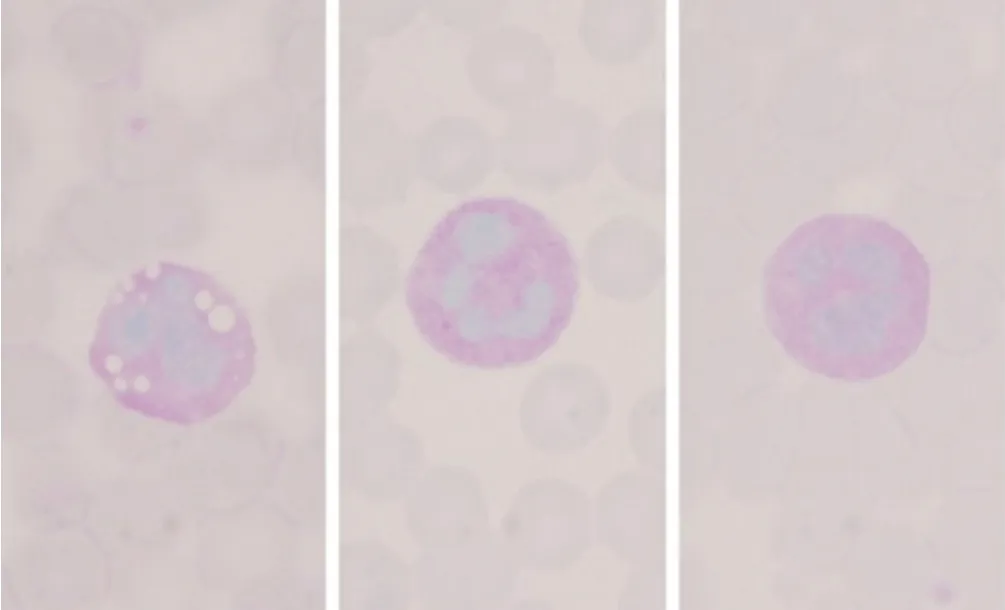
图5 NLsDM患者、正常人和感染患者的中性粒细胞(PAs,×1 000)(从左到右)Figure 5 Neutrophil of NLsDM patients,healthy individuals and infected patients(PAs staining)(from left to right)
3 讨论
1953年JORDANs[5]在临床表现为肌营养不良的兄弟二人中首次发现白细胞胞内脂肪滴。1966年,ROZENsZAJN等[6]在一对患者严重先天性鱼鳞病的姐妹外周血白细胞中发现类似现象,并将之命名为Jordan's小体。1985年该疾病被命名为Chanarin-Dorfman综合征,又称NLsDI。2001年,LEFÈVRE等[7]确认该病致病基因为CGI-58。NLsDM的发现相对较晚。1994年,WEssALOWsKI等[8]首次描述了1例表现为肌无力、肝肿大和高CK的4岁男性患儿,其肌细胞及外周血粒细胞内均可见脂肪滴沉积,患儿9岁的姐姐同样存在高CK及粒细胞脂肪滴沉积,2人均无先天性鱼鳞病症状,当时认为是临床表型较轻的变异型NLsDI。2007年,FIsCHER等[9]报道了首例经基因检测证实的NLsDM病例;陈涓涓等[10]于2009年报道了我国首例NLsDM病例。截至2020年,国内外累计报道经基因检测证实的NLsDM病例70余例,但是国内尚未发现NLsDI病例[1]。
NLsDM患者男女比例无统计学差异,任何年龄均可发病,但多起始于成年人,进展缓慢,主要临床表现为单纯肌病、骨骼肌+心肌病及心肌血管病[11],如肌无力、肌肉疼痛、活动后易疲劳及无症状性高CK血症[12]。无症状高CK血症患者年龄一般偏小,表明在短期内肌纤维中脂肪的蓄积并不影响肌肉的收缩功能[13]。30岁左右出现缓慢进展的肌无力症状,不对称性肢体无力为其特点之一,且以右侧肢体受累明显。受累肌肉以承重肌(如肩胛带肌、椎旁肌、大腿后部肌肉)较为突出,上肢重于下肢,近端重于远端。除单纯骨骼肌受累外,其他器官也可受累,一般无皮肤损害。心脏损害在NLsDM患者中较多见,一般晚于肌无力出现,表现为心悸、气喘、易疲劳以及水肿、咳嗽、夜尿增多等心功能不全症状,也可出现心绞痛症状[14]。ZHANG等[15]进行的一项针对国内45例NLsDM患者的研究发现,患者表现为无症状CK增高2例、单纯骨骼肌病18例、单纯心肌病4例、骨骼肌和心肌同时受累21例;除此之外,患者可合并糖尿病、高脂血症、胰腺炎、感音神经性耳聋等。MAssA等[16]进行的一项包含34例NLsDM患者的研究表明,患者除了存在骨骼肌受累外,还存在心肌损害(32%)、肝脏损害(23%)、糖尿病(23%)、身材矮小(18%)、胰腺炎(15%)、神经性耳聋(9%)、甲状腺功能减退(6%)以及认知障碍(3%)。
NLsDM患者中性粒细胞的形态异常与感染时的空泡变性较为相似,但是二者又存在明显不同,主要表现为以下几点:(1)中毒性改变的空泡变性只见于中性粒细胞,而NLsDM患者的中性粒细胞、嗜酸粒细胞、嗜碱粒细胞及单核细胞胞质中均可见空泡;(2)中毒性改变除可见空泡变性外,一般还伴有中性粒细胞的中毒颗粒、杜勒小体等其他形态学异常;(3)中毒性改变的空泡变性仅见于部分中性粒细胞,而NLsDM患者的绝大部分中性粒细胞胞质中均可见空泡,且空泡的形状较圆、数量较多(1个细胞中可达10个以上)。通过以上形态学的差异,基本可区分NLsDM与感染时的空泡变性。但是,由于正常人外周血中的单核细胞、嗜酸粒细胞及嗜碱粒细胞的比例较低,特别在感染时会进一步降低,而且部分感染患者只有空泡变性,不伴有中毒颗粒等其他形态学异常,导致通过以上要点进行鉴别会比较困难。如果患者形态学特点不够典型,可加做NAP染色。NLsDM患者中性粒细胞胞质中存在脂肪沉积,可能会影响其胞质中酶活性,因此NAP呈阴性反应;而感染患者胞质中酶活性明显增强,阳性率和积分值均明显增高。相比MPO和PAs,NAP能够更好地将二者进行区分。
文献报道NLsDM患者外周血和骨骼肌油红O染色可见脂肪滴沉积,是筛查NLsDM的重要辅助手段[11]。但是,也有个别无脂肪沉积的病例[17-18]。而且,油红O染色操作繁琐、费时长,外周血中性粒细胞更不容易着色,经常出现假阴性。相比而言,外周血瑞-姬氏染色和NAP操作简单,在临床实验室均可常规开展,更容易发现白细胞的形态异常。因此,对于临床中发现的高CK血症、隐匿起病的骨骼肌无力或有心肌损伤症状的患者,如果外周血白细胞出现上述典型的形态学特征,应考虑NLsDM的可能性,建议尽快完善PNPLA2基因检测以明确诊断。
作者贡献:邢莹设计研究方案、负责论文起草;普程伟、尚柯负责进行实验及图片采集;屈晨雪负责最终版本修订,对论文负责。
本文无利益冲突。

