恩他卡朋联合复方左旋多巴治疗帕金森病的疗效及对血清生物标记物的影响
巩利,马倩倩
帕金森病(Parkinson’s disease,PD)是常见的神经系统变性疾病[1]。复方左旋多巴是临床治疗PD 的常用药物,但随着病程进展及用药时间的延长,部分患者可能发生症状波动或产生异动症,疗效降低[2]。恩他卡朋是一种儿茶酚-O-甲基转移酶(catechol-O-methyltransferase,COMT)抑制剂,与复方左旋多巴同服有增效作用,但对运动症状及异动症的影响仍有争议[3]。研究发现,淀粉样蛋白β1-42(amyloid β1-42,Aβ1-42)、尿酸(uric acid,UA)、胱抑素C(cystatin C,CysC)及表皮生长因子(epidermal growth factor,EGF)等生物标记物与PD的发生发展有关,但药物疗效与上述生物标记物的表达的相关性尚不明确[4]。本研究即观察恩他卡朋联合复方左旋多巴治疗PD的疗效,及其对血清Aβ1-42、UA、CysC、EGF水平的影响,以期为临床治疗提供参考依据。
1 资料与方法
1.1 一般资料
选择2019 年1 月至2020 年11 月我科收治的PD 患者104 例。纳入标准:符合PD 的临床诊断标准[1];年龄40~80 岁,性别不限;至少1 个月的左旋多巴治疗史且在近1个月内剂量稳定,无剂末效应;近3 个月内未接受其他系统治疗;患者或其主要照料者能正确填写日常记录。排除标准:既往使用或正在接受恩他卡朋或其他抗PD 药物治疗;继发性PD;其他类型痴呆;合并癫痫、脑血管疾病及颅内占位性病变等;合并严重焦虑、抑郁、精神分裂症;合并谵妄、失语症、意识障碍等不便开展认知功能评估者;入组前3个月内使用中枢兴奋剂、血管扩张药物、华法林、抗抑郁药及其他影响本试验的药物者;具有严重剂量高峰异动症者;对本研究药物过敏或有明确禁忌证者。本研究所有受试者均知情并自愿参与,研究经医院伦理委员会审核批准通过。
采用电脑R2.0 软件生成随机分组码,按1∶1 比例随机分为观察组和对照组,每组52例。2组患者的年龄、性别、体质量指数(body mass index,BMI)、受教育年限、病程、Hoehn-Yahr分级比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
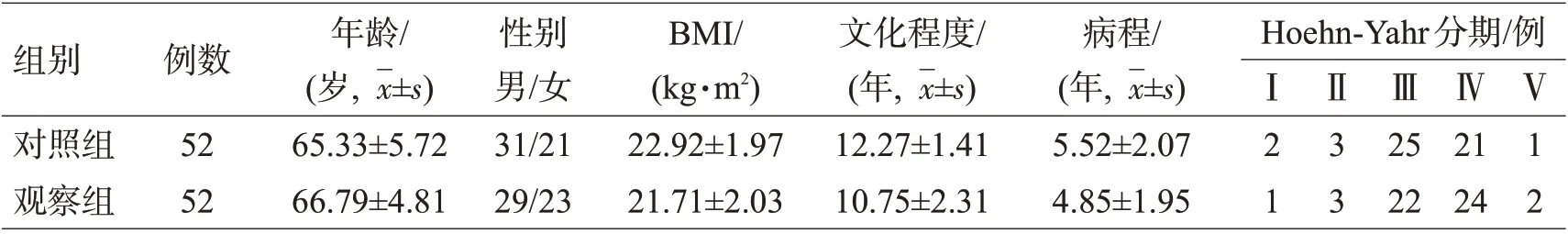
表1 2组一般资料比较
1.2 方法
1.2.1 治疗方法 2组用药前停服左旋多巴片至少12 h。对照组患者给予复方卡比多巴(精华制药集团股份有限公司,每片含卡比多巴25 mg,左旋多巴0.25 g)餐前1 h 或餐后1.5 h 口服,初始剂量为137.5 mg/次,3 次/d。1 周后根据病情调整每隔3~4天增加半片(137.5 mg)直至最佳剂量,最大剂量不超过400 mg/d(以左旋多巴含量计)。在对照组基础上,观察组加用恩他卡朋(芬兰奥立安大药厂,200 mg/片),200 mg/次,1 次/d;可根据病情调整服药次数与复方卡比多巴一致。2组均持续治疗12周。
1.2.2 观察指标 ①于治疗前和治疗4周、12周,采用帕金森病统一评分量表(unified Parkinson's disease rating score,UPDRS)[5]的第Ш分量表评价患者运动功能。②分别于治疗前及治疗12 周后,采用蒙特利尔认知评估量表(montreal cognition assess,MoCA)[6-8]评价认知功能,包括定向力、延迟回忆、抽象、语言、注意、记忆、命名、视空间与执行功能8个领域;评分<26分表示存在认知功能障碍,得分越低则认知功能障碍越重。③于治疗前及治疗12 周后,采用采用帕金森病生活质量问卷-39(the 39-item Parkinson's disease questionnaire,PDQ-39)[9]评价生活质量,包括身体活动、日常生活行为、精神健康、屈辱感、社会支持、认知、交流与身体不适8个维度,总分0~156分,得分越高表示生活质量越差。④晨取空腹静脉血5.0 mL,酶联免疫吸附试剂盒检测Aβ1-42、UA、CysC和EGF水平。
1.2.3 安全性评价 治疗前、后各进行1次肝、肾功能、心电图、血尿便常规检查,记录用药期间相关不良反应发生情况。
1.3 统计学处理
采用SPSS 22.0统计学软件处理数据。符合正态分布及方差齐性的计量资料以(±s)表示,组间比较采用独立样本均数t检验;计数资料以率表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 2组治疗前后UPDRS-Ⅲ评分比较
治疗前及治疗4周后,2组的UPDRS-Ⅲ评分差异无统计学意义(P>0.05);治疗12周后,2组患者的UPDRS-Ⅲ评分均低于同组治疗前,且观察组低于对照组(均P<0.05),见表2。
表2 2组治疗前后UPDRS-Ⅲ评分比较(分, ±s)

表2 2组治疗前后UPDRS-Ⅲ评分比较(分, ±s)
注:与治疗前比较,①P<0.05;与对照组比较,②P<0.05
组别对照组观察组例数52 52治疗前32.66±5.71 33.64±5.53治疗4周30.35±5.02 28.23±4.64治疗12周25.21±3.53①21.66±2.79①②
2.2 2组治疗前后MoCA评分比较
治疗前,2组的MoCA评分差异无统计学意义(P>0.05);治疗12 周后,2 组的MoCA 评分均高于同组治疗前(均P<0.05),但2组间差异无统计学意义(P>0.05),见表3。
表3 2组治疗前后MoCA评分比较(分, ±s)

表3 2组治疗前后MoCA评分比较(分, ±s)
注:与治疗前比较,①P<0.05
组别对照组观察组例数52 52治疗前22.84±2.17 21.25±1.93治疗后24.84±2.17①25.25±1.93①
2.3 2组治疗前后PDQ-39评分比较
治疗前,2组的PDQ-39评分差异无统计学意义(P>0.05);治疗12周后,2组的PDQ-39评分均低于同组治疗前,且观察组低于对照组(均P<0.05),见表4。
表4 2组治疗前后PDQ-39评分比较(分, ±s)
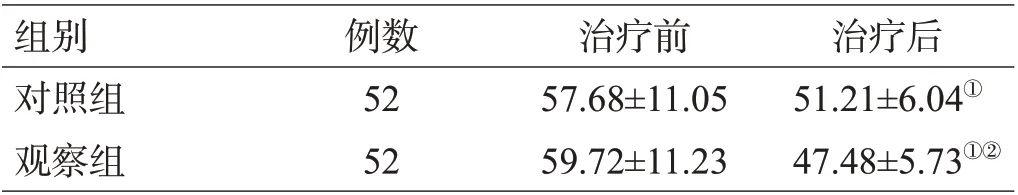
表4 2组治疗前后PDQ-39评分比较(分, ±s)
注:与治疗前比较,①P<0.05;与对照组比较,②P<0.05
组别对照组观察组例数52 52治疗前57.68±11.05 59.72±11.23治疗后51.21±6.04①47.48±5.73①②
2.4 2组治疗前后血清Aβ1-42、UA、CysC、EGF水平比较
治疗12周后,2组患者的血清CysC水平均降低,Aβ1-42、UA、EGF 水平升高(均P<0.05),且观察组的改善幅度高于对照组(均P<0.05),见表5。
表5 2组治疗前后血清Aβ1-42、UA、CysC、EGF水平比较(±s)
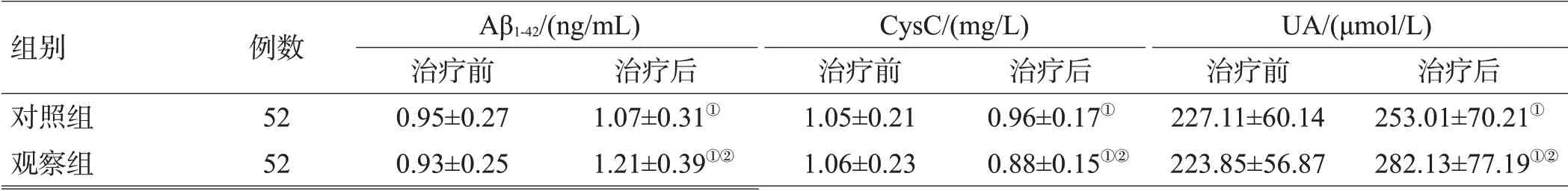
表5 2组治疗前后血清Aβ1-42、UA、CysC、EGF水平比较(±s)
组别对照组观察组例数52 52 Aβ1-42/(ng/mL)治疗前0.95±0.27 0.93±0.25治疗后1.07±0.31①1.21±0.39①②CysC/(mg/L)治疗前1.05±0.21 1.06±0.23治疗后0.96±0.17①0.88±0.15①②UA/(μmol/L)治疗前227.11±60.14 223.85±56.87治疗后253.01±70.21①282.13±77.19①②

注:与治疗前比较,①P<0.05;与对照组比较,②P<0.05
2.5 安全性评价
治疗期间,2 组均无因试验药物不良反应而退出者。观察组轻度头痛1例,恶心3例,异动症1例,不良反应率9.62%;对照组恶心3例,直立性低血压1例,头痛1例,异动症1例,不良反应率11.54%;2组不良反应发生率差异无统计学意义(P>0.05)。
3 讨论
PD的发病机制目前尚未完全阐明,主要认为与中脑黑质致密部及蓝斑神经元脱失导致多巴胺(dopamine,DA)分泌减少有关[10]。通过减少DA 降解或补充外源性DA 能在一定程度上缓解症状[11]。但DA 难以透过血-脑屏障,左旋多巴作为多巴胺的前体物质,可通过血-脑屏障入脑,经多巴脱羧酶脱羧后在脑内转化产生DA,可发挥治疗作用[12]。本研究对照组使用复方左旋多巴制剂治疗12周后,PD症状得到明显缓解,认知功能及肌强直均有所改善。但随着病程进展,药物作用可能逐步下降,且左旋多巴向DA 转化率偏低,需逐步增加用药剂量且长期维持用药,容易发生直立性低血压、恶心、呕吐等不良反应,甚至出现运动并发症[13]。
新一代COMT抑制剂恩他卡朋具有选择性强、活性高及毒性小等特点,与左旋多巴制剂同服可提高左旋多巴的生物利用度,优化和延长其作用,发挥增效作用[14]。本研究结果显示,观察组加用恩他卡朋治疗后,UPDRS-Ⅲ评分降低明显多于对照组(P<0.05),能更好地缓解PD患者的运动症状。PDQ-39评分亦显示,观察组的降分率明显多于对照组(P<0.05),生活质量改善更明显。DA 代谢过程中可生成超氧自由基、半胱氨酸等神经毒性物质,故在长期、高剂量使用左旋多巴制剂过程中不良反应发生率较高[15]。而使用恩他卡朋辅助治疗可减少左旋多巴的用量,减少相关副反应。本研究中,2组不良反应率差异无统计学意义(P>0.05),但观察组仍表现出下降趋势,用药安全性较好。
认知功能障碍是PD 患者最常见的非运动症状之一,约20%~50%的PD 患者伴发轻度认知功能障碍[16]。PD 患者发生认知功能障碍的机理尚不明确,多认为与DA 神经元变性丢失有关,神经免疫炎症及氧化应激在该病理生理过程中发挥着重要作用[17]。Aβ1-42是Aβ的主要形式之一,极易聚集且神经毒性较强,可诱导一氧化氮的生成而介导神经炎症级联反应以及氧化应激反应,诱导神经元的坏死或凋亡。PD 患者的脑内Aβ1-42异常增多而导致聚集沉积,损伤脑神经元,外周血Aβ1-42则相应减少,与PD 认知功能损害程度关系密切[18]。CysC 也被证实与短暂性脑缺血、多发性硬化及阿尔茨海默病等关系密切,可参与炎症反应而诱导神经细胞的再生,在脑神经元损伤的情况下,CysC可被激活而升高,以保护细胞损伤[19]。EGF也被证实是一种很有希望的提示PD 患者认知功能损伤的敏感生物学标志物,且其水平越低患者的认知功能损伤越明显[20]。梁若冰等[21]研究显示,脑内CysC与Aβ1-42具有共表达性,可抑制淀粉样蛋白的异常聚集沉积,在PD患者中具有明显的血清Aβ1-42低表达和CysC高表达,且与PD分期、认知功能损伤程度有关。UA是一种天然自由基清除剂和抗氧化剂,UA 含量降低时往往提示机体氧化应激系统激活,抗氧化能力降低[22]。本研究中,2组治疗后血清CysC 水平降低,Aβ1-42、UA、EGF 水平升高,而观察组的改善幅度高于对照组(P<0.05)。多项研究表明,恩他卡朋辅助左旋多巴制剂治疗PD 能够减轻患者的氧化应激反应,提高临床症状缓解效果[23],也有助于改善认知功能障碍、焦虑抑郁、幻觉等精神症状,减少感觉异常症状,降低体位性低血压等自主神经症状[24]。提示恩他卡朋辅助治疗PD 可能通过减轻神经炎症及氧化应激程度。认知功能评价结果显示,2 组治疗后MoCA评分均较同组治疗前提高(P<0.05),但2组间差异无统计学意义(P>0.05)。这可能与观察时间较短有关,也可能与样本量偏小有关。
综上所述,与单用左旋多巴相比,恩他卡朋联合左旋多巴治疗PD 能好地改善患者运动症状、提高患者生活质量;血清CysC水平降低,Aβ1-42、UA、EGF水平升高的幅度较高;且安全性较好。对临床用药具有一定的参考价值。

