石墨炉原子吸收光谱法与电感耦合等离子体质谱法对大米粉中镉含量的检测价值分析
杨建伟
(天津市宝坻区疾病预防控制中心理化检验科,天津 301800)
大米作为我国日常主食之一,其食用安全直接关系到人民的生命安全及健康保障,近年来随着现代化工业的快速发展,农产品重金属污染问题也日益严重,其中以大米镉含量超标最为突出,受到大众的广泛关注[1]。镉(Cadmium,Cd)是重金属中主要污染元素之一,其生物毒性强,进入人体后可在肾脏累积,对肾脏、肺均具有严重损害,且可软化骨骼,导致钙质流失,对人们身心健康造成了严重威胁[2,3]。我国食品安全标准(GB 2762-2017)[4]规定,镉大米标准规定值为≤0.2 mg/kg,其标准检测方式包括石墨炉原子吸收光谱法(graphite furnace atomic absorption spectrometry,GFAAS)、电感耦合等离子体质谱法(inductively coupled plasma-mass spectrometry,ICP-MS)等,其检验原理、检出限、灵敏度及不确定度等各不相同,因而检出结果存在一定差异[5]。现本研究以大米粉为样品,采用GFAAS 法与ICP-MS 法进行镉含量检验,通过二者检测结果的对比,分析其对大米镉含量的检验准确性及可行性,现报道如下。
1 材料与方法
1.1 样品与试验材料 样品:国粮院ACAS-PT1044大米粉,规格0.080 mg/kg。质控样:①GBW(E)100350 大米粉成分分析标准物质,镉含量(0.11±0.01)mg/kg,北京钢研纳克检测技术股份有限公司,②GBW(E)100349 大米粉成分分析标准物质,镉含量(0.41±0.01)mg/kg,北京钢研纳克检测技术股份有限公司。镉元素标准溶液:选自国家钢铁材料测试中心钢铁研究总院,Cd 浓度分别为0、0.5、1.0、2.0、5.0、10.0 μg/L。硝酸:优级纯,德国默克有限公司。磷酸二氢铵(99.0%):成都市科龙化工试剂厂。试验用水均为超纯水,出自赛多利斯有限公司。
1.2 仪器设备 电子天平:BS224S 型,北京赛多利斯仪器系统有限公司;密闭微波消解仪:MDS-6 型,上海新仪微波化学科技有限公司;电感耦合等离子体质谱分析仪:ICP-MS(型号iCAP-RQ),美国安捷伦科技有限公司;原子吸收光谱仪:Zeenit650p 型,德国耶拿分析仪器股份公司;电子控温加热板:ECH-1型,上海新仪微波化学科技有限公司;可调电热板:Mb 型,北京科伟永兴仪器有限公司;超纯水仪:赛多利斯有限公司。
1.3 方法
1.3.1 样品前处理 采用微波消解前处理方式,通过电子天平取样品(0.3000±0.005)g 置于微波消解仪内,随后注入硝酸8 ml,密封后实行微波消解系统进行梯度消解。消解梯度:步骤1:功率400 W,升温时间5 min,保持时间5 min,红外温度210 ℃。步骤2:功率800 W,升温时间5 min,保持时间15 min,红外温度210 ℃。步骤3:功率1200 W,升温时间5 min,保持时间10 min,红外温度210 ℃。消解完毕后冷却至室温,待排气后进行赶酸操作,于180 ℃温度条件下将试样赶酸至绿豆大小,冷却至室温后转至50 ml 容量瓶中,采用超纯水进行多次洗涤,随后将洗涤液完全转移到容量瓶中,定容至50 ml 刻度线,充分混匀后备用,做空白与6 平行实验。
1.3.2 GFAAS 法检测①标准储备液配置:取1 ml 镉单元素标准溶液(1000 μg/ml)置于10 ml 容量瓶中,通过硝酸(0.5%)定容至10 ml 刻度线,制取100 μg/ml 镉标准储备液,随后以相同方式,逐级稀释制备100 ng/ml镉标准储备液;②标准工作液配置:取300 μl 镉标准储备液(100 ng/ml)置于10 ml 容量瓶中,通过硝酸(0.5%)定容至10 ml 刻度线,制取3 ng/ml 镉标准使用液,随后分别取0.3、0.6、0.9、1.2、1.5、2.4、3.0 ng/ml 7 个标准点,通过仪器自动稀释标准使用液3 ng/ml获得线性关系;③GFAAS 上机测定:仪器预热后,调整至最佳条件,以磷酸二氢铵(1%)为基体改进剂,升温程序:干燥:温度75 ℃,升温速率6 ℃/min,保持20 min,总时间29.5 min;干燥:温度120 ℃,升温速率5 ℃/min,保持10 min,总时间16 min;灰化:温度350 ℃,升温速率100 ℃/min,保持15 min,总时间17.3 min;灰化:温度450 ℃,升温速率250 ℃/min,保持15 min,总时间15.4 min;自动归零:温度450 ℃,保持6 min,总时间6 min;原子化:温度1500 ℃,升温速率1500 ℃/min,保持3 min,总时间3.7 min;除残:温度2450 ℃,升温速率500 ℃/min,保持4 min,总时间5.9 min。随后通过硝酸(0.5%)自动稀释标准曲线,测定标准曲线、样品溶液、空白溶液及质控溶液中的镉含量。
1.3.3 ICP-MS 法检测 ①标准储备液配置:采用重量法配置26 种金属元素的混合标准曲线,随后取250 μl 多元素标准溶液(100 μg/ml)置于25 ml 聚乙烯瓶中,称取25g 硝酸溶液(2%),制备1 μg/ml 标准储备液;②标准工作液配置:分别取25、125、250、375、500 μl 标准储备液中取置于25 ml 聚乙烯比色管内,并称取25 g 硝酸溶液(2%),获取1、5、10、15、20 ng/ml 5 个标线点金属元素混合标准曲线的浓度线性关系;③Icp-ms 上机测定:提前预热,调谐仪器至最佳条件:测试真空度5e-007 mbar,排风0.4 mbar,氩气减压阀0.6 MPa,氦气减压阀0.15 MPa,涡轮分子泵速1000 Hz,等离子体废气0.4~0.6 mbar,随机背景<1cps(4.5),氧化物离子(Ceo+/Ce+)<2%。随后通过硝酸溶液(2%)配制标准曲线,最后上机测定标准曲线、样品溶液、空白溶液及质控溶液中的镉含量。
1.4 观察指标 ①比较GFAAS 法与ICP-MS 法检测样品镉含量的标准曲线方差及检出限,食品安全国家标准中镉的测定方法检出限[6]为0.001 mg/kg,定量限为0.003 mg/kg,镉成分标准曲线相关系数国家标准[7]为0.999~0.9999;②比较两种检测方式的精密度,对本次质控样[GBW(E)100350 大米粉成分分析标准物质与GBW(E)100349 大米粉成分分析标准物质]的镉含量进行检测,比较其测定值与相对标准偏差(RSD),测定值越接近,准确性越高,RSD 越小精密度越高;③比较两种方式的加标回收率,采用加标回收法进行验证,GFAAS 法的加标量分别为0、1、2、3 mg/kg,ICP-MS 法的加标量分别为0、5、10、15 mg/kg;④比较两种方式在平行实验中的精密度,取考核样品做6 平行试验,分别采用GFAAS 法与ICP-MS 法测定其镉含量,RSD 越小,表示精密度越高;⑤比较两种检测方式的不确定度,其不确定度来源包括重复性测量、仪器设备、容量瓶、温度、容积误差、称重偏差、标准物质、标液配制、标曲拟合、前处理及测定产生的基体干扰等。
2 结果
2.1 GFAAS 法与ICP-MS 法的标准线性方程及检出限比较 GFAAS 法与ICP-MS 法的相关系数及检出限均符合国家规定标准,且ICP-MS 法的检出限低于GFAAS 法,见表1。
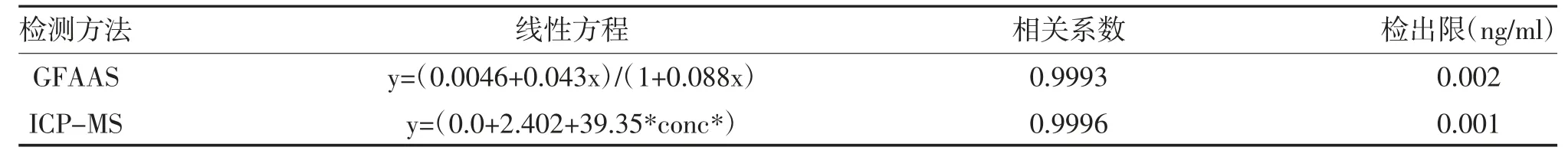
表1 GFAAS 法与ICP-MS 法的标准曲线方程及检出限比较
2.2 GFAAS 法与ICP-MS 法的准确度、精密度比较相较于GFAAS 法,ICP-MS 法对质控样镉含量的测定值与其标准值更为接近,且RSD 更低,可见ICPMS 法的准确度及精密度均高于GFAAS 法,见表2。2.3 GFAAS 法与ICP-MS 法的加标回收率比较ICP-MS 法的加标回收率高于GFAAS 法,见表3。
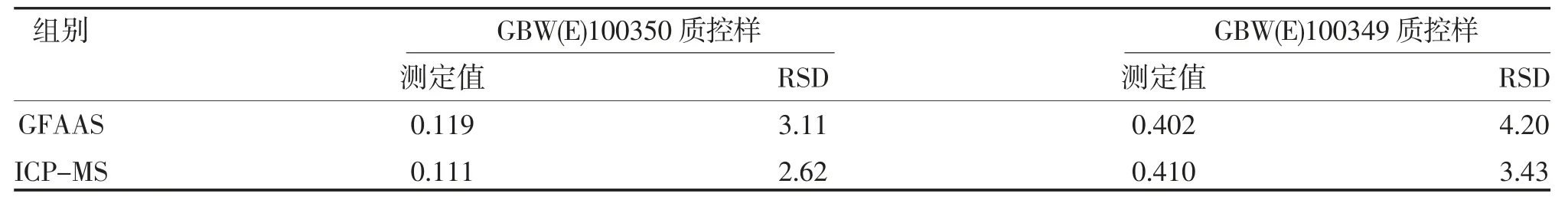
表2 GFAAS 法与ICP-MS 法的精密度比较(mg/kg,%)
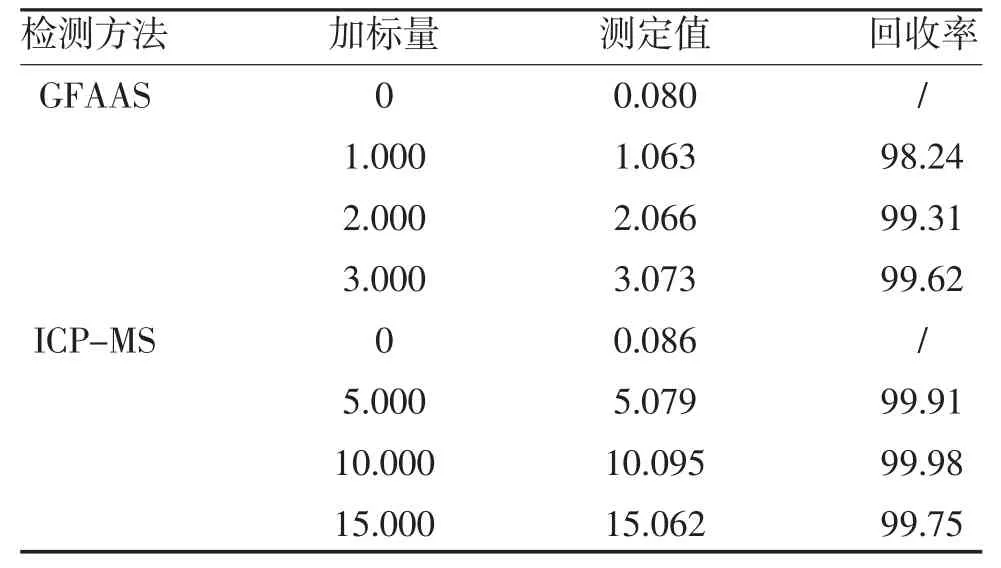
表3 GFAAS 法与ICP-MS 法加标回收率比较(mg/kg,%)
2.4 GFAAS 法与ICP-MS 法在平行实验中的精密度比较 ICP-MS 法在不同样品镉含量测定中的RSD 均小于GFAAS 法,其精密度高于GFAAS 法,见表4。
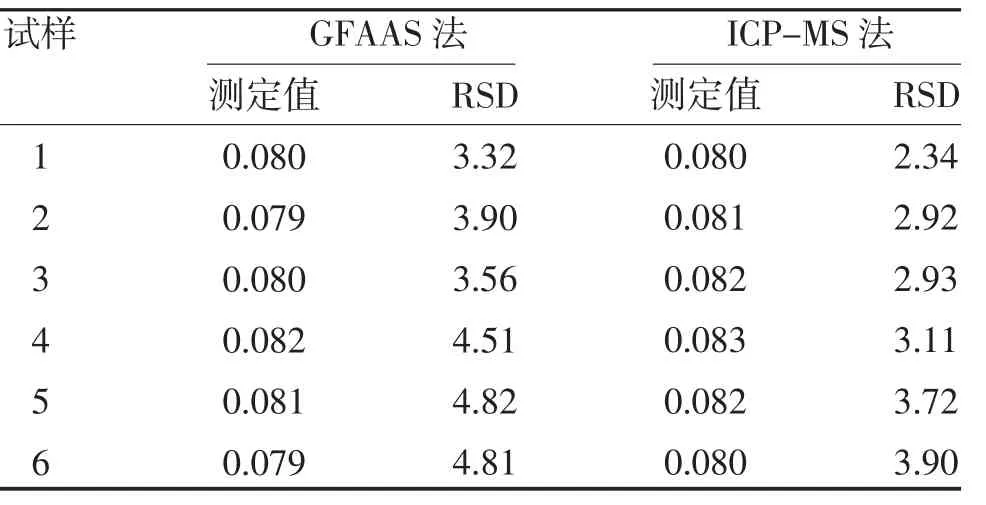
表4 不同样品中GFAAS 法与ICP-MS 法的镉含量测定值比较(mg/kg,%)
2.5 GFAAS 法与ICP-MS 法的不确定度比较 ICPMS 法的各项不确定度数值均小于GFAAS 法,见表5。

表5 GFAAS 法与ICP-MS 法的不确定度比较
3 讨论
我国作为传统的农耕国家,大米等粮食重金属污染问题一直备受关注,现阶段工业化进程使得国内生态环境日益恶化,土壤的重金属污染致使水稻生长环境遭到严重破坏,且水稻的生长特性易引起镉元素富集,导致“镉大米”的出现,为当前粮食安全带来了较大隐患[8,9]。在此背景下,加强大米中镉的检测监管力度,是杜绝“镉大米”流向餐桌的重要方式。GFAAS 是利用石墨材料制成的原子化器经电流加热进行的原子吸收分析方式,其样品均需进行原子化,可有效避免原子浓度的稀释,灵敏度高,适用于多种痕量金属元素的检测[10,11]。但该方式中酸浓度可对原子吸收仪的准确度及平行度造成较大影响,需前处理方案将酸尽量赶尽,不仅过程复杂、费时费力,且存在污染环境问题,对人体及环境设施均有较大危害[12-14]。此外,当前GFAAS 检测中,一种空心阴极灯通常无法发射多种金属元素频率,因此原子吸收光谱无法同时测定多种元素,且石墨管及空心阴极灯寿命较短,其稳定性通常较差[15,16]。ICP-MS是近年来快速发展的新型元素/同位素分析检测技术,可结合ICP 的高温(7000K)电离特性与四极杆质谱计的高灵敏度特点[17],其动态线性范围广,可实现10-12~10-6数量级浓度的直接测定,且精密度高,检测速度快,是国内公认的最佳痕量、超痕量无机元素分析技术,其应用已涉及多个领域[18-20]。此外,ICP-MS 还可快速测定同位素比值,且消解后无需赶酸,可减少污染,具有安全、高效、检测范围广等应用优势[21,22]。
本研究结果显示,GFAAS 法与ICP-MS 法的相关系数及检出限均符合国家规定标准,其中ICPMS 法的检出限低于GFAAS 法,这与杨晓忱[23]报道一致。提示两种方式对大米粉镉含量的测定参数均在标准范围内,二者均具有较高可行性,但相较于GFAAS 法,ICP-MS 法的检出限更低,更有利于低浓度样品的检测。在质控样检测中,ICP-MS 法的准确度及精密度均高于GFAAS 法,表明CP-MS 法对大米粉镉含量的测定更为准确,其误差更小,检测价值更高。此外,ICP-MS 法的加标回收率高于GFAAS法,可见ICP-MS 法的镉残留量更少,在重金属含量的检测中具有更高的适用性,与沈银梅等[24]研究观点相符。同时,ICP-MS 法在平行试验中的精密度均高于GFAAS 法,此结果也再次证实,ICP-MS 法对镉含量的检测准确性优于GFAAS 法,与吴雁均[25]研究结果一致。最后,在不确定度的对比中,CP-MS 法的各项不确定度均小于GFAAS 法,表明CP-MS 法的检测质量高于GFAAS 法,其整体方案更为可行。
综上所述,相较于GFAAS 法,ICP-MS 法在大米粉镉含量检测中的检出限更低,且准确度、精密度及加标回收率更高,不确定度较低,其检测价值更为显著。但ICP-MS 法的检测成本通常高于GFAAS法,鉴于二者均符合国家标准,检测机构可依据具体情况及实际需求进行选择。

