新生儿序贯接种两种乙肝疫苗的效果分析
陈娟
摘要:目的:分析新生儿序贯接种两种乙肝疫苗的效果。方法:回归性分析我院200例序贯接种乙肝疫苗的新生儿,按实际接种疫苗分组(实验组、对照组),100例/组。选取时间:2017年11月至2018年3月。对照组仅接种酿酒酵母、实验组接种酿酒酵母+CHO基因疫苗。对收集数据进行统计分析后,对比两组12月龄时乙肝表面抗体水平。结果:两组12月龄时乙肝表面抗体水平对比无明显差异(P>0.05)。结论:新生儿序贯接种酿酒酵母与接种酿酒酵母+CHO基因疫苗实际效果对比明显差异,均为作为新生儿序贯接种方案。
关键词:新生儿;乙肝疫苗;酿酒酵母;CHO基因疫苗
【中图分类号】 R186 【文献标识码】 A 【文章编号】2107-2306(2022)12--01
乙肝是传染科常见的疾病之一,指乙型肝炎病毒持续感染>6个月,最终导致肝脏发生不同程度炎症坏死、纤维化的慢性传染性疾病,有数据显示世界范围内每年超80万患者死于乙肝病毒感染[1]。母婴传播是乙肝病毒传染较常见的途径,也被称为垂直传播,是指在为围生期通过胎盘、产道或哺乳,由亲代传染给子代的方式,故临床在新生儿阶段多采取序贯接种乙肝疫苗的方式治疗、预防乙肝。目前用于新生儿序贯接种的乙肝疫苗主要包括酿酒酵母、CHO基因疫苗,随着临床治疗经验的积累,开始逐渐将二者联合用于新生儿序贯治疗中,但目前临床对酿酒酵母+CHO基因疫苗序贯接种的研究较少,部分临床研究者仍抱有嚴重的怀疑态度[2]。鉴于此,本次研究筛选出200例序贯接种乙肝疫苗的新生儿作为研究对象,对比仅接种酿酒酵母、接种酿酒酵母+CHO基因疫苗两种接种方案的实际应用价值,现报道如下:
1资料与方法
1.1一般资料
2019年1月至2021年12月,回顾性分析我院序贯接种乙肝疫苗的新生儿,选出200例按动态随机法分组(实验组、对照组),100例/组。两组男女比例分别为52∶48、59∶41;对照组出生时间最短者8h、最长者20h、均值为14.58±1.99h;实验组出生时间最短者8h、最长者19h、均值为14.63±2.05h。组间性别比例、年龄区间的数据差异小(P>0.05),有可比性。
纳入标准:(1)临床资料完整度者;(2)患儿/家属对研究知情并签订同意书;(3)均为足月产儿。
排除标准:(1)乙肝疫苗接种禁忌新生儿;(2)合并严重呼吸系统疾病患儿;(3)拒绝配合研究者。
1.2方法
所有新生儿均采用0、1、6月的免疫程序(出生24h内、1月龄与6月龄分别接种一次)。注射部位上臂三角肌肉,免疫剂量为5ug。对照组三次均接种酿酒酵母(深圳康泰生物制品有限公司;国药准字:H20053054;1.0ml:20μg*3支);实验组第一次、第三次接种酿酒酵母(与对照组相同),第二次接种CHO基因疫苗(华北制药金坦生物技术股份有限公司;国药准字:S20103001;10微克/0.5毫升)。接种前需详细评估新生儿是否存在乙肝疫苗接种禁忌症,接种乙肝疫苗后需注意观察接种儿是否存在明显的药物过敏反应,及时作出针对性处理。
1.3观察指标
与接种儿12月龄时检查其体内乙肝表面抗体水平。静脉采血4-5ml血液,随后放置于离心机中分离血清,使用SPRRIA的方法检测受检者乙肝表面抗体水平。
1.4统计学处理
采用SPSS 23.0软件分析及处理数据,计数资料采用百分比表示,采用х2检验;计量资料以(x±s)表示,采用t检验,以P<0.05为差异具有统计学意义。
2结果
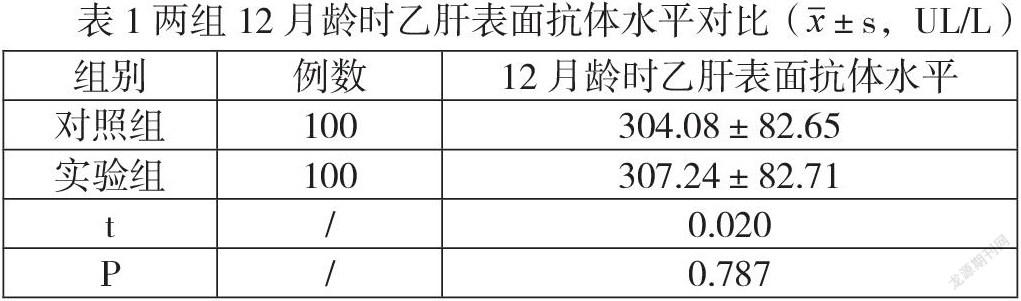
2.1对比两组12月龄时乙肝表面抗体水平
两组12月龄时乙肝表面抗体水平对比无明显差异(P>0.05),见表1。
3讨论
乙肝是一种传染性较强的疾病,主要感染的病原体为乙肝病毒,母婴传播是该乙肝病毒最直接的传播途径,临床数据显示超90%的乙肝病毒感染的患者均是经母婴传播,因此新生儿期实施科学的序贯接种乙肝疫苗意义重大[3-4]。
酿酒酵母疫苗、CHO基因疫苗是目前临床用于乙肝病毒新生儿期序贯治疗常用的两种选择,其中国内酿酒酵母疫苗最早是由深圳康泰生物制品有限公司在1993年研制出的,是目前临床应用最广泛的一种乙肝疫苗[5];CHO基因疫苗是国际上公认的第二代乙肝疫苗,临床大研究显示酿酒酵母疫苗、CHO基因疫苗均具有较好的母婴阻断效果[6]。近年来临床开始将以上两种乙肝疫苗联合用于新生儿贯序治疗中并取得了较理想的治疗效果。本次研究结果如下:两组12月龄时乙肝表面抗体水平对比无明显差异(P>0.05)。研究结果提示上述两种接种方案的有效性对比无明显差异,两组新生12月龄是乙肝表面抗体水平均能达到300UL/L,临床多将>300UL/L作为乙肝疫苗接种有效性的指标[7];乙肝表面抗体是乙肝病毒作用于人体,表面抗原刺激机体免疫系统产生的保护性抗体,可以中和乙肝病毒,临床多将其作为判断机体是否感染乙肝病毒或是否产生免疫力的重要指标,故本文研究结果提示对照组及是实验组的乙肝疫苗注射方案均能在接种者体内产生较优质的乙肝病毒抗体,能发挥很好的保护作用[8]。酿酒酵母疫苗又叫重组乙型肝炎疫苗,该疫苗是由重组酵母菌表达的乙型肝炎病毒表面抗原(HBsAg)经纯化并加入铝佐剂,通过培养该重组酵母菌来表达乙肝表面抗原,成本较低,从而得以大量生产[7];CHO基因疫苗是利用哺乳动物细胞基因生产的疫苗,通过重组CHO工程细胞表达乙肝表面抗原,经加工后制作使用,表达的乙型肝炎表面抗原更接近天然形式,疫苗稳定性好,但成本较高[9]。上述两种乙肝疫苗均属于基因工程免疫疫苗,均具有较好的免疫和母婴阻断的效果,同时对新生儿的安全性也具有一定保障。临床有研究提出由于机体对有没得的应答情况与疫苗的抗原结构具有较高的相关性,故临床在面对重组的酵母乙型肝炎疫苗免疫后的低应答或无应答者,可使用高剂量的重组CHO疫苗,由此提升提高免疫成功率[10]。
综上所述,仅接种酿酒酵母与联合接种CHO基因疫苗在新生儿乙肝序贯治疗中均具有较高的应用价值,安全性均具有保障。
参考文献:
[1]夏伟,唐悃,曾陵君,等.新生兒两种重组乙型肝炎疫苗序贯接种的免疫原性和不良反应观察[J].中国疫苗和免疫,2020,26(1):30-33.
[2]曾倩,高德强,李玉荣,等.新生儿乙肝疫苗接种与一过性表面抗原血症相关性研究[J].中国实用儿科杂志,2020,35(6):482-484.
[3]马丽亚,任卫星,马华,等.新生儿接种两种剂型乙型肝炎疫苗不同时间的免疫水平比较[J].现代生物医学进展,2020,20(7):1317-1321.
[4]叶明,徐璐,赵子华,等.合并巨细胞病毒感染对小儿乙型肝炎疫苗初次免疫应答的影响[J].肝脏,2021,26(5):554-556.
[5]安和兵,吕佳,王腾飞,等.HBsAg阳性母亲的新生儿接种乙肝疫苗后的免疫应答远期保护效果研究[J].河北医药,2021,43(17):2654-2656,2660.
[6]隋吉林,朱宗龙,杨俊英,等.昌平区146例10μg重组乙肝疫苗初次免疫新生儿5年免疫效果观察[J].国际病毒学杂志,2020,27(4):317-320.
[7]王文祥,马敬仓,刘景顺,等.2014-2018年山东省菏泽市乙肝疫情及新生儿乙肝疫苗接种情况监测[J].医学动物防制,2020,36(6):578-581.
[8]王菊英,刘瑶瑶,李锋.新生儿乙肝表面抗原阳性的确认及原因分析[J].中国免疫学杂志,2020,36(11):1370-1373.
[9]PARK,YOUNG-KYOUNG,JUNG,SANG-MIN,LIM,HYUNG-KWON,et al.Effects of Trx2p and Sec23p expression on stable production of hepatitis B surface antigen S domain in recombinant Saccharomyces cerevisiae[J].Journal of Biotechnology,2012,160(3/4):151-160.
[10]李本科,纪民,赵旭.母亲乙肝病毒感染状况对其子代疫苗接种效果影响的分析[J].公共卫生与预防医学,2020,31(2):138-140.

