二溴一氯硝基甲烷在紫外光照下的降解规律及反应路径
黄婷婷 邓 琳 文隆佳
(东南大学土木工程学院, 南京 211189)
饮用水消毒副产物(DBPs)对人体有致畸、致癌和致突变作用[1].随着消毒剂的单独或联合使用,越来越多的DBPs被检测了出来[2],其中含氮消毒副产物(N-DBPs)分布范围广泛[3],且因其显著的细胞毒性和遗传毒性而成为研究的热点[4-5].卤代硝基甲烷(HNMs)是含氮消毒副产物的典型代表,其毒性超过三卤甲烷、卤乙酸和卤代呋喃酮等消毒副产物[5],因而被美国环保署(USEPA)列入优先控制消毒副产物的最高等级.

1 材料与方法
1.1 化学药品与试剂
本实验中所有化学药品为分析纯或色谱纯.磷酸氢二钠和磷酸二氢钠均购于国药集团有限公司,次氯酸钠和溴化钠分别购于科密欧有限公司和上海源叶生物有限公司,二溴一氯硝基甲烷购于Quality Control Chemicals, 甲基叔丁基醚购于阿拉丁生化科技有限公司.其中,磷酸氢二钠、磷酸二氢钠、次氯酸钠和溴化钠均为分析纯,二溴一氯硝基甲烷和甲基叔丁基醚均为色谱纯,其质量分数分别为97.4%和99.9%.实验中所有水溶液均采用超纯水配制.
1.2 实验装置
紫外光降解实验在容积为500 mL的带盖圆柱形石英反应器(长20.0 cm,直径9.0 cm,壁厚1.0 cm,见图1)中进行.反应器配备了冷阱流动装置,通过水循环为反应器降温,将反应溶液温度控制在(22±2)℃.利用铁架台固定低压汞灯在反应器中央,其发射波长为254 nm.实验选用的低压紫外灯功率分别为6、10和16 W,用辐照计(UV-B)分别测量紫外灯灯管上、中、下端的表面光强,取其平均值,分别为9.1、15.5和22.6 mW/cm2.
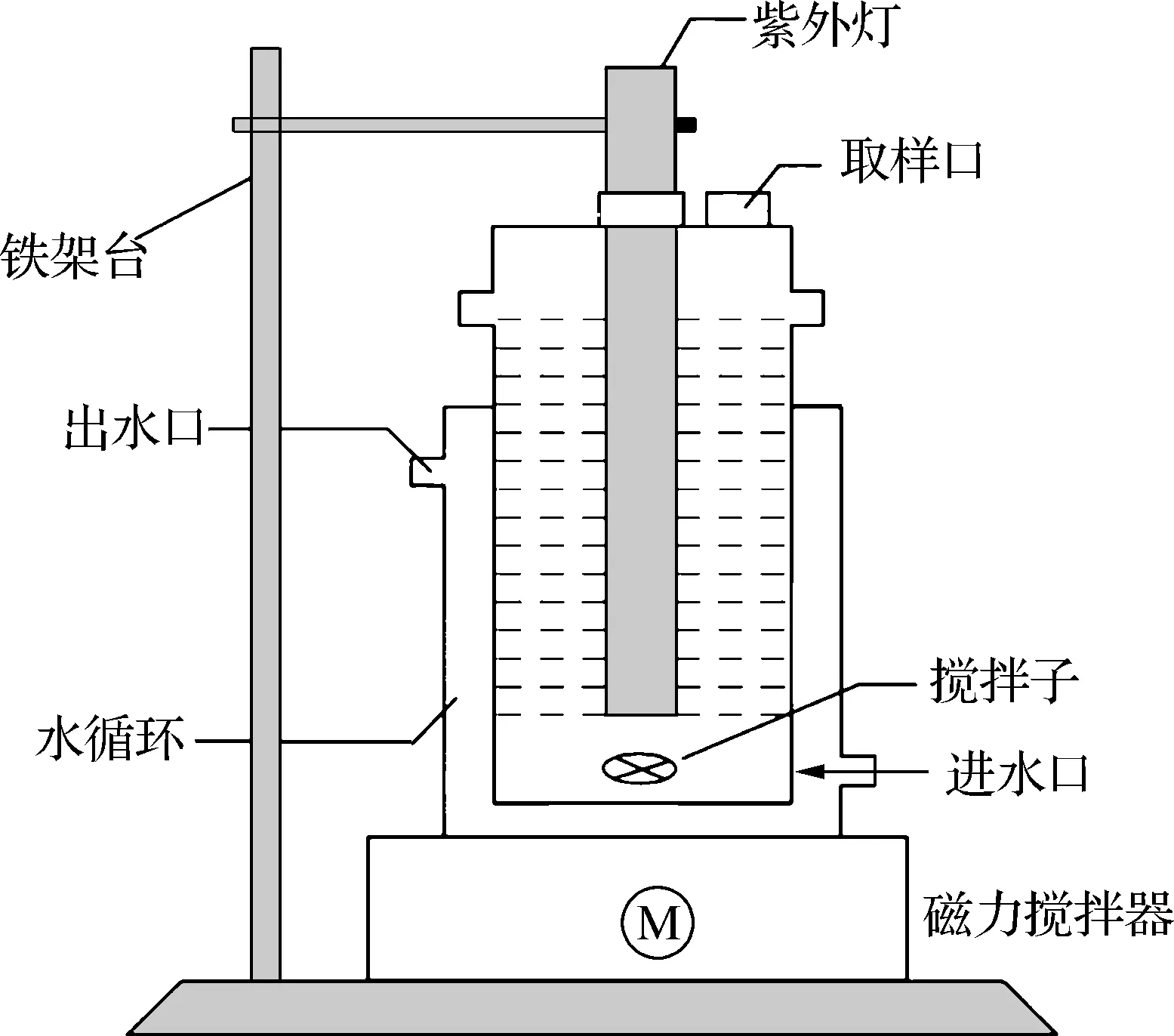
图1 紫外光降解实验装置
1.3 实验方法
实验制备500 mL的DBCNM溶液加入至反应容器中,采用浓度20 mmol/L的磷酸盐缓冲液调节溶液的pH值,并打开磁力搅拌器混匀溶液.根据不同的反应条件进行实验,按照设定好的时间间隔(0、0.5、1.0、2.0、3.0、4.0、5.0 min)用移液管从反应器中取出5.0 mL样品注入10.0 mL棕色带盖小玻璃瓶中,再加入2.0 mL甲基叔丁基醚进行萃取,放置于摇床振荡10 min,然后静置5 min. 待混合液分层后,将1.0 mL上层萃取液装入进样瓶中,采用气相色谱电子捕获检测器(GC/ECD)进行检测分析.所有实验均重复2次.
1.4 分析方法
实验使用仪器为安捷伦6890A GC-ECD型气相色谱仪,色谱柱型号为HP-1(30 m×0.25 mm×0.25 μm).实验样品经萃取之后装入进样瓶中,按USEPA551.1[13]方法测定溶液中一氯硝基甲烷(CNM)、一溴硝基甲烷(BNM)、BCNM、BDCNM和DBCNM的浓度.仪器检测条件为:升温至50 ℃后保持5 min,然后以10 ℃/min的速度上升至140 ℃,再以20 ℃/min的速度上升至280 ℃;样品的进样量为1.0 μL,进样口温度为235 ℃,检测器温度为280 ℃,使用流速为1.0 mL/min的高纯度氮气作为载气[13]. 硝态氮的测定采用紫外分光光度法,具体方法参照HJ/T 346—2007[14]. Br-和Cl-的浓度通过装有分析柱(4 mm×250 mm)的离子色谱仪(ICS-1100,Thermo)进行测定.
1.5 标准曲线
标准曲线制作步骤:首先取定量的DBCNM标准物质溶入一定体积的甲基叔丁基醚中制作成质量浓度10 mg/L的标准储备液,在低温密封环境中保存;随后将标准储备液稀释制备成质量浓度分别为10、20、50、100、200、400和500 μg/L的一系列待测样品,然后各取1 mL待测样品进行GC/ECD检测.DBCNM的标准曲线如下:ADBCNM=200.72CDBCNM+1 828.64,R2= 0.999 1.其中,ADBCNM表示DBCNM在气相色谱中的出峰面积,Hz;CDBCNM表示DBCNM的质量浓度,μg/L.
1.6 毒性的计算
文献[7]采用LC50和50%TDNA分别量化DBPs化合物的细胞毒性效力和遗传毒性效力,HNMs的细胞毒性和遗传毒性见表1.反应溶液中HNMs的细胞毒性指数(CTI)和遗传毒性指数(GTI)反映水质的潜在健康风险,计算公式分别如下[7,11]:
(1)
(2)
式中,x为特定的HNMs种类;n为HNMs的种类数;Cx为每种HNMs的浓度;LC50为半致死浓度;50%TDNA为尾矩浓度-反应曲线的中点.

表1 HNMs的细胞毒性和遗传毒性[7]
2 结果与讨论
2.1 UV光强对DBCNM光降解的影响
为了探究UV光强对DBCNM光降解的影响,实验在DBCNM的初始质量浓度为200 μg/L、pH值为7、温度为(22±2)℃的条件下,分别考察DBCNM在黑暗和紫外光照(光强分别为9.1、15.5、22.6 mW/cm2)条件下的降解率.实验结果如图2所示,在黑暗条件下,DBCNM的降解缓慢,反应5 min后,DBCNM从初始质量浓度200 μg/L降至191 μg/L,降解率仅为4.5%;而在紫外光强分别为9.1、15.5、22.6 mW/cm2的条件下,反应5 min后,DBCNM从初始质量浓度200 μg/L分别降至61.6、49.32、29.2 μg/L,光降解率分别为 69.20%、78.10%、85.40%.由此可知,DBCNM的降解率随UV光强的增加而增加. 此外,根据下式计算可得,随着光照强度由9.1 mW/cm2逐渐增加至22.6 mW/cm2时,DBCNM的半衰期也由3.465 min提高到1.814 min:
(3)
式中,T1/2为DBCNM的半衰期;k为DBCNM的降解速率常数.

图2 光照强度对DBCNM光降解的影响


表2 DBCNM光降解反应动力学拟合方程
2.2 初始浓度对DBCNM光降解的影响
为了探究DBCNM的初始浓度对其光降解的影响,本实验在紫外光强度为15.5 mW/cm2、pH值为7、温度为(22±2)℃的条件下,考察了DBCNM在不同初始质量浓度(50、100、200、300 μg/L)下的光降解,实验结果如图3所示.随着反应时间的增加,DBCNM的浓度逐渐降低.当反应进行到5 min时,DBCNM的光降解率分别为90.90%、89.00%、78.10%、73.62%.由此可知,DBCNM的初始浓度越小,其光降解率便越高.主要有2个方面的原因:①初始浓度的增加会导致DBCNM吸收光子的竞争增强,即溶液中DBCNM分子数增多后,单位分子平均接受的光子量随之减少,能够被降解的机率也相应下降;②随着初始浓度的增加,DBCNM光解产生中间产物的浓度也会增加,中间产物与DBCNM竞争吸收光子导致DBCNM的光降解率下降[17].

图3 初始质量浓度对DBCNM光降解的影响
将图3中DBCNM的光降解数据进行一级反应动力学拟合(见表2).结果表明,DBCNM在光降解过程中的-ln(C/C0)与反应时间t之间成线性关系,符合一级反应动力学规律.
2.3 pH值对DBCNM光降解的影响
pH是饮用水处理中重要的控制参数之一.本实验在紫外光强度为15.5 mW/cm2、DBCNM初始质量浓度为200 μg/L、温度为(22±2)℃的条件下,考察了pH值(5、6、7、8和9)对DBCNM降解的影响.实验结果如图4所示,当pH值为5、6和7时,反应5 min后,DBCNM光降解率分别为54.0%、75.60%和78.10%;而当pH值为8和9时,反应2 min后已降解完全.由此可知,DBCNM的光降解受pH值的影响较大,碱性条件有利于DBCNM的光降解. Fang等[18]的研究表明:HNMs的光降解速率随摩尔吸光系数增大而增大,而摩尔吸光系数随pH值的增大而增大,高pH值有利于DBCNM吸收更多的光子能量. 因此,在碱性条件下DBCNM的光降解速率明显加快.
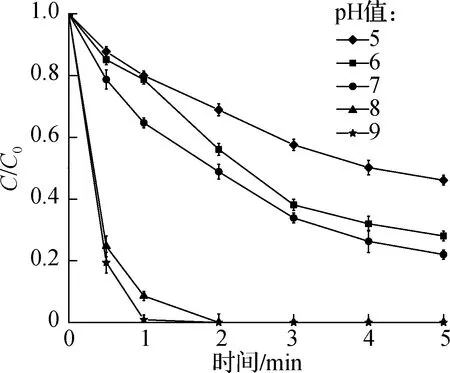
图4 pH值对DBCNM光降解的影响
2.4 自由氯浓度对DBCNM光降解的影响
自由氯在水处理中常被用来去除病毒、细菌等有害微生物,然而氯与UV联合处理时会产生 ·OH 和活性氯物种(RCS)等强氧化性基团[19],从而提升有机物降解的效率.为了探究自由氯对DBCNM光降解的影响,本实验在紫外光强度为15.5 mW/cm2、DBCNM初始质量浓度为200 μg/L、pH值为7、反应温度为(22±2) ℃的条件下进行.实验结果如图5所示,在不添加自由氯的情况下,反应5 min后,DBCNM光降解率为 78.10%;当向反应体系中分别添加质量浓度1.0和2.0 mg/L的自由氯时,反应5 min后,DBCNM的光降解率分别提高了7.47%和14.76%.由此可知,添加自由氯会促进DBCNM的光降解,且随自由氯的浓度增大,DBCNM的光降解率增大,其主要原因是UV与氯联合产生了·OH和RCS[19],促进了DBCNM的降解.
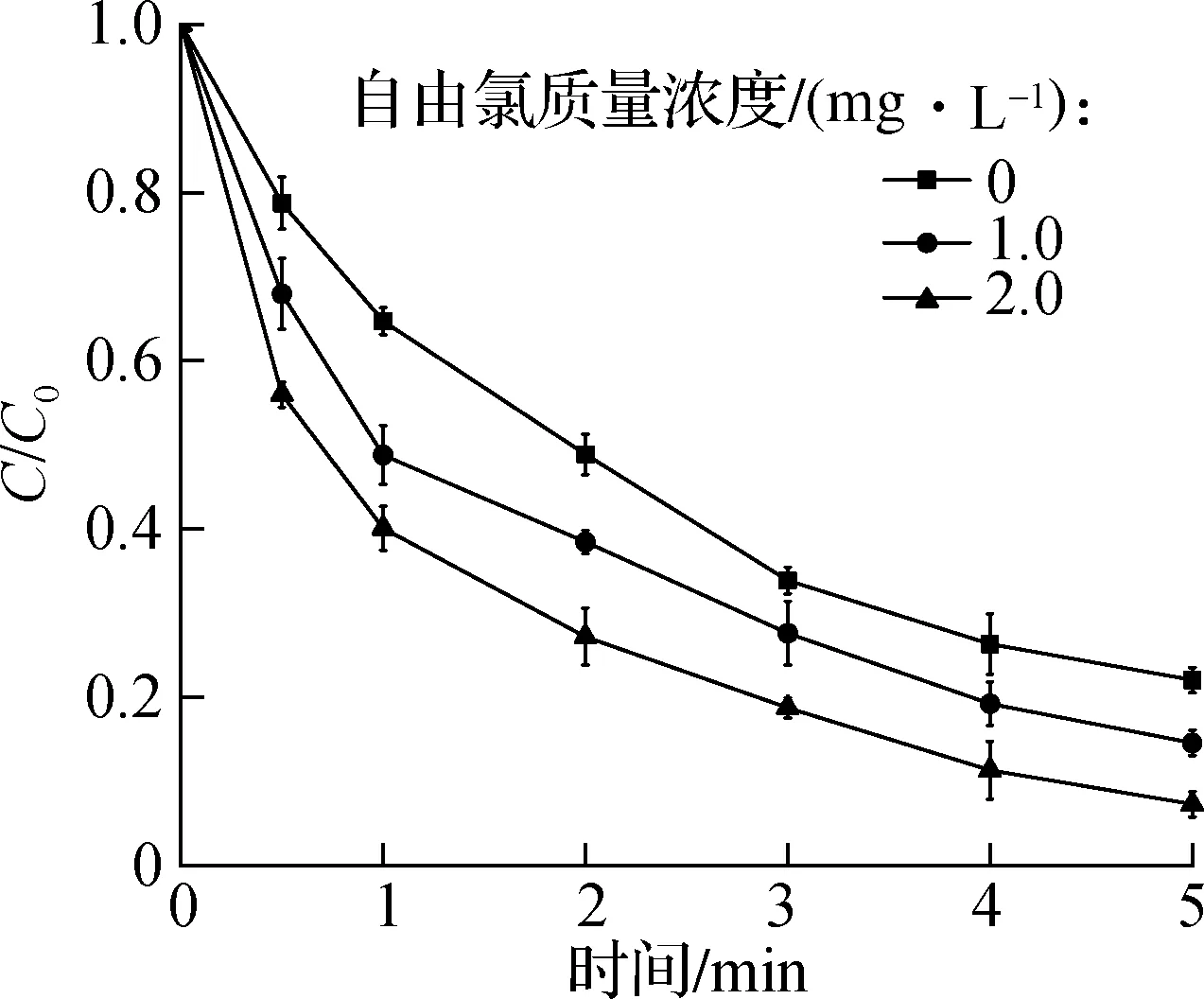
图5 自由氯浓度对DBCNM光降解的影响
此外,在DBCNM的光降解过程中产生了其他HNMs,其结果如图6所示.在不添加自由氯时, DBCNM在光降解的过程中仅检测到微量的CNM和BCNM,这是由于DBCNM发生了C—Br键断裂[20-21], 生成了BCNM和CNM;当添加质量浓度1.0 mg/L的自由氯时,反应2 min后,BDCNM的生成量增加至17.7 μg/L,随后开始下降,5 min后降至9.1 μg/L,呈现先增加后减少的趋势,同时在反应溶液中检测到BNM、BCNM和CNM;当添加质量浓度2.0 mg/L的自由氯时,BDCNM、BNM、BCNM和CNM的生成规律与添加质量浓度1.0 mg/L自由氯的生成规律基本类似,但生成量有所增加.由此可知,在光降解的过程中,DBCNM 转化为其他HNMs的趋势随自由氯浓度的增加而愈发显著.其原因是反应溶液中自由氯在紫外光照下产生更多的·OH和RCS 等活性自由基[13],能进一步氧化DBCNM,尤其是RCS 的参与促使DBCNM分子上的Br或H被Cl取代,更容易转化成其他HNMs.因此,自由氯浓度越大,转化为其他种类的HNMs的生成量也随之增加,并呈现由溴代硝基甲烷(Br-HNMs)逐渐向氯代硝基甲烷(Cl-HNMs)转化的趋势.

(a) 不添加自由氯
为了进一步研究自由氯对DBCNM光降解过程中细胞毒性指数和遗传毒性指数的影响,根据表1中各HNMs细胞毒性及遗传毒性数据计算图6中DBCNM在光降解过程中各个时间点的细胞毒性指数和遗传毒性指数的变化,结果如表3所示. 反应体系中添加质量浓度1.0 mg/L自由氯与未添加自由氯相比,形成HNMs的细胞毒性略有增加,遗传毒性显著增加;添加质量浓度2.0 mg/L自由氯与添加质量浓度1.0 mg/L自由氯相比,形成HNMs的细胞毒性有所减少,遗传毒性没有明显变化.总体而言,添加自由氯会导致反应体系中细胞毒性和遗传毒性发生改变,但不随自由氯浓度增加而增加.因为反应体系中加入一定浓度的自由氯,在紫外光照下会产生·OH和RCS攻击DBCNM,导致其他HNMs的生成增加;同时,自由氯浓度的升高也加快了HNMs的降解,这种拮抗作用致使自由氯浓度对HNMs细胞毒性和遗传毒性的影响变得更加复杂[22].通常而言,HNMs的细胞毒性由高到低依次为Br-HNMs、Br(Cl)-HNMs、Cl-HNMs,遗传毒性由多卤代HNMs向单卤代HNMs逐渐降低[11].通过表3可以发现,在添加自由氯的DBCNM光降解过程中,形成其他HNMs的细胞毒性以BNM和BDCNM的贡献为主,遗传毒性以BNM、BDCNM和BCNM的贡献为主.
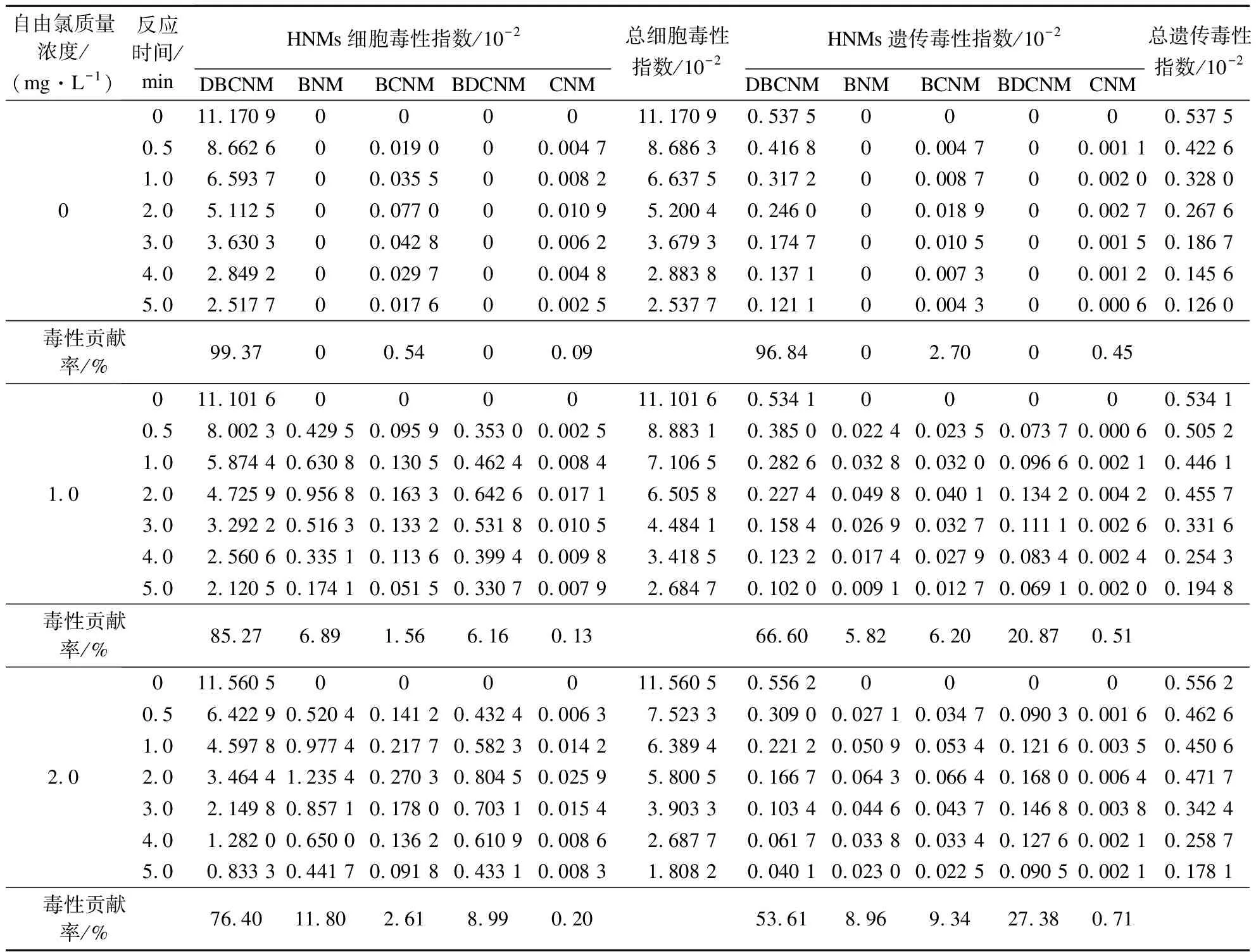
表3 自由氯对DBCNM光降解过程中毒性变化的影响
2.5 溴离子对DBCNM光降解的影响

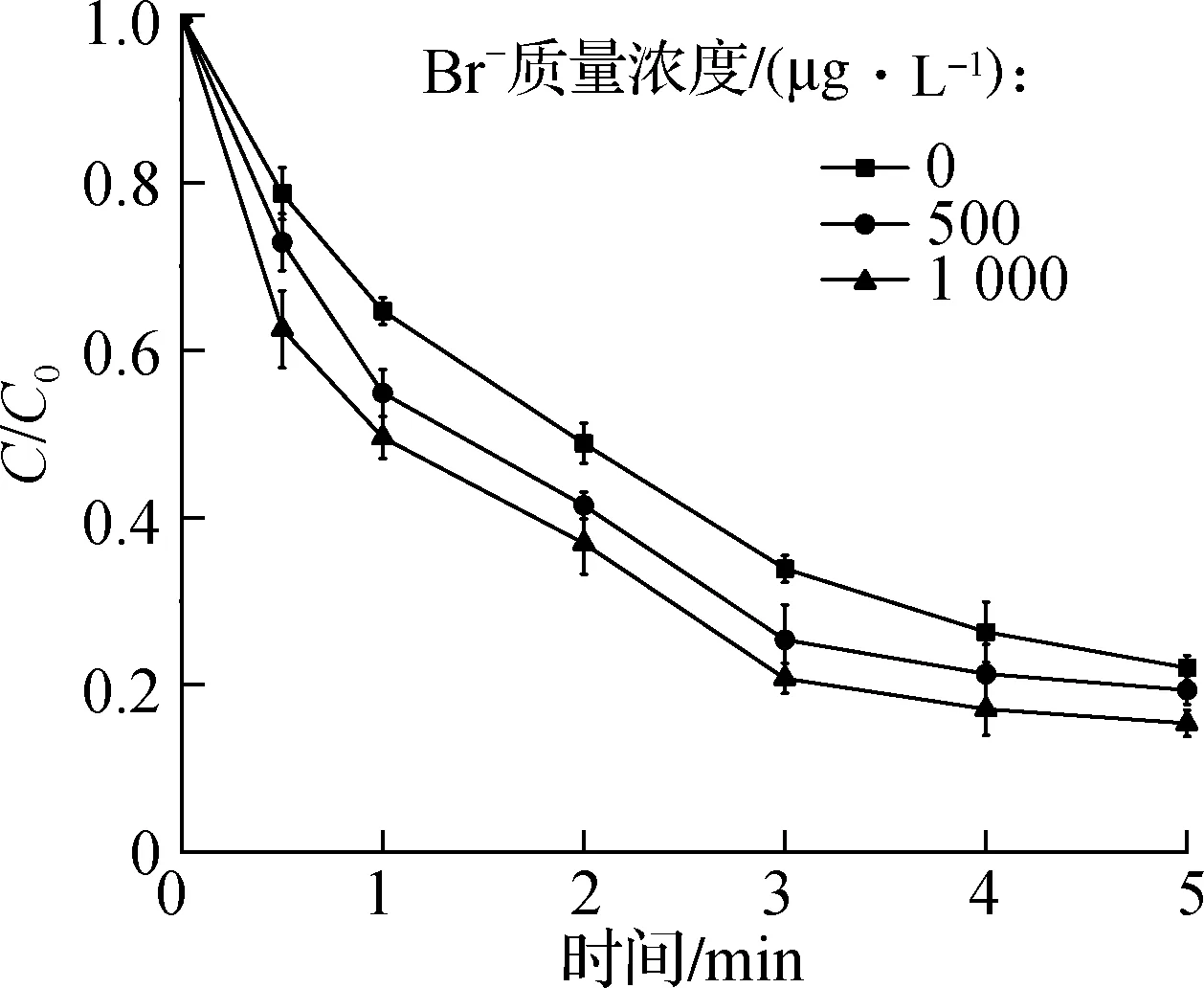
图7 溴离子浓度对DBCNM光降解的影响
当反应溶液中添加溴离子后,DBCNM在光降解过程中转化为其他种类HNMs,如图8所示.当添加质量浓度500 μg/L的溴离子时,在DBCNM的光降解过程中检测到BNM、CNM和BCNM的生成.与不添加溴离子的情况相比,CNM、BNM的最大生成量分别从5.49、0 μg/L增加至11.15、1.96 μg/L,BCNM的最大生成量由5.44 μg/L减少至4.59 μg/L.当反应溶液中添加质量浓度 1 000 μg/L的溴离子时,BNM、BCNM和CNM的形成规律与添加质量浓度500 μg/L溴离子的情况类似,但生成量增加.整体而言,溴离子浓度的增加加速了DBCNM的光降解,同时也有利于DBCNM向其他种类HNMs的转化,尤其是单卤代HNMs (CNM、BNM).其主要原因是RBS的参与促进了DBCNM分子上C—Br键和C—Cl键的断裂,导致DBCNM 降解为低溴代的HNMs,并呈现由多Br-HNMs逐渐向单Br-HNMs转化的趋势.
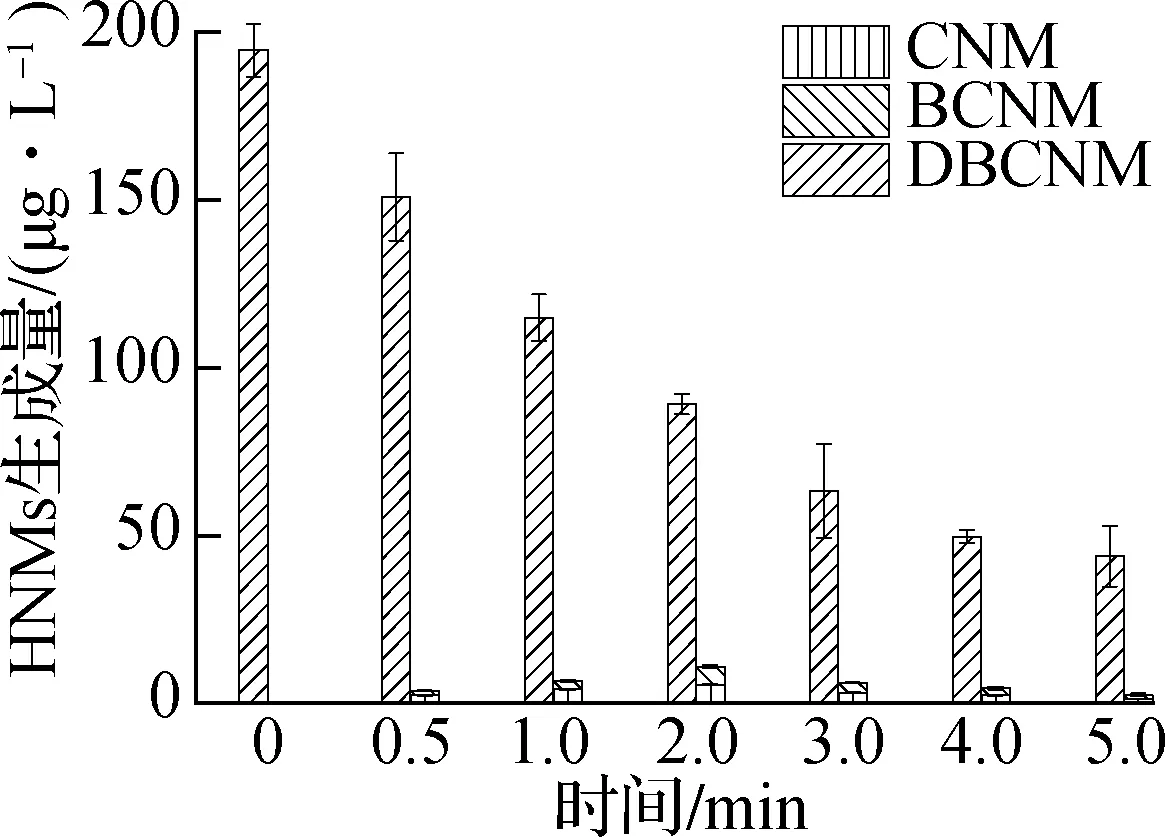
(a) 不添加Br
2.6 DBCNM的光降解反应路径


图9 DBCNM的光降解路径

图10 DBCNM光降解过程中的离子浓度变化
3 结论
1)DBCNM在黑暗条件下几乎不降解,在紫外光照为15.5 mW/cm2时能够快速降解并符合一级反应动力学规律,其降解速率常数为0.303 9 min-1,且DBCNM的光降解率随光照强度的增加而增大.
2)DBCNM的光降解率随初始质量浓度的增加而下降,随pH值的增加而上升,DBCNM的光降解速率在碱性条件下显著加快.
3)自由氯和溴离子的添加加快了DBCNM的光降解,并促使DBCNM转化为其他HNMs.随着自由氯和溴离子浓度的增加,转化为其他的HNMs越多,并分别呈现由Br-HNMs向Cl-HNMs转化、多Br-HNMs向单Br-HNMs转化的趋势.在添加自由氯的DBCNM光降解过程中,形成其他HNMs的细胞毒性以BNM和BDCNM的贡献为主,遗传毒性以BDCNM、BCNM和BNM的贡献为主.


