纳米Fe3O4/皂石复合材料的制备及去除2,4-二氯苯酚的性能研究
吴丽梅,刘 垄,王晓龙,唐 宁,王 晴
(1.沈阳建筑大学材料科学与工程学院,沈阳 110168;2.沈阳建筑大学机械工程学院,沈阳 110168)
0 引 言
氯酚类(CPs)有机物是一种结构稳定且难以降解的污染物[1-2],其污染面广且毒性较大,容易对环境和人类造成严重危害[3]。如何处理环境中的氯酚类污染物,已经成为当前的研究热点[4-5]。2,4-二氯苯酚(2,4-DCP)是一种常见的氯酚类有机化合物,常用于医学、农药、石油化工等领域,使用后的2,4-DCP通常被直接丢弃或倒入水流域中,给水环境带来了巨大的危害[6]。目前去除2,4-DCP的技术包括生物[7]、物理[8]和化学[9-10]方法。生物法是指利用生物自身独特的结构特点和物质组成来去除水中2,4-DCP,该方法存在去除量小、效率低及操作难度较大等缺点[11];物理法则是利用吸附剂大的表面积和孔结构吸附2,4-DCP,但该方法不能解决污染物本身带来的危害[12];化学法主要是通过化学反应改变2,4-DCP的分子结构和组成从而去除2,4-DCP,然而部分催化剂的催化能力不足,污染物不能完全被去除[13]。近年来,研究者们利用吸附-氧化还原法提升了2,4-DCP的去除效率。其中,纳米Fe3O4是一种含有Fe2+和Fe3+的磁性材料,具有较大的比表面积和较强的表面电子转移特性,且通过磁选法可以很容易地从溶液中分离出来,目前已被广泛应用于无机和有机污染物降解等领域[14-15]。
目前,通过共沉淀法合成的纳米Fe3O4颗粒尺寸不均匀且易发生团聚,降低了颗粒表面活性,导致其对污染物降解效率较低。在Fe3O4纳米颗粒表面形成包裹层或制备纳米Fe3O4复合材料是解决团聚问题的有效方法[16-18]。蒙脱石、累托石和皂石等矿物材料作为催化剂的良好载体,具有成本低、环保和高效的特点;另外,矿物材料还具有大的比表面积、表面电荷和稳定性好等优点,可通过吸附、催化、沉淀和氧化还原等过程将污染物固定,阻断其迁移,从而降低污染物的污染性[19-20]。目前,研究者利用天然蒙脱石和累托石等矿物材料优异的表-界面性质改善纳米Fe3O4团聚问题[21-22]。然而,天然矿物材料成分复杂,难以提纯,在一定程度上限制了Fe3O4/矿物复合材料对污染物的去除。人工合成的矿物材料不仅能保留天然矿物材料主要的组成成分及结构特点,还可以得到纯度较高且化学性质稳定的矿物材料。水热合成法不仅操作简单,还可以较容易地模拟矿物材料的形成过程[23]。对此,国内外研究学者不断探索人工合成矿物材料。其中,皂石是一种可利用水热法合成的矿物材料,因其实验装置相对简单,操作容易控制,受到研究者们的关注[24]。
皂石是一种2 ∶1型的层状硅酸盐矿物[25],具有纯度高、结晶性好、结构可调和表-界面性质可控等特性[26],被广泛应用于能源再生、环境治理等领域[27-28]。Nikolopoulou等[29]将TiO2负载到皂石表面,得到了TiO2颗粒分散均匀、高比表面积和高催化活性的TiO2/皂石复合材料。Kameshima等[30]通过对皂石表-界面性质的调控,得到了具有更高活性和稳定性的ZrO2/皂石复合材料。说明皂石作为载体材料与金属氧化物之间可产生协同效果,在水处理领域有广泛的应用潜力。
以合成皂石为基体,在其表面原位合成纳米Fe3O4,有效改善了纳米Fe3O4易团聚等缺陷。Fe3O4颗粒在皂石表面分散较均匀,暴露出了更多的活性位点,有利于2,4-DCP的降解。本研究对Fe3O4/矿物基复合材料的制备和应用具有重要意义。
1 实 验
1.1 材 料
九水硅酸钠(Na2SiO3·9H2O)、碳酸氢钠(NaHCO3)和七水硫酸亚铁(FeSO4·7H2O)购自天津市北辰方正试剂厂,六水氯化镁(MgCl2·6H2O)购自天津市瑞金特化学品有限公司,六水氯化铝(AlCl3·6H2O)购自天津市大茂化学试剂厂,硫酸铁(Fe2(SO4)3·nH2O,n=6~9)购自国药集团化学试剂有限公司,氢氧化钠(NaOH)购自天津市奥普升化工有限公司。以上试剂均为分析纯。
1.2 皂石的制备方法
将8.00 g NaHCO3、16.40 g NaOH和4.80 g Na2SiO3溶于250 mL蒸馏水中,完全溶解后制得溶液A,将0.74 g AlCl3和3.04 g MgCl2加入到25 mL蒸馏水中充分搅拌制得溶液B,将溶液B缓慢加入到溶液A中,得到溶液C(nSi∶nAl∶nMg=3.38 ∶0.62 ∶3.00)。将得到的溶液C倒入反应釜(容积为150 mL、材质为PPL)并置于烘箱中,在200 ℃下反应24 h,待反应结束后冷却至室温,将反应后的溶液放入离心管中,在6 000 r/min的转速下离心10 min,反复离心洗涤5次,最后将洗涤后的产物置于冷冻干燥机,干燥12 h,获得皂石[24]。
1.3 纳米Fe3O4/皂石复合材料的制备方法
磁性纳米Fe3O4是采用Fe2(SO4)3·nH2O(n=6~9)和FeSO4·7H2O与NaOH共沉淀法合成[31]。将2.78 g Fe2(SO4)3·nH2O(n=6~9)和7.99 g FeSO4·7H2O分别溶于200 mL和60 mL水中,完全溶解后混合到一起充分搅拌,并加入2.50 g皂石继续搅拌,用1 mol/L NaOH溶液调节pH值至9~10,并在室温下静置至纳米Fe3O4/皂石完全沉淀。用V(蒸馏水) ∶V(乙醇)=1 ∶1的溶液洗涤沉淀物,真空干燥,获得纳米Fe3O4/皂石复合材料。
1.4 表征方法
采用X射线衍射仪(型号为Shimadzu 6000),利用在30 mA和40 kV下产生的Cu-Kα辐射测定样品结构;使用傅里叶变换红外光谱仪(FTIR,型号为Thermo Scientific Nicolet iS5)以透射模式测定样品表面官能团;采用扫描电子显微镜(SEM,型号为Zeiss Sigma 300)在10 kV加速电压下,以捕获材料表面形貌;采用透射电子显微镜(TEM,型号为JEOL JEM-2100)在200 kV的加速电压下表征样品微观形貌;采用X射线荧光光谱(XRF,型号为S2 RANGER)对皂石和纳米Fe3O4/皂石复合材料表面元素类型及含量进行分析;使用液相色谱-质谱联用仪(LC-MS,型号为安捷伦1290II-6460)对2,4-DCP降解产物进行定性分析;采用紫外可见分光光度计(UV754N)测定溶液吸光度值。
1.5 纳米Fe3O4/皂石复合材料去除2,4-DCP的试验方法
将1.0 g 2,4-DCP溶解于1.0 L蒸馏水中,作为贮备液。分别称取纳米Fe3O4/皂石复合材料、Fe3O4和皂石各0.1 g并加入到100 mL 2,4-DCP溶液中进行对比试验。2,4-DCP质量浓度分别为25 mg/L、50 mg/L、100 mg/L、200 mg/L、300 mg/L、400 mg/L、500 mg/L、800 mg/L、1 000 mg/L和1 200 mg/L,在298 K下充分混合搅拌,探讨溶液浓度对2,4-DCP去除效果的影响规律。取0.1 g Fe3O4/皂石加入到浓度为500 mg/L的2,4-DCP溶液中,探讨反应时间和溶液pH值对复合材料去除2,4-DCP效果的影响。采用紫外可见分光光度计测量溶液在286 nm处的吸光度,并根据吸光度和浓度之间的线性关系,分析纳米Fe3O4/皂石复合材料对溶液中2,4-DCP的去除效果。
使用紫外分光光度计,利用吸光度值换算出溶液中污染物的质量浓度。材料对污染物的去除量可由式(1)计算得出:
(1)
式中:C0表示溶液的初始质量浓度,mg/L;Ce表示污染物在溶液中平衡时的质量浓度,mg/L;qe表示材料去除量,mg/g;V表示溶液体积,mL;m是加入的材料质量,g。
2 结果与讨论
2.1 材料表征
2.1.1 纳米Fe3O4/皂石复合材料的结构特征
图1为Fe3O4、皂石和纳米Fe3O4/皂石复合材料的XRD谱。由图1可知,Fe3O4的特征衍射峰分别出现在2θ=18.5°、30.2°、35.5°、43.1°、53.8°、57.0°和62.7°处,分别对应其(111)、(220)、(311)、(400)、(422)、(511)和(440)晶面,与标准卡片(JCPDS No.19-0629)一致[1]。Fe3O4的特征衍射峰峰形尖锐且未检测到其他杂质相,表明所制备的Fe3O4具有较高的结晶度和纯度。合成皂石的特征衍射峰出现在2θ=7.1°、19.5°、28.9°、35.0°、52.8°和60.3°处,分别对应其(001)、(110)、(005)、(130)、(150)和(060)晶面[32]。Fe3O4/皂石的XRD谱是由皂石和Fe3O4的特征衍射峰组成,未发现其他杂质。同时,在皂石表面合成纳米Fe3O4的过程中并没有破坏两种材料的晶体结构,获得了纯度高且结晶性好的纳米Fe3O4/皂石复合材料。
图2为Fe3O4、皂石和纳米Fe3O4/皂石复合材料的FTIR谱。由图2可知,三种材料中3 423 cm-1、2 345 cm-1和1 637 cm-1处谱带可归因于水分子的振动,994 cm-1和458 cm-1处谱带归因于Si—O拉伸振动,651 cm-1处是由Mg—OH基团的弯曲振动引起的[33]。816 cm-1处是由Si—O—Al的振动引起的,这归因于皂石中硅氧四面体的Si部分被Al置换。Fe3O4谱中582 cm-1处的峰归因于Fe—O的拉伸振动[34]。然而纳米Fe3O4/皂石复合材料中994 cm-1处的Si—O振动强度降低以及峰形变宽,表明Fe3O4的合成过程中皂石表面的Si—O与Fe3O4存在相互作用。582 cm-1和458 cm-1处的谱带消失可能是Fe3O4中Fe—O结合到皂石表面导致的。因此,Fe3O4可能在合成过程中结合到皂石的表面,这与图1的XRD结果相符。
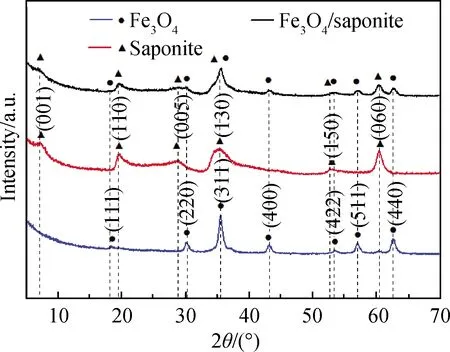
图1 Fe3O4、皂石和纳米Fe3O4/皂石复合材料的XRD谱Fig.1 XRD patterns of Fe3O4, saponite and nano-Fe3O4/saponite composites

图2 Fe3O4、皂石和纳米Fe3O4/皂石复合材料的FTIR谱Fig.2 FTIR spectra of Fe3O4, saponite and nano-Fe3O4/saponite composites
2.1.2 纳米Fe3O4/皂石复合材料的微观形貌及元素组成
图3为Fe3O4、皂石和纳米Fe3O4/皂石复合材料的SEM和TEM照片。由图3可知,纳米Fe3O4颗粒尺寸在10~20 nm,并且发生了明显的团聚(见图3(a)),这是因为纳米Fe3O4颗粒粒径小,比表面积大,易发生团聚。皂石边缘部分显示出了明显的层状结构(见图3(b))。从复合材料中可以看出纳米Fe3O4颗粒负载到层状结构的皂石表面,且表面较粗糙,这是由纳米Fe3O4颗粒负载到皂石表面引起的,并且Fe3O4和皂石结合过程中并没有破坏皂石的层状结构(见图3(c))。采用TEM表征了纳米Fe3O4/皂石复合材料的微观形貌。皂石表面Fe3O4的尺寸在10 nm左右(见图3(d)),与图3(a)相比,复合材料表面的Fe3O4颗粒较均匀地分散于皂石表面,在一定程度上改善了Fe3O4的团聚问题。综上,复合材料的形成能够有效改善纳米Fe3O4的团聚问题,为Fe3O4晶体生长提供适宜的环境。

图3 Fe3O4、皂石、纳米Fe3O4/皂石复合材料的SEM照片和纳米Fe3O4/皂石复合材料的TEM照片Fig.3 SEM images of Fe3O4, saponite, nano-Fe3O4/saponite composites and TEM image of nano-Fe3O4/saponite composites
使用X射线荧光光谱分析皂石和纳米Fe3O4/皂石复合材料的元素类型及含量(见表1)。皂石中主要含有Al、Na、Mg和Si元素,其中Si元素含量最多。Al的存在是因为部分硅氧四面体中的Si被Al所置换,Mg元素构成了皂石镁氧八面体,Na元素则是以阳离子的形式存在于皂石层间。纳米Fe3O4/皂石复合材料中含有大量Fe元素且没有检测到其他元素,表明复合材料中存在大量的Fe3O4,且没有其他杂质,这与XRD的结果相吻合。

表1 皂石和纳米Fe3O4/皂石复合材料的XRF分析Table 1 XRF analysis of saponite and nano-Fe3O4/saponite composites
2.2 纳米Fe3O4/皂石复合材料对2,4-DCP去除效果的影响因素
2.2.1 溶液质量浓度
溶液质量浓度对2,4-DCP去除效果的影响规律如图4所示。首先,取0.1 g纳米Fe3O4/皂石复合材料、0.1 g Fe3O4和0.1 g皂石分别加入到100 mL pH值为6的2,4-DCP溶液中反应10 min。研究结果表明:随着2,4-DCP溶液浓度增大,纳米Fe3O4/皂石复合材料对2,4-DCP的去除量逐渐增大;在2,4-DCP溶液浓度为300 mg/L时,纳米Fe3O4/皂石对2,4-DCP的去除量为90.41 mg/g,而2,4-DCP溶液浓度为1000 mg/L时的去除量为178.46 mg/g,比300 mg/L时增大了近一倍;再增大2,4-DCP溶液浓度时,Fe3O4/皂石对2,4-DCP的去除效果不变,已达到饱和。纳米Fe3O4和皂石相比于纳米Fe3O4/皂石复合材料,在不同浓度下对2,4-DCP的去除量均低于纳米Fe3O4/皂石复合材料。Fe3O4和皂石在溶液浓度为1 000 mg/L时对2,4-DCP的去除量分别为73.63 mg/g和102.49 mg/g,并达到饱和。皂石相比于Fe3O4有着更高的去除效果,这可能归因于通过单一共沉淀法制备的Fe3O4易发生团聚,在去除2,4-DCP的过程中Fe2+的活性未能完全表现出来。总之,纳米Fe3O4/皂石复合材料有效提高了Fe3O4和皂石对2,4-DCP的去除能力。
2.2.2 反应时间
反应时间对2,4-DCP去除效果的影响规律如图5所示。取0.1 g Fe3O4/皂石复合材料加入到500 mg/L pH值为6的2,4-DCP溶液中,观察反应时间对2,4-DCP去除效果的影响。研究结果表明:随着反应时间的增长,Fe3O4/皂石复合材料对溶液中2,4-DCP的去除量逐渐增大,在1 min内对2,4-DCP的去除量已经达到71.93 mg/g,基本占整个去除量的60%,这可能归因于复合材料表面的初始吸附和反应活性位点数量较多,加快了对2,4-DCP的吸附和降解速率;2~4 min时,2,4-DCP的去除速率变得缓慢,并且在5 min后开始饱和,最大去除量为118.00 mg/g。

图4 溶液质量浓度对2,4-DCP去除效果的影响Fig.4 Effect of solution mass concentration on 2,4-DCP removal efficiency

图5 反应时间对2,4-DCP去除效果的影响Fig.5 Effect of reaction time on 2,4-DCP removal efficiency

图6 溶液pH值对2,4-DCP去除效果的影响Fig.6 Effect of solution pH value on 2,4-DCP removal efficiency
2.2.3 溶液pH值
溶液pH值对2,4-DCP去除效果的影响规律如图6所示。取0.1 g纳米Fe3O4/皂石复合材料加入到500 mg/L的2,4-DCP溶液中,通过NaOH和HCl调节溶液的pH值,反应10 min后观察溶液pH值对2,4-DCP去除效果的影响。在酸性条件(pH<7)下,纳米Fe3O4/皂石复合材料对2,4-DCP的去除效果较好,溶液pH值在2和4时,去除量分别为91.06 mg/g和107.41 mg/g。这可能归因于酸性条件能够促进复合材料表面发生电子转移,避免了Fe2+和Fe3+发生沉淀,保证复合材料表面有足够的Fe2+参加反应,有利于2,4-DCP的去除。随着pH值不断降低,复合材料对2,4-DCP的去除量略有降低,这可能归因于强酸环境破坏了纳米Fe3O4/皂石复合材料的结构,不利于2,4-DCP去除。然而,在pH≥10时,纳米Fe3O4/皂石复合材料对2,4-DCP的去除量几乎为零。这可能归因于在碱性条件下,体系中Fe2+易发生水解反应形成沉淀,在表面形成覆盖层阻碍反应进行,从而抑制了对2,4-DCP的去除效率。在中性条件(pH=7)下,纳米Fe3O4/皂石复合材料对2,4-DCP的去除量为108.78 mg/g。由此可见,在弱酸条件下,有利于纳米Fe3O4/皂石复合材料对2,4-DCP的去除,而在弱碱条件下降低了对2,4-DCP的去除效率,当溶液pH值为6时,最大去除量为119.38 mg/g。
2.3 动力学研究
为了分析纳米Fe3O4/皂石复合材料的吸附机制,使用准一级和准二级模型对纳米Fe3O4/皂石复合材料吸附浓度为500 mg/L的2,4-DCP进行了表征测定。
准一级动力学模型通常用来描述固/液体系间初始阶段的动力学吸附过程[35],准一级速率表达式如下:
log(q1-qt)=logq1-k1t
(2)
基于吸附质在吸附剂上化学吸附假设的准二级动力学模型涉及通过共享或电子交换作用的化合价力[36],该模型如下:
(3)
其中:qt是t时刻纳米Fe3O4/皂石复合材料吸附的污染物量,mg·g-1;k1和k2是反应速率常数,单位分别为min-1、g·mg-1·min-1;q1和q2分别是准一级和准二级吸附的最大吸附容量,mg·g-1。对于准一级动力学,k1可以由斜率确定;对于准二级动力学,k2可以由直线的截距确定。计算结果的所有参数列于表2中。

表2 动力学模型参数Table 2 Kinetic model parameters
使用准一级和准二级动力学模型对2,4-DCP(见图7(a)、(b))的吸附情况进行了拟合。由表2可知,纳米Fe3O4/皂石复合材料吸附2,4-DCP的准一级和准二级R2值分别为0.946 22和0.993 97,表明准二级动力学模型更适于描述纳米Fe3O4/皂石复合材料对2,4-DCP的吸附,其平衡处的最大吸附量为126.262 6 mg·g-1,反应速率常数k2=0.014 79 g·mg-1·min-1。准二级动力学模型说明Fe3O4/皂石对水中2,4-DCP的去除过程涉及表面吸附和化学反应机理。
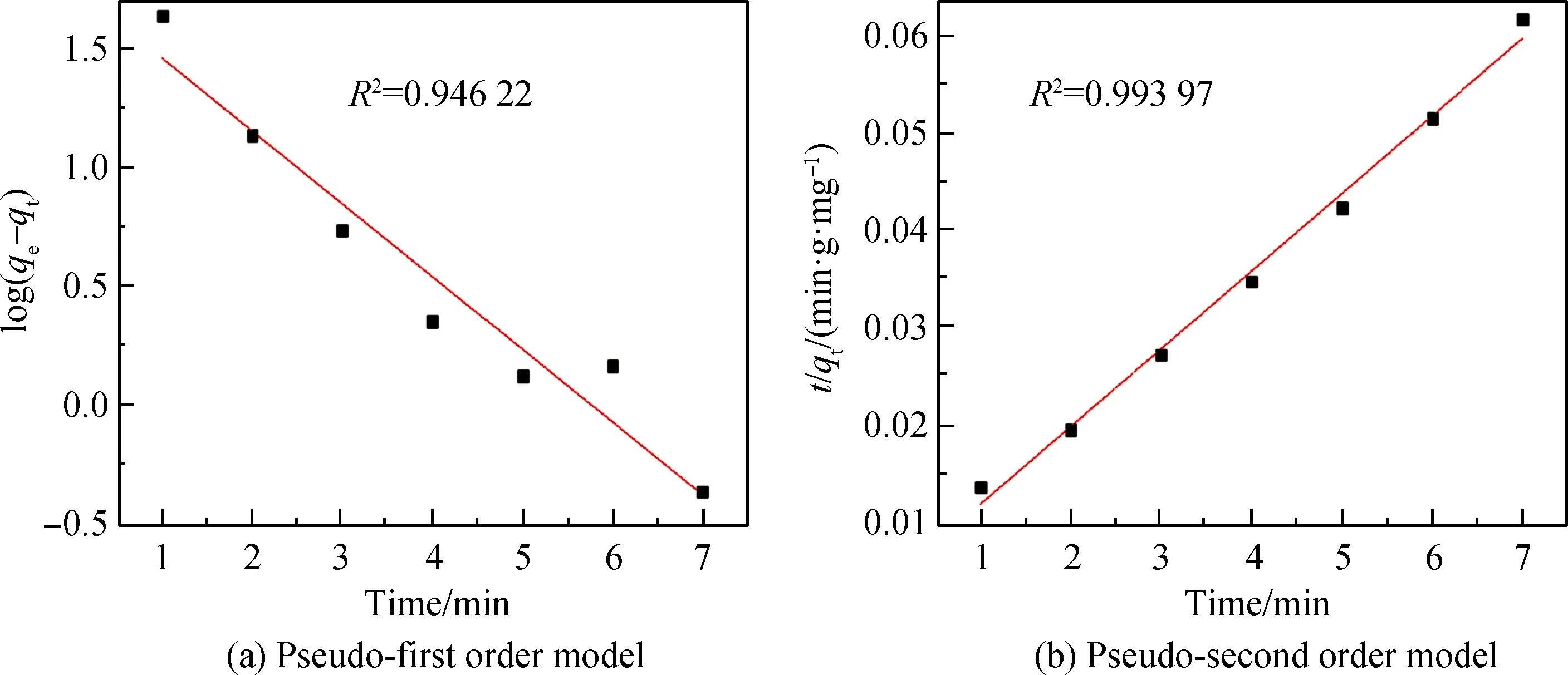
图7 纳米Fe3O4/皂石复合材料去除2,4-DCP的动力学模型拟合Fig.7 Kinetic model fitting for 2,4-DCP removal by nano-Fe3O4/saponite composites
2.4 去除机理及降解产物分析
根据2.3节的动力学分析,Fe3O4/皂石对2,4-DCP的去除是吸附和还原共同作用的结果。溶液中的2,4-DCP一部分被吸附到Fe3O4/皂石表面(见式4),另一部分被吸附到Fe3O4的活性位点上,Fe3O4在水溶液中被腐蚀析出大量的Fe2+参与反应(见式5),进而使2,4-DCP被还原降解,发生脱氯反应,生成氯酚等中间产物(见式6)。
对上述复合材料的表征、试验结果和机理进行探讨,并通过LC-MS进一步分析了纳米Fe3O4/皂石吸附降解2,4-DCP前后的产物(见图8(a)、(b))。图8中m表示质量数,z表示电荷数,m/z表示相对分子质量。降解前,在分子量为161~163处有较大峰值,2,4-DCP分子量占80%以上。经吸附降解后,分子量为161~163的峰值降为0,而在112、127和129处出现了新的峰值,计算表明此处对应氯酚等物质[37]。以上结果说明,2,4-DCP经过Fe3O4/皂石吸附降解后,脱氯得到了氯酚等中间产物,由大分子量转变为小分子量,因此在Fe3O4/皂石对2,4-DCP的去除过程中,同时存在着吸附和降解作用。
2,4-DCP+Fe3O4/saponite→2,4-DCP/Fe3O4/saponite(吸附到复合材料表面)
(4)
Fe3O4+H+→Fe2+/Fe3++H2O
(5)
Fe2++2,4-DCP+H+→Fe3++2-CP/4-CP+middle product
(6)
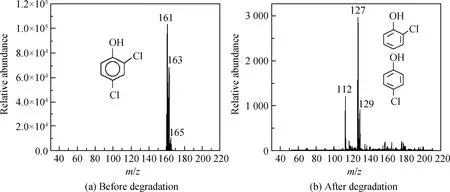
图8 2,4-DCP降解前后的LC-MS图谱Fig.8 LC-MS spectra of 2,4-DCP before and after degradation
3 结 论
(1)采用水热合成法和共沉淀法制备了纯度高且结晶性好的纳米Fe3O4/皂石复合材料,Fe3O4颗粒较均匀地分散在皂石表面,使复合材料的活性位点增加,有助于提升对2,4-DCP的去除效果。
(2)纳米Fe3O4/皂石复合材料改善了Fe3O4和皂石对2,4-DCP的去除效果,纳米Fe3O4/皂石复合材料在溶液pH值为6时,对2,4-DCP的最大去除量为178.46 mg/g;反应时间和溶液pH值对去除效果有重要影响,弱酸性条件下更有利于去除2,4-DCP,Fe3O4/皂石在5 min时对2,4-DCP的去除量达到饱和。
(3)纳米Fe3O4/皂石复合材料对2,4-DCP的去除过程更符合准二级动力学模型,去除过程主要包括吸附和降解两个过程;降解过程中Fe2+的还原性使2,4-DCP发生了脱氯反应,生成了氯酚等中间产物。

