纤维素/木质素共热解过程中的气相反应
杨华美,蒋菊,刘望,张秉哲,徐盼盼
(徐州工程学院 材料与化学工程学院,江苏 徐州 221018)
热解技术是生物质能转化制备高值燃料和高值化学品最成熟有效的应用技术,是生物质气化发电技术的重要环节[1-3].在生物质热解过程中不可避免的3个步骤如下:1)生物质固体结构被破坏,发生初次热解,产生可挥发性物质;2)可挥发性物质从固体颗粒中逸出,发生气固反应;3)可挥发性物质继续裂解、碰撞和重组,发生气相反应[2,4-5].由于纤维素和半纤维素同木质素结构上的不同[6],导致两者热解行为的明显差异:前者热解残渣率低,热失重温度区域较窄(300~380 ℃),主要以糖、呋喃、醛等为主要热解产物;后者热解残渣率高,热失重温度区域宽,在140~540 ℃,主要以酚、芳烃为主要热解产物[4,7-10].在实际应用中,生物质往往作为一个整体进行热解转化,各组分间的相互作用决定着生物质整体热解过程和产物分布的复杂性,影响了生物质转化应用的经济性和技术可控性.
为了研究生物质各组成成分单独热解及共热解时相互作用的内在机理,研究者采用热重分析仪(TGA)及其红外联用技术(TGA-FTIR)、居里点裂解器、管式炉裂解装置等对生物质各组成成分共热解特性和产物分布情况开展了相关研究[4,6-9,11-12].本课题组前期利用热重分析仪和居里点裂解-气相质谱研究了纤维素和木质素共热解过程中的相互作用及热解产物分布情况.结果表明:纤维素与木质素共热解过程中存在明显的相互作用,与热解温度和混合比例具有一定相关性[9].但由于居里点裂解反应器反应时间较短,产物进行气相反应的程度低,CO、CO2和短链烃(C1—C5脂肪烃)等产物产率较低,不利于研究纤维素与木质素共热解在气相反应过程中的相互作用.然而,短链烃(C1—C5脂肪烃)是纤维素、木质素热解的重要(中间)产物[13-15],其形成分布对研究生物质热解过程和机理具有重要指导意义.因此,本论文采用两段裂解反应器进行纤维素与木质素共热解实验,将气相反应与初次热解、气固反应尽可能分开;并利用在线气相色谱仪对热解产物(特别是轻质组分)进行定量分析,通过实验结果与理论计算结果的对比研究,探讨生物质热解过程中纤维素和木质素之间的相互作用及对产物分布的影响情况.
1 实验部分
1.1 样品与设备
实验样品:酶解木质素(lignin,质量分数96%)、纤维素(cellulose)购自aladdin,CAS:9004-34-6.纤维素和木质素混合样品质量比设定为3∶7、5∶5和7∶3,并命名为C3L7、C5L5和C7L3.
实验设备:两段裂解反应器进行样品热解;热解气相产物利用在线气相色谱仪(岛津2014-FID/TCD和岛津2010-FID)进行定量检测.
1.2 两段裂解反应器-在线气相分析
利用如图1所示的实验装置在241 kPa、750 ℃下,对木质素、纤维素和不同比例混合样品(C3L7、C5L5和C7L3)进行快速热解实验.两段裂解反应器(TSTR)由加热炉和石英管构成;石英管中塞入石英棉,分成2个等温区域:第1区域用于样品的热解,热解后残渣被截留在第1区域,而可挥发性物质随载气进入第2加热区;可挥发性物质在第2加热区继续进行气相反应.由于可挥发性气相产物与热解残渣进行了及时分离,因此,该实验装置能够在尽可能避免气固反应的情况下,研究纤维素和木质素共热解时的气相反应和产物分布情况.实验步骤如下:取1 mg样品用石英砂包裹,并用铁丝和磁石固定在第1加热区上方,该区域温度在100 ℃以下,不会引起样品的分解;按照图1连接实验装置,调节第2加热区在加热炉内的长度使气相反应时间为0.5 s;以氦气(He)作为载气通过热解反应器内的石英管,排出石英管内空气.将TSTR加热至预期温度(750 ℃),待气相色谱仪(GC)基线稳定后,旋转六通阀,连接TSTR与GC,再次稳定GC基线.待GC基线稳定且热解反应器内温度稳定后,移去磁石,包裹有样品的石英砂掉入加热区,石英砂和热解残渣停留在第1加热区域;热解形成的可挥发性物质(气相成分)随载气进入第2加热区;经过气相反应后的所有热解产物随载气进入在线GC系统进行定量分析.
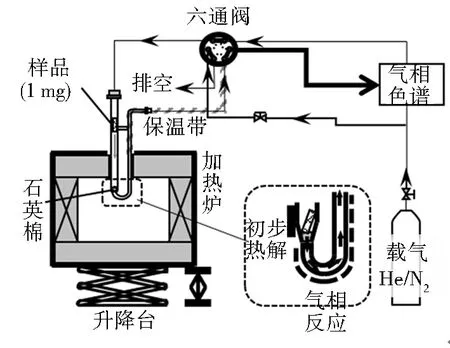
图1 两段裂解反应器-在线气相色谱分析装置Fig.1 Schematic diagram of two stage tubular reactor and online gas chromatograph(TSPR-online GC)
1.3 产物定量分析与理论分布
采用Gaskuropack54、VZN-1 2根填充柱和PoraBOND Q、TC-1701 2根毛细管柱分析产物情况,GC条件设置、定量分析方法及色谱峰对应物质参照文献[5,16].1)色谱峰通过标准物质的对比或通过与GC/MS色谱图进行定性鉴定;2)当标准物可用时,利用热解产物相应的标准物质绘制标准曲线,利用气相色谱峰面积折算进行定量;3)当标准物质不可用时,以甲烷为标准物,利用“有效碳个数”对产物进行定量分析,如式(1)、式(2)所示.FID为质量型检测器,故色谱峰对应化合物可利用式(1)、式(2)计算产物的产率.CO和CO2利用TCD检测,由于CH4在2种检测器中均可检出,故以CH4为参考进行质量折算.
产物i质量(标准物不可用)
(1)
产物i的产率
(2)
式中,mi为产物i的质量,g;msample为原料质量,g;Ai为产物i对应的峰面积;Mi为产物i的摩尔质量,g/mol;ACH4为CH4对应的峰面积;NCH4为CH4的物质的量,mol;Ri为有效碳的响应指数;wi为产物i的产率,%.
由于GC分析条件及仪器限制,产物中的较大分子质量和极性较大的化合物未进行定量分析,该实验中统称为“不可测化合物(UDCs)”,其产率通过式(3)进行计算.
wUDCs=100%-∑wi,
(3)
式中,wUDCs为UDCs的产率,%;∑wi为可检出产物的总产率,%.
按照纤维素与木质素混合比例,将木质素与纤维素单独热解产物的实验产率进行加权叠加计算,作为纤维素与木质素共热解产物的理论产率(C3L7exp、C5L5exp、G7L3exp).若理论产率与实验产率相等,则木质素与纤维素的热解过程是相互独立的,不存在相互作用;若理论产率大于实验产率,则木质素与纤维素共热解对该产物的形成表现为抑制作用;若理论产率小于实验产率,则木质素与纤维素共热解对该产物的形成表现为促进作用.
2 结果与分析
2.1 纤维素和木质素热解产物分布
纤维素与木质素热解产物分布及不同质量比共热解理论分布结果如图2a所示.热解产物分为残渣(Char)、无机气体(IGas)、C1—C5脂肪烃(LHs)、芳烃(AHs)、非芳基含氧化合物(LOCs)和酚类化合物(PHLs).木质素热解所得产物及产率大小排序为残渣>无机气体>C1—C5脂肪烃,而纤维素热解产物及产率大小排序为无机气体>非芳基含氧化合物>C1—C5脂肪烃.纤维素与木质素不同比例共热解时对产物形成的相互作用如图2b所示.由图2a可知,木质素单独热解残渣率为24.67%(质量分数,下同),而纤维素单独热解残渣率仅为1.92%.两者共热解时,残渣率在混合质量比为3∶7时最高,为25.77%,略高于木质素单独热解时的残渣率,表现为对残渣形成的促进作用(图2b).由前期研究结果可知,纤维素热解温度为300~380 ℃,热失重速率较快;而木质素热解温度为140~540 ℃,热失重速率较为缓慢.在两者共热解过程中,纤维素热解所得可挥发物被木质素网状结构捕获,从而促进了固体产物的形成,提高了残渣率.随纤维素比重的增加,共热解残渣率不断下降,此时,两者共热解对残渣的形成表现为抑制作用(图2b),且纤维素比重越高,抑制作用越强.可能是由于纤维素热解形成较多的小分子化合物,在从固体样品中逸出的过程中,与木质素结构作用,加速了木质素网状结构的破坏,提高了木质素的热解速率.
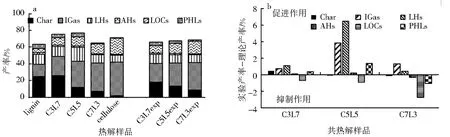
a.热解产物分布;b.共热解时对产物形成的相互作用.图2 纤维素和木质素热解产物分布及共热解对产物形成的相互作用Fig.2 Product distribution and interaction of cellulose and lignin co-pyrolysis
2.2 无机气体
纤维素和木质素热解所得无机气体(IGs)主要为一氧化碳(CO)、二氧化碳(CO2)和水(蒸汽,H2O),其产率分布及共热解对IGs的影响如图3所示.由图3可知,木质素热解IGs产率为14.90%,随纤维素比重的增加,IGs产率不断增加;纤维素单独热解IGs产率达到39.76%.CO作为纤维素和木质素热解的主要产物之一,其产率随纤维素比重的增加而增加,两者共热解对CO的形成表现为抑制作用,如图3b所示.CO2产率在纤维素与木质素质量比为5∶5时达到最大,为8.93%;由图3b可知,纤维素与木质素共热解对CO2的形成表现为促进作用,纤维素与木质素混合质量比为5∶5时促进作用最强,主要是由于纤维素含氧量较木质素高,在热解过程中可提供富氧环境,利于CO2的形成,而抑制CO的形成.H2O的产率随纤维素比重的增加而增加:木质素单独热解时产率为4.40%,而纤维素单独热解时产率为11.33%.由图3b可知,纤维素与木质素共热解对H2O的形成表现为促进作用,且纤维素比重越大,促进作用越明显.

a.热解产物IGs分布;b.共热解时对IGs形成的相互作用.图3 纤维素和木质素热解产物IGs分布及共热解对IGs形成的相互作用Fig.3 IGs distribution and interactions for IGs information during cellulose and lignin co-pyrolysis
2.3 C1—C5烃
由图2得知,纤维素和木质素共热解经气相反应后能够提高C1—C5烃的总产率,促进脂肪烃的形成.木质素单独热解可得较多的CH4(4.80%),见图4a,主要由木质素结构中甲氧基的断裂形成;纤维素单独热解产生较少甲烷,产率仅为0.39%.CH4产率随纤维素占比的增加而增加,在质量比为5∶5时,CH4产率达到最大,为5.46%,然后随纤维素占比的增加而下降.由图4b可知,纤维素和木质素共热解对CH4的形成具有明显的促进作用.
纤维素单独热解所得C2烃产率明显高于木质素单独热解所得C2烃产率,且以乙烯为主.由图4a可知,C2烃产率随纤维素占比的增加而增加,在质量比为5∶5时,达到最大,为3.90%;然后随纤维素占比的增加而下降.由图4b可知,在质量比为5∶5时,纤维素和木质素共热解对C2烃的形成具有一定的促进作用.但在质量比为3∶7和7∶3时,两者共热解对C2烃的形成表现为抑制作用,特别是在纤维素比重较大时(7∶3),抑制作用尤为明显.木质素单独热解所得C3烃产率高于纤维素单独热解所得C3烃产率.C3烃可能来源于木质素基本结构单元上的4位取代C3烃基,或是源于芳环开环破裂形成的C5烃.由图4可知,C3烃产率随纤维素占比的增加而增加,在质量比为5∶5时达到最大,为4.13%,然后随纤维素占比的增加而下降.由图4b可知,纤维素和木质素共热解对C3烃的形成具有明显的促进作用,特别是在纤维素与木质素质量比为5∶5,促进作用尤为明显.
木质素单独热解所得C4烃和C5烃产率高于纤维素单独热解所得C4烃和C5烃产率.木质素主要由对-羟基苯基、愈创木基和紫丁香基3种基本单元组成.这3种结构在650 ℃以上会发生芳环开环反应生成C2烃、C4烃和C5烃,伴随着CO的生成.其中,C5烃主要源于苯酚结构的开环反应,而C4烃主要源于愈创木酚结构的开环反应.由图4b所示,当纤维素比重较低时,共热解对C4烃的形成表现为促进作用,当两者质量比为7∶3时,共热解抑制了C4烃的形成.当两者质量比为5∶5时,纤维素和木质素共热解促进了C5烃的形成,而在纤维素与木质素质量比为3∶7和7∶3时,则表现为对C5烃形成的抑制作用.

a.热解产物LHs分布;b.共热解时对LHs形成的相互作用.图4 纤维素和木质素热解产物LHs分布及共热解对LHs形成的相互作用Fig.4 LHs distribution and interactions for LHs information during cellulose and lignin co-pyrolysis
2.4 非芳基含氧化合物
经气相反应后,纤维素热解产物中非芳基含氧化合物(LOCs)的产率明显高于木质素.纤维素和木质素热解主要LOCs及其产率如图5a所示.纤维素热解主要LOCs包括甲醇、乙醛、乙酸、呋喃和D-阿洛糖.而木质素热解主要LOCs为甲醇和乙酸.甲醇产率随纤维素占比增加而增加,在纤维素与木质素质量比为5∶5时,甲醇产率达到最高,为2.75 %,然后随纤维素占比增加而降低.由图5b可知,纤维素与木质素共热解气相反应中促进了甲醇的形成.乙醛作为纤维素热解的主要产物,其产率随纤维素占比的增加而增加,但由图5b可知,与理论产率相比,纤维素与木质素共热解气相反应中抑制了乙醛的形成.木质素热解产生乙酸主要通过4位取代基结构中的脱羧反应,而纤维素主要通过脱氧-乙酰基反应形成乙酸.在纤维素和木质素共热解过程中,乙酸产率随纤维素占比变化并不明显,如图5a所示.通过与理论计算产率相比,在纤维素与木质素质量比为3∶7时,纤维素与木质素共热解明显促进了乙酸的形成;随纤维素占比的增加,对乙酸形成了促进作用减弱,并在纤维素与木质素质量比为7∶3时转化为抑制作用.D-阿洛糖是纤维素初次热解的主要产物之一,在气相反应中进一步发生裂解反应形成其他含氧化合物、烃和无机气体.由图5b可知,纤维素与木质素共热解对D-阿洛糖的形成表现为抑制作用,即实验产率低于加权理论产率,这可能是由于木质素热解气相产物的存在促进了D-阿洛糖分解为IGs和LHs,从而在纤维素和木质素共热解过程中对IGs和LHs形成了促进作用(图2).呋喃是纤维素热解的重要中间产物,由图5a所示,呋喃产率随纤维素占比的增加而增加.与理论产率相比,纤维素与木质素共热解对呋喃的形成表现为抑制作用.
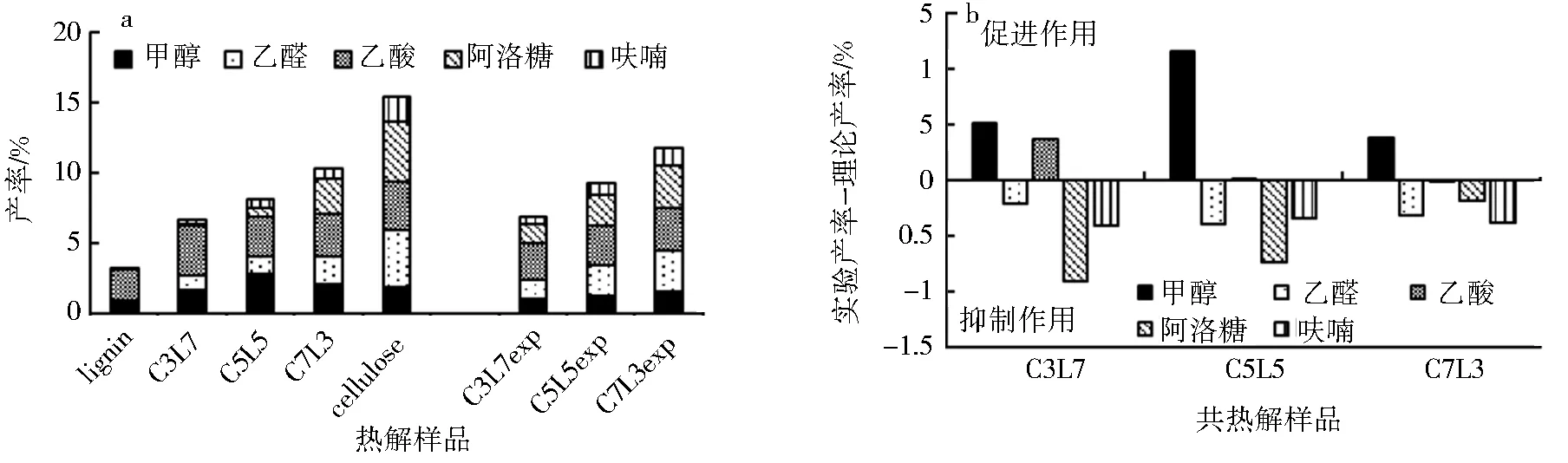
a.热解产物LOCs分布;b.共热解时对LOCs形成的相互作用.图5 纤维素和木质素热解产物主要LOCs分布及共热解对主要LOCs形成的相互作用Fig.5 Main LOCs distribution and interactions for LOCs information during cellulose and lignin co-pyrolysis
2.5 酚类化合物(PHLs)
酚类化合物是木质素热解的主要产物之一,而纤维素热解所得PHLs产率则很低,仅检测到少量苯酚(phenol)和甲基酚(cresol).由图6可知,苯酚产率随纤维素比重的增加而增加,但当纤维素与木质素质量比为7∶3时,苯酚产率迅速降低.由图6可知,4-乙基愈创木酚(4-EMOP)、邻苯二酚(catechol)和紫丁香酚(2,6-DMOP)产率随纤维素占比的增加迅速降低,纤维素与木质素共热解对该3种酚的形成表现为抑制作用.当纤维素与木质素以质量比7∶3进行共热解时,对所有可检测PHLs的形成均表现为抑制作用;当纤维素与木质素质量比3∶7和5∶5时,对苯酚和甲基苯酚的形成表现为促进作用;当纤维素与木质素质量比为3∶7时,共热解对二甲基苯酚(2,6-DMP,2,3-DMP)的形成表现为抑制作用,而当纤维素与木质素质量比为5∶5时,共热解对二甲基苯酚的形成表现为促进作用.这主要是由于在气相反应过程中,当纤维素与木质素质量比为5∶5时,反应体系中存在较多的烃自由基,可与木质素芳基结构发生取代反应、自由基聚合反应而生成较多的烃基苯酚.
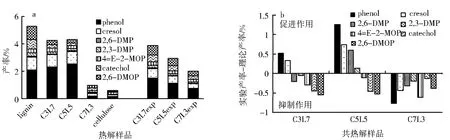
a.热解产物PHLs分布;b.共热解时对PHLHs形成的相互作用.图6 纤维素和木质素热解产物主要PHLs分布及共热解对主要PHLs形成的相互作用Fig.6 PHLs distribution and interactions for PHLs information during cellulose and lignin co-pyrolysis
2.6 芳烃(AHs)
纤维素结构中无芳基结构,其热解产物中的AHs主要通过气相反应过程中C1—C5烃的聚合反应形成.木质素热解所得AHs可通过酚羟基的氢取代或烃基取代反应得到,或是通过气相反应过程中C1—C5烃的聚合反应形成.经气相反应后,木质素与纤维素热解所得AHs总产率随纤维素占比的增加而降低(图7).苯的产率随纤维素占比增加而不断降低.在纤维素与木质素等质量比5∶5时,共热解对苯的形成表现为促进作用,而在混合质量比为3∶7或7∶3时,纤维素与木质素共热解对苯的形成表现为抑制作用.由图7b可知,纤维素与木质素共热解对甲苯的形成表现为抑制作用.乙苯产率在混合质量比为3∶7和5∶5时与木质素单独热解时相似,无明显变化,而在混合质量比为7∶3产率迅速下降.二甲基苯(XLY)产率在纤维素与木质素等质量比5∶5共热解时最高.由图7b可知在混合质量比为3∶7和5∶5时,纤维素与木质素共热解明显促进了乙基苯和二甲基苯的形成.在纤维素占比较低时,苯乙烯实验产率高于理论加权产率,纤维素与木质素共热解促进了苯乙烯的形成;随着纤维素占比的增加,纤维素与木质素共热解对苯乙烯的形成表现为抑制作用.由图7a可知,萘和甲基萘产率相对较低,在混合质量比为3∶7和5∶5时,纤维素与木质素共热解对苯乙烯的形成具有明显的促进作用;当混合质量比为7∶3时,两者共热解能够促进甲基萘的形成,而抑制了萘的形成.

a.热解产物PHLs分布;b.共热解时对PHLs形成的相互作用.图7 纤维素和木质素热解产物主要AHs分布及共热解对主要AHs形成的相互作用Fig.7 AHs distribution and interactions for AHs information during cellulose and lignin co-pyrolysis
3 结论
1)经气相反应后,纤维素与木质素热解产物主要包括残渣、无机气体、C1—C5脂肪烃、芳烃、非芳基含氧化合物和酚类化合物.
2)纤维素和木质素进行共热解时,在气相反应中的相互作用较为复杂,各类产物产率分布与纤维素和木质素共热解配比具有密切关系,但并不能通过加权计算进行产物分布的预测.
3)当纤维素与木质素混合质量比为3∶7时,对残渣、无机气体、C1—C5脂肪烃(LHs)、芳烃(AHs)和酚类化合物(PHLs)的存在表现为促进作用,而对非芳基含氧化合物(LOCs)的存在表现为抑制作用.
4)当纤维素与木质素混合质量比为5∶5时,对无机气体、C1—C5脂肪烃(LHs)、芳烃(AHs)和酚类化合物(PHLs)的存在表现为促进作用,而对残渣和非芳基含氧化合物(LOCs)的存在表现为抑制作用.此配比下,纤维素与木质素共热解相互作用最为明显.
5)当纤维素与木质素混合质量比为7∶3时,对无机气体、C1—C5脂肪烃(LHs)的存在表现为促进作用,而对残渣、非芳基含氧化合物(LOCs)、芳烃(AHs)和酚类化合物(PHLs)的存在表现为抑制作用.

