全自动化学发光分析仪检测孕酮和人绒毛膜促性腺激素的性能验证
黄晓楠,刘玉林
(遂宁市中心医院检验科,四川 遂宁 629000)
孕酮(PROG)和人绒毛膜促性腺激素(β-hCG)是目前临床应用最广泛的激素检测项目,在妇产科等科室得到广泛的应用。其检测方法不断变迁,从放射免疫测定法到酶联免疫测定法再到化学发光免疫测定法。雅培i2000SR 全自动化学发光分析仪采用了化学发光微粒子免疫分析法(CMIA)定量测定人血清的激素水平。依据ISO 15189:2012《医学实验室质量和能力认可准则》[1]和《医疗机构临床实验室管理办法》[2],雅培i2000SR 全自动化学发光分析仪在用于检测项目前,须对其性能进行验证,确保其能够满足临床需求,保证检验质量。本研究参照美国临床和实验室标准协会(CLSI)颁布的EP 系列文件及CNAS-GL037《临床化学定量检验程序性性能验证指南》[3]对i2000SR 全自动化学发光免疫分析仪上检测的PROG 和β-hCG 的精密度、正确度、线性范围、临床可报告范围进行验证和评价,现报道如下。
1 资料与方法
1.1 一般资料 收集2021 年4 月1 日-30 日到遂宁市中心医院进行健康体检人员的外观正常的新鲜血清,-20 ℃保存备用。
1.2 仪器与试剂 雅培i2000SR 全自动化学发光免疫分析仪;孕酮测定试剂盒(批号21450UI01);人绒毛膜促性腺激素测定试剂盒(批号19561UI01)。
1.3 校准品 美国雅培公司的原装校准品:孕酮校准品(批号20003UI01);人绒毛膜促性腺激素校准品(批号20306UI01)。
1.4 质控品 美国伯乐公司的免疫分析质控品:水平1(批号40381),水平2(批号40382);卫生部临床检验中心2021 年第一次内分泌室间质量评价质控品5 份(样本编号202111、202112、202113、202114、202115)。
1.5 方法
1.5.1 精密度验证 选取2 个不同浓度的样本,其中1 个样本被测浓度水平在医学决定水平左右或参考区间左右,每天测定1 次,每次重复测定4 次,连续测定5 d,分别计算总均值、批内标准差及实验室内标准差(中间);根据厂家要求的标准差、有效自由度及C 值计算得到验证值(V),如测量的批内标准差、实验室内标准差(中间)小于或等于验证值,则验证合格。
1.5.2 正确度验证 参考CLSI EP15-A2 文件[4],用20个血清标本(高中低值,包含医学决定水平)或5 个室间质评样本与通过ISO15189 认证的检验机构进行比对试验。≥80%的标本偏移<1/2 总允许误差(TEA),其中包含医学决定水平,则认为正确度验证通过。
1.5.3 线性范围的验证 参考CLSI EP6-A 文件[5],选择高值样本(浓度接近厂家说明书标示的高限值)和低值样本进行验证。将高值样本按0、0.2、0.4、0.6、0.8、1 稀释度稀释,每个浓度测定2 次。做线性回归分析,得出实测值与理论值的线性关系Y=aX+b,计算相关系数(R2),得到的线性范围并与厂家声称的进行比较。
1.5.4 临床可报告范围的验证 选取已知浓度在分析测量范围内的高值样本1 份(接近测量范围上限),用厂家推荐的稀释液按照厂家推荐的稀释倍数对该样本进行稀释,之后将样本及稀释样本重复测定2 次,计算平均值。以样品原倍结果平均值作为理论浓度,将样品进行稀释后得出的结果的均值为还原浓度,再计算还原浓度与理论浓度的偏差,偏差小于或等于该项目TEA 时的最大稀释倍数则为该项目的最大稀释倍数。可报告范围高限则采用线性区间高限与最大稀释倍数的乘积,低限采用线性范围低限。
1.6 统计学方法 采用SPSS 19.0 和Excel 2018 对数据进行处理和分析。计量资料以()表示,行t检验;计数资料以(%)表示,行X2检验;以P<0.05 为差异有统计学意义。
2 结果
2.1 精密度结果 PROG 和β-hCG 的批内标准差和实验室内标准差均小于验证值,验证通过,见表1。
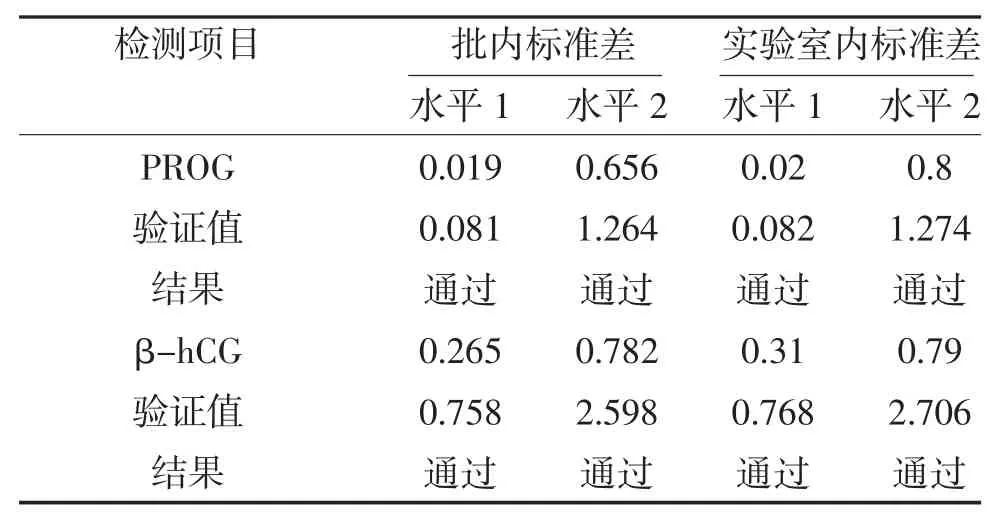
表1 PROG 和β-hCG 的精密度结果
2.2 正确度结果 PROG 和β-hCG 偏倚均小于1/2 TEA,验证通过,见表2、表3。
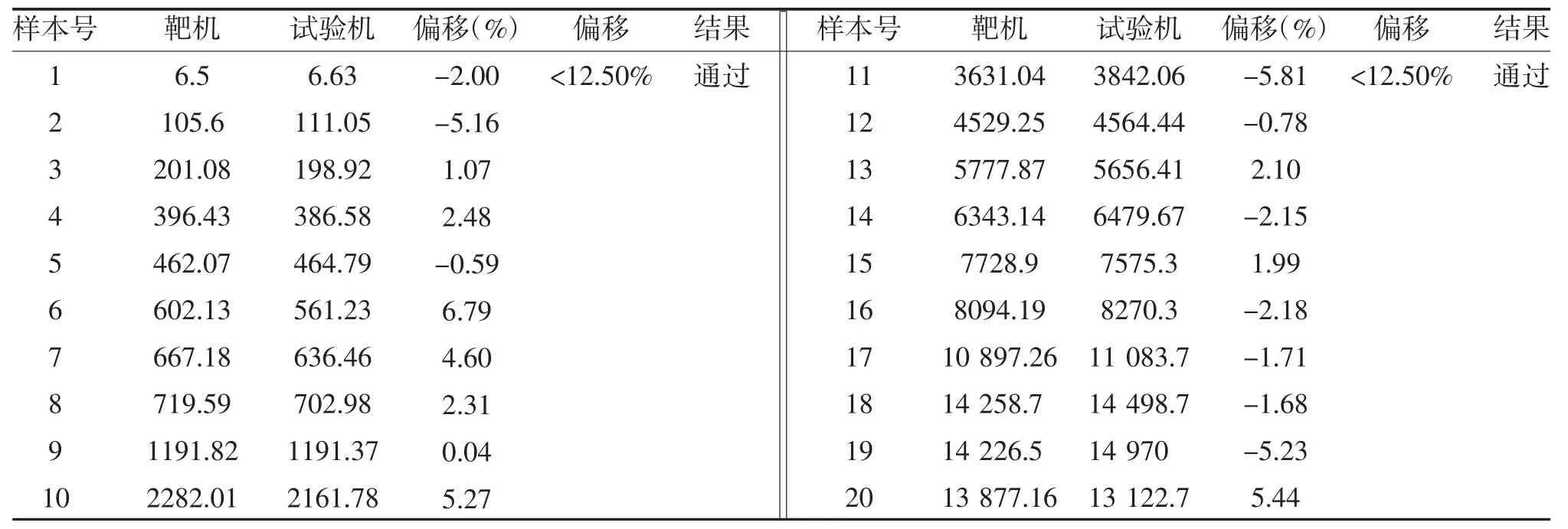
表2 β-hCG 正确度结果
2.3 线性范围结果 验证项目的斜率a 值均在(1.00±0.03)范围内,R2>0.99,且测定的线性范围在厂家声称的范围内,验证通过,图1、表4、表5、图2。
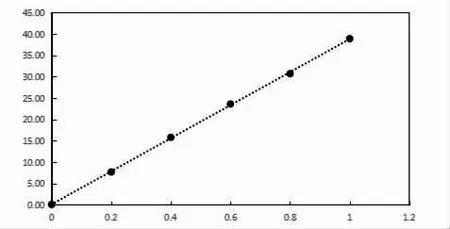
图2 PROG 线性回归
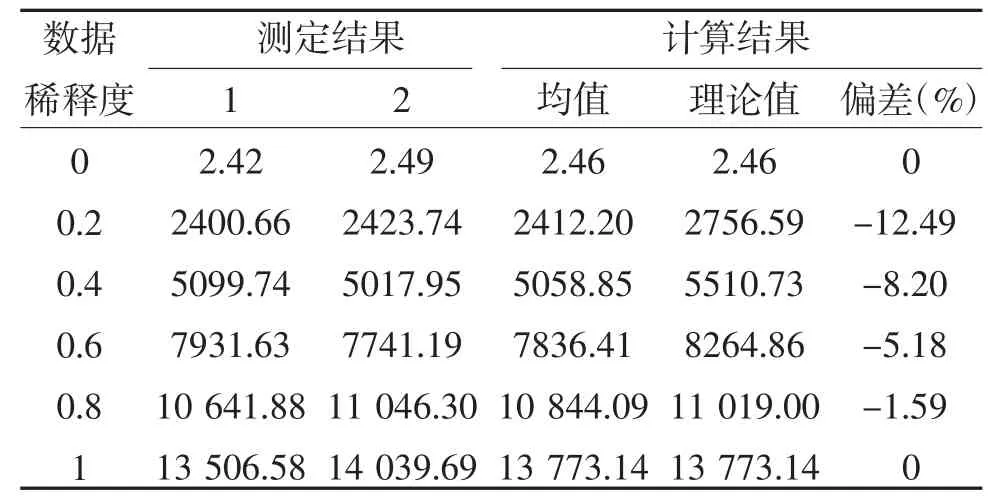
表4 β-hCG 线性范围验证
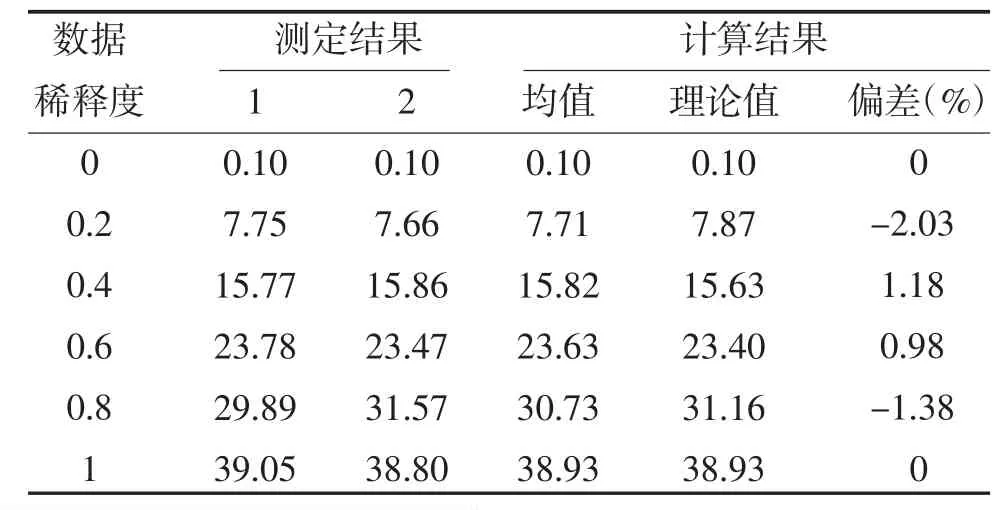
表5 PROG 线性范围验证
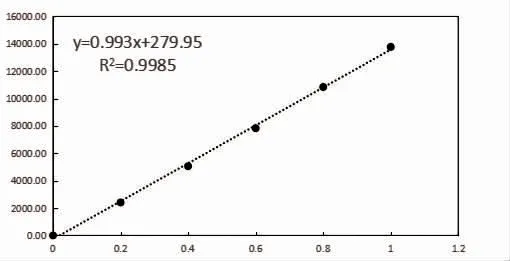
图1 β-hCG 线性回归
2.4 临床可报告范围 PROG 的临床可报告范围是0.1~389.3 nmol/L,β-hCG 的临床可报告范围是2.46~206 597.1 mIU/ml,见表6。

表6 PROG 和β-hCG 的临床可报告范围
3 讨论
依据ISO15189 相关要求,参考美国临床实验室标准协会(CLSI)的系列文件和标准建立性能验证方案[5-7],检测仪器在应用于临床前需要对其检测的检验项目进行性能验证,以保证其质量并满足临床需求。验证内容包括但不局限于精密度、正确度、线性范围、临床可报告范围等。雅培i2000SR 全自动化学发光分析仪采用微粒子化学发光原理定量检测标本,与传统方法相比检测速度快、灵敏度高、操作简单、故障率低[8]等特点,检测血清标志物的性能验证已有相关报道[9-12],结果均符合厂家声明。但厂家给出的性能验证及指标参数仅代表厂家的实验指标,本实验室的检测环境,如温湿度,实验用水及仪器状态等与厂家并非完全一致,故使用前须进行性能验证[13]。
精密度是重复测定值之间的一致性,是检测系统的基本分析性能指标之一,可反映检测系统的随机误差[14,15]。本研究显示,雅培i2000SR 全自动化学发光分析仪检测PROG 和β-hCG 的批内CV 和批间CV 均低于验证值,符合厂家声明,满足临床需求,说明该仪器检测的重复性好。有研究证实[16],雅培i2000SR 全自动化学发光分析仪性能稳定。正确度是大批检验结果的均值与真值的一致程度,正确度验证是与通过了ISO15189 的临床试验进行比较。本研究选用自留标本和卫生部质控样本进行测定,结果偏倚均小于12.5%,符合厂家声明,与杨佳[17]的结论一致。线性范围指测定值与稀释倍数呈线性关系的范围,采用线性稀释回收法[9],保证样本的检测结果在线性范围内准确可靠。本次试验结果显示,验证项目的斜率a 值均在(1.00±0.03)范围内,R2>0.99,且测定的线性范围在厂家声称的范围内,说明实测值与理论值具有良好的相关性,结果符合要求。黄学强等[18]也证明β-hCG 结果在线性范围内可靠。本次验证通过稀释的方法对临床可报告范围进行测定,结果显示PROG 的临床可报告范围为0.1~389.3 nmol/L;另外,β-hCG 的临床可报告范围在2.46~206 597.1 mIU/ml,与曾令恒等[19]报道的2.6~199000 mIU/ml 基本一致,证明雅培i2000SR 全自动化学发光分析仪的检测能力符合要求。
综上所述,雅培i2000SR 全自动化学发光分析仪检测PROG 和β-hCG 的精密度、正确度、线性范围、临床可报告范围符合ISO15189 要求并与厂家声明一致,可满足临床需求。

