硫普罗宁修饰的银纳米簇应用于苦味酸的检测
张彦,康晶晶,高鹏飞,苏艳,伍建林
(1.山西大学 化学化工学院,山西 太原 030006;2.澳门科技大学 中医药质量研究国家重点实验室,澳门)
0 引言
苦味酸(2,4,6-三硝基苯酚,PA)是一种常见的有毒、有刺激性气味、不能降解的硝基化合物。几十年来被广泛用于制药、皮革、工业爆破、烟花行业和染料行业中[1-2],在其生产和使用过程中不可避免的被释放到空气、土壤和地下水中,带来一系列的环境污染问题[3]。而且,在生物系统中苦味酸的邻位硝基被还原为氨基,苦味酸被转化为2-氨基-4,6-二硝基苯酚,表现出比苦味酸更强的诱变活性[4]。因此,快速、灵敏地检测苦味酸对于保护人类健康和监测环境污染是非常必要的。
近年来,基于苦味酸的检测方法有质谱法[5]、电化学法[6]、气相色谱法[7]等,但这些方法成本高、耗时长或样品前处理比较复杂、干扰大,因而其实际应用受到限制。荧光光谱法成本低廉、响应时间快、操作简单、选择性高。银纳米簇作为一种新型的荧光材料,具有较大的斯托克斯位移、优越的生物相容性以及独特的光学性质[8-9],在生物传感、新型催化剂、生物标记、荧光成像等领域得到了广泛的应用[10]。化学还原法的操作简单、反应速率快,因此通常采用化学还原法来制备银纳米簇[11]。银纳米团簇的粒径、稳定性、荧光特性等性质与配体有很大的关系,通过引入不同配体,不仅可以实现更好的稳定性,而且也可以增强团簇的发光性能。硫醇是含有巯基的生物小分子化合物,由于巯基和金属原子的亲和力较强,硫醇保护的银纳米簇不仅具有较高的稳定性,还具有良好的生物相容性[12]。硫普罗宁(N-(2-巯基丙酰基)甘氨酸,Tiopronin)是一种生物相容性优良的巯基药物,能够与金属形成很强的金属-硫键,常用作金属纳米粒子的稳定剂[13-14]。
本文以硝酸银为原料,硫普罗宁为稳定剂,硼氢化钠为还原剂,在室温下成功合成了发绿色荧光的银纳米簇。基于PA可使AgNCs荧光发生猝灭,建立了检测PA含量的荧光分析方法,可快速检测水体环境中的苦味酸。
1 实验部分
1.1 试剂和仪器
硝酸银、硫普罗宁(TP)、硼氢化钠、苦味酸等均为分析纯。BR(Britton-Robinson Buffer So⁃lution)缓冲溶液用0.04 mol/L磷酸(H3PO4)、硼酸(H3BO3)、醋 酸(CH3COOH)和 0.2 mol/L NaOH溶液配制。紫外可见分光光度(Hitachi,U-2910);爱丁堡稳态瞬态荧光光谱仪(FLS920);红外光谱仪(珀金埃尔默仪器有限公司,Paragon 1000);纳米粒径电位分析仪(马尔文,NanoZS90);透射电子显微镜(JEOL有限公司,JEM-2100);暗箱式自动紫外分析仪(上海市安亭电子仪器厂,ZF-2C);pH酸度计(上海梅特勒-托利多仪器公司,FE20);数显智能控温磁力搅拌器(巩义市予华仪器有限责任公司,KQ-500)。
1.2 银纳米簇的制备
在洁净的圆底烧瓶,依次加入5 mL 0.06 mol/L硫普罗宁(TP),5 mL 0.01 mol/L AgNO3溶液混和均匀,有白色絮状物生成。室温下搅拌30 min后,将500 μL 1 mol/L的硼氢化钠水溶液迅速加入到混合溶液中反应5 h,溶液从黑棕色变为黄棕色。将制得的银纳米簇保存在4℃的冰箱中备用。
1.3 苦味酸浓度的测定
将120 μL AgNCs溶液分散于pH=5.0的BR缓冲溶液中,测量荧光光谱。然后,将不同浓度的PA溶液依次加入到上述溶液中,室温孵育1 min后在激发波长为376 nm,发射波长为520 nm下记录其荧光光谱。同上述条件下,AgNCs溶液中加入1.8×10-3mol/L的干扰物,包括有:Na+、K+、Ni2+、Mg2+、Ca2+、Al3+、Ba2+、Pb2+、Cu2+、Hg2+、Zn2+、Cd2+、Fe3+、Cr3+、Co2+、Mn2+、Cl-、Br-、Ac-、S2-、CO32-、SO42-、ClO4-、BrO3-、NB(硝基苯)、PHE(苯酚)、IPA(间苯二甲酸)、o-NP(邻硝基酚)、m-NP(间硝基酚)、p-NP(对硝基酚)、o-DHB(邻苯二酚)、p-DHB(对苯二酚)、o-phen(邻菲罗啉)、2-DNP(2-硝基苯酚)、2,4,6-三硝基甲苯(TNT),扫描且记录其荧光变化;最后,掺入干扰物的混合溶液中加入9.0×10-5mol/L的PA溶液,测定荧光强度。
1.4 实际样品的检测
采用标准加入法对实际水样中PA的含量进行测定,实际水样取自山西大学令德湖水和实验室自来水。使用过滤器将水样过滤,再以10 000 r·min-1离心10 min,除去水中杂质。将1 mL水样、120 μL的AgNCs和BR缓冲溶液混合,测定荧光光谱,并将不同浓度PA溶液加入上述溶液中,测其荧光光谱。
2 结果与讨论
2.1 AgNCs的性能表征
通过多种分析手段来表征AgNCs的形貌、尺寸、结构和荧光性质。透射电子显微镜(图1(a))显示,AgNCs的粒径较均匀、分散性较好,平均粒径为2.96 nm。如红外光谱(图1(b))所示,1 752 cm-1附近为TP中游离羧基中的羰基伸缩振动,而在AgNCs中该处的吸收峰峰强度明显降低,说明羰基与银配位附着至AgNCs的表面;比较AgNCs和TP的红外光谱曲线可以发 现 ,TP的 S−H 拉 伸 带(2 540 cm-1)在AgNCs的光谱中消失,说明了Ag与TP分子形成了硫醇盐,进一步证明了AgNCs的成功合成[10]。XPS 结果显示,S 2p能谱中有 162.4(S−Ag),163.6(S−H),164.8(S 2p1/2)三个特征吸收峰(图 1(c))。Ag 3d5/2峰和 Ag 3d3/2峰的结合能分别位于367.9 eV和374.08 eV处( 图 1(d)),367.9 eV 处 的 峰 介 于 Ag(I)(367.5 eV)和纯Ag(0)(368.2 eV)之间,进一步证明了硫普罗宁包覆的银纳米团簇已经被成功合成。

图1 (a)AgNCs的TEM图像和粒径分布直方图;(b)TP和AgNCs的红外光谱图;AgNCs的高分辨X射线光电子能谱图(c)S 2p;(d)Ag 3dFig.1 (a)TEM image and particle size distribution ofAgNCs.(b)Infrared spectra of TP andAgNCs.High resolution X-ray pho‐toelectron spectroscopies ofAgNCs(c)S 2p,(d)Ag 3d
通过紫外可见吸收光谱可得AgNCs在376 nm附近表现出明显的吸收峰(图2(a)),归因于其表面的n→π*跃迁。荧光光谱显示AgNCs的最佳激发和发射波长分别为376 nm和520 nm。从插图上可以看到AgNCs在日光灯下为黄棕色,而在365 nm紫外灯照射下发出绿色荧光。如图2(b)所示,使用376 nm波长的光照射40 min后,AgNCs的荧光强度仍能保持在95%以上,说明该纳米簇具有良好的抗光漂白性。此外,AgNCs的Zeta电位为−16.4 mV,表明该纳米簇带负电性,在水溶液中有良好的稳定性。当在4℃下保存5个月后,AgNCs的荧光强度仍能保持相对稳定(图2(c))。

图2 (a)AgNCs、AgNO3和TP的紫外可见吸收光谱图,AgNCs荧光激发和发射光谱图,插图:AgNCs在可见光和365 nm的紫外光下的照片;(b)在AgNCs的荧光强度与紫外灯照射时间的关系图;(c)在4℃下保存5个月AgNCs的荧光强度图Fig.2 (a)UV-visible absorption spectra ofAgNCs,AgNO3and TP.Fluorescence excitation(red lines)and emission spectra(blue lines)ofAgNCs.Inset:pictures ofAgNCs under visible light and ultraviolet light of 365 nm.(b)Relationship between fluorescence intensity ofAgNCs and exposure time of ultraviolet lamp.(c)The fluorescence intensity ofAgNCs stored at 4℃for 5 months
2.2 探究PA的最佳检测条件
考察了孵育时间、AgNCs的用量、pH值对苦味酸检测的影响。将PA加入到AgNCs中,荧光强度在1 min内快速下降,并在接下来的20 min内保持稳定(图3(a)),因此,AgNCs对PA有较快的响应。当AgNCs用量为120 μL时,荧光强度降低值F0-F值最大(图3(b)),因此,选用120 μL AgNCs作为检测苦味酸的最佳浓度。如图3(c)所示,pH值对加入PA后荧光强度的降低值F0-F基本无太大影响,但当pH>5.0时,AgNCs自身的荧光强度F0降低(图3(c)插图),所以选择pH=5.0的BR缓冲液进行后续的检测实验。
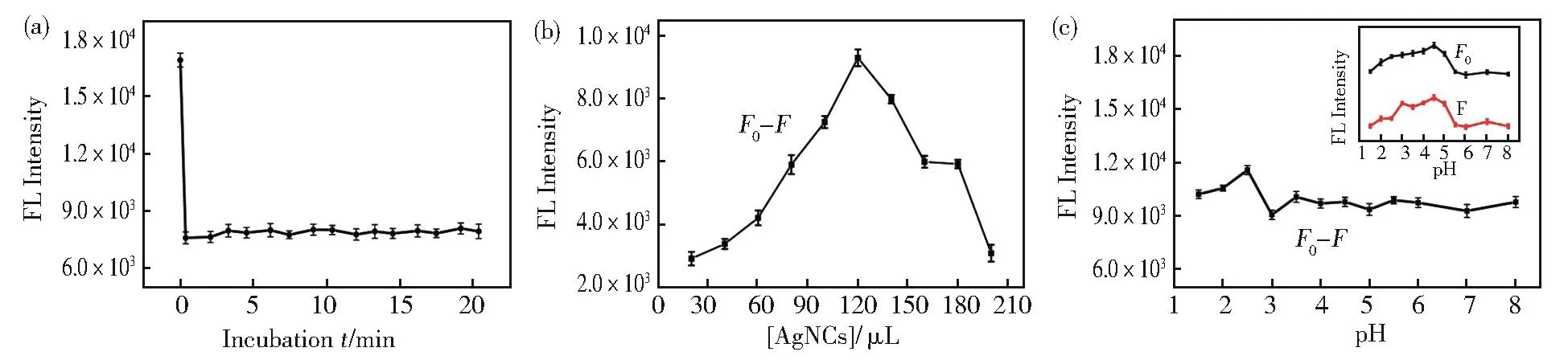
图3 (a)孵育时间对AgNCs荧光强度的影响;(b)AgNCs的用量对检测PA的影响;(c)pH值对AgNCs传感PA的影响,插图为pH值F0和F值的影响。F0和F分别是不加入PA和加入PA时AgNCs的荧光强度值Fig.3 (a)Effect of incubation time on fluorescence intensity ofAgNCs.(b)The effect of various dosages ofAgNCs on the detection of PA.(c)The influence of pH value on the detection of PA.Inset:The effect of pH on F0and F
2.3 测定苦味酸的选择性和抗干扰性
为了探索AgNCs对PA的荧光传感方法是否可用于实际样品中PA的特异性检测,考察了水体系中可能存在的阳离子、阴离子和不同硝基酚类化合物等潜在干扰物质对AgNCs和加入PA后AgNCs的荧光响应情况。如图4所示,常见干扰物和其他硝基化合物的存在对AgNCs的荧光强度只产生轻微的干扰。只有加入PA后,AgNCs的荧光强度才会发生明显降低。这说明本文构建的荧光检测方法对PA具有较好的选择性,可用于实际样品中PA的检测。

图4 AgNCs对PA与常见干扰物和其他硝基酚类化合物等潜在干扰物质的选择性实验Fig.4 Selectivity ofAgNCs for the coexistence of PAwith common interferents and other nitrophenols
2.4 对PA检测的灵敏度
如图5所示,当PA的浓度从0增加到138 μmol/L时,AgNCs的荧光几乎完全猝灭,而且相对荧光强度与PA浓度呈现两段良好的线性关系:PA 浓度在 3.99×10-7mol/L~4.69×10-6mol/L范围内,线性方程为 log(F0∶F)=0.039[PA](μmol/L)+0.006,线性相关系数 R2=0.993;PA浓度在范围内4.69×10-6mol/L~1.38×10-4mol/L,线性方程为 log(F0∶F)=0.004[PA](μmol/L)+0.205,R2=0.999,检 出 限 为 0.045 μmol/L。该方法的检出限低于国家环境保护总局(GB3838-2002)规定的地表水生产饮用水中PA的最低允许浓度(2.2 μmol/L)。将本文的PA检测方法与已报道的基于发光纳米材料的方法进行了比较,如表1所示。与其他方法相比,本文中AgNCs的合成不需加热,仅需室温下制备,合成步骤和反应时间也基本与文献报道相当,而且对PA的检测具有较高的灵敏度。
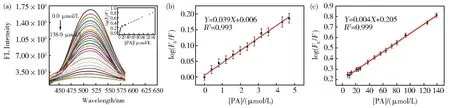
图5 不同浓度的PA对AgNCs的荧光响应图(a)及相对荧光强度与PA浓度的线性关系,见(b)和(c)Fig.5 Fluorescence response diagram ofAgNCs in different concentrations of PA(a),and the linear relationship between relative fluorescence intensity and concentrations of PA,see(b)and(c)

表1 AgNCs与其他荧光纳米材料测定PA的比较Table 1 Comparison between theAgNCs and other fluorescent nanomaterials for the determination of PA
2.5 检测苦味酸机理的探究
苦味酸即为2,4,6-三硝基苯酚,其结构式如图6(a)所示,三个硝基有很强的吸电子作用,使酚羟基电子云密度降低,氢原子容易解离从而表现强酸性质(pKa=0.25)[4]。AgNCs中的TP配体上的胺基和羧基因去质子化后表现出碱的性质,因此PA可能通过酸碱相互作用与AgNCs中的TP结合,同时电子云从富电子的AgNCs向吸电子的PA中偏移,进而导致荧光猝灭[15]。荧光寿命测试结果(图6(b))显示AgNCs的平均寿命为2.99 ns,加入苦味酸后的荧光寿命为2.65 ns。加入苦味酸前后AgNCs的荧光寿命变化可以忽略,进一步证实了PA与AgNCs进行了结合,通过酸碱诱导电子转移使AgNCs的荧光发生了猝灭,该检测机理与已报道的研究工作一致[2]。此外,如图6(c)所示,AgNCs的激发光谱与PA的紫外-可见吸收光谱有很大程度的重叠,这表明PA诱导AgNCs的荧光猝灭还有可能源于内滤效应。基于AgNCs的PA检测方法在3.99×10-7mol/L至1.38×10-4mol/L范围内呈现两段良好的线性关系(图5),说明酸碱诱导电子转移和内滤效应同时存在于AgNCs的猝灭过程。在PA的浓度较高并大于4.69×10-6mol/L时,空间位阻效应增强,酸碱作用诱导电子转移的作用减弱,内滤效应成为主导因素,PA对AgNCs的猝灭程度亦有所减缓。

图6 (a)AgNCs与PA相互作用示意图;(b)不加入和加入PA的AgNCs荧光寿命谱图;(c)PA的紫外可见吸收光谱(黑色线)和AgNCs的荧光激发光谱(红色线)Fig.6 (a)Schematic of interaction betweenAgNCs and PA.(b)The fluorescence lifetime spectra ofAgNCs without and with PA.(c)The UV-visible absorption spectrum of PA(black line)and the fluorescence excitation spectrum ofAgNCs(red line)
2.6 对PA检测的精密度
精密度对于分析检测方法是非常重要的参数之一,本文探讨了AgNCs在日内和日间对不同浓度PA检测的精密度RSD,重复检测次数为6 次,进样的浓度分别为 0.8 μmol/L、2.5 μmol/L、10.4 μmol/L、50.0 μmol/L、100.0 μmol/L,如表2所示,日内分析的RSD值在0.31%~1.55%之间,日间分析的RSD值在1.03%~2.67%之间。这些结果有力地证明了基于银纳米簇检测PA的方法重现性较好,可以应用于实际样品的分析检测。

表2 在日内和日间对不同浓度PA检测结果的精密度Table 2 The results of precision assessment for different levels of PAin intra-day and inter-day,respectively
2.7 实际样品分析
采用标准加入法将建立的荧光检测方法应用于令德湖和实验室自来水中PA的含量测定。将浓度为2.37、5.07、10.43 μmol/L的PA溶液分别加入到实际水样中,表3检测结果显示,PA的回收率在96.1%~108.3%之间,说明将此方法应用于检测实际样品中苦味酸有良好的可靠性。

表3 AgNCs荧光传感体系检测实际水样中的PATable 3 Fluorescence sensing system ofAgNCs for the detec‐tion of PAin water samples
3 结论
以硫普罗宁为配体,硼氢化钠为还原剂,在室温下通过一锅法制备出具有绿色荧光的AgNCs。基于PA对AgNCs荧光的猝灭作用,构建了检测PA的荧光传感方法。该方法灵敏度较高,响应迅速,具有良好的选择性和重现性,已成功应用于实际水样中的PA的检测,说明AgNCs对PA的检测具有较高的实际应用价值。

