儿童恶性肿瘤合并噬血细胞综合征的临床特点分析①
宋 曼,海力其古丽·努日丁,王学梅,严 媚
(新疆医科大学第一附属医院儿内一科,乌鲁木齐830011)
噬血细胞综合征又称为噬血细胞性淋巴组织细胞增生症(Hemophagocytic lymphohistiocytosis,HLH),是由细胞因子风暴引起的淋巴细胞和单核巨噬细胞系统增生、活化,产生大量炎症因子,导致的以全身组织细胞活化为特征的临床综合征[1]。根据HLH 的病因分为原发性和继发性两大类,原发性HLH 包括家族性和免疫缺陷相关性,主要是由相关基因突变所引起,是一种常染色体或X 连锁隐性遗传性疾病[2];继发性HLH 可继发于感染、恶性肿瘤、自身免疫性疾病、代谢性疾病、器官移植术后等[3]。原发性的HLH,其临床诊断难度较大,以儿童多见;继发性较原发性相对常见,可发生于各年龄段[4]。HLH 是由多种潜在病变引起的一组临床表现及相关实验室检查相似的炎症反应性疾病,发病机制目前尚不明确,年龄越小,临床表现差异越大,如不及时就诊,病情会迅速恶化[5]。在上述众多病因中,恶性肿瘤合并HLH 尤为突出。因此,能够早期识别HLH,对潜在的病因做出评估非常重要。本研究回顾性分析新疆医科大学第一附属医院儿科中心诊治的55 例儿童继发性HLH患儿的资料,通过比较儿童恶性肿瘤合并HLH 组和非恶性肿瘤合并HLH 组的临床资料、实验室部分指标、诊疗及预后的差异,进行总结归纳,进一步明确儿童恶性肿瘤合并HLH 的临床特点,从中筛选出真正影响预后的相关因素,为儿科临床医生在诊治及改善患儿生存质量方面提供新的思路。
1 资料与方法
1.1 一般资料收集2015年1月—2020年12月新疆医科大学第一附属医院儿科中心收治的55例儿童继发性HLH 患儿临床资料,根据病因分为恶性肿瘤合并HLH 组和非恶性肿瘤合并HLH 组。恶性肿瘤合并HLH 组17 例,男性11 例,女性6 例,平均年龄为6岁11 个月;非恶性肿瘤合并HLH 组38 例,男性19例,女性19 例,平均年龄为2 岁3 个月。两组患儿一般资料差异无统计学意义(P>0.05)。本研究通过新疆医科大学第一附属医院伦理委员会批准,患儿监护人签署知情同意书。
1.2 诊断标准入组标准符合国际组织细胞协会HLH-2004诊断标准[6],符合以下8条中的5条即可诊断:(1)发热超过1 周,热峰超过38.5℃;(2)脾脏肿大(肋缘下≥3 cm);(3)血细胞减少(累及外周血两系或三系),包括血红蛋白(Hb)<90 g/L,血小板计数(PLT)<100×109/L,中性粒细胞<1.0×109/L;(4)高脂血症[(甘油三酯(TG)>3 mmol/L]和(或)低纤维蛋白原血症[(纤维蛋白原(FIB)<1.5 g/L];(5)在骨髓、肝脏、脾脏或者淋巴结内找到噬血细胞;(6)铁蛋白(SF)>500 ng/mL;(7)NK 细胞活性降低或缺如;(8)可溶性CD25(sCD25)升高。
1.3 治疗方案在恶性肿瘤合并HLH 组的17 例患儿中:结合患儿病情,在排除化疗禁忌后,均给予原发肿瘤相应的化学治疗,同时给予静脉注射丙种球蛋白治疗;在化疗过程中,骨髓抑制期的患儿根据病情均积极给予输注成分血、粒细胞集落刺激因子等相应支持治疗,当合并感染时积极给予抗感染治疗。在非恶性肿瘤合并HLH 组的38 例患儿中,参照HLH-2004 指南,针对病因,积极治疗原发病,同时积极治疗HLH,辅以丙种球蛋白支持治疗;在治疗过程中,根据患儿病情,均给予支持对症处理。
1.4 观察指标
1.4.1 两组患儿病因及临床资料的收集 收集55 例HLH 患儿的病因如感染相关性、恶性肿瘤相关性、自身免疫相关性等;临床指标包括:发热、肝脾淋巴结肿大、黄疸、出血、皮疹、呼吸系统受累、浆膜腔积液、神经系统受累情况等;实验室检查结果包括:血常规(白细胞计数、中性粒细胞计数、红细胞计数、血红蛋白、血小板计数)、纤维蛋白原、甘油三酯、胆红素、血清铁蛋白、低蛋白血症(白蛋白<30 g/L)、噬血现象、乳酸脱氢酶、总胆红素、C-反应蛋白等,通过比较两组患儿的临床资料、实验室部分指标的差异,进一步明确儿童恶性肿瘤合并HLH的临床特点。
1.4.2 随访及结局 对两组患儿出院后随访1年,记录所有患儿的结局(存活或死亡)及生存时间。对于生存患儿,总生存时间定义为诊断时间至随访时间;对于死亡患儿,生存时间定义为确诊时间至死亡时间。共52例完成随访,失访3例。
1.4.3 预后及影响因素分析 根据生存时间,通过采用Kaplan-Meier法绘制两组患儿的生存曲线。以恶性肿瘤合并HLH、性别、年龄、白细胞计数、中性粒细胞计数、红细胞计数、血红蛋白、血小板计数、C-反应蛋白、纤维蛋白原、甘油三酯、铁蛋白、乳酸脱氢酶、总胆红素作为自变量,采用多因素Cox比例风险回归模型分析患儿预后影响因素。
1.5 统计学处理采用SPSS19.0 软件进行数据分析,计量资料以均数±标准差(±s)或中位数及四分位数表示,满足正态和方差齐性的组间比较采用独立样本t检验,不满足的采用非参数秩和检验;计数资料以例(%)表示,组间比较采用χ2检验。采用Kaplan-Meier方法绘制恶性肿瘤合并HLH 组和非恶性肿瘤合并HLH 组的生存曲线,应用多因素Cox比例风险模型研究预后的独立影响因素,P<0.05 为差异有统计学意义。
2 结果
2.1 两组患儿临床表现和实验室指标比较55 例HLH 患儿中,17 例患恶性肿瘤,22 例有感染症状,12例患自身免疫性疾病,4 例患有其他疾病。在恶性肿瘤合并HLH 组的17 例患儿中,急性淋巴细胞白血病有10 例,霍奇金淋巴瘤有3 例,间变大细胞淋巴瘤有1 例,急性髓系白血病有1 例,混合细胞白血病有1例,骨髓增生异常综合征1例。非恶性肿瘤合并HLH组的38例患儿中,感染相关性HLH包括EB病毒感染8例,巨细胞病毒感染1例,细菌感染2例,肝炎病毒2例,结核分枝杆菌1例,布氏杆菌2例,真菌感染3例,利什曼原虫1 例,支原体感染2 例;自身免疫相关性HLH包括系统性红斑狼疮3例,幼年型特发型关节炎6 例,干燥综合征1 例,自身免疫性肝炎1 例;肾病综合征1 例;其他分类包括2 例再生障碍性贫血,1 例朗格汉斯细胞组织增生症,1 例原因不明。在临床表现上,与非恶性肿瘤合并HLH 组比较,恶性肿瘤合并HLH 组更容易出现呼吸系统受累、浆膜腔积液、黄疸等临床表现(P<0.05);肝脾淋巴结肿大、皮疹、出血、神经系统受累等临床表现差异无统计学意义(P>0.05),见表1。与非恶性肿瘤合并HLH 组比较,恶性肿瘤合并HLH 组白蛋白及血小板计数均偏低,差异有统计学意义(P<0.05);而白细胞计数、中性粒细胞计数、红细胞计数、血红蛋白、噬血现象、C-反应蛋白、纤维蛋白原、甘油三酯、铁蛋白、乳酸脱氢酶、总胆红素水平差异均无统计学意义(P>0.05),见表2。

表1 两组患儿临床表现比较/例(%)

表2 两组患儿实验室检查结果比较
2.2 随访结果经治疗后至随访结束日期,恶性肿瘤合并HLH 组17 例患儿中,1 例失访,失访率为5.9%;3 例死亡(2 例死于肿瘤复发,1 例死于感染),病死率为18.7%。在非恶性肿瘤合并HLH 组38例患儿中,2例失访,失访率为5.3%;4 例死亡:(1) 感染相关性HLH中,1例死于感染,1例死于呼吸衰竭;(2)自身免疫性疾病相关HLH中:1例死于原发病;(3)其他病因中,1 例死于HLH+弥散性血管内凝血;病死率为11.1%。
2.3 两组患儿预后分析通过采用Kaplan-Meier法绘制两组患儿的生存曲线,结果显示恶性肿瘤合并HLH组患儿的中位生存时间为4个月,非恶性肿瘤合并HLH 组患儿的中位生存时间9 个月,两组生存情况差异有统计学意义(χ2=5.550,P=0.018),见图1。应用多因素Cox比例风险模型研究发现,恶性肿瘤合并HLH、年龄>3 岁、红细胞水平、血红蛋白浓度是预后的独立影响因素,见表3。
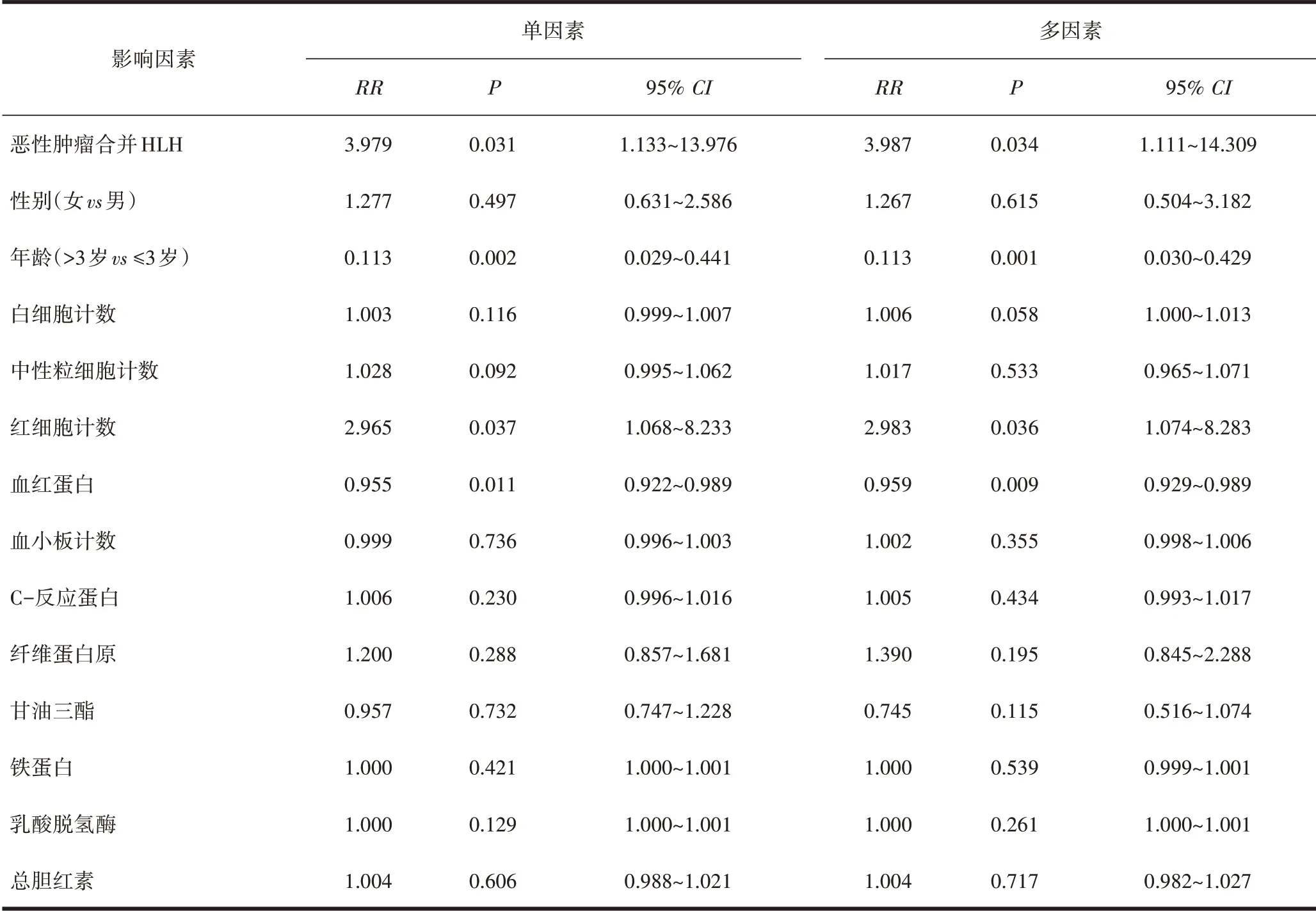
表3 预后因素Cox比例风险回归模型
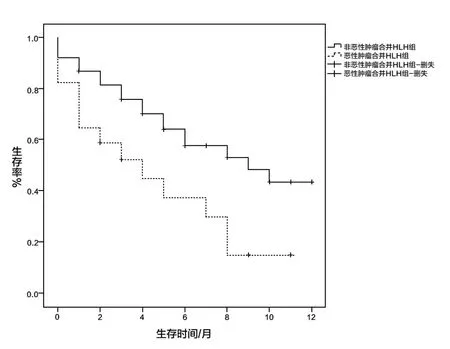
图1 两组患儿的生存曲线
3 讨论
HLH 基础性疾病多,成因复杂。研究表明,感染是HLH 的主要病因,本研究纳入的55 例患儿中,感染相关性HLH 有22 例,占40%,其中EB 病毒(Epstein barr Virus,EBV)感染占14.55%,这与张潇然等[7]的研究结果一致。相关研究提示,较为常见的易并发HLH 的恶性肿瘤有白血病、淋巴瘤等[8]。本研究中恶性肿瘤合并HLH 组的17 例患儿中,白血病有12例,和其他恶性肿瘤亚型相比,所占比例最高,究其原因,主要考虑急性白血病为儿童时期最常见的恶性肿瘤。在HLH 的众多病因中,当潜在病因是恶性肿瘤时,恶性肿瘤和HLH 在临床症状和相关实验室检查方面都有交叉和重叠之处,所以两者既互相独立又密切相关。因此,能够及时诊断HLH,对潜在的病因做出判断显得极其重要[9]。
本研究表明,恶性肿瘤合并HLH 组更容易出现呼吸系统受累、浆膜腔积液、低蛋白血症、黄疸;恶性肿瘤合并HLH 组较非恶性肿瘤合并HLH 组年龄偏大、血小板计数偏低,且总体预后较差。恶性肿瘤合并HLH 组之所以容易出现呼吸系统受累、浆膜腔积液,考虑恶性肿瘤患者经放化疗后免疫功能处于抑制状态,增加了各种病原微生物感染的几率,当炎性渗出明显时,部分患儿也可能有浆膜腔积液的表现[10]。恶性肿瘤是一种消耗性疾病,患者在放化疗时,最常见的副作用为胃肠道反应,出现饮食欠佳、呕吐等,导致合成白蛋白的原料不足;其次,在治疗过程中,化疗等药物的应用,会导致肝功能受到影响,一旦肝功能下降,导致合成白蛋白的能力下降,因此恶性肿瘤合并HLH 组更容易出现低蛋白血症。黄疸的主要反应指标为胆红素,在恶性肿瘤合并HLH 组中,积极给予病因治疗是主要措施[11],而长期应用化疗药物会引起肝功能受损,导致胆红素代谢障碍,最终引起黄疸[12]。在HLH 的病程中,患儿随着年龄的增加患恶性肿瘤的概率会越大[13],从而导致恶性肿瘤合并HLH 组较非恶性肿瘤合并HLH 组年龄偏大。而血小板计数偏低主要考虑当恶性肿瘤侵犯骨髓时,使造血功能受到抑制。同时本研究结果显示恶性肿瘤合并HLH、年龄>3 岁、红细胞水平、血红蛋白浓度是预后的独立影响因素,这一结论和李俊平[14]的研究结果一致。总之临床中应积极改善贫血状态,利于病情的控制及改善预后。本研究生存曲线提示,恶性肿瘤合并HLH 的预后较非恶性肿瘤合并HLH 偏差。有研究显示,对于部分实体瘤患者,免疫检查点抑制剂的应用取得了显著的疗效[15];当恶性肿瘤合并HLH 的患儿对化疗方案的疗效欠佳时,可考虑采用挽救治疗或应尽早采用骨髓移植治疗[16]。
综上所述,HLH 的潜在病因较多,当HLH 患儿年龄偏大,出现血小板计数偏低、低蛋白血症、呼吸系统受累、黄疸时,应警惕其潜在病因是否为恶性肿瘤。此时需积极完善相关检查,进一步明确诊断,以争取最佳治疗时间,提高患儿生存率。

