808 nm近红外光激发黑色二氧化钛对前列腺癌细胞的杀伤作用*
宫满成, 倪文君, 董文静, 袁润强
中山市人民医院 1泌尿外科, 3化疗科(广东中山 528403);2珠海市人民医院泌尿外科(广东珠海 519000)
前列腺癌是泌尿外科常见的恶性肿瘤之一,在男性罹患肿瘤中,其发病率排名第二,也是非皮肤性肿瘤中最常见的一种。在不同地区和不同种族之间前列腺癌发病率存在差异,据统计大洋洲地区发病率高于亚洲及北非地区[1-3]。癌症数据统计显示,其居男性恶性肿瘤发病率首位,病死率居第2位[2]。近年来我国的前列腺癌发病率也明显升高。虽然前列腺癌根治手术越来越完善,对于转移性前列腺癌患者,也可以采取内分泌等多种治疗方法,但是每年仍然有很多人会死于该种疾病[4]。因此寻找更好的治疗方法显得尤为重要。近几十年来,光疗包括光动力疗法(PDT)和光热疗法(PTT)[5-7],作为一种非常有前景的癌症治疗技术而受到广泛关注。光疗的作用原理是光催化而产生的活性氧(ROS)可以与癌细胞的细胞膜及其内部结合并相互反应,最终导致癌细胞的死亡[8-9],达到治疗癌症的作用。有研究学者报道,作为一种无机光敏剂,二氧化钛(TiO2)一直被用于紫外线光动力治疗癌症[10-11]。然而,在TiO2介导的光动力学治疗肿瘤的过程中,由于紫外光温度过高[12]、穿透深度过浅以及毒性[13]等原因,阻碍了其在临床的进一步研究及应用。为了解决以上问题,我们合成了一种可以被近红外光激发的黑色TiO2纳米材料。与紫外光相比,利用近红外光作为激发光解决了温度过高、穿透深度过浅以及毒性等问题,具有非常好的肿瘤治疗前景。我们于2020年3月至2021年10月进行了该实验研究(项目已通过医院伦理委员会审查)。我们采用简单的煅烧法和原位可控固相反应相结合的方法成功合成了黑色TiO2纳米材料。其具有吸收可见光和近红外光的能力,作为一种新型的光敏剂具有良好的肿瘤治疗效果。
1 材料与方法
1.1 材料 TiO2粉(包含71%锐钛矿和29%金红石)购自德国德固赛有限公司,氢化硼钠(NaBH4,98%)购自阿拉丁试剂(上海)有限公司,乙二胺、无水乙醇购自天津科美尔中国化学试剂有限公司,CCK-8购自于日本Dojindo Corp 公司。ELX800 全自动酶标仪购自美国 Bio-Tek公司,FV1000 激光共聚焦显微镜购自日本 Olympus 公司。
1.2 合成方法 将1.0 g TiO2粉(记作TP)分散于50 mL去离子水中,磁搅拌30 min。在继续搅拌的同时,缓慢滴加7 mL乙二胺至pH值达到11,将混合物转移到有3个颈连接冷凝器管的100 mL烧瓶中,并在95 ℃下维持48 h。自然冷却至室温后,收集得到的溶液,用去离子水冲洗多次,在60 ℃下干燥24 h。然后将获得的粉末在700 ℃煅烧2 h(记为TP-700)。取0.5 g制备的样品与0.5 g NaBH4在室温下充分混合30 min。然后将混合物转移至瓷船中,置于管状炉中,在350 ℃氩气中退火1 h。自然冷却至室温,得到黑色TiO2NPs(记为b-TP-700),用去离子水洗涤3次,除去未反应的NaBH4。为了比较,在同样的条件下加入NaBH4合成了未煅烧的TP(记为b-TP)。
1.3 细胞培养 人前列腺癌细胞株LNCaP购自中国科学院细胞库,使用RPMI 1640完全培养基,37 ℃、5% CO2恒温培养箱中进行培养。培养适当时间后显微镜下观察细胞形态和密度,确定细胞生长状况,待细胞密度生长至80%左右,用 0.25%的胰蛋白酶消化,按合适比例进行细胞传代,待细胞生长至对数期时进行实验。
1.4 b-TP-700的毒性检测 将前列腺癌LNCaP细胞以4×103接种于96孔板,用一系列b-TP-700浓度(0、31.25、62.50、125.00、250.00、500.00、1 000.00 μg/mL)处理细胞12、24、48 h。采用细胞计数试剂盒(CCK-8)评估细胞活力。所有实验严格按照产品说明书进行。简单的说,将上述处理好的细胞,每孔加入20 μL的CCK-8,轻轻摇晃后,放入孵箱继续培养1.5 h。酶标仪检测450 nm处的OD值。实验重复3次。
1.5 利用荧光共聚焦显微镜观察b-TP-700对前列腺癌细胞的毒性 LNCaP细胞接种于培养皿中,在37℃,含5% CO2的培养基中培养过夜。将达到80%~90%融合的细胞与1 000.00 μg/mL的b-TP-700共培养24 h。取出培养液,用磷酸盐缓冲液(PBS)冲洗多次。随后用calcein-AM和PI溶液共染细胞15 min。
1.6 CCK-8检测b-TP-700介导的光动力学对前列腺癌细胞的杀伤作用 为了检测b-TP-700介导的光动力学疗法对LNCaP细胞的治疗效果,将LNCaP细胞以4×103接种于96孔板中并培养24 h,然后更换为含有的不同浓度的b-TP-700(31.25、62.50、125.00、250.00、500.00 μg/mL)的培养液孵育。96孔板分别暴露于激光照射(1 W/cm,808 nm)0~7 min(即0、1、3、5、7 min)。利用CCK-8法检测各组细胞的活力。
1.7 检测b-TP-700介导的光动力学过程中ROS的产生量 LNCaP细胞在含有250 μg/mL的b-TP-700的培养液中培养,利用激光(1 W/cm,808 nm)照射细胞5 min,用2,7-二氯-二氢荧光双乙酸(DCFH-DA)溶液替代细胞培养液,再孵育30 min。未进行激光照射的细胞作为对照组。随后,我们利用荧光显微镜监测绿色荧光,因为活性氧(ROS)可以促使DCFH-DA转化为高荧光的2,7-二氯荧光素(DCF)。
1.8 裸鼠成瘤实验 12只BALB/c-nu雌性裸鼠,5~6周龄,体重19~23 g;通过随机数字表将12只裸鼠分为3组:(1)LNCaP细胞组。(2)250 μg/mL的b-TP-700处理组:LNCaP细胞在含有250 μg/mL的b-TP-700的培养液中培养5 min。(3)250 μg/mL的b-TP-700+激光(1 W/cm,808 nm)照射组:LNCaP细胞在含有250 μg/mL的b-TP-700的培养液中培养并利用激光(1 W/cm,808 nm)照射细胞5 min。用带6号针头的注射器抽取0.2 mL含2×107个活细胞的细胞悬液,接种于每只裸鼠的右后背部。接种3周后,麻醉无痛处死裸鼠,切取移植瘤。
2 结果
2.1 b-TP-700的毒性检测 不同浓度的b-TP-700处理LNCaP细胞,细胞的活力没有明显的降低,并且各组之间的细胞活力差异无统计学意义(P>0.05),见表1。同时我们从荧光显微镜的结果可以看出,500.00 μg/mL的 b-TP-700作用LNCaP细胞24 h后,细胞没有出现明显形态学改变,也未见明显的死细胞。见图1。

表1 不同浓度的b-TP-700处理LNCaP细胞12、24、48 h后各组的细胞活力情况
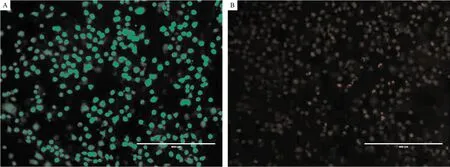
注:A:钙黄绿素染色细胞后利用荧光共聚焦显微镜观察细胞,细胞未出现明显形态学改变;B:PI染色细胞后利用荧光共聚焦显微镜观察细胞,未见明显的死细胞
2.2 b-TP-700介导的光动力学疗法对前列腺癌细胞的杀伤作用 在激光激发时间相同的情况下,随着b-TP-700浓度的增加,LNCaP细胞的活力明显下降。在相同浓度的b-TP-700作用于LNCaP细胞时,随着激光激发时间的延长,LNCaP细胞的活力明显下降(P<0.05),见表2。

表2 不同浓度的b-TP-700及不同的激光激发时间对LNCaP细胞活力的影响
2.3 检测b-TP-700介导的光动力学疗法中ROS的产生量 在激光的激发下,b-TP-700组可以检测到由DCF产生的明显的绿色荧光(图2-A),相反,在对照组中却几乎观察不到明显的绿色荧光(图2-B)。
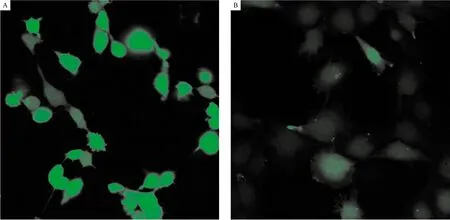
注:A:250 μg/mL的b-TP-700作用于LNCaP细胞,并利用激光激发5 min;B:对照组没有激光激发
2.4 裸鼠成瘤实验 250 μg/mL的b-TP-700+激光(1 W/cm,808 nm)照射组形成的肿瘤明显小于LNCaP细胞组和250 μg/mL的b-TP-700处理组,差异有统计学意义(P<0.05)。LNCaP细胞组和250 μg/mL的b-TP-700处理组所形成的肿瘤大小差异无统计学意义(P>0.05),见图3。

注:A:裸鼠成瘤实验所形成的肿瘤组织;B:裸鼠成瘤实验的结果
3 讨论
我国前列腺癌发病率与病死率逐年增加,已成为威胁男性健康的主要疾病。2018年全球癌症统计结果显示,全球前列腺癌新发病例约130万,有35.9万人因前列腺癌而死亡。在世界范围内,前列腺癌的发病率仅次于肺癌[14],占男性恶性肿瘤的第2位。因此,寻找一种有效的前列腺癌的治疗方式显得尤为重要。
光动力疗法是一种非常有前景的癌症治疗技术,近几十年来得到了飞速发展而受到广泛关注。光动力疗法主要从以下3个方面起到杀伤肿瘤细胞的效果:第一,直接杀伤肿瘤细胞。光动力疗法通过直接作用于线粒体、细胞膜以及溶酶体发挥其肿瘤杀伤作用。光动力疗法作用于线粒体会促使细胞发生凋亡,光动力疗法作用于溶酶体会促使细胞出现自噬,光动力疗法作用于细胞膜会诱导细胞发生坏死。目前的研究结果显示这几种方式都参与了光动力疗法对肿瘤细胞的杀伤作用[15]。第二,光动力疗法产生的活性氧损伤肿瘤内部血管内皮细胞,导致血流停滞与渗漏,从而起到杀伤肿瘤的效果。第三,光动力疗法发挥作用过程中会产生大量的炎性细胞因子,导致肿瘤免疫抑制,可以长期抑制肿瘤细胞的生长。在光动力疗法发挥杀伤肿瘤作用的过程中,光敏剂是光动力疗法发挥作用的基础,其在特定波长的激发光照射下起着能量传递的作用,进而产生活性氧类细胞毒性物质。因此,光敏剂的优劣是制约光动力疗法发展的关键因素。
近年来,随着纳米技术的迅速发展,纳米材料为光动力学治疗带来了新的契机。纳米材料是指介于1~100 nm的材料,因其特殊的尺寸而使其拥有更高的可塑性,在肿瘤治疗领域具有广泛的应用前景[16]。由于实体瘤血管壁间隙较宽、血管密集、淋巴回流受阻,对大分子物质具有滞留性和选择高通透性,而正常组织则恰恰相反[17]。实体瘤内的这种现象被称为增强渗透与滞留效应(enhanced permeability and retention effect,EPR),可使纳米材料进入并停留于肿瘤组织[18],属于被动靶向效应。纳米材料具有生物相容性,不会向免疫系统发出警报,并且可生物降解形成无害的代谢产物[19]。综合以上纳米材料的各种特性,奠定了纳米材料在肿瘤治疗领域的重要地位。
TiO2作为一种无机光敏剂,一直被用于紫外线光动力治疗癌症[10-11]。然而,随着研究的逐步深入,研究学者逐步发现紫外光产生的温度过高[11],而且紫外光穿透深度不足以及紫外光本身具有一定的毒性[13],所以以TiO2作为光敏剂的光动力学疗法一直没有应用到临床。针对以上困境,我们将TiO2经过高温煅烧,改变了其吸收光谱,我们称之为黑色TiO2。与之前的TiO2需利用紫外光激发相比,黑色TiO2利用近红外光作为激发光解决了温度过高、穿透深度过浅以及毒性等问题,具有非常好的肿瘤治疗前景。我们研制的黑色TiO2其吸收峰位于近红外区600~800 nm之间(红色到深红色),非常适宜做光动力疗法光敏剂。因为波长过高的激光能量较低不能激发氧分子最终形成ROS,而波长过低的激光其穿透组织的深度则不够(激光的波长与其穿透组织的深度成正比)[20]。
首先我们利用CCK-8实验检测黑色TiO2的毒性,从我们的CCK-8的实验结果可以看出用含有不同浓度的黑色TiO2的培养液培养LNCaP细胞,前列腺癌LNCaP细胞的活力未见明显的变化。这表明黑色TiO2本身没有细胞毒性。从荧光显微镜的结果我们可以看出,黑色TiO2并不会引起细胞形态的改变。这也进一步证明了黑色TiO2本身没有细胞毒性。随后我们研究发现利用808 nm的激光激发后,随着黑色TiO2浓度的增加及激光照射的时间延长,LNCaP的细胞活力明显降低。该实验结果证明了黑色TiO2作为新型的光敏剂,在808 nm的激光激发下,通过光动力学作用能明显的杀伤肿瘤细胞,降低细胞的活力。为了进一步探讨黑色TiO2作为光敏剂通过光动力学疗法杀伤肿瘤细胞的机制,我们检测了黑色TiO2作为光敏剂介导光动力学治疗过程中活性氧的产生量。从实验结果我们可以看出,利用808 nm激光激发黑色TiO2介导的光动力学治疗过程中有大量的活性氧产生,这可能是黑色TiO2作为光敏剂通过光动力学疗法杀伤肿瘤细胞的机制之一。在裸鼠成瘤实验中我们发现利用黑色TiO2介导的光动力学疗法处理过的LNCaP的成瘤能力明显降低,在体内实验水平验证了黑色TiO2作为光敏剂通过光动力学疗法杀伤肿瘤细胞的可行性,为前列腺癌的治疗提供了一种新的思路、新的方法。
综上所述,我们自主研发的黑色TiO2可以作为一种新型的无机光敏剂,其可以被808 nm激光激发,在黑色TiO2介导光动力学疗法过程中产生了大量的ROS,对前列腺癌细胞具有明显的杀伤作用,有望成为一种新的、有效的前列腺癌的治疗方法。
利益相关声明:所有作者均声明无利益冲突。
作者贡献说明:课题设计:宫满成、倪文君。细胞实验及动物实验:宫满成、董文静。论文撰写及修改:宫满成、董文静、袁润强。

