影响1-羟基-2-氧-1,8-萘啶-3-甲酰胺类HIV整合酶链转移抑制剂抗整合酶链转移活性的主要因素
康家雄,李爱秀,靳玉瑞
目前,人类免疫缺陷病毒(human immunodeficiency virus, HIV)感染引起的艾滋病(acquired immunodeficiency syndrome, AIDS)严重威胁人类健康。HIV整合酶(integrase, IN)是病毒复制过程中的关键酶,负责将病毒RNA经反转录合成的双链DNA整合到宿主细胞DNA中,该整合过程包括3′-加工(3′-processing,3′-P)和链转移(strand transfer, ST)阶段。近年来,病毒DNA与宿主DNA连接的ST阶段是以IN为靶标开发抗HIV药物的关注热点,现已有5个整合酶链转移抑制剂(integrase strand transfer inhibitors, INSTIs)被FDA批准用于治疗AIDS患者/HIV感染者,包括第一代雷格特韦(raltegravir, RAL)、埃替格韦(elvitegravir,EVG)和第二代多替拉韦(dolutegravir, DTG)、比特拉韦(bictegravir, BIC)和卡博特韦(cabotegravir, CAB)。通过对INSTIs疗效和耐药性的研究表明,RAL和EVG因低耐药基因屏障和强交叉耐药性导致疗效受限,DTG、BIC和CAB具有相对较好的耐药基因屏障,对部分RAL/EVG耐药突变毒株仍具有一定的抑制效力。HIV作为一种高变异性RNA病毒,易对包括INSTIs在内的抗HIV药物产生耐药性,尤其是交叉耐药性,增加了AIDS患者治疗失败、疾病进展及死亡的风险。因此,开发低毒、高效、选择性强的新型INSTIs具有重要意义。1-羟基-2-氧-1,8-萘啶-3-甲酰胺因细胞毒性低、选择性指数高且对RAL/EVG/DTG耐药突变毒株具有高抑制效力,近年来已成为研发INSTIs极具吸引力的结构母核。本研究采用遗传函数逼近法(genetic function approximation, GFA)构建了10个1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs的二维定量构效关系(2d-quantitative structure-activity relationship, 2D-QSAR)模型,选出最优模型,探讨影响抑制剂抗INST活性的主要微观结构因素。
1 材料与方法
1.1 选择软件 CambridgeSoft公司开发的Chem Draw 16.0软件,IBM公司开发的SPSS Statistic 22.0软件,Accelrys公司开发的Discovery Studio 2.5软件,Graphpad公司开发的Prism 7.0软件,和Tripos公司开发的SYBYL8.1软件,Chemical Computer Group公司开发的MOE2009.10软件。
1.2 1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs的结构与活性数据 采用文献[14]报道的32个1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs,其化学结构与活性数据分见图1和表1。将所有抑制剂的活性数值IC转化成pIC(-logIC),数值分布范围为4.02~8.70,其中IC代表抑制剂抗INST活性的半数抑制浓度(单位为μmol/L)。
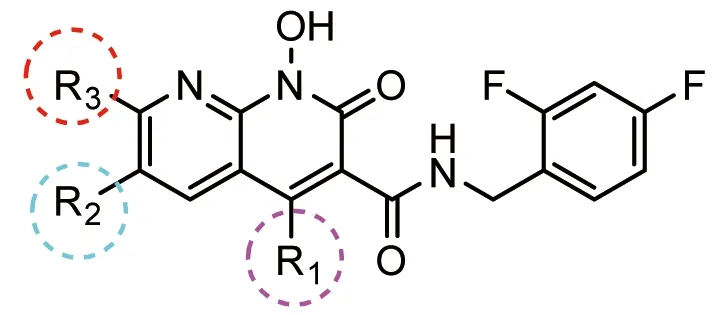
图1 INS TIs抑制剂的化学结构

表1 INS TIs的抑制剂的实验值、预测值及残差
1.3 分子结构优化 药物构象对药效有较大影响,因技术限制尚未解析出HIV IN全酶晶体结构,未获取药物与受体IN结合的活性构象,故采用分子的低能构象作为可能的药效构象进行替代研究。采用SYBYL8.1软件对32个化合物进行能量优化以得到其低能构象,参数选择Powell能量梯度法,Tripos力场,迭代次数1000,Gasteiger-Huckel电荷,能量收敛限定Gradient为0.001 kal/J。
1.4 描述符选取与数据集拆分 采用Discovery Studio 2.5软件计算32个化合物的电拓扑状态、空间等265个描述符,剔除为0的描述符剩117个描述符。利用SPSS Statistic 22.0软件分析117个描述符的相关性,将相关系数>0.7的描述符任意择其一剔除,剩31个描述符用于2D-QSAR研究(表2)。根据随机挑选原则,以3∶1的比例拆分数据集。其中,训练集包含24个化合物,用于构建2D-QSAR模型,测试集包含8个化合物,用于验证2D-QSAR模型的可靠性。

表2 用于构建2D-QSAR模型的描述符

2 结 果

pIC=-2.763+5.9522JX-0.051507Dipole_mag+0.022866Jurs_PNSA_1-0.039667Strain_Energy
公式(1)



表3 最优2D-QSAR模型的4个描述符
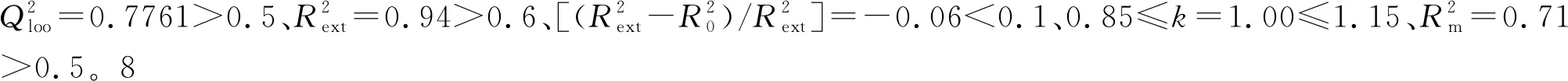

图2 训练集与测试集化合物实验值与预测值的线性拟合示意图
3 讨 论
1-羟基-2-氧-1,8-萘啶-3-甲酰胺因细胞毒性低、选择性指数高且对RAL/EVG/DTG耐药突变毒株具有高抑制效力,近年来已成为研发INSTIs极具吸引力的结构母核。目前,有关1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs的研究主要集中于结构骨架C-3位侧链苯基、C-4位、C-6位及C-7位的结构修饰及抗INST、抗HIV的药理活性测试方面,影响抑制剂抗INST活性的分子微观结构因素尚不明确。定量构效关系(quantitative structure-activity relationship, QSAR)作为计算机辅助药物设计的四大核心技术之一,可用于探究药物微观结构与生物效应之间的定量关系,现已被广泛应用于药物、农药等生物活性分子的合理设计中。本研究选取Zhao等报道的32个1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs为研究对象,采用GFA构建抑制剂抗INST活性与选择的微观结构描述符之间的2D-QSAR模型,并基于优选的最佳模型探析影响抑制剂抗INST活性的主要微观结构因素,以期为抑制剂的进一步合理设计与结构修饰提供理论依据。
从本实验构建的最优2D-QSAR模型见公式(1)可知,描述符JX、Dipole_mag、Jurs_PNSA_1和Strain_Energy是影响1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs抑酶活性的主要微观结构因素。根据描述符系数的绝对值可以看出,JX是影响1-羟基-2-氧-1,8-萘啶-3-甲酰胺类INSTIs抗INST活性的最重要微观结构因素,而Dipole_mag、Strain_Energy和Jurs_PNSA_1对活性的影响相对较小。Balaban的J指数是Balaban于1982年根据Randic联通性指数X的类似形式定义的一种新的拓扑指数,其特点是简并度较低、结构选择性高。该指数是建立在分子图加权后的距离矩阵基础上而构造产生的,对芳香键与单键予以区分,其能较为全面地反映分子的构造结构信息。JX属于Balaban的J指数,其与活性成正相关性,且相关系数的绝对值最大,意味着增大该参数值能显著提高抑制剂的抗INST活性(如化合物10>化合物16)。Dipole_mag是指分子摩尔偶极距,其与活性成较小的负相关性,其显著增大表明对活性不利(如化合物3<化合物30)。Strain_Energy即应变能又称变形能,是指以应变和应力的形式贮存于分子内部的势能,其与活性成较低负相关性表明分子中增加该值对活性不利(如化合物12<化合物2)。分子局部电荷表面Jurs参数是由原子的部分电荷映射到原子的溶剂可及表面积上计算得出的,该套参数结合了分子形状和电子信息等特征,常用于表征分子在生物体内的传输特性。属于分子局部电荷Jurs参数的Jurs_PNSA_1是指分子中部分负电荷原子的溶剂可及表面积的总和,与活性成正相关,表明增大该值可提高抑制剂的抗INST活性,但其相关系数的绝对值最小,故对抑制剂抗INST活性影响很小(如化合物22>化合物20)。


