基于项目化学习的化学计算教学探索
李芳芳 沈坤华


摘要:以“配制84消毒液”为项目主题,开展与物质的量有关的各种化学计算教学,学生通过“计算制取氯气时各种反应物的需求量、生成物的产量、电子的转移量“制取84消毒液时氢氧化钠的需求量…‘构建氧化还原类型计算模型”三个项目任务,将各种物理量的计算结构化,可视化。
关键词:项目化;化学计算:物质的量;84消毒液
文章编号:1008-0546( 2022 )llx-0019-04
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2022.llx.005
一、问题提出及研究现状
《高中化学课程标准(2017年版2020年修订)》(以下简称《课标》)中提出了项目化学习的概念。[1]项目式学习(Problem based learning或Project basedleaming,简称PBL)是一种创造性解决实际问题的学习方式,注重帮助学生解决真实世界中复杂、非常规具有挑战性的问题,是以小组合作的形式,培养学习者沟通合作、批判创新的高阶认知能力和工作方式。
PBL要与《课标》对应,一旦两者对应起来,就能确保这份学习经历是值得投入时间,学术的严谨性就建立起来了。《课标》要求能运用定量计算说明物质的组成与变化;能从质量守恒分析化学变化,用化学计量单位定量分析化学反应及其伴随的能量转化;能从定性和定量结合上收集证据,通过定性分析和定量计算推出合理结论;能用数据、图表、符号等处理实验信息。化学计算是中学化学中一个重要的组成部分,也是学生在化学学习中的一个难点,学起来枯燥乏味,在评价测试中又不易得分。怎样调动学生学习化学计算的积极性,选用最合适的方法准确而快速地解决计算问题,对于学生提高学习效率有着重要的意义。在实际的教学过程中要贴近生活、社会实际,重视化学与其他学科的联系,充分认识化学实验的独特价值,精心设计实验探究活动,创设真实且富有价值的问题情境,促进学生化学计算学习方式转变,实施“教、学、评”一体化。[2]本设计以“配制84消毒液”为项目主题,适合在学业水平测试复习或选考科目一轮复习中化学计算模块展开教学。
二、设计思路
项目化学习的本质特征有“四真”:真实目标、真实情境、真实学习、真实评价。确定真实目标,根据课程主题和核心内容选择真实情境并形成课堂目标,课堂目标指向解决更高水平的真实问题,在问题的解决中落实核心知识、素养、方法、思维。图1是本课的设计思路。
1.选择真实的情境
真实的情境贴近生活实际,让学生在不知不觉中进入学习的状态,本节课主要是化学计算的复习,若是按部就班地给出一些计算题目让学生做后再讲,会使课堂过于沉闷,学生兴趣不高,效率低下。
将核心素养更好地落实到核心知识中来,打破计算知识的零碎化,利用疫情期间一瓶难求的84消毒液作为本节课的核心素材,借用制取消毒液这个真实情境来制定学习目标,安排教学任务。
学习目标如下:
(1)通过制取84消毒液,回顾无机物转化的一般方法,提高实验设计和分析的能力,强化变化观念与平衡思想。
(2)通过定量的计算,找到制备过程中最合适的药品取用量,培养问题分析和问题解决能力。
(3)掌握氧化还原反应电子转移量的计算。
(4)通过实验的改进,药品无污染化处理,增强学生的科学态度与社会责任感。
2.设计有效的情境问题
化学源于生活,寓于生活,用于生活,在教学过程中如果从学生熟悉的生活场景来设问引入,可以引导学生一步步地走向学习的目标。在本节课的开头,从新冠肺炎疫情出发,消毒液一瓶难求,你有好办法吗?提问式引入,引导学生回忆消毒液的成分和如何制取。紧接着抛出另一个问题:实验室如何制氯气?引导学生回顾实验室制取氯气的方法.引出化学方程式:2KMnO4+ 16HCl - 2MnCl2+2KCl+SCl2↑ +8H2O,进入正题,进行与物质的量有关的一系列计算。
三、教学实录
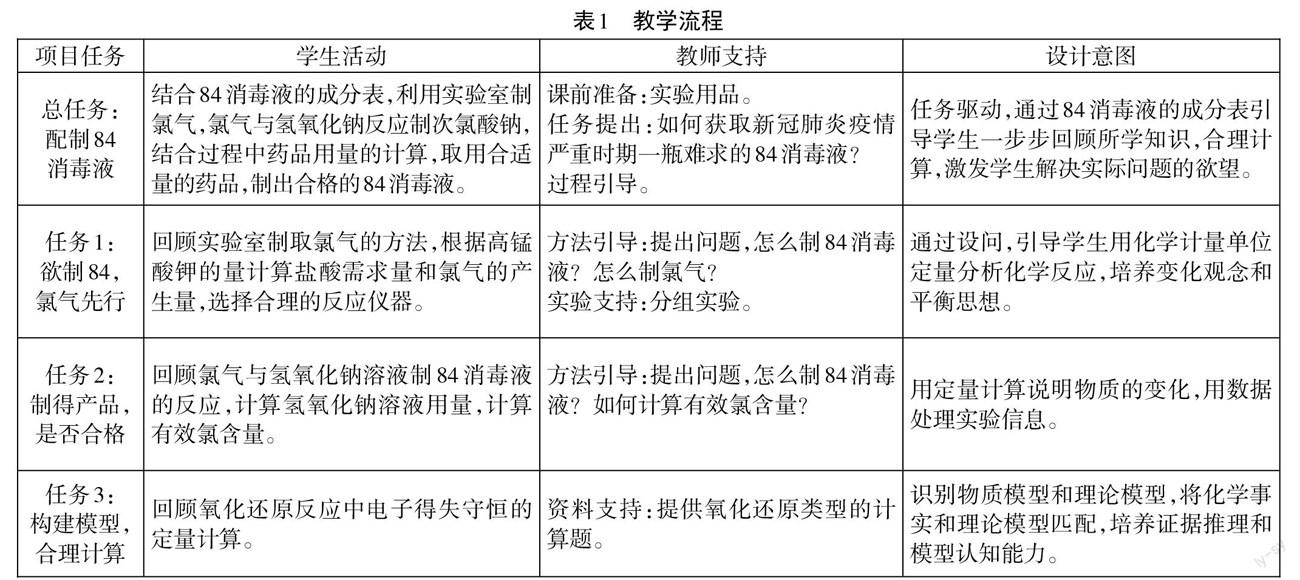
本设计以“配制84消毒液”为项目主题,教学流程如表1。
1.创设情境
[引入情境]这段时间,新冠病毒又有抬头,想当初,84消毒液一瓶难求,如果这个难题摆在你面前,你有什么好办法吗?
[展示]一瓶84消毒液,有效成分:次氯酸钠。
[生]自己制。
[问题驱动1]我们怎么制氯气呢?
[生]学生各种回答:可以用二氧化锰和浓盐酸加热,高锰酸钾和盐酸,电解饱和食盐水……
[师]实验室常用二氧化锰和浓盐酸加热制氯气,也可用高锰酸钾和盐酸,请大家写出二氧化锰和高锰酸钾分别和盐酸反应的方程式。
[学生]书写反应方程式。
2.欲制84,氯气先行
[问题驱动2]现在有药品:KMnO4固体和10 mol/L的盐酸,仪器:大针筒若干。老师在大针筒中加入了0.316 g KMnO4固体(M=158 g/mol),请问:①为了不浪费药品,吸人多少毫升盐酸比较合适?②考虑气体的产量,应选用什么规格的大针筒来收集气体?(可供选择的针筒有50 mL、100 mL、200 mL;常温常压下,气体的摩尔体积约为24.5 Umol)
[生]列方程式進行计算,教师投影展示。
[师]通过计算,制取氯气的时候需选用200 mL的针筒,现在每个小组桌上,药品有KMnO4固体、浓盐酸、氢氧化钠溶液;仪器有大针筒若干,三通阀。先拔出200 mL针筒的活塞,往针筒内加入电子天平称出的0.316 g KMnO4固体,装上活塞,推到最里面,连接到三通阀的一端,再用另一个较小的针筒吸取稍大于1.6 mL的浓盐酸(为了使KMn0。反应更充分),接到三通阀另一接口,调节阀门使两针筒相通,将浓盐酸推入装KMnO4固体的大针筒,观察反应进行。如图2,图3所示。
[学生分组实验]观察现象,针筒中产生黄绿色气体。
[追问]假设刚才我们的实验过程中KMnO4(0.316 g)全部消耗完,反应过程中转移了多少个电子?
[生]计算,教师展示学生书写的计算过程。
求得电子转移量为0.01 NA。
[问题驱动3]如何利用刚才得到的氯气来制取84消毒液?
[生]用氢氧化钠溶液吸收。
[师]我们来计算一下,要把0.005 mol的氯气全部制成84消毒液,理论上需要2.0 mol/LNaOH溶液多少mL?
[学生分组实验]用针筒吸取25 mL NaOH溶液,接上三通管后,联通装氯气的针筒,观察针筒内气体体积的变化。
[追问]我们来算一下,这样制出来的84消毒液中有效氯的理论含量有多少?能不能和市面上出售的84消毒液媲美。一般市面上的84消毒液的有效氯含量在4%-7%左右。(84消毒液有效氯指含氯化合物中氧化能力相当的氯气量。算法:次氯酸钠的物质的量×2×35.5÷消毒液质量,0.4 mol/LNaOH溶液密度近似等于1.1g/mL)
[生]计算得[0.005×2×35.5÷(0.005×2×35.5+5×1.1)]×100%-6%,合格。
[师]刚才我们计算并实践了氯气与氢氧化钠溶液反应制84消毒液的过程。Cl:与冷的NaOH溶液反应:Cl2+2NaOH=NaCl+ NaClO+H2O,产物就是84消毒液的主要成分。但是实际上这个反应是放热的,随着反应温度升高还会有副反应,Cl:与热的NaOH溶液反应:3Cl2+6NaOH=△=5NaCl+ NaClO3+ 3H2O。
[真题展示]Cl:与NaOH溶液反应可生成NaCl、NaCIO和NaCl03,c(CI-)和c(ClO-)的比值与反应温度有关。用24 g NaOH配成的250 mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应及溶液体积变化)。求:(I)NaOH溶液的物质的量浓度____mol/L。
(2)某温度下,反应后溶液中c(Cl-)= 6c(ClO-),则溶液中c(CIO-)=____mol/L。
[模型构建]
氧化还原型的计算关键是找到电子得失守恒和原子个数守恒,再列出相应的方程式进行解答。
本试题要求学生能运用化学符号和定量计算等手段说明物质的组成及其变化,能从质量守恒的观点看待和分析化学变化,能运用化学计量单位定量分析化学变化。
四、教学反思
项目化学习要求在课前有明确的项目主目标(制取一瓶84消毒液);在教学实施过程中对项目进行拆解,制定具体的项目规划(次目标有:如何制取氯气?有了氯气怎么制84消毒液?);引导学生自主学习,合作探究(通过计算如何选择合适的药品量,仪器规格),项目终端要有产品展示(得到84消毒液),评价交流(有效氯含量如何?)。
1.有效情境,环环相扣
真实的情境素材能唤醒学习意愿,链接旧有知识,引起情感共鸣,让学生从中发现与学习有关的问题,构建概念、提炼观点、训练思维、情感共鸣……情境素材越是贴近生活,越能驱动学生积极参与。本节课将枯燥的化学计算寄托在物质制取的真实情境下,让学生带着明确的目的去计算,为后续的84消毒液的制取打下理论基础。如在用针筒制取氯气的时候学生会想,要是计算不准确的话选错了针筒,容积不够,氯气泄漏出来后果就不堪设想!
2.减少污染,注重环保
用针筒来制取氯气的装置密封性非常好,现场几乎闻不到刺激性气味,包括氯气的处理全部在针筒内完成,在教室内做这个实验完全没有污染。
3.课后延伸,深度学习
课后学生围着实验仪器很感兴趣,有位同学发现原来无色的浓盐酸有点发黄,顺着这个疑惑,让学生去找原因,引导几个比较感兴趣的同学形成了一个研究小组。他们重复课堂上制取氯气的实验,反复研究后得出一条大家都觉得可行的结论:实验过程中,从盐酸的试剂瓶里吸取液体时用到了不锈钢制取的针头,查阅资料发现,常用的不锈钢针头为铁素体不锈钢,除了主体元素为铁元素以外还含11%-30%的铬元素,以及少量的钼、钛、铌等元素。当针头进入盐酸溶液吸取液体时,与盐酸反应形成二价铁,二价铁在空气中慢慢被氧化成三价铁之后颜色就出现黄色了。当学生得出这一结论后,再引导学生试着用实验验证。研究小组的同学将针头取下后浸泡在盐酸里,24小时后盐酸的颜色变成了绿色。用硫氰化钾检验有血红色产生,说明的确有三价铁离子生成,但是为什么颜色那么绿呢?联想到三价铬离子的颜色也是亮绿色的,应该是铬也与盐酸反应出现了三价铬离子,由于条件有限,未能后续验证。通过這次研究小组的学习,将课堂上发现的问题进行自主研究,不仅解了疑惑,还对合金、铁及其化合物的知识有了更深刻的认识。将短短40分钟的课堂学习延伸到课堂之外,拓展了学习场域,实现了深度学习。
参考文献
[1] 中华人民共和国教育部.普通高中化学课程标准(2017年版2020年修订)[s].北京:人民教育出版社,2020.
[2] 王磊.基于学生核心素养的化学学科能力研究[Ml.北京:北京师范大学出版集团,2017.

