螯合剂强化Fe/过硫酸盐体系的研究进展
周明亮,林英姿,b
(吉林建筑大学 a.松辽流域水环境教育部重点实验室;b.市政与环境工程学院,吉林 长春 130118)
由于硫酸根自由基具有很强的氧化性能,能高效去除难降解污染物,所以近些年基于硫酸根自由基的高级氧化技术备受关注,被广泛应用于地表水、地下水、土壤修复等领域[1]。过一硫酸盐(PMS)和过二硫酸盐(PDS)是产生硫酸根自由基的几种最基本的途径[2],活化过硫酸盐的技术热活化、超声活化[3]、光活化、辐射活化、金属活化、碳材料活化[4]和有机物(如酚类,醌类等)活化[5]等,在所有已报道的有效过渡金属中,铁因其丰度大、效率高和环境友好的特性更适合广泛使用[6]。虽然Fe2+活化过硫酸盐可以降解有机化合物,但是Fe2+活化PS 技术仍有局限性,一方面,Fe2+快速转化为Fe3+导致PS活化快速停止,另一方面,过量的Fe2+导致众所周知的清除硫酸盐自由基,如式(R1)所示,这导致氧化效率下降[7]。采用零价铁(ZVI)可以更充分地利用Fe2+和更少的自由基淬灭来提高氧化效率[8],但是Fe2+在随着反应过程的进行而逐渐变成Fe3+会导致沉积物和铁泥的形成。使用金属螯合剂能使沉积物溶剂化并且可以活化过硫酸盐从而促进污染物的分解,所以近些年有学者利用金属螯合剂来强化Fe/过硫酸盐体系。通过在反应体系中加入金属螯合剂使Fe0羟基化,从而抑制Fe0表面氧化铁的形成,促进铁离子从Fe0表面释放,一方面通过增大及保持铁离子在体系中的浓度,拓宽了铁/过硫酸盐体系反应的pH 适用范围;另一方面螯合剂的加入也可以充分保持金属离子的氧化态和还原态[9],从而维持Fe2+在体系中的含量。金属螯合剂可分为有机和无机两类。
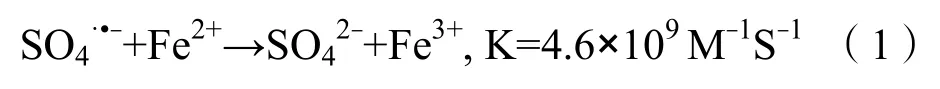
1 无机螯合剂强化Fe/过硫酸盐体系
1.1 无机聚磷酸盐
无机聚磷酸盐,包括焦磷酸钠(TSPP)、六偏磷酸钠(HXMP)、三聚磷酸钠(STPP)等。其价格较低螯合能力中等,有优异的扩散与胶溶力,但其容易水解失效尤其在较高温度下。使用无机聚磷酸盐可以达到减蚀的效果但要求水中需要有足够的钙离子浓度,因为水中若没有Ca2+或Ca2+浓度过低,就不能形成良好的保护膜而无法缓蚀,同时无机聚磷酸盐本身易与钙、镁等金属离子结合形成水垢,且pH适用范围较窄只适用于碱性介质,而且更为严重的问题是造成水体富营养化。所以人们长期以来就一直在研发新型的金属螯合剂,以取代传统聚磷酸盐。
1.2 亚硫酸盐螯合剂
亚硫酸盐(Na2SO3,S(IV))是一种典型的工业污染物,是一种优良的还原剂,广泛用于废水处理[10-11]。亚硫酸盐的还原性可加速Fe3+还原为Fe2+,从而在较宽pH 范围内显著增强废水中污染物的催化去除[12]。亚硫酸盐离子是三角形的锥形结构,其中S 原子含有孤对电子作为配位原子,铁可以提供SO32−的空位轨道从而形成复合体。此外,Fe/O2/S(IV)络合物在有氧的情况下能产生许多活性物质,如SO3•−和SO5•−。据报道,氧气在产生SO4•−中起重要作用,使用亚硫酸盐可作为引发剂[13]。此外,S(IV)和Fe3+之间的直接络合过程(R1)可形成FeSO3+络合物,该络合物可逐渐分解为Fe2+和SO3•−(R2),生成 SO3•−,SO4•−,通过各种链式反应(R3)-(R4)生成强氧化性的自由基[11]。
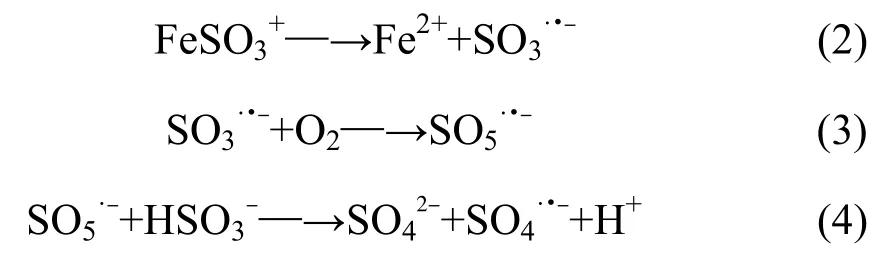
2 有机螯合剂强化Fe/过硫酸盐体系
2.1 氨基羧酸型螯合剂
最常见的氨基羧酸型螯合剂有乙二胺四乙酸(EDTA)、硝酸三乙酸(NTA)、二乙烯三胺五甲酸(DTPA)、N,N'-乙二胺二琥珀酸(EDDS)、N-羧基乙基乙二胺三乙酸(HEDTA)等。这些氨基羧酸盐非常稳定不易水解。它们的钠盐具有非常高的溶解度和强大的络合能力,并且它们具有较大的络合稳定常数和良好的耐碱性,但它们的分散性较弱,不容易被生物降解。由于EDTA 与铁离子的强络合效能,并能够加速Fe2+的溶出使其参与均相反应,是基于螯合剂强化过硫酸盐体系的研究中使用最多的螯合剂[14]。虽然EDTA 既便宜又方便,但其主要缺点是释放到环境中会产生相关的环境后果。EDTA 属于极难降解的螯合剂,由于较差的光、化学和生物降解性而延长其持续性,在某些情况下,它可能会强化相应毒性效应的阈值。EDTA 在水生环境中的不可生物降解性以及其造成的毒害性是其实际应用的绊脚石。
为解决传统Fe(Ⅱ)活化过硫酸盐过程中Fe 有效性较低的问题,王琰涤[15]等采用可生物降解的EDDS(乙二胺二琥珀酸)螯合Fe(Ⅲ)活化过硫酸盐处理水溶液中的TCE(三氯乙烯),实验得出Fe3+与过硫酸盐反应降解TCE 的降解率在10%以下,当加入EDDS 后60 min 内TCE 去除率可达99.7%。结果表明EDDS 螯合Fe(Ⅲ)活化过硫酸盐技术能够产生以·•OH 为主的活性氧自由基,从而快速高效去除水溶液中TCE。
NTA 螯合能力极强,其经济效益远高于传统络合剂EDTA[16],且易被生物降解,在Y.V.Nancharaiah的报道中在好氧条件下微生物颗粒能够完全降解NTA 与Fe3+/Fe2+形成的络合物[17]。马红芳[18]等采用NTA 强化零价铁/过硫酸盐降解橙黄G,结果表明NTA 能够强化Fe0/PMS 体系降解OG 的氧化效能,加入NTA 后,体系中生成的Fe3+/Fe2+能与其迅速形成络合物,既缓解了Fe0表面钝化层的形成,促进Fe0界面对PMS 的直接活化,又提高了溶液中溶解性铁的浓度,促进均相作用对PMS 的活化分解。
亚氨基二琥珀酸(IDS)是一种新型的氨基多羧酸螯合剂,具有强的螯合过渡金属分子能力以及优异的可降解性[19]。尤洪星[20]发现IDS 对大多数金属的螯合能力接近EDTA 的水平,在螯合Fe3+以及Cu2+时效果远远好于EDTA,并且在碱性条件下仍有较好的螯合性能。由于它优良的生物可降解性能,我们可以预料在不久的将来,它会广泛取代目前的金属螯合剂而运用于各类氧化还原体系。
2.2 羟基羧酸型螯合剂
羟基羧酸,如酒石酸(TA)、草酸(Ox)、葡萄糖酸(GA)、柠檬酸(CA),没食子酸(GA)等,螯合力较强,但分散力较差,更易于被生物化学降解[21]。但羟基羧酸和过渡金属离子之间产生的螯合体稳定性并不高,只能在高pH 值环境和过量螯合物的出现下,才能更高效地掩蔽碱土金属分子。酒石酸的螯合力相对较弱,而草酸、葡萄糖刺激酸等则属强力螯合物,其中以葡萄糖刺激酸最为良好的全能螯合物。而柠檬酸钠则对钙镁以及土壤中重金属离子的螯合力都很强,且对人类健康和自然环境都相对安全。
Liang[22]等在Fe/过硫酸盐体系中使用柠檬酸作为螯合剂,试图通过提供合适的螯合物/Fe2+摩尔比来控制溶液中亚铁离子的含量。结果为柠檬酸/Fe2+摩尔比为1/5 时处理效果最佳。
Xue[23]对比了Fe3O4/H2O2均相体系下EDTA、琥珀酸、柠檬酸、酒石酸和羧甲基-β-环糊精(CMCD)六种螯合剂的加入对体系降解PCP 的影响,研究发现,六种螯合剂都可以显著促进氧化铁中铁离子的溶解,溶液中的螯合剂结合会于浸出的铁离子相结合,启动均相芬顿链式反应,促进污染物的降解。结果表明在Fe3O4/H2O2均相体系中草酸的促进效果最好。
Dong[24]等发现GA 可以促进Fe(III)/Fe(II)循环并生成更稳定的[Fe(III)(GA)]+,[Fe(III)(GA)2]-,[Fe(II)(GA)]和[Fe(II)(GA)2]2−并促进PS 分解从而产生更多自由基,可大幅提升PS/Fe 体系降解碘帕醇,甲基橙(MO)、刚果红(CR)和双氯芬酸(DCF)等污染物的效能和速率,并发现GA 在活化PS/Fe(III)方面优于EDTA、EDDS 和CA,原因是GA 具有更高的电子转移效率。
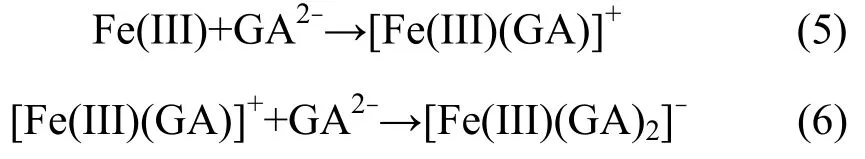
2.3 聚羧酸型螯合剂
丙烯酸(PAA)、甲基丙烯酸(MMA)、马来酸酐(HPMA)、衣康酸等都属于具有羧基的复合单体共聚后的高聚物,在某种条件下可起到与螯合物质相似的效果。聚羧酸型螯合物的最大的优点是有优异的胶体特性和扩散功能,且pH 值适用范围广,但其络合力较弱,所以需将其加以共聚或改性以提高螯合性能。
2.4 有机磷酸盐型螯合剂
氨基三亚甲基磷酸盐(ATMP)、羟基亚乙基二磷酸(HEDP)、乙二胺四亚甲基磷酸(EDTMP)、二乙烯三胺五甲叉膦酸(DTPM-PA)等都属于有机磷酸盐类螯合剂。这类金属螯合剂的螯合力比氨基羧酸类、磷酸盐类都强,且螯合稳定性较好,因此各种金属分子在被螯合后并不会轻易分解,且化学稳定程度较高,易于被生物化学降解,但其生物降解产物会释放含氮磷类产物导致土壤和水体的富营养化,最后造成环境污染,所以已逐渐被淘汰。
3 结 论
向Fe/过硫酸盐体系加入环境友好且可生物降解的螯合剂后会大大提升体系降解效能,螯合能力强、环境友好以及可生物降解的螯合剂有柠檬酸(CA)、次氨基三乙酸(NTA)、乙二胺二琥珀酸(EDDS)、亚氨基二琥珀酸(IDS)等,近年来螯合剂强化芬顿、类芬顿体系的研究较多,但强化Fe/过硫酸盐体系的文章较少,值得继续探究。

