α-苯乙胺拆分研究
吴卫忠 蒋燕华
(1. 常州大学 石油化工学院,江苏 常州 213164;2. 常州寅盛药业有限公司,江苏 常州 213000)
光学活性的α-苯乙胺是一种被广泛地用来代替光学活性的天然生物碱作用外消旋体酸的拆分试剂,也可用来作为不对称合成的手性源[1,2]。因此,拆分消旋α-苯乙胺一直受到人们的重视[3,4]。经典的拆分方法是用光学活性的酒石酸等与其形成光学活性的非对映体盐,再进行分解和分离[5]。由于拆分剂酒石酸的水溶性很好,所以它的回收是利用其钙盐不溶于水,经分离后得到酒石酸钙盐。然后酒石酸钙盐再与硫酸反应,生成酒石酸和硫酸钙沉淀,经过分离,酒石酸水溶液浓缩得到拆分剂酒石酸。这一方法使用了钙盐和硫酸,增加了反应步骤,产生了大量固废。
本文采用不溶于水的L-谷氨酸作为拆分剂[6,7],在混合溶剂中对消旋α-苯乙胺进行拆分,拆分效果优于酒石酸。由于拆分剂L-谷氨酸不溶于水,所以直接酸化就可以高收率的回收L-谷氨酸。
1 实验部分
1.1 试剂与仪器
消旋α-苯乙胺由常州市华阳科技有限公司提供,实验其他试剂均为市购AR试剂。
1.2 合成路线
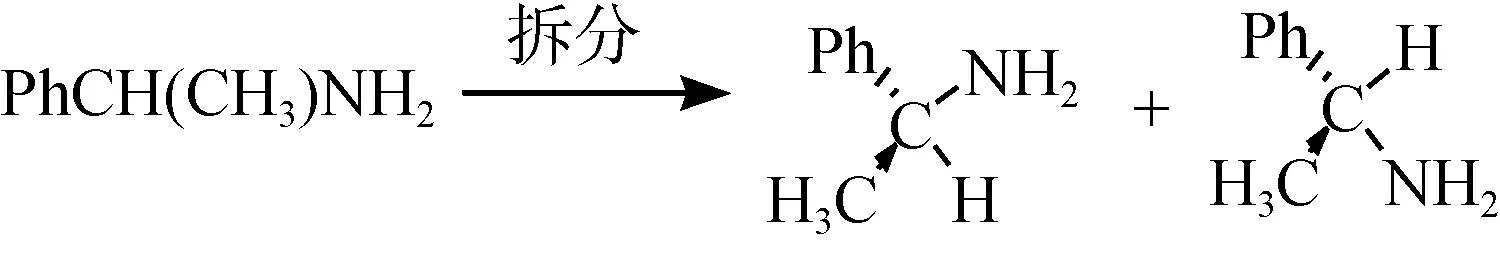
1.3 反应方法
(1) 在1 L四口反应瓶中,加入一定量的L-谷氨酸和190 g甲醇,加热回流。在2 h内滴加121 g(1 mol)消旋α-苯乙胺。加毕,保持回流1 h。滴加甲苯,加毕,慢慢降温到50 ℃左右,加入晶种,缓慢降温(5 ℃/h),快速搅拌,有结晶析出时,保温到基本上全部结晶为止。然后降温到5 ℃。过滤,得到140 g(-)-α-苯乙胺-(+)-谷氨酸盐湿品。
(2) 在500 ml四口反应瓶中,加入140 g(-)-a-苯乙胺-(+)-谷氨酸盐湿品和200 g甲醇,搅拌回流1 h,冷却到5 ℃。过滤。在50 ℃真空干燥5 h,得到128 g(-)-α-苯乙胺-(+)-谷氨酸盐精制品。
(3) 在500 ml四口反应瓶中,加入50 g固碱和120 g水组成的溶液,然后加入128 g(-)-α-苯乙胺-(+)-谷氨酸盐精制品,搅拌1 h,静止分出油层,水层用二氯乙烷(50 ml×3)萃取3次,合并萃取液和油层,常压回收溶剂(下次套用),减压收集 94~95 ℃/26 mm Hg馏分,得到S-(-)-α-苯乙胺54 g,比旋度:-39.4°,收率89%。
(4) 由(1)得到的母液常压回收甲醇,减压回收甲苯(套用),残液冷却后加入由(3)得到的萃余液,分出油层;水层用二氯乙烷(80 ml×3)萃取3次,合并萃取液和油层,常压回收溶剂(套用),减压收集90~95 ℃/26 mmHg馏分,得到混合α-苯乙胺62 g(通过雷尼镍催化加氢,可以转化成消旋α-苯乙胺(加氢收率95%),再用于拆分),收率92.5%。
(5) 在1 L四口反应瓶中,加入由(4)得到的萃余液,用稀硫酸中和到pH=3.2。过滤,80 ℃ 真空干燥,得到拆分剂148 g,比旋度:+31.2°(c=1.6 mol/L盐酸)。
2 结果与讨论
2.1 L-谷氨酸用量对拆分效果的影响
固定其他条件不变,改变L-谷氨酸用量对拆分效果的影响见表1。

表1 L-谷氨酸用量对拆分效果的影响Tab. 1 Effect of L-glutamic acid dosage on resolution effect
由表1可以看出,随着L-谷氨酸用量的增加,S-(-)-α-苯乙胺的收率和比旋光度都有提高,当用量达到1.05 mol时,收率达到最高值。
2.2 甲苯用量对(-)-α-苯乙胺-(+)-谷氨酸盐收率的影响
固定其他条件不变,改变甲苯的用量对(-)-α-苯乙胺-(+)-谷氨酸盐收率的影响见表2。
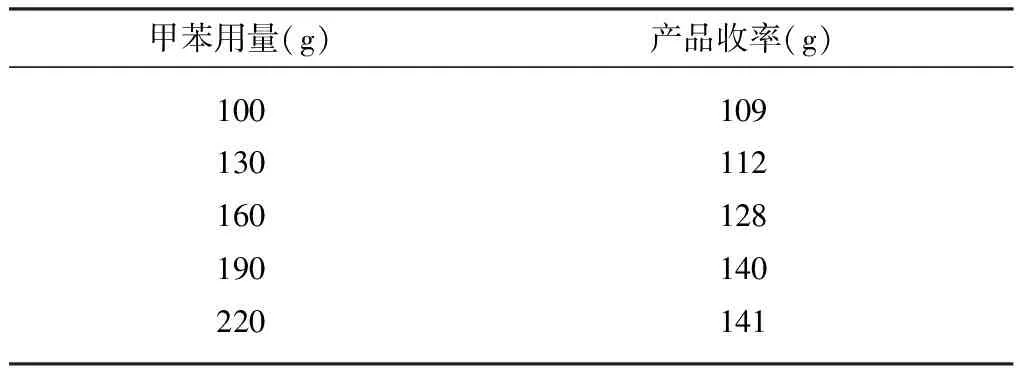
表2 甲苯用量对(-)-α-苯乙胺-(+)-谷氨酸盐收率的影响Tab. 2 Effect of toluene dosage on the yield of (-)-α-phenylethylamine-(+)-glutamate
由表2可以看出,甲苯用量为190 g时,(-)-α-苯乙胺-(+)-谷氨酸盐得到140 g。用量再增加,对收率的影响很小。
2.3 稀硫酸浓度对回收拆分剂质量的影响
固定上述较好条件不变,改变稀硫酸的浓度,结果见表3。
由表3可以看出,随着稀硫酸浓度的增加,回收拆分剂的比旋光度有所增加,但随即明显下降。这是由于随着硫酸浓度的增加,析出的拆分剂中夹带大量的硫酸钠,使得回收得L-谷氨酸的比旋光度下降。

表3 稀硫酸浓度对回收拆分剂质量的影响Tab. 3 Effect of dilute sulfuric acid concentration on the quality of recovered resolution agent
3 结论
本文采用不溶于水的L-谷氨酸作为拆分剂,在混合溶剂中对消旋α-苯乙胺进行拆分,拆分剂L-谷氨酸可以直接酸化高收率的回收。较好的反应条件是:拆分剂的用量1.05 mol,甲苯用量190 g, 稀硫酸浓度15%。S-(-)-α-苯乙胺收率89%,比旋光度:-39.4°;回收混合α-苯乙胺收率92.5%;回收拆分剂收率95.9%,比旋光度:+31.2°。

