高三化学复习中实施深度学习的途径和方法
——以NH4HCO3沉淀金属离子为例
河北 晏富强 李 颖
深度学习是学生基于理解层次的学习,以高阶思维的发展和实际问题的解决为目标,整合现有知识,积极主动地、批判性地学习新的知识,再将它们融入已有的认知结构中形成模型,且能将已有的模型迁移到新情境中的一种学习。深度学习的核心是提升学生适应未来社会发展和自身发展所必备的关键能力,而基于化学学科的深度学习是依据高中化学学科核心素养的五个构成要素去实施的,能有效培养和提高学生学科核心素养。教师实施基于核心素养的高中化学深度教学,在基本方法和实施策略上要探寻教师“深度教”与学生“深度学”的最佳契合点,才能使高中化学课堂呈现出“深入、深化、深刻”的课堂新样态。通过对学生提出的问题进行梳理和整合,结合高考评价体系对学生学科核心素养的具体要求,笔者认为要开展深度学习,应该就以上问题从四个方面展开。
一、回归教材深入学习

二、补充资料深化学习
教师要做到使学生在学习课本知识的基础上,适当补充必要的知识,提升学生的独立思考、逻辑推理、信息加工、自主学习的能力。此过程教师应特别注重将化学知识与生产生活相结合,突出化学学科知识的实用性,同时也应深化学生对高中理论知识的理解并达到能用理论知识进行推理和判断的目的,笔者通过设计实验方案、优化方案再用实验进行验证。
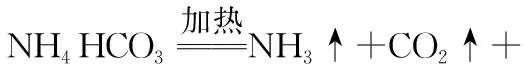
2.查阅资料得知常温常压下,Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11,K分解(H2CO3)=30,Ksp[Fe(OH)2]=8×10-16,Ksp(FeCO3)=3.2×10-11,Kb(NH3·H2O)=1.8×10-5,K分解(NH3·H2O)=0.75。
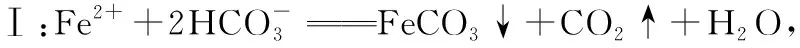
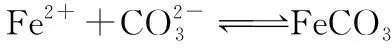


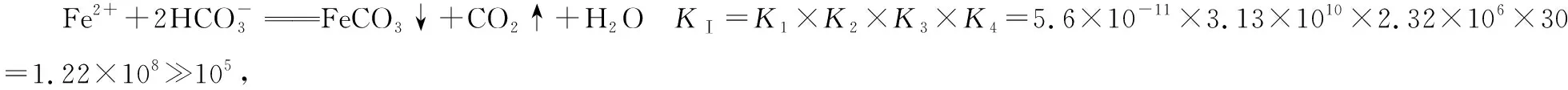

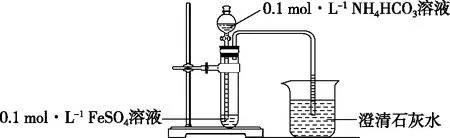
图1

K1=1/Ksp[Fe(OH)2]=1.25×1015
K2=Kw/Ka1(H2CO3)=2.32×10-8
K3=1/Ka1(H2CO3)=2.32×106

K4=30
K5=Kw/Kb(NH3·H2O)=5.56×10-10

K6=K分解(NH3·H2O)=0.75

教师通过化学实验验证,引导学生设计定量实验方案,测量FeCO3沉淀中Fe(OH)2的量,学生通过小组讨论的方式设计两种实验方案:
方案1:在图1实验的基础上,将沉淀过滤、洗涤、干燥、称量,对比称量的质量和理论质量。
方案2:在图1实验中得到的沉淀用如图2所示装置测量CO2的体积,对比测量的体积和理论体积。
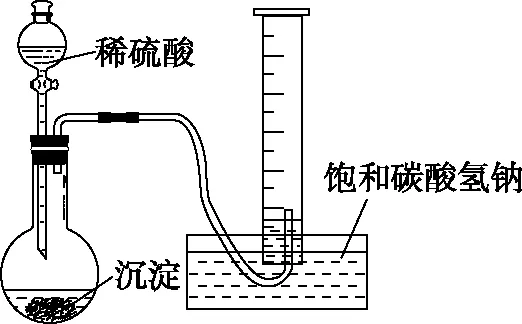
图2
学生通过实验发现:方案1干燥时间过长,由于托盘天平精确度较低,导致称量困难,加上实验中过滤损失的量,故而实验误差较大;方案2则比较容易操作,最后,通过实验数据计算得出FeCO3质量分数为95.2%,比较纯净。
进行深度学习让学生深刻理解化学反应的本质,在此基础上通过设计、完善实验方案、实际操作实验、改进实验方案来验证理论推测。教师可以通过此过程提升学生变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识的学科核心素养。
三、理论计算深刻理解
学生在深度学习过程中要充分利用化学原理的理论知识,先分析微粒的种类再进行定量计算,从化学反应原理的角度深刻理解工业生产。
1.NH4HCO3溶液中离子浓度计算
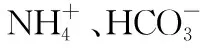
pH≈7.8,c(OH-)=10-6.2mol·L-1,
若Fe2+完全形成碳酸盐沉淀,则c(Fe2+)≤10-5mol·L-1,
Qc[Fe(OH)2]=c(Fe2+)·c2(OH-)=10-17.4 根据计算得知使用NH4HCO3作为沉淀剂,生成FeCO3的同时也不会有Fe(OH)2生成。 2.25℃新配制的0.1 mol·L-1的NaHCO3溶液中离子浓度计算 c(H+)=[Ka1(H2CO3)·Ka2(H2CO3)]0.5 pH=8.3c(OH-)=10-5.7mol·L-1, 若Fe2+形成碳酸盐完全沉淀,则c(Fe2+)≤10-5mol·L-1, Qc[Fe(OH)2]=c(Fe2+)·c2(OH-)=10-16.4 根据计算得知使用NaHCO3作为沉淀剂,生成FeCO3的同时也不会有Fe(OH)2生成。工业生产中使用NaHCO3作为沉淀剂和使用NH4HCO3作为沉淀剂相比成本高、会引入杂质且不易分离,所以不使用NaHCO3。 3.25℃新配制的0.1 mol·L-1Na2CO3溶液中离子浓度计算 若Fe2+形成碳酸盐完全沉淀,则c(Fe2+)≤10-5mol·L-1, Qc[Fe(OH)2]=c(Fe2+)·c2(OH-)=1.8×10-10>Ksp[Fe(OH)2] 根据计算得知使用Na2CO3作为沉淀剂,生成FeCO3的同时也会有Fe(OH)2生成。故使用Na2CO3与NH4HCO3相比前者成本高、沉淀的同时会生成Fe(OH)2、会引入杂质且不易分离,所以不使用Na2CO3。 学生通过深度学习就可以建立解答类似问题思维模式和解题方法,不仅能够解答高考题中Fe2+、Mg2+、Zn2+、Mn2+、Co2+、Sr2+离子使用NH4HCO3转化为碳酸盐沉淀的问题,还能够进一步解答使用(NH4)2CO3将Mg2+转化为Mg(OH)2·MgCO3的问题。如2019年全国卷Ⅰ26题:硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工业。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如图3所示: 图3 回答下列问题: (4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为。 深度教学并不追求教学内容的难度和深度,不是指教学内容越深越好,而是教师对于知识的构成要素不停留在符号层面,丰富教学的层次,实现知识教学的价值。高三化学教学中教师要注重学生提出的疑问,整合课内外相关知识,通过微观辨析和理论计算让学生深刻理解问题的答案,延伸课堂教学,通过实验的方式提升学生必备的关键能力。
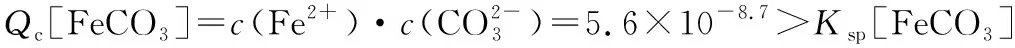
四、建立模型拓展应用