Starch-AA-CS三元共聚物对酸溶液中碳钢的缓蚀作用
侯道林杨武魁董社英
(西安建筑科技大学化学与化工学院,西安 710311)
碳钢具有优异的机械与加工性能,是制造工业设备的常用结构材料,但其易受环境侵蚀,故表面会聚集较多的腐蚀产物,因此需要定期酸洗除锈[1]。盐酸(HCl)是酸洗常用的无机酸之一,但金属基体会在酸洗过程中遭到腐蚀,从而引发安全隐患乃至严重事故[2]。添加缓蚀剂是减缓金属腐蚀较为常用的方法之一,根据成分主要分为有机和无机缓蚀剂2 大类,有机缓蚀剂具有较低的环境毒性、用量较少且效率高等优点,成为近年来的研究热点[3]。Ardakani 等[4]合成了一种由咪唑鎓衍生的离子液体聚合物[3-丁基-1-乙烯基溴化咪唑鎓](PIL),PIL 属于抑制阴极为主的混合型抑制剂,投加量为400×10-6时对低碳钢的缓蚀率高达96%;赵清等[5]通过添加季铵盐和席夫碱基团对羧甲基壳聚糖进行了改性,首次合成了2 种羧甲基壳聚糖衍生物作为P110 钢在二氧化碳环境中的绿色缓蚀剂,此类缓蚀剂能在金属表面形成一层致密的具有疏水性的保护膜,从而保护金属不被腐蚀;陈淑君等[6]将广玉兰叶提取物作为一种在1 mol·L-1盐酸中应用的新型缓蚀剂,并探讨了其性能及机理,结果表明,在298 K 时,缓蚀率为85%,且分子动力学模拟显示其是一种物理与化学共吸附型的缓蚀剂;Haque 等[7]在室温下合成了乙二胺修饰葡萄糖、四亚甲基二胺修饰葡萄糖和六亚甲基二胺修饰葡萄糖3 种不同碳链长度的葡萄糖衍生物,结果显示,在1 mol·L-1盐酸环境中的缓蚀率可达97.04%。
根据绿色科学发展原则,原料的选择应该来源广泛、无毒无害且价格低廉[8]。壳聚糖(Chitosan,CS)又称脱乙酰甲壳素,通过改性可改善水溶性问题,从而实现在缓蚀方面的应用。如改性后的十二烷基硫酸钠改性壳聚糖 (SLC)[9],投加量500 mol·L-1时在盐酸环境中的缓蚀率为96.44%;银纳米-壳聚糖复合材料 (SNPs-CT-NC)的投加量为150 mol·L-1时,在工业冷却水中的缓蚀率可达97.6%[10]。淀粉(Starch)可被烯丙基磺酸钠改性后成为一种接枝共聚物(CS-SAS-AAGC)[11],当投加量仅为50 mol·L-1时,其缓蚀率可达到97.2%。对Starch 和CS 单一的改性已有研究,但二者直接聚合并用于碳钢缓蚀鲜有报道,故以Starch、AA 和CS 作为原料,制备出三元共聚物SAAC。通过FT-IR 和XRD 来对SAAC的结构进行表征,利用电化学方法和失量法研究在HCl 环境下对碳钢的缓蚀效果,并结合SEM 和EDS研究其在碳钢表面的缓蚀机理。
1 实验部分
1.1 试剂与仪器
木薯淀粉,食品级,吉林省杞参食品有限公司;壳聚糖,分析纯,上海思域化工科技有限公司;氢氧化钠、盐酸、硫酸、硝酸铈铵、乙醇,分析纯,西安化学试剂厂。
Quanta FEG 250 型场发射环境扫描电子显微镜,美国FEI 公司;Bruker D8 Advance 型X 射线衍射仪,德国布鲁克公司;CHI660B 电化学工作站,上海辰华仪器有限公司;FTIIR-8400S 型红外光谱仪,日本岛津有限公司。
1.2 淀粉-丙烯酸-壳聚糖三元共聚物(SAAC)的合成[12]
将1.0 g 淀粉在90 ℃下溶于50 mL 蒸馏水中,1 h 后保持温度在50 ℃,之后称取1.0 g 壳聚糖溶于50 mL 丙烯酸溶液(中和度为6.0%)中,再将2种溶液进行混合,添加3%的Ce(NH4)2(NO3)6后在氮气下反应5 h,反应结束后用乙醇沉淀,洗涤后常温干燥12 h 可得最终产物SAAC。
1.3 结构的表征
红外表征:型号为FTIR-8400S 的红外光谱仪,扫描范围为4 000~500 cm-1,采用溴化钾压片法表征结构。X 射线衍射测定条件:靶材Cu,管电压40 V,管电流40 mA。
1.4 缓蚀性能测试
1.4.1 电化学测试法
电化学工作站(型号为CHI660B)是电化学实验的主要仪器。以饱和甘汞电极为参比电极、铂丝为辅助电极和暴露面积为1.0 cm2的Q235 碳钢为工作电极,在303 K 下,将工作电极浸泡在测试液中30 min 以上,使体系达到稳定的开路电位(OCP),再分别进行阻抗和极化曲线的测试,极化曲线电位区间-0.8~0.1 V,扫速1 mV·s-1。
1.4.2 静态失量法
失量实验所用样品为Q235 钢(50 mm×25 mm×2 mm),缓蚀剂的性能评价参照SY/T 5405-1996 酸化用缓蚀剂性能试验方法及评价指标[13]。
1.5 腐蚀形貌表面分析
分别采用型号Quanta FEG 250 型场发射环境扫描电子显微镜(SEM)和型号HYDAC 的X 射线能谱分析仪(EDS)对酸浸泡实验前后碳钢的表面形貌及特定区域内的元素分布进行分析[14]。浸泡实验为:将处理好的碳钢浸泡在不同浓度SAAC 的1 mol·L-1HCl 溶液中8 h,干燥后分析其腐蚀形貌。
2 结果与讨论
2.1 产物SAAC 的结构
Starch、AA 和CS 发生的三元共聚反应具有原料易得、条件温和、操作简单的优点,所生成缓蚀剂(SAAC)的结构如图1所示。
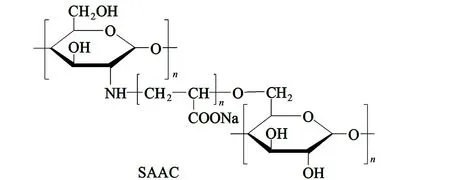
图1 SAAC 的结构示意图Fig.1 Schematic diagram of the SAAC structure
2.2 SAAC 缓蚀剂的结构分析
图2是AA、Starch、CS 和SAAC 的红外光谱和X 射线衍射图谱。

图2 SAAC 的红外光谱图(a)和X 射线衍射图谱(b)Fig.2 FT-IR spectra (a)and XRD (b)of SAAC
由图2(a)可知,SAAC 在3 465、1 182 和1 625 cm-1处分别出现了—OH、C—O 和COO—的伸缩振动吸收峰,表明AA 分别与CS 的—NH2和Starch 的—OH 发生接枝反应,从而接入主链。在图2(b)中,SAAC 在20.37°处出现的衍射峰,包含CS 和Starch 的衍射峰区,并未出现Starch 在15.21°、22.96°和CS 在23.28°处出现的结晶峰。说明在AA 加入后三元聚合物的结晶度有所缺失,Starch 和CS 的原始结构受到破坏,由此推断合成了三元共聚物SAAC[15-18]。
2.3 SAAC 浓度与缓蚀性能的关系
图3是不同投加量下的Tafel 曲线与交流阻抗谱图,探讨SAAC 浓度与缓蚀性能的关系。

图3 不同浓度SAAC 下Q235 碳钢的极化曲线(a)和EIS 图(b)Fig.3 Polarization curve (a)and EIS diagram (b)of Q235 carbon steel under different concentrations of SAAC
通过图3(a)与表1可知,随着SAAC 的投加量增加,工作电极表面上的腐蚀电流密度(Icorr)逐渐减小,由4.936×10-4A·cm-2降至5.036×10-5A·cm-2,且自腐蚀电位向正向移动,表明SAAC 主要抑制阳极反应,所以SAAC 可归类为以抑制阳极腐蚀为主的混合型缓蚀剂[19]。由图3(b)与表2可知,随着SAAC 投加量的增加,其阻抗谱图中的阻抗直径逐渐增大,同时介电常数(Cdl)值减少,此时缓蚀性能越来越强,这是由于SAAC 与碳钢表面的吸附膜越来越厚,从而阻隔腐蚀介质与碳钢的接触[20]。

表1 SAAC 在1 mol·L-1HCl 中的极化参数Table 1 The polarization parameters of SAAC in 1 mol·L-1HCl
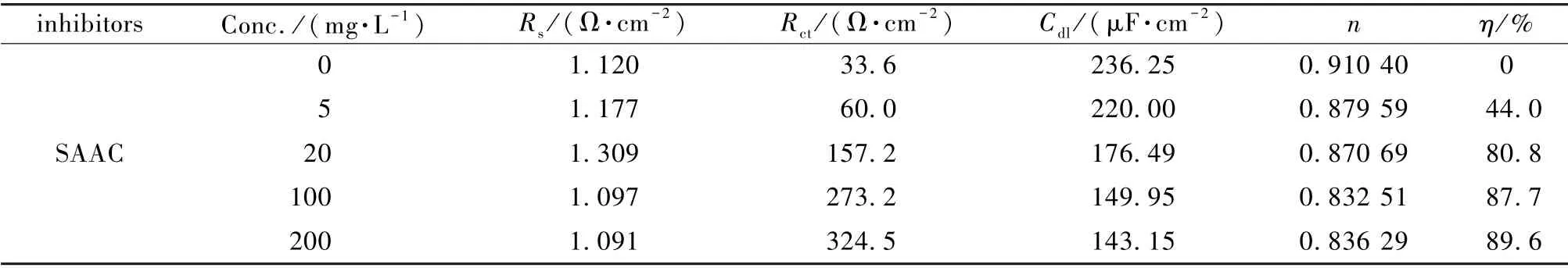
表2 SAAC 在1 mol·L-1HCl 中的EIS 参数Table 2 EIS parameters of SAAC in 1 mol·L-1HCl
2.4 腐蚀时间与缓蚀性能的关系
图4是不同腐蚀时间下的极化曲线与交流阻抗谱。
从图4(a)和表3可知,随着腐蚀时间的增大,Icorr由5.036×10-5

表3 不同腐蚀时间的极化参数Table 3 The polarization parameters at different corrosion time
A·cm-2升至3.105×10-4A·cm-2,且自腐蚀电位向负方向移动。当腐蚀时间不超过24 h 时,Icorr出现1 个变化较为平缓的区间,说明在24 h 内缓蚀剂的稳定性较好,之后缓蚀效果出现了较大程度的下降,可能是出现了保护膜部分脱落,导致碳钢部分活性位点暴露。结合图4(b)和表4可知,腐蚀时间在24 h 以内的阻抗直径有所降低,与极化曲线结果相同。

表4 不同腐蚀时间的EIS 参数Table 4 EIS parameters at different corrosive time

图4 不同腐蚀时间下Q235 碳钢的极化曲线图(a)和EIS 图(b)Fig.4 The polarization curves (a)and EIS diagram (b)of Q235 carbon steel at different corrosion times
2.5 静态失量实验
静态失量试验的结果与参数如表5所示。
由表5数据得到缓蚀率随着SAAC 浓度的增大而增加,且低浓度时增加较快,之后增加平缓,与电化学结果相似,但随温度升高,缓蚀率有所下降,可能表明SAAC 的热稳定性较差。

表5 不同温度下Q235 碳钢的失量实验参数Table 5 Weight loss test parameters of Q235 carbon steel at different temperatures
2.6 SAAC 缓蚀剂的吸附等温模型
图5为不同温度下SAAC 的吸附等温模型图。
缓蚀剂浓度与表面覆盖度的比值(C/θ)与缓蚀剂浓度(C)之间的关系图呈线性关系(图5),表明SAAC 抑制剂在钢表面的吸附符合Langmuir 等温吸附模型。吸附参数计算公式如(1)~(3)[21]:式(1)~(3)中:θ为表面覆盖度;η为缓蚀率,%;Kads为吸附平衡常数;R是气体常数;T为温度。

图5 不同温度下SAAC 的吸附等温模型图Fig.5 The adsorption isotherm model diagram of SAAC at different temperatures
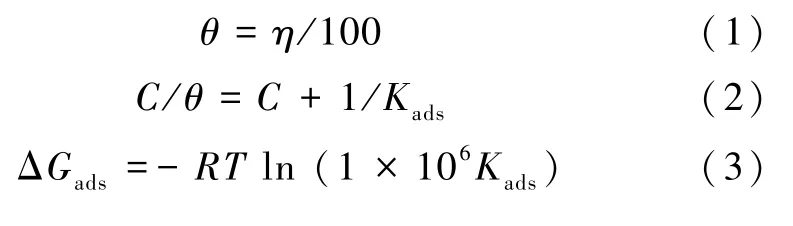
通过计算得到303、313 及323 K 时缓蚀剂的吉布斯自由能(ΔGads)分别为-30.17、-29.12 及-29.22 kJ·mol-1,表明SAAC 在碳钢表面的吸附过程为自发过程。ΔGads介于-40 kJ·mol-1和-20 kJ·mol-1之间,表明缓蚀剂在碳钢表面发生了物理与化学共吸附,这是因为碳钢表面的负电荷可与质子化SAAC 正离子发生静电吸附(物理吸附),而缓蚀剂结构中羧基、羟基以及N 原子上存在着孤对电子,可与碳钢表面的Fe 原子形成配位键,紧密地吸附在碳钢表面(化学吸附)[22]。
2.7 腐蚀形貌及腐蚀产物元素分析
图6是碳钢表面的腐蚀形貌及腐蚀产物表征。
图6(a)和图6(b)分别是碳钢在浸泡实验后的SEM 图,其中图6(a)为未添加SAAC 的空白样,可观察到碳钢表面较为粗糙,腐蚀严重,且聚集了较多的腐蚀产物,而添加SAAC 后腐蚀程度明显减弱,表面较为平整,且腐蚀产物明显减少[图6(b)];图6(c)和图6(d)分别是图6(a)和图6(b)EDS 元素分析的特定区域,其分析结果由图6(e)和图6(f)可知,SAAC 加入后,Cl、C 和O 的元素含量均增加,且出现新的N 元素,而Fe 元素含量降低,说明加入SAAC 后,其含N 基团与碳钢的Fe 原子进行了配位结合,从而使其吸附于碳钢表面,起到缓蚀作用[22]。

图6 未添加SAAC (a),(c),(e)及添加后(b),(d),(f)的腐蚀形貌及元素成分Fig.6 Corrosion morphology and element composition without SAAC (a),(c),(e);with SAAC (b),(d),(f)
图7是在盐酸溶液中加入SAAC 后碳钢表面的面扫元素分布图。
从图7(a)、图7(c)也可以观察到,Cl、O 元素的含量较大,由图7(b)、图7(d)中可以看出,C 及Fe元素的含量较小,这与图6(f)结果基本一致,N 元素未检出可能由于所选取点N 的含量小。

图7 盐酸腐蚀后碳钢表面的面扫元素分布图:(a)O;(b)Fe;(c)Cl;(d)CFig.7 The elemental mapping images (a)O;(b)Fe;(c)Cl;(d)C of the carbon steel surface after hydrochloric acid corrosion
3 结论
将木薯淀粉与壳聚糖通过丙烯酸接枝后合成的三元接枝共聚物SAAC,测试其在1 mol·L-1HCl溶液中对碳钢的缓蚀作用。在303 K 且投加量为200 mg·L-1时,缓蚀率可达90.1%。SAAC 缓蚀剂属于混合型抑制剂,在碳钢表面的吸附符合Langmuir吸附模型,且物理吸附和化学吸附共存。

