理论与实验相结合促进所学知识的理解与应用
——以化工精馏实验为例
*李学慧 胡润丰 吴正舜
(华中师范大学化学学院国家级实验教学示范中心 湖北 430079)
化工基础实验是化学、应用化学等专业的一门必修基础实验课,课程的目的旨在通过实验加深学生对化工基础基本概念的认识,验证有关的化工单元操作的理论,培养学生理论联系实际的能力。通过实验操作和对实验现象的观察,使学生掌握一定的基本实验技能;通过对实验数据的采集、分析,整理,培养学生处理数据的能力(列表、作图、解析);通过编写实验报告,使学生书写科研报告的能力得到锻炼。最终使学生初步掌握处理工程问题的实验方法和理论联系实际的能力。
目前,实验课是学生在学校内理论与实验相结合的最好方式之一,但由于化工实验设备台套的限制,理论课与实验课不能同歩,导致学生上实验时要么理论课还没有学习,学生不知道这个实验具体要验证什么知识点;上完理论课后又没有时间来反思做过的实验与所学的理论知识来进行关联,对于理论知识都没学懂的学生就更难到这一步了。虽然学生在上实验课前按要求都有过预习,根据实验课前老师与学生的互动,发现大部分学生对于实验的基本原理还不是很清楚,对于如何进行实验数据处理更无从谈起。因而导致学生理论与实验的脱节,对于所学的知识到底有什么用以及用在何处,并不是很清楚,且所学的一些知识都是零散的,没有时间也没有课后反思去把所学的理论知识进行整合,没有达到实验的教学目的,学生为了学分而去完成了实验这个环节而已。
因此,对于化工基础实验课可以进行实验课的教学改革,目前化工实验大都属验证性的实验,为了保证实验课的教学质量,理论课必须在实验课之前,如果由于台套数的限制,理论课与实验课不一定要同步完成,但实验课一定要在上完理论课后来完成。不能将实验课早于理论课并在指定时间点去完成,由于学生学习与接受知识的程度不尽相同,应该把去上实验课的时间交还给学生自己去决定,实验课可以在对应的理论课学习完后根据学生自己的学习进度以及掌握知识的程度来随时预约实验,不一定要在理论课的同一学期,可在理论课学习之后以组为单位来预约,预约时不能早于理论课学习之前预约,学生必须完成规定化工实验的学时数才能拿到相应的学分。这就要求学生预约实验之前必须要已经学完该实验的理论课,在此基础上能根据实验内容提出对于实验过程中还不清楚的地方,比如为什么要这样做,不这样做会出现什么样的问题,是什么原因导致出现这样的实验现象,实验中要采集哪些实验数据,这些实验数据如何处理,所得的实验结果与理论是否一致等。只有多问几个为什么并能用所学的理论知识来进行解答,这样才能将实验真正用来巩固所学的知识,加深对所学知识的理解与升华。
同时对实验课教师也提出了新要求,带实验的教师要对该实验所涉及的基本理论知识点做到心中有数,因此,不建议用研究生来替代理论课教师带化工实验,尤其更不能用非本专业的研究生,下面以化工精馏实验为例来谈一谈如何将实验与理论知识相结合,让学生使所学的知识得到融会贯通与升华。
目前化工基础中的精馏实验的目的是:
(1)熟悉板式精馏塔的结构、流程及各部件的结构作用;(2)了解精馏塔的正确操作,学会正确处理各种异常情况;(3)用作图法确定精馏塔全回流与部分回流时的理论板数,并计算出全塔效率。
1.精馏实验分离的原理与实验操作流程图
精馏是用于分离液体混合物的一种单元操作[1],它是利用被分离液体混合物的相对挥发度不同,被分离的组分进行多次的部分冷凝或多次的部分汽化将其进行完全分离的过程。显然要实现精馏分离,必须要使被分离的组分在汽、液二相区来完成,单一相是没有分离作用;其精馏分离的原理如图1所示,组成为xF的液体混合物,经加热温度上升至O点沸腾,对应的泡点温度为TB,进一步加热进入气液二相,在某一温度下液相M与气相N互成平衡,虽然气相N中的易挥发组分要比与之成平衡的液相M中的易挥发组分要大的多,但离纯组分A与B二点还有一定差距,为了分离得到纯组分,液相M须进一步加热而部分气化,气相N须进一步的部分冷凝,二者均须再次进入气液二相区进一步分离,气相N部分冷凝必须要向其提供冷量,液相M部分气化必须要向其提供热量,精馏分离过程中的冷量与热量是通过塔顶液相回流和塔底汽相回流来完现的,每经历一次气-液平衡过程就得到了一次分离提纯,这种在化工单元操作过程中提供气液接触进行传质传热分离的场所就是所谓的实际塔板。

图1 精馏分离原理图
塔板除了实际的塔板外,还有理论板,精馏塔的分离能力可以用理论塔板数的多少来表示,理论板是指偏平衡的气-液二相进入这块后,在这块板上进行传热传质后离开这块板的气液二相达到平衡时所对应的这块板;对于一定结构的精馏塔,各种操作因素,如回流比、回流液量、上升蒸气的速度及填料的性能等均会影响其分离能力,导致实际精馏分离操作过程中,离开每一块板的气-液二相并没有达到平衡,因而,精馏分离过程中,存在着塔板效率,塔板效率的定义如下:

式中,N1为不包含塔釜再沸器的理论板数;N2为不包含塔釜再沸器精馏塔中实际的提供气液接触的实际板数,可以从实验装置中直接得到。要确定精馏塔的塔板效率,就要确定精馏塔中的理论板数,而理论板数的确定方法有逐板计算法与作图法,由于二种方法本质是一样的,而作图法要比逐板计算法更简单直观,避免了繁锁的计算过程。即离开同一块板上的气液二相组成满足相平衡,而二板之间的气-液二相之间的组成满足对应段的物料衡算关系式,得到的物料衡算关系式也就是所谓的操作线,由于精馏塔内的气液二相的摩尔流量假定为恒摩尔流,因而对应段的物料衡算线均为直线。
了解了精馏塔的精馏分离原理后就知道了精馏实验装置的组成部分及各部件的作用,具体的实验流程图如下图2所示,实验装置主要由进料口之上的精馏段与进料口以及进料口之下的提馏段组成的精馏塔、塔顶提供冷量的全凝器以及提供热量塔釜再沸器、回流控制阀调节冷液回流进入塔内的冷量、塔釜再沸器中的电加热装置通过调节加热功率控制加入塔内的热量,此外还有原料罐、进料泵、塔顶产品罐、塔底产品罐以及原料液进入塔之前与塔底产品进行换热以回收余热的换热器。

图2 精馏实验装置流程图
2.实验数据的处理方法
(1)乙醇-正丙醇相对挥以度的确定
乙醇-正丙醇精馏分离实验过程中要根据乙醇-正丙醇的丰平衡数据来确定其相对挥发度α,实验中给定了的乙醇-正丙醇相平衡数据如下表1所示,而相对挥发度与相平衡数

表1 乙醇-正丙醇相平衡数据(摩尔分率)
据之间的关系如下:

通过Origin或Polymath[2]等相关软件可以拟合出乙醇-正丙醇的平均相对挥发度α=2.01,具体的拟合过程如下图3所示。
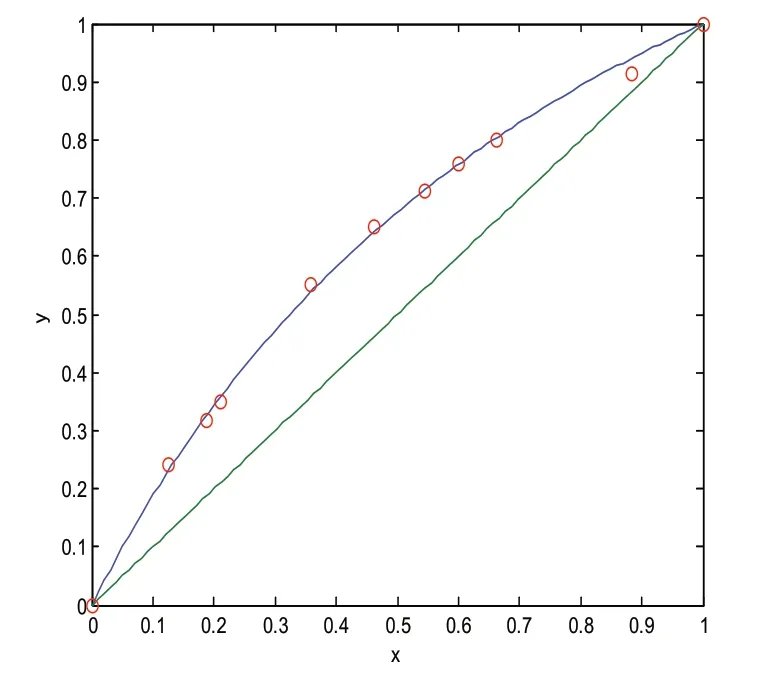
图3 乙醇-正丙醇相对挥发度拟合图
(2)理论板数与塔板效率的确定
本实验的目的中要求确定精馏塔全回流与部分回流时的理论板数及其对应的塔板效率,对于全回流时的理论板数的确定可以通过测定全回流稳定时塔顶与塔底对应的浓度xD与xW,从上面的拟合可知其相对挥发度α,由此可以得到相图,因为全回流时精馏段与提高馏段操作线均与对角线重合,然后在相平衡线与操作线(对角线)之间作梯级,梯级的个数即为达到上述分离结果对应全回流的理论板数,具体如图4(a)所示;对于部分回流时的理论板数同样也是待部分回流稳定后测定塔顶与塔底对应的浓度xD与xW,测定原料液的进料组成xF以及对应的进料温度tF,查相关物性数据得到进料组成下泡点温度TB、进料混合液的恒压比热容以及对应的汽化潜热,由些可计算出进料中液相所占的分率q,对于过冷液体进料其q的计算式如下:

于是进料线即精馏段与提馏段二线交点的轨迹方程为:

如图4(b)中的线段MO,而操作过程中回流比R是自行控制设定的,且塔顶的组成xD测定得到,因此精馏段的操作线为:

如图4(b)中的线段NO,连接图4(b)中O点与对角线上点K(xW,xW),得到提馏段操作线KO,然后在相平衡线与操作线之间作梯级,同样,梯级的个数即为达到上述分离结果对应部分回流时的理论板数。
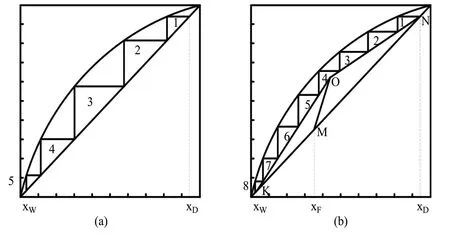
图4 作图法求解全回流与部分回流时的理论板数
根据作图法求取理论板,之所以可以用作图法求取理论板,它的实质就是同一块板上流出的汽液二相满足相平衡关系,二块板之间的汽液二相满足对应段的物料衡算关系。从图4中可知:达到相同分离程度所需的理论板数全回流时对应的理论板数最少,或者说对于给定的精馏塔所能达到的分离能力最大。
3.实验中异常情况处理
实验中异常情况的处理由于实验学时的限制,基础上没有进行该部分的操作,而这部分操作对于精馏操作中存在塔板效率的理解又非常重要;通过该部分的操作对于理论课中所学的塔板负荷性能图中的雾沫夹带上限线、漏液线、液泛线、液相负荷上限线以及液相负荷下限线的理解有了更直观的认识,加深了所学知识的理解与巩固。如果采取实验预约制,学生可以不受实验学时的限制,在预习好实验的基础上可以使用实验装置进行各种不同方案的实验,并对不同实验方案下出现的各种现象用所学的知识加以分析和解释,既提高了实验操作技能,又把所学的理论与实验相结合,从而提高了用所学知识去分析与解决问题的能力,此外,还提高了学生的学习兴趣,不仅仅是为了完成实验而去实验,保证实验教学质量的同时,提高了学生的学习效率。
4.反思与提高
化工精馏实验除了了解板式精馏塔的结构、流程及各部件的结构作用外,通过实验观察全回流与部分回流实验中温度沿塔高的分布、全塔效率的求取以及实验过程中所出现的一些异常现象,来加深对理论课中所学的一些基本知识点的理解,并在运用过程中得到提高。
如对于有一精馏塔,直径1m,有20块塔板,板效率为60%,原设计用于精馏分离含A摩尔分率(下同)为xF=0.5的A-B溶液,所得馏出液中易挥发组分A的组成xD=0.96,釜液中易挥发组分的组成xW=0.04。若已知C-D的平均相对挥发度分别为2.0;现想用该塔来分离C-D混合溶液,原料液中易挥发组分的组成也是xF=0.5,也是泡点进料,问用这个精馏塔能否用来分离C-D混合溶液也得到xD=0.96与xW=0.04的产品。
显然,如果对整个精馏实验搞清楚了,对于处理这样的题应该很容易了。首先根据全塔板效率的定义可知该精馏塔在给定的操作条件下对应的理论板数为20×0.6=12(块)。同样操作条件下全回流时达到相同的分离任务所需的理论板最少,若这个需要的最少理论板数比塔中已有的理论板还要大时则达不到上述分离任务,若比已有的理论板要小时则可以达到上述分离任务,因此,根据全回流时最小理论板数可由芬斯克(Fenske)公式进行计算并扣除塔釜再沸器一块得到塔内最少理论板为:
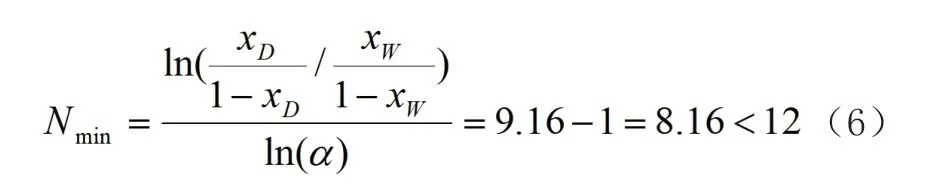
因此,用这个精馏塔能否用来分离C-D混合溶液也得到xD=0.96与xW=0.04的产品。
此外,对于某连续操作精馏塔如下图5(a)所示,已知料液摩尔组成xF=0.2,料液以饱和液体状态直接加入塔釜,塔顶设全凝器,全塔共两块理论板(包括塔釜),塔顶摩尔采出率D/F=1/3,回流比R=1,泡点回流,此条件下物系的相平衡关系可表示为y=4x,试计算塔釜流出液的组成xW=?

图5 操作流程图与其对应的相图中的表示
要求解此类问题,首先要能将流程图转化为用相图形式表达的分离过程,如图5(b)所示,然后再利用理论板与操作线所表达的实质:同一块理论板上流出的汽液二相组成满足相平衡关系,二块板之间的汽液组成二相满足对应段的物料衡算关系,然后再来解此题就很简单了。由塔顶摩尔采出率D/F=1/3,根据全塔物料衡算有下式:

由此得方程:

又因A点的坐标为(xD,xD),点B在相平衡线上,且点A与点B的纵坐标相同,则点B的坐标为(xD/4,xD),C点也要相平衡线上,且C点的横坐标为塔釜馏出液的组成xW,则点C的坐标为(xW,4xW),从上图中的(b)可知:点D的横坐标与点B的相同,点D的纵坐标与点C的相同,即点D的纵标为(xD/4,4xW),而点D在精馏段操作线上,且精馏段操作线为:
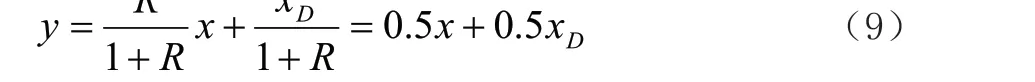
将点D的坐标代入精馏段操作线方程有:

联合公式(8)、公式(10)可求解出塔釜流出液的组成xW=0.01743。
5.结论
本文针对化工实验设备台套数少、理论课与实验课不能同步的情况,为了提高实验教学质量,提出先理论后实验的预约制可以克服上述问题,避免了学生在没学理论课的情况下就去做实验,导致实验教学质量难以保证;采用上述措施既提高了实验设备的利用率,又保证了实验教学质量,提高了学生兴趣的同时,使学生能用所学的知识去解释实验过程中出现的一些现象,提高了分析解决问题的能力,为以后从事科学研究打下了良好的基础;此外,本文还以精馏实验为例,介绍了理论与实验相结合才能使所学的知识得到融会贯通与提高。

