曲妥珠单抗对HER2 阳性晚期食管癌患者的疗效观察
陈智翔
(广东省韶关市第一人民医院 普通外科,广东 韶关 512000)
0 引言
食管癌是全球十大恶性肿瘤之一,其病理类型主要为食管鳞癌(ESCC)和食管腺癌(EAC),我国食管癌发病率居世界前列,食管癌患者的五年生存率仅为20.9%,我国的食管癌90%以上为鳞状细胞癌,少数为腺癌,目前占我国肿瘤死亡率的第4位[1]。目前治疗早期食管癌主要采用手术切除,然而对于早期患者临床症状并不典型,多数患者到医院就诊时已为中晚期,而对于晚期中年龄较大的患者,因年龄大、体质差、伴发基础疾病,大多不能耐受同步放化疗和手术治疗。人表皮生长因子受体2(HER2)是由定位于17q12号染色体上的原癌基因编码的长度为185ku的跨膜蛋白,食管癌中有0%~35%HER2基因扩增,0%~56%HER2蛋白表达[2]。随着分子靶向药物在许多实体肿瘤的成功运用,分子靶向治疗已成为食管癌的新方案。曲妥珠单抗能够特异性的与机体P185糖蛋白相结合,继而抑制供应肿瘤血管的增生和细胞增殖,且具有高效低毒作用[3]。本研究选取HER2阳性晚期食管鳞癌患者给予相应的治疗方法,研究内容如下。
1 资料及方法
1.1 一般资料
选取本院2016年12月-2018年12月收治的28例HER2阳性晚期食管癌患者的临床资料进行观察对比,随机将其分为对照组与研究组各14例。对照组患者男11例,女3例,年龄59~82岁,平均(73±17)岁,病灶直径6~14cm,平均(10.26±2.47)cm,研究组患者男10例,女4例,年龄60~81岁,平均(71±20)岁,病灶直径5~16cm,平均(11.02±2.66)mm。两组临床资料比较具有可比性(P>0.05)。本研究所有患者均接受调强放疗,研究组在放疗的基础上使用曲妥珠单抗联合替吉奥加奥沙利铂,患者一般临床资料详见表1。本研究经医院医学伦理委员会批准,所有患者及家属均知情同意并签署同意书。
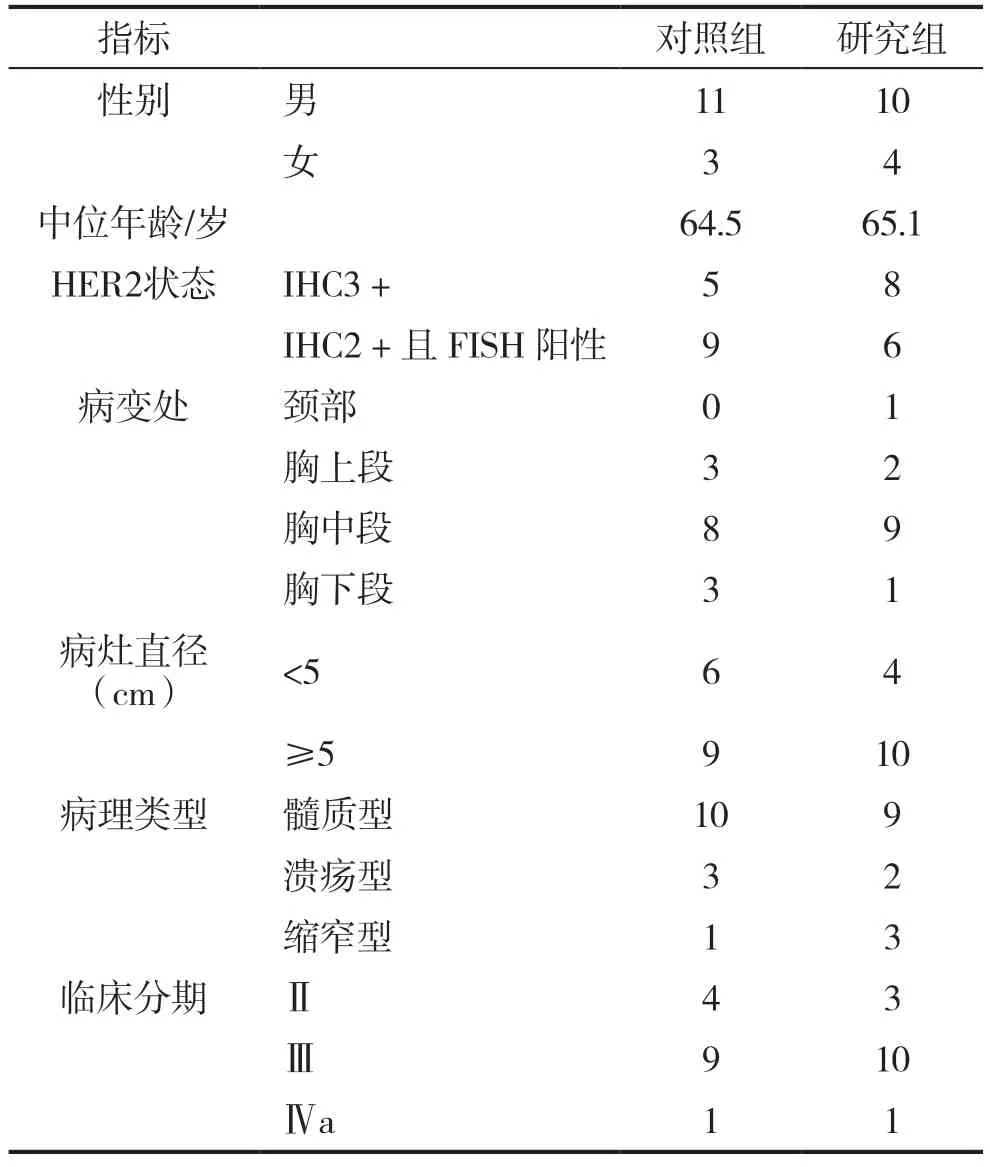
表1 对照组和研究组临床资料对比
1.2 入选标准
入选患者应符合以下标准:①病理学证实为ESCC晚期[4];②符合HER2阳性的评估标准;③食管未见溃疡、穿孔现象;④Karnofsky70分及以上(即生活可自理,但不能维持正常生活工作);⑤符合RECIST实体瘤的疗效评价标准且有1个及以上可测量病灶[5];⑥入选前未行手术、放化疗、其他抗肿瘤治疗;⑦通过检查血常规、心电图、肝肾功能等正常,未见明显放疗禁忌情况;⑧患者本人意识清楚、无精神疾病。
1.3 排除标准
入选患者应排除以下标准:①患者有重要器官的严重疾患或严重感染;②因合并其他疾患,不能耐受放疗;③复发食管癌患者;④患有精神疾病;⑤资料不完善者。
1.4 治疗方法
两组均接受调强放疗,每周进行一次实时影像检查保证治疗的精准度。对照组患者予以调强放射治疗,研究组患者在对照组治疗基础上同时联合曲妥珠单抗进行增敏治疗。放射治疗:使用设备为Varian Trilogy直线加速器,调制使用6MV X线,患者仰卧,注意保持呼吸平稳,热塑膜固定体位,层距3~5mm,进行CT扫描并标记体表;临床靶体积包括上下3cm和前后左右外放7mm;计划靶区需考虑靶区移动和摆位误差,外放5mm;处方剂量为95%PTV60~70Gy/30~35f;在横断面逐层注意把控靶区剂量分布,受照剂量是否危及器官,不断优化治疗方案,两肺V20的剂量低于30%,肺部的平均剂量低于15Gy,脊髓的最高放射剂量需要低于40Gy。研究组口服曲妥珠单抗(上海罗氏制药有限公司,国药准字J20170037)联合:替吉奥(齐鲁制药有限公司,国药准字H20100151)40mg/m2,口服,第1~14d,2次/d,3周为1个周期,奥沙利铂(远大医药黄石飞云制药有限公司,国药准字H20103129)在每个周期的第1d进行静滴治疗,治疗剂量为130mg/m2。第一周期第一天曲妥珠单抗剂量为8mg/kg,随后将剂量调整为6mg/kg,同时根据患者治疗期间临床症状随时进行调整。
1.5 观察指标
患者在治疗前后1个月复查食管造影、胸腹部CT以评价疗效,评价疗效依据实体瘤疗效评价标准1.1版本进行[6]:①客观缓解率(RR),达到完全或部分缓解的患者;疾病控制率(DCR),达到完全缓解(CR)、部分缓解(PR)、稳定(SD)的患者;无进展生存期(PFS),从开始治疗到疾病进展(PD)或死亡的时间;②不良反应:根据医疗记录,参照WHO抗肿瘤药物不良反应评价标准、RTOG急性放射损伤评价标准进行评价。
1.6 统计学分析
使用SPSS统计软件分析所得的计量资料(t)、计数资料采用例数(n,%)进行数据分析,组间比较使用卡方检验,以P<0.05为差异有统计学意义。
2 结果
2.1 近期治疗
对照组和研究组均达到评价疗效标准,其中对照组CR4例,PR4例,SD3例,PD3例,RR57.14%,DCR78.57%;研究组CR5例,PR6例,SD2例,PD1例,RR78.57%,DCR92.86%,两组患者RR、DCR比较,差异有统计学意义(P<0.05),如表2所示。
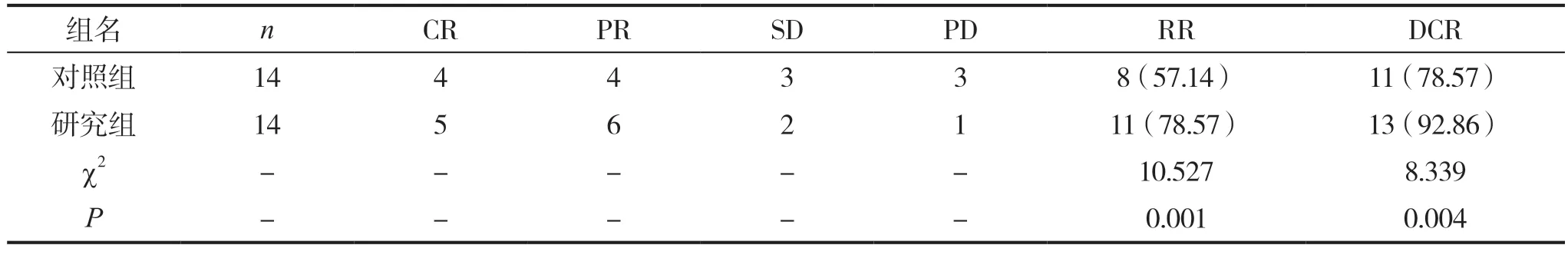
表2 对照组和研究组患者近期疗效对比[n(%)]
2.2 远期治疗
对照组与研究组在1~3年的生存率分别为64.29%、50.00%、35.57%和78.57%、64.29%、42.86%;对照组患者无进展生存时间为18个月,研究组患者无进展生存时间为23个月。对于研究组患者一、二、三年生存率及PFS均明显长于对照组。两组相比一、二年的生存率差异无统计学意义(P<0.05),三年生存率显示有统计学差异(P>0.05),见表3。
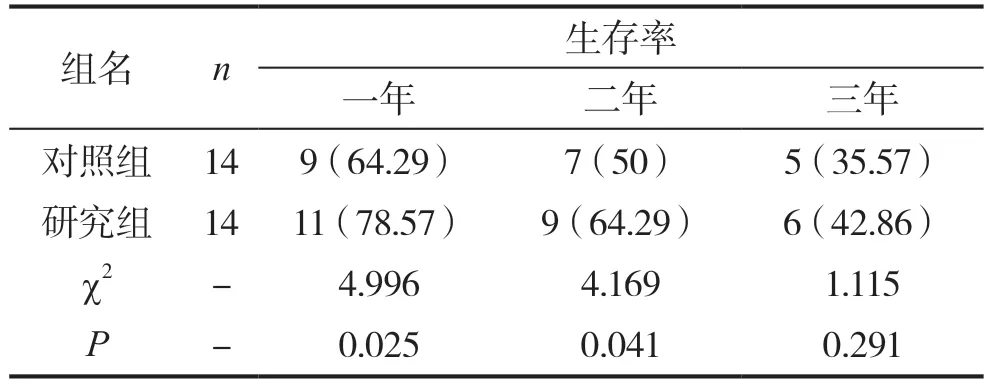
表3 对照组和研究组患者远期疗效对比[n(%)]
2.3 不良反应比较
两组患者治疗期间相关不良反应主要包括白细胞减少、血清肌酐升高、血清胆红素升高等,放射性肺炎、中性粒细胞减少、血红蛋白减少、血小板减少、食管炎、腹泻、发热等。组间比较差异无统计学意义(P>0.05),见表4。
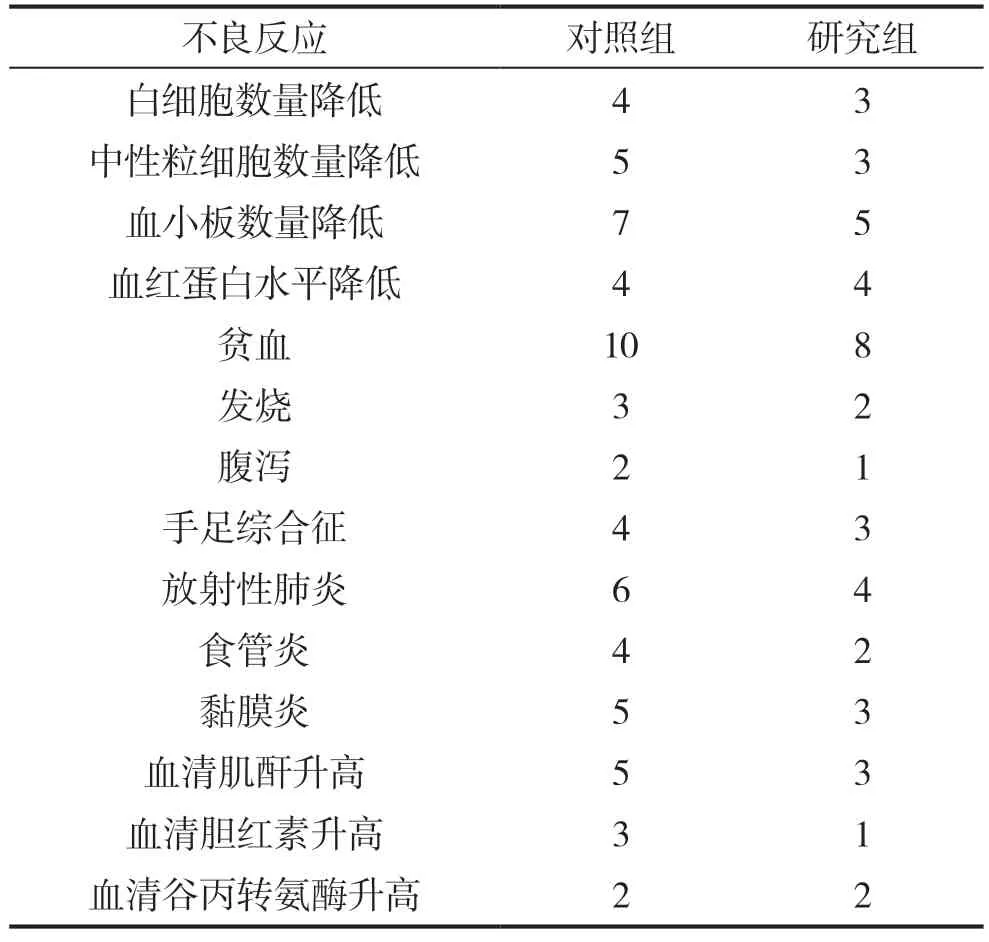
表4 对照组和研究组患者不良反应对比
3 讨论
近年来,随着化疗和放疗技术及手术方式的发展,食管癌的临床治疗有了很大的进展,但手术和放化疗的临床疗效均不能令人满意,生存率低,预后性差,手术和放化疗后五年生存率分别为15%~39%和8%~15%[7]。目前对于食管癌的发病原因较多,其与遗传、饮食及外界理化等均有一定关系,其中不良生活习惯和饮食习惯是引发食管癌的重要因素,长期吸烟、大量饮酒、长期食用烫食快食腌制类食品等,加之年龄因素、有食管癌家族病史等,这些危险因素协同作用,为食管癌的发生发展提供机会。食管癌因初期症状不明显,少数病人会出现胸骨后烧灼样、食管异物感、针刺样疼痛等症状,但多数患者确诊时已属于局部晚期,此时患者往往出现不同程度吞咽困难,因此对于局部晚期食管癌采用同步放化疗是治疗该部分患者的标准方案[8]。
HER2是人类表皮生长因子受体(EGFR)家族的第2个癌基因成员,其与恶性肿瘤的发生发展及转移密切相关[9]。多数研究表明,在多种肿瘤中均发现HER2的高表达状态,如乳腺癌、胃癌、结直肠癌、肺癌、膀胱癌、卵巢癌等30%以上的人类肿瘤组织,目前关于HER2阳性乳腺癌的研究成果最多,研究结果显示,HER2的表达水平越高,乳腺癌患者的恶性程度越高,治疗效果越差[10]。Petit T等[11]认为HER2与肿瘤转移关系密切,从两方面可以证明:一是对于乳腺癌细胞HER2基因的表达水平与肿瘤细胞增殖、侵袭能力密切相关;二是对于具有HER2的肿瘤细胞在转染后拥有转移能力。近年来靶向及生物治疗成为肿瘤治疗的热点,邓勇军[12]等研究通过对HER2高表达食管癌细胞株EC109分为赫赛汀治疗组、CBP治疗组、赫赛汀联合CBP治疗组,发现当赫赛汀单药、CBP单药或赫赛汀联合CBP,三种方式均能有效抑制EC109细胞增殖:当体内药物浓度高于1PPC(血浆峰浓度)时,赫赛汀联合CBP对EC109细胞的增殖抑制效应、诱导EC109细胞平均凋亡率对比二组单药效应显著增强(P<0.05),结果显示,赫赛汀对HER2高表达的OEl9食管腺癌细胞裸鼠移植也具有明显地抑制癌组织生长并减少淋巴结转移,且对食管鳞癌细胞株中高表达HER2同样具有良好的效果,这与本研究结果相符。
曲妥珠单抗是目前主要用于HER2阳性乳腺癌的辅助治疗,它也是第1个被美国食品和药物管理局(FDA)批准用于治疗实体瘤的大分子单克隆抗体[13]。虽然曲妥珠单抗已获批应用于治疗HER2阳性胃癌患者,且多项研究表明,对于食管癌患者的中HER2阳性肿瘤患者,曲妥珠单抗联合同步放化疗能起到增敏的作用,但仍需要多中心、大样本的随机临床试验证实[14]。Safran等[15]择l9名HER2阳性且未发生严重转移的EAC患进行I期临床试验,治疗药物使用曲妥珠单抗联合化疗药(紫杉醇+顺铂),患者的中位生存期、二年生存率均显著提高(24个月、50%),使用曲妥珠单抗加入治疗未增加化放疗副作用。
目前虽然有众多关于曲妥珠单抗对HER2阳性乳腺癌患者和HER2阳性胃癌患者的研究,但关于曲妥珠单抗对HER2阳性食管癌患者的研究较少,本研究使用曲妥珠单抗联合替吉奥加奥沙利铂治疗HER2阳性晚期ESCC治疗患者有较好的控制率,且不良反应可耐受,但由于本研究样本量小,观察和随访时间短,远期疗效评价仅依托中位 PFS数据,效果相对局限,可能存在总生存期不精确的情况,需要在之后的随访中逐步确认,且由于本研究是回顾性分析,未能对局部控制率及远处转移率进一步分析,曲妥珠单抗单用或联用其他药物对食管癌患者是否有效也应纳入研究范围。
本研究研究组使用曲妥珠单抗联合替吉奥加奥沙利铂也是基于安全性和有效性综合考虑。本研究将HER2阳性晚期ESCC患者分为对照组和研究组,由于病患的特殊性,选取病理较少,两组各14例,且大部分属于老年患者,这类患者由于不能手术且身体无法承受化疗,故均选用IMRT放疗[16],研究组配合使用曲妥珠单抗联合替吉奥加奥沙利铂治疗,对两组进行随访观察,近期治疗中,研究组和对照组的RR,DCR分别是78.57%,92.86%和57.14%,78.57%,差异有统计学意义(P<0.05);远期治疗中,研究组和对照组在一、二年的生存率分别78.57%,64.29%和64.29%,50%,差异有统计学意义(P<0.05),三年的生存率分别为42.86%和35.57%,差异无统计学意义(P>0.05),同时研究显示,研究组的PFS为23个月,优于对照组18个月,虽然统计学结果提示两组患者在一、二、三年的生存率差异不同,但对比对照组研究组患者的生存率更高且PFS更优。对比分析两组患者的不良反应,研究组的不良反应较少,且两组患者的治疗不良反应多数为Ⅰ~Ⅱ度,予以对症处理后症状均明显缓解。综上所述,曲妥珠单抗可以提高HER2阳性晚期食管癌患者的RR,DCR且能有效控制不良反应,虽提升一、二、三年生存率不是很明显,但依旧显示有效,可在临床推广。

