营养配方饮食结合心脏康复治疗对老年慢性心力衰竭患者心功能的影响
高 英,郭 璇,史 超,刘志强
(新疆医科大学第一附属医院1心血管病中心综合心脏内科,2护理部,乌鲁木齐 830054)
慢性心力衰竭(Chronic heart failure,CHF)是心肌病、血流动力学负荷过重及炎症等多种因素造成的心室泵血或充盈功能障碍,是心脏疾病发展至终末阶段的综合症候群,临床主要表现为呼吸困难、运动耐力下降、水肿等,对患者生活质量造成极大影响[1-2]。目前临床对于CHF 的治疗主要以强心、利尿、扩血管及心脏康复锻炼等方式为主,能在短期维持血流稳定,提高心肌耐力,但无法逆转损伤的心脏功能[3]。CHF 作为一种慢性消耗性疾病,患者大多病程较长、营养状态不佳、体能较差,此类疾病患者需低盐、清淡饮食,忌过饱,多数患者自制力差,无法满足病情控制需求,可加重心功能代谢障碍,形成恶性循环,影响患者预后[4-5]。因此,在CHF 患者治疗中进行合理有效的饮食干预具有重要意义。营养配方饮食是根据患者的疾病及身体状态进行饮食规划,以改善患者营养状态的一种干预方法,被证实可改善慢性疾病患者的体能状态,促进机体恢复[6]。本研究将探讨对老年CHF 患者实施营养配方饮食干预结合心脏康复治疗对其心肺功能及临床转归的影响,现报道如下。
1 资料与方法
1.1 一般资料以新疆医科大学第一附属医院心血管病中心综合心脏内科2020年1月—2021年1月收治的120 例CHF 患者为研究对象,随机分为两组,其中对照组 60 例,男性 31 例,女性 29 例,年龄 62~85岁,平均年龄(68.42±6.20)岁;研究组男性33 例,女性27例,年龄60~86岁,平均年龄(69.21±5.46)岁。本研究通过新疆医科大学第一附属医院伦理委员会批准,患者知情同意。
1.2 纳入与排除标准纳入标准:(1)60岁以上;(2)符合《中国心力衰竭诊断和治疗指南2018》对CHF 的标准[7];(3)无原发性消化道疾病。排除标准:(1)存在循环功能不稳定且预计生存期<6 个月者;(2)不稳定性心绞痛、心肌梗死及先天性心脏病者;(3)严重肝肾功能障碍者。
1.3 方法
1.3.1 心脏康复治疗方法 两组患者入院后予以心内科基础治疗,待病情稳定后由心内科医师与康复治疗师共同制定心脏康复疗法,使用德国Cortex 运动心肺功能测试系统,根据峰值耗氧量(peak oxygen consumption,peak VO2)设定运动强度,初起时强度以50%~60% peak VO2,运动 30 min,包括 5 min 热身运动和 5 min修整期,运动频率为每周5 d,连续运动12周。
1.3.2 饮食干预 对照组在心脏康复治疗基础上实施常规饮食指导,包括叮嘱患者坚持少食多餐,保持营养的多样化和丰富性,多摄取富含维生素及纤维素的食材,注意低钠饮食,避免食用生冷刺激性及油腻食物,强心苷治疗期间(洋地黄类药物)保持低钙饮食。研究组在心脏康复治疗基础上实施营养配方饮食,由主治医师、责任护士和1 名营养师组成专病一体化饮食指导小组,为患者制定餐食搭配,具体原则如下:(1)适当的能量摄入,能量需求取决于干重(无水肿)状态下的活动受限程度及心衰程度,理想摄入量为25~30 kcal/kg,超重患者应以低能量平衡饮食(100~1 200 kcal/d)减轻心脏负荷。(2)注意水、电解质平衡,美国纽约心脏病协会(New York Heart Association,NYHA)心功能分级≥Ⅲ级者每日盐分摄入应控制为1 g 左右,<Ⅲ级者应控制在2.5~5 g,服用利尿剂且尿多者可不限盐;注意控制饮水量。(3)低脂膳食,摄入ω-3 多不饱和脂肪酸,优化脂肪酸结构。(4)充足的优质蛋白质摄入,每日蛋白质摄入量>1.0 g/kg,重度营养不良患者可增加至1.2~1.5 g/kg。(5)适当补充B 族维生素,少食多餐,戒烟酒。(6)膳食处方的制定:通过半定量食物频率问卷了解患者饮食模式,并调查活动情况制定膳食处方,超重患者可按照3~5 kg体重递减,体重较轻患者则递增,逐渐至标准体重。摄入能量根据食物交换法粗略计算每日各类食物摄入量。(7)膳食指导:对患者实施营养教育。
1.4 指标的测定
1.4.1 营养指标的测定 包括上臂肌围(Arm muscle circumference,AMC)、上臂肱三头肌皮褶厚度(Triceps skinfold,TSF)、体重(Body weight,BW);AMC 测量方法:以软皮尺测量上臂中点自然维度,AMC=上臂维度-(3.4×TSF);TSF 测量方法:自然垂肩情况下,以手提起患者背部左侧肩峰至尺骨鹰嘴连线中点上方2 cm 处,测量皮褶厚度,干预前及干预后3 个月测定。
1.4.2 实验室生化指标的测定 干预前后抽取患者空腹静脉血5 mL,使用迈瑞BS280 全自动生化分析仪检测血清白蛋白(Albumin,ALB)、前白蛋白(Prealbumin,PAB)、高密度脂蛋白(High-density lipoprotein,HDL)、低密度脂蛋白(Low-density lipoprotein,LDL)、甘油三酯(Triglyceride,TG)、总胆固醇(Total cholesterol,TC)。
1.4.3 心肺功能的测定 干预前后使用德国Cortex 运动心肺功能测试仪检测:峰值摄氧量(peak VO2)、二氧化碳通气当量斜率(Ventilatory equivalent for carbon dioxide,VE/VCO2,slope)、无氧阈氧耗量(Oxygen consumption ant anaerobic threshold,VO2AT)。
1.4.4 临床转归指标的测定 干预前后抽取患者空腹静脉血,生化分析仪检测B 型钠尿肽前体(pro-brainnatriureticpeptide,pro-BNP)水平,迈瑞 DC-N3S 彩色多普勒超声检测计算患者左心射血分数(Left ventricular ejection fractions,LVEF)。
1.5 统计学处理采用SPSS 26.0 软件进行统计学分析,计量资料以均数±标准差()表示,采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较干预过程中,对照组中途退出2 例、失联1 例,研究组退出1 例,共记录116例患者资料。两组患者性别、年龄、NYHA 分级和病因比较,差异无统计学意义(P>0.05),见表1。

表1 两组患者基本资料的比较
2.2 两组患者营养状况比较干预后,与对照组比较,研究组AMC、TSF 升高,差异有统计学意义(P<0.05),见表2。
表2 两组营养状况的比较()
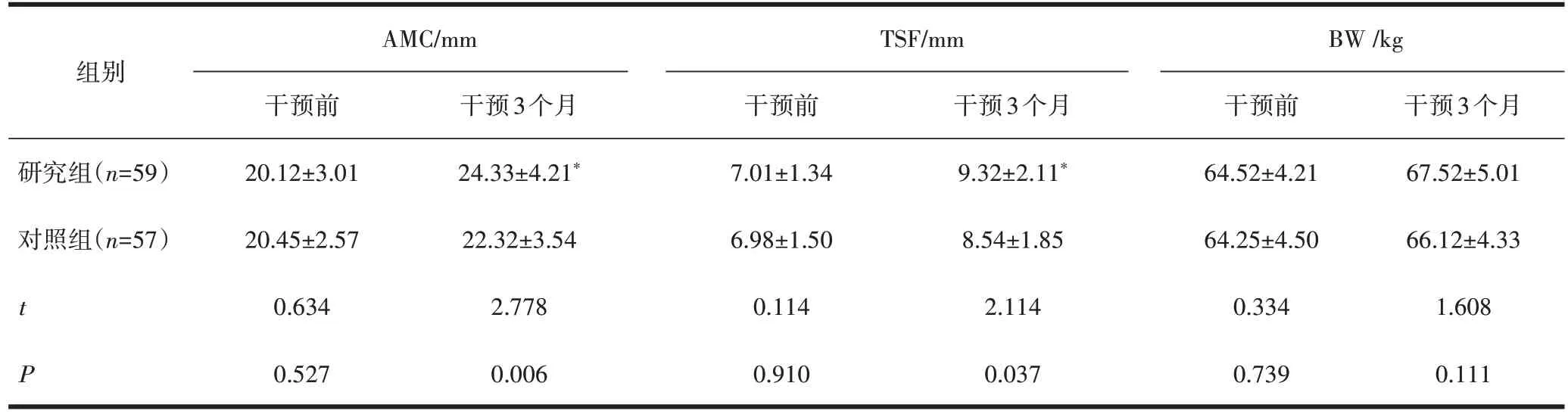
表2 两组营养状况的比较()
注:与对照组干预3个月后比较,*P<0.05。
组别AMC/mm干预前BW/kg干预前TSF/mm干预前干预3个月研究组(n=59)对照组(n=57)20.12±3.01 20.45±2.57干预3个月24.33±4.21*干预3个月9.32±2.11*22.32±3.54 7.01±1.34 6.98±1.508.54±1.85 64.52±4.21 64.25±4.50 67.52±5.01 66.12±4.33 t P 0.114 0.910 0.634 0.527 2.778 0.006 2.114 0.037 0.334 0.739 1.608 0.111
2.3 两组患者生化指标比较干预后,与对照组比较,研究组ALB、PAB 升高,差异有统计学意义(P<0.05),见表3。与干预前比较,干预后,两组患者的ALB、PAB、HDL 均提高,LDL、TC 均降低,差异有统计学意义(P<0.05),见表4。
表3 两组患者ALB与PAB的比较()
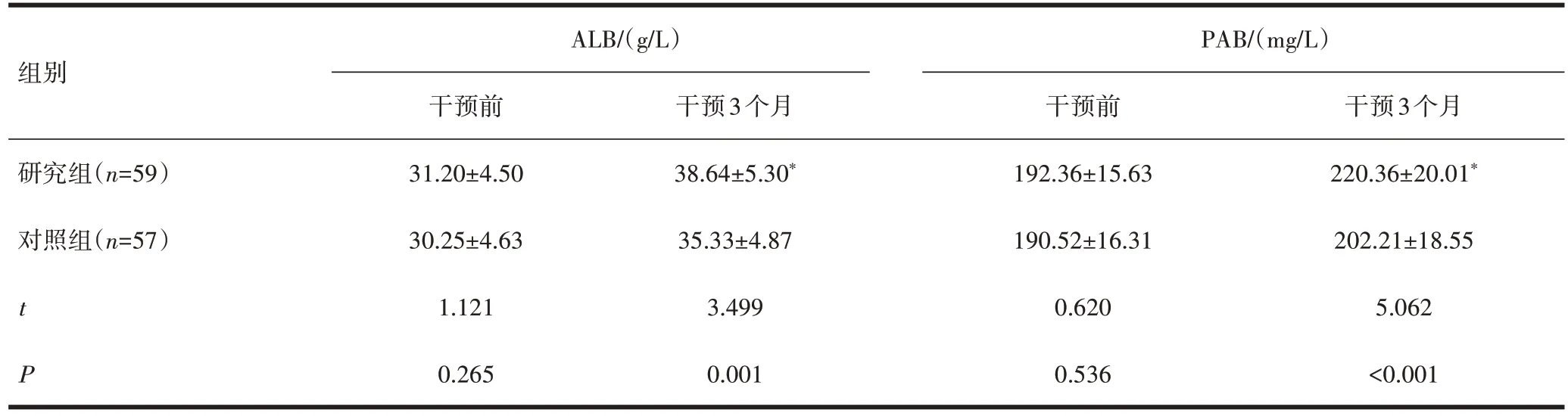
表3 两组患者ALB与PAB的比较()
注:与对照组干预3个月后比较,*P<0.05。
ALB/(g/L)PAB/(mg/L)组别研究组(n=59)对照组(n=57)干预前31.20±4.50 30.25±4.63干预3个月38.64±5.30*35.33±4.87干预前192.36±15.63 190.52±16.31干预3个月220.36±20.01*202.21±18.55 t P 1.121 0.265 3.499 0.001 0.620 0.536 5.062<0.001
表4 两组患者血脂指标的比较()
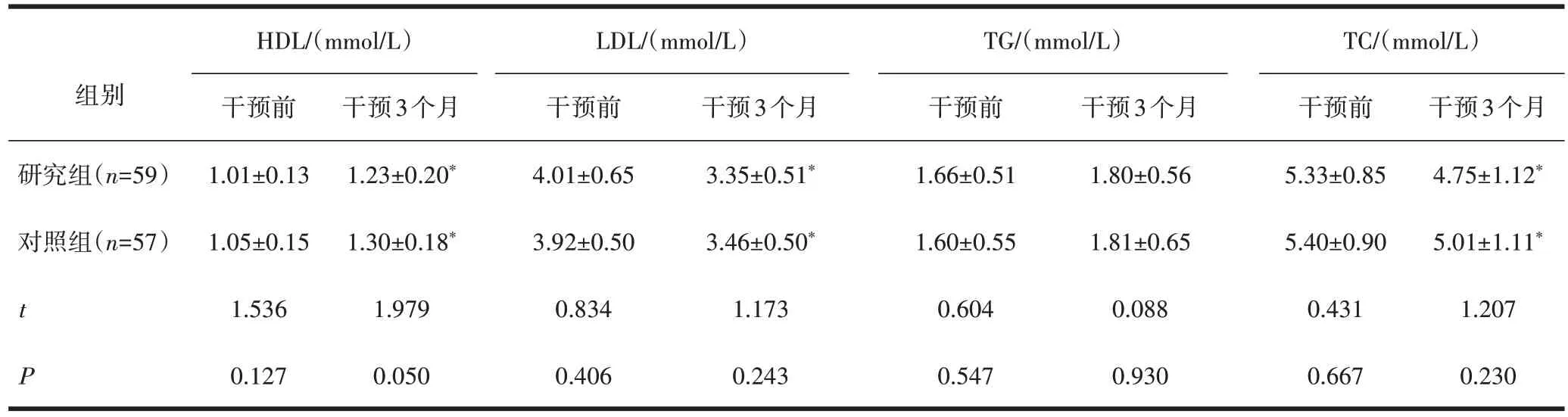
表4 两组患者血脂指标的比较()
注:与本组干预前比较,*P<0.05。
HDL/(mmol/L)LDL/(mmol/L)TG/(mmol/L)TC/(mmol/L)研究组(n=59)对照组(n=57)组别t P干预3个月4.75±1.12*5.01±1.11*1.207 0.230干预前1.01±0.13 1.05±0.15 1.536 0.127干预3个月1.23±0.20*1.30±0.18*1.979 0.050干预前4.01±0.65 3.92±0.50 0.834 0.406干预3个月3.35±0.51*3.46±0.50*1.173 0.243干预前1.66±0.51 1.60±0.55 0.604 0.547干预3个月1.80±0.56 1.81±0.65 0.088 0.930干预前5.33±0.85 5.40±0.90 0.431 0.667
2.4 两组患者心肺功能比较干预后,与对照组比较,研究组 peak VO2、VO2AT 升高,VE/VCO2slope 降低,差异有统计学意义(P<0.05),见表5。
表5 两组患者心肺功能的比较()
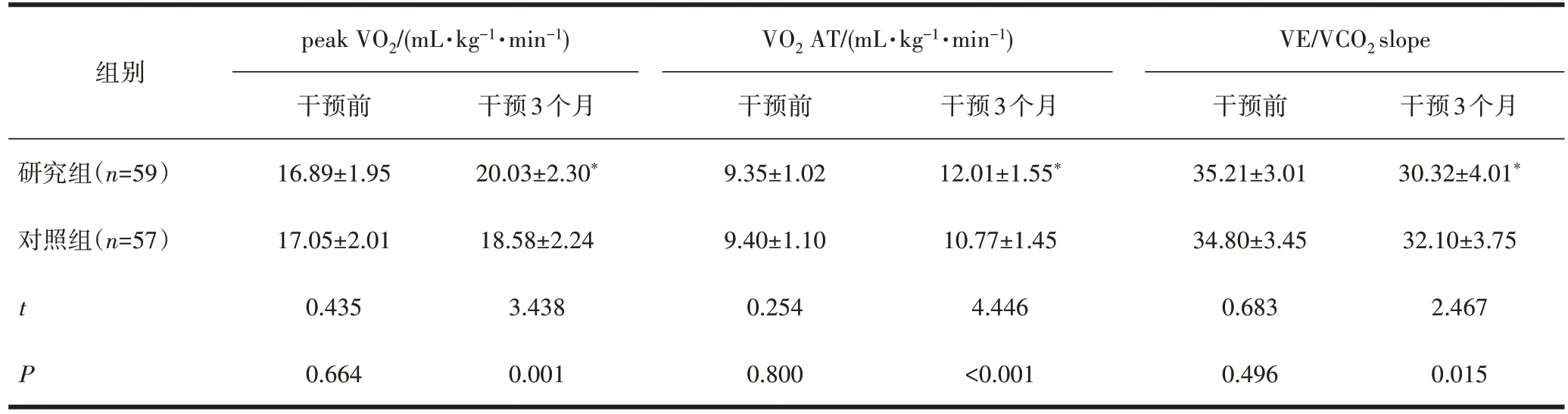
表5 两组患者心肺功能的比较()
注:与对照组干预3个月后比较,*P<0.05。
peak VO2/(mL·kg-1·min-1)VO2 AT/(mL·kg-1·min-1)组别研究组(n=59)对照组(n=57)t P干预前16.89±1.95 17.05±2.01 0.435干预3个月20.03±2.30*18.58±2.24 3.438干预前9.35±1.02 9.40±1.10 0.254干预3个月12.01±1.55*10.77±1.45 4.446 VE/VCO2 slope干预前35.21±3.01 34.80±3.45 0.683干预3个月30.32±4.01*32.10±3.75 2.467 0.015 0.6640.0010.800<0.0010.496
2.5 两组患者临床转归指标比较干预后,与对照组比较,研究组pro-BNP 降低,LVEF 升高,差异有统计学意义(P<0.05),见表6。
表6 两组患者临床转归指标的比较()
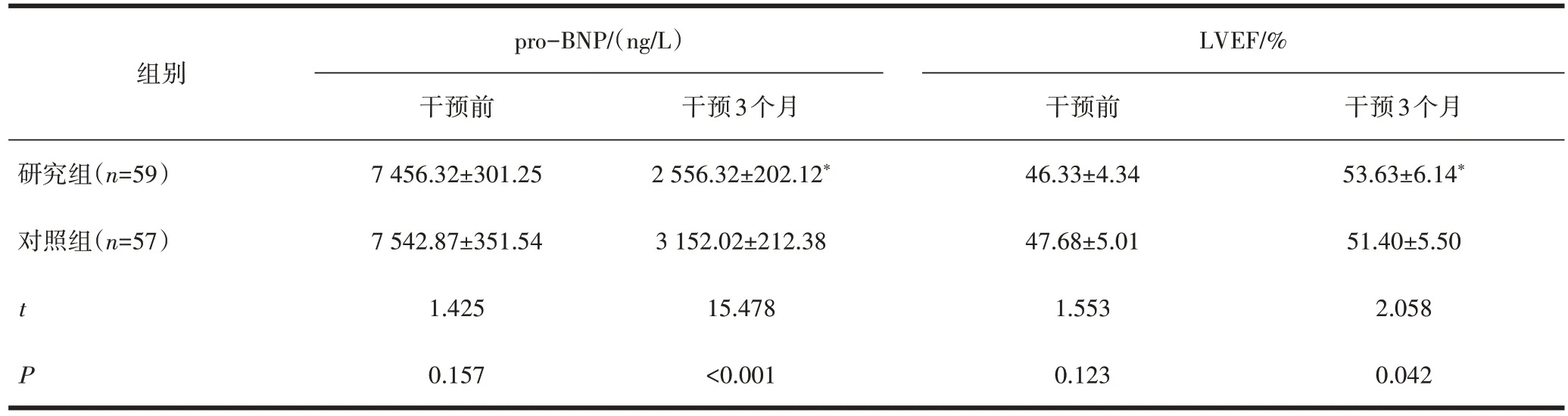
表6 两组患者临床转归指标的比较()
注:与对照组干预3个月后比较,*P<0.05。
组别LVEF/%研究组(n=59)对照组(n=57)pro-BNP/(ng/L)干预前7 456.32±301.25 7 542.87±351.54干预3个月2 556.32±202.12*3 152.02±212.38干预前46.33±4.34 47.68±5.01干预3个月53.63±6.14*51.40±5.50 t P 2.058 0.042 1.425 0.157 15.478<0.001 1.553 0.123
3 讨论
CHF 患者受病情影响存在不同程度的食欲下降及营养摄入吸收障碍,且交感神经系统的激活使患者的热量损耗增加,多处于营养不良的状态[8-9]。长期的营养不良可导致心脏代谢障碍加重,另外因患者的饮食控制不佳,可加重对病情的影响,增加病死、病残率,极大增加了临床医疗负担和家庭社会负担,因此在CHF 治疗过程中加强营养干预十分必要[10]。
本研究结果中研究组干预后的peak VO2、VO2AT高于对照组,VE/VCO2slope 低于对照组,提示对CHF患者实施心脏康复治疗联合营养配方饮食,有利于改善营养状态及心肺功能恢复。CHF 患者的心脏康复治疗虽可提高心肌耐受力但也会增加患者热量的耗损,因此辅以必要的营养干预具有重要作用。营养配方饮食干预是由多职能的专业人员组成饮食指导小组,开展的原则是既要保证适当的能量摄入,满足患者的营养需求,又要控制体重增长,避免增加心脏负担,通过饮食配合药物治疗,改善其营养状况,为心肌代谢提供更多的能量[11-12]。孙璐等[12]对CHF患者实施个性化饮食干预,结果患者的临床总有效率高于常规治疗的患者,且营养状态评估较常规治疗患者有明显改善,表明营养配方饮食对改善CHF患者心肌功能有积极作用。
本研究还显示研究组干预后的pro-BNP 低于对照组,LVEF 高于对照组,提示营养配方饮食干预结合心脏康复治疗有利于改善老年CHF 患者病情。中华重症医学会分会营养支持指导意见中指出,重症CHF 患者应及早恢复经口进食,以恢复肠道正常生理功能,满足肠道黏膜营养需求,能减少胃肠功能紊乱造成的代谢障碍,减少CHF相关危险因素[13]。研究证实,高脂、蛋白质摄入不足、微量元素失衡可增加CHF 患者心脏末期舒张压和收缩压,降低LVEF,此外CHF 患者盲目的限制钠盐的摄入可破坏钠平衡,导致神经内分泌及电解紊乱,使病情恶化[14]。营养配方饮食干预不是盲目的限制钠盐的摄入,破坏钠平衡,而是有针对性的控制,大大减少了影响病情的相关危险因素,减缓患者的病理变化,为身体机能的恢复提供了更好的条件。Sanches 等[15]认为地中海式饮食或阻止高血压饮食方法能防止CHF 的发生,证实了饮食干预对机体健康的重要性。常兴[16]研究中认为,对老年CHF 患者实施自制营养膳食处方能促进其病情的恢复,改善营养状况,与本研究观点一致,证实了营养配方饮食干预对于促进患者的临床转归有积极意义。
综上所述,在老年CHF 患者中基础治疗时实施营养配方饮食干预结合心脏康复治疗,能改善患者营养状态和心肺功能,利于促进临床转归,在今后CHF 患者的治疗中可将营养配方饮食干预纳入治疗方案。

