卡培他滨联合多西他赛治疗复发乳腺癌的临床效果
刘威
(河南商丘市民权县人民医院 肿瘤科,河南 商丘 476800)
乳腺癌是女性的一大“杀手”,作为一种恶性肿瘤,具有较高的致死率,严重威胁女性生命健康。随着生活节奏的加快,乳腺癌的病发率逐年上升,且极易出现复发转移的情况。化疗依然是控制乳腺癌病情发展的重要手段,但是随着蒽环类、紫杉醇等药物的使用,常有药物耐药性情况发生并直接影响控制效果。复发性乳腺癌患者5年的生存率较低,治疗较为困难,选用合适的化疗药物治疗具有重要的临床价值。卡培他滨具有较好的靶向作用,可用于复发性乳腺癌的治疗,对提高患者临床疗效、延长生存周期、提高生存质量具有重要作用,目前在复发性乳腺癌治疗中应用广泛。此外,研究发现,卡培他滨与多西他赛等蒽环类药物联用时,可有效避免交叉耐药状况的发生。基于此,本文选取90 例复发乳腺癌患者进行研究,结果汇报如下。
1 资料与方法
1.1 一般资料
选取2019年7月至2020年7月在河南商丘市民权县人民医院接受治疗的90 例复发乳腺癌患者作为研究对象,按照随机数字表法将患者分成观察组(n=45)与对照组(n=45)。对照组患者均为女性;年龄36~68 岁,平均年龄(52.14±5.41)岁;转移情况:骨转移12 例,脑转移18 例,其他部位转移15 例。观察组患者均为女性;年龄35~67 岁,平均年龄(51.13±5.42)岁;骨转移13 例,脑转移19 例,其他部位转移13 例。两组患者年龄、转移情况等基线资料比较,差异无统计学意义(>0.05),具有可比性。本研究经医院伦理委员会审核批准。
1.2 纳入与排除标准
纳入标准:①经过病理学以及免疫组化检查确诊,符合复发转移乳腺癌诊断;②经医学影像学诊断具有明显病灶转移存在;③之前进行过含蒽环类药物化疗,但疗效不理想;④Karnofsky 预后评分均在70 分及以上,功能状态评分在0~2 分之间;⑤患者知情同意。
排除标准:①伴急性传染病及感染疾病者;②伴严重肾脏、肝脏器官功能不全者;③伴精神疾病遗传基因及家族遗传史者;④临床资料缺失者;⑤治疗期间放弃治疗者;⑥合并免疫系统严重病变者。
1.3 治疗方法
对照组患者采用多西他赛治疗。患者给予75 mg/m多西他赛注射液(深圳万乐药业有限公司,国药准字H20060127,规格:1.0 mL∶40 mg),用药方式为静脉滴注,用药时间为患者每个化疗周期第1 d,化疗周期为21 d。
观察组患者采用卡培他滨联合多西他赛治疗。多西他赛使用剂量与时间与对照组相同。在此基础上,患者口服950 mg/m卡培他滨(上海罗氏制药有限公司,国药准字H20073024,规格:0.5 g),每天2 次,用药时间为患者化疗周期第1~14 d,化疗周期为21 d。
两组患者均连续治疗2 个周期。
1.4 观察指标
①比较两组患者的临床疗效。根据《WHO 关于实体瘤疗效评价标准》对两组患者的临床疗效进行评估。临床疗效分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),其中病灶完全消失记为CR;病灶面积缩小50% 以上记为PR;病灶面积缩小<25% 记为SD;病灶面积增加25% 以上或出现新病灶记为PD。客观有效率(ORR)=(CR+PR)/ 例数×100%。②比较两组患者血清肿瘤标记物水平。分别于治疗前及治疗2 个周期后,抽取患者空腹静脉血5 mL,以3 000 r/min 的速度离心5 min,取上层清液备用;采用电化学发光法测定血清中癌胚抗原(CEA)、糖类抗原125(CA125)、糖类抗原153(CA153)、糖类抗原199(CA199)等肿瘤标记物含量,严格按照试剂盒说明进行操作。③比较两组患者不良反应发生率。观察治疗期间患者胃肠道反应、肝功能受损、骨髓抑制及脱发等症状发生情况。④比较两组患者生存质量。分别于治疗前与治疗2 个周期后,采用Karnofsky功能状态评分标准(KPS)评估,分值范围在0~100 分,分值越高,说明患者生存质量越高。
1.5 统计学方法

2 结果
2.1 两组临床疗效比较
观察组(62.22%)ORR 明显高于对照组(31.11%),差异有统计学意义(<0.05),见表1。
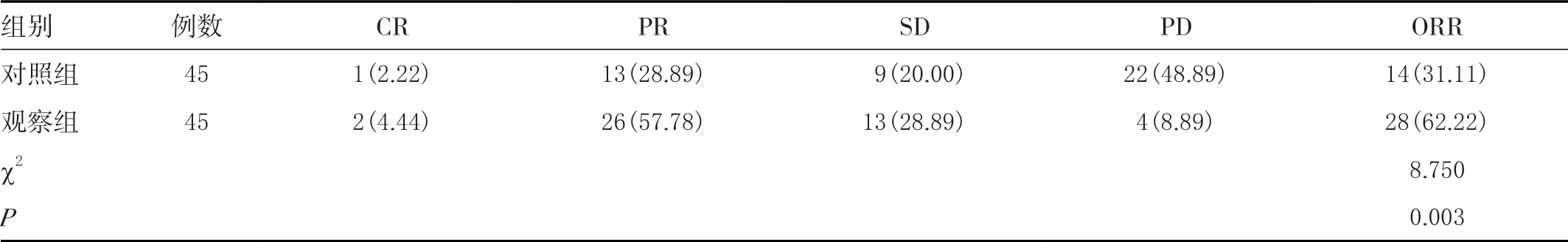
表1 两组临床疗效比较[n(%)]
2.2 两组治疗前后血清肿瘤标记物水平比较
治疗前,两组CEA、CA125、CA153、CA199 水平比较,差异无统计学意义(>0.05);治疗后,两组CEA、CA125、CA153、CA199 水平均明显低于治疗前,且观察组各指标水平明显低于对照组,差异均有统计学意义(<0.05),见表2,续表2。

续表2 两组治疗前后血清肿瘤标记物水平比较(±s) 单位:U·mL-1

表2 两组治疗前后血清肿瘤标记物水平比较(±s) 单位:U·mL-1
2.3 两组不良反应发生率比较
两组患者的不良反应发生率比较,差异无统计学意义(>0.05),见表3。
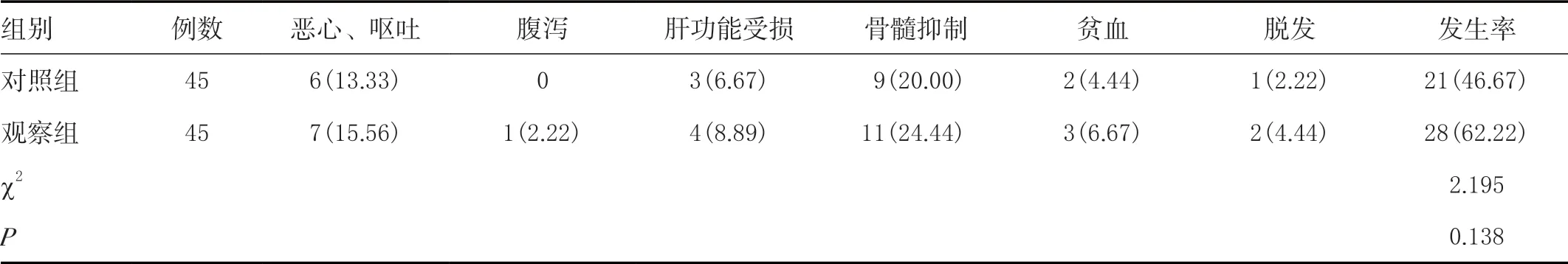
表3 两组不良反应发生率比较[n(%)]
2.4 两组治疗前后生存质量比较
治疗前,两组KPS 评分比较,差异无统计学意义(>0.05);治疗后,两组KPS 评分均明显高于治疗前,且观察组评分明显高于与对照组,差异均有统计学意义(<0.05),见表4。

表4 两组治疗前后生存质量比较(±s) 单位:分
3 讨论
乳腺癌早期具有较强的隐匿性,多数患者确诊时病情已发展至中晚期,错过手术最佳治疗时机。晚期乳腺癌患者主要通过化疗手段治疗,该阶段治愈难度较大,多以缓解临床症状、延长患者生命周期为治疗目标,以提高患者生命质量。晚期乳腺癌常用的化疗药物为蒽环类药物。该类药物的有效率为30%~40%,但其不良反应较多,且患者耐药性强,使该类药物的缓解率大大降低。由于复发转移乳腺癌患者体内肿瘤有较强的耐药性,蒽环类药物的治疗效果欠佳。当前,亟需找到一种安全可靠、有一定疗效的化疗药剂来控制肿瘤生长,提高患者生活质量,延长患者生存时间。
多西他赛是一种紫杉类药物,能够作用于癌细胞,抑制肿瘤细胞分裂和增值,加快肿瘤细胞凋亡,减少肿瘤细胞作用于人体的时间,以达到抗肿瘤的作用。有研究表明,多西他赛治疗复发转移乳腺癌过程中可通过影响微管蛋白影响细胞分裂,降低DNA 合成过程中肿瘤细胞的含量,减少肿瘤细胞增殖。卡培他滨是一种口服化疗药物,可以利用其自身氨基甲酸脂结构,对肝脏强羟酸酯酶产生特异性,提高小肠吸收作用,而且会与肿瘤细胞中的胸苷磷酸化酶相互作用生成抑制杀伤肿瘤细胞的5- 氟尿嘧啶,对人体伤害较小,该药物在临床上已得到广泛应用。多西他赛、卡培他滨两者药物作用机制不同,但其联合使用疗效明显,能促进乳腺癌患者肿瘤细胞的抑制,且两者联合治疗复发性乳腺癌有效率可达30%~70%。此外,研究发现,多西他赛与卡培他滨的抗肿瘤药性存在区别,胸腺嘧啶磷酸化酶不仅能通过多西他赛提高活性,更能充分发挥卡培他滨的治疗效果。
在本研究中,观察组(62.22%)ORR 明显高于对照组(31.11%),差异有统计学意义(<0.05),这提示联合治疗可促进治疗效果的提高。究其原因,多西他赛通过对微管蛋白进行加工修饰,促使其转化为微管,从而对该蛋白解聚起到较好的抑制作用,进而有效抑制肿瘤转移;卡培他滨进入机体会被迅速吸收,可充分提高药物利用率,有助于生成脱氧氟胞苷及脱氧氟尿苷,在胸腺嘧啶磷酸化酶(TP)作用下进行转变,以抑制肿瘤细胞增殖;两者联用,能够有效增强肿瘤细胞抑制效果,避免肿瘤细胞进一步转移,从而提高治疗效果。
CEA、CA125、CA153、CA199 是乳腺癌患者常用的肿瘤标记物,随着病情进展,CEA、CA125、CA153、CA199 水平会明显升高。其中,CEA 具有广谱性,CA125、CA153、CA199 在乳腺癌患者体内呈现出高表达状态,通过化疗可使其水平明显下降。因此可将上述标志物作为监测病情发展与评价治疗效果的重要指标。本研究中,两组治疗后CEA、CA125、CA153、CA199水平明显下降,且观察组水平显著低于对照组,差异均有统计学意义(<0.05),这提示联合治疗会降低肿瘤标记物水平。究其原因,在TP 酶作用下,卡培他滨可转化为5- 氟尿嘧啶,对肿瘤细胞DNA 合成、分裂起到抑制作用;而多西他赛可促进TP 酶活性增强,具有促进微管稳定性增强的效果。两种药物联用可加强抗肿瘤作用,从而有效改善CEA、CA125、CA153、CA199 等肿瘤标记物水平。
卡培他滨联合多西他赛治疗复发转移乳腺癌的方式,对患者损伤较小。两种药物的治疗机制相互配合,并不会增加用药后的不良反应。本研究中,观察组治疗期间的不良反应发生率为62.22%,对照组为46.67%,两组比较无统计学差异,这提示联合治疗并不会增加患者的不良反应。究其原因是卡培他滨虽具有一定的细胞毒性,但因其可选择性作用于机体,降低对正常组织细胞的影响,从而减小药物副作用,降低机体不良反应。此外,与对照组比较,观察组KPS 评分明显更高,究其原因是多西他赛联合卡培他滨具有较好的协同作用,因其作用机制不同,在提高临床治疗效果的同时,能够有效预防毒性交叉出现,促进患者预后的改善,最终促进生存质量的提高。
综上所述,复发乳腺癌应用多西他赛联合卡培他滨治疗,可提高临床治疗效果和生存质量,降低机体血清CEA、CA125、CA153、CA199 水平及不良反应发生率。

