制备工艺条件对催化剂15%Mn/CePO4低温脱硝活性的影响
仵 静,李 飞,黄 伟,侯 鑫,龚 甍
(西安元创化工科技股份有限公司,陕西 西安 710061)
化石燃料在高温燃烧条件下产生氮氧化物(NOx),其中90%以上的NO来源于煤、石油和天然气的燃烧。伴随着燃煤烟气的过度消耗和汽车尾气的过度排放,大气中氮氧化物含量不断增加,从而引起了一系列环境问题[1-3],如酸雨、雾霾和光化学污染等,由此可见,氮氧化物的脱除刻不容缓。氨选择性催化还原氮氧化物(NH3-SCR)技术是减少固定源和移动源氮氧化物排放并得到工业应用的一种技术。该技术优势:(1) 还原剂NH3有较高的选择性;(2) 脱硝反应可以在低温下进行,如Smirniotis P G等[4]报道的催化剂可在120 ℃使脱硝率达100%。(3) 高空速,如Long R Q等[5]报道的铁系催化剂可以在空速460 000 h-1有较好的脱硝效果。
目前,我国工业化催化剂主要是V-W-Ti系催化剂,脱硝性能优越,但自身存在以下不足[6-7]:(1) V基催化剂有强的氧化二氧化硫的能力,导致还原一氧化氮活性降低;(2) 温度区间窄,中低温催化活性低,高温生成氧化亚氮导致催化活性降低;(3) 五氧化二钒毒性较强,易挥发,对周围环境有很大的影响[8]。所以,非V基催化剂成为研究重点。针对NH3-SCR反应,催化剂必须有酸中心和氧化还原中心[9]。由于过渡金属含磷化合物有特殊的表面酸性和氧化还原中心,李飞等[10]已经合成磷酸铈催化剂,但不足之处是其催化反应温度区间窄,低温活性较低。本文以价格低廉的铈和锰为活性组分,采用水热合成法合成催化剂CePO4和催化剂15%Mn/CePO4,考察合成方法、焙烧温度、水热合成温度、O2浓度、NO含量及NH3/NO比例对催化剂15%Mn/CePO4低温脱硝活性的影响。
1 实验部分
1.1 催化剂制备
称取0.01 mol硝酸亚铈(4.34 g)溶于去离子水中,搅拌均匀澄清后将其加入装有0.005 mol的焦磷酸(0.89 g)水溶液中,搅拌均匀,以一定速率加入6.00 g尿素,等待尿素完全溶解,将溶液置于水热反应釜中110 ℃反应16 h,待其慢慢冷却至室温,将沉淀产物减压过滤用水冲洗,再放入烘箱,110 ℃干燥24 h,最后以升温速率小于20 ℃·min-1升温至500 ℃焙烧4 h,最终得到磷酸盐脱硝催化剂CePO4。
称取0.01 mol硝酸亚铈(4.34 g)溶于去离子水中,搅拌均匀澄清后将其加入装有0.005 mol的焦磷酸(0.89 g)水溶液中,搅拌均匀,以一定速率加入6.00 g尿素,等待尿素完全溶解,再称取0.01 mol醋酸锰(7.47 g)水溶液慢慢搅拌加入其中,搅拌均匀,将溶液置于水热反应釜中110 ℃反应16 h,待其慢慢冷却至室温,将沉淀产物减压过滤用水冲洗,再放入烘箱,110 ℃干燥24 h,最后以升温速率小于20 ℃·min-1升温至500 ℃焙烧4 h,最终得到磷酸盐和氧化锰复合脱硝催化剂15%Mn/CePO4。
1.2 催化剂表征
XRD采用荷兰Panalytical BV公司X’pert powder X射线衍射仪测定,Cu靶,工作电压40 kv,工作电流200 mA,扫描速率8°·min-1、扫描范围10°~80°。
比表面和孔径分布采用ZXF-05型自动吸附仪测定,样品在350 ℃真空处理1 h,N2为吸附质,77 K测定。
NH3-TPD,样品100 mg,程序升温至150 ℃,并在此温度N2吹扫30 min,150 ℃下脉冲吸附NH3,降温至50 ℃吹扫物理吸附的NH3,最后从50 ℃程序升温至800 ℃脱附NH3,升温速率10°·min-1。
1.3 催化剂活性测试
将制备的催化剂进行压片,研磨,筛取出粒径(40~60)目的颗粒进行活性测试,反应条件:NO含量1 000×10-6,NH3含量1 000×10-6,O2浓度3.5%,N2为平衡气,反应温度(150~350) ℃,空速20 000 h-1,反应进出口氮氧化物浓度采用傅立叶红外变换光谱仪在线检测。
2 结果与讨论
2.1 制备方法
在NO含量1 000×10-6、NH3含量1 000×10-6、反应温度(150~350) ℃和空速20 000 h-1条件下,不同制备方法对催化剂15%Mn/CePO4低温脱硝活性的影响如图1所示。

图1 不同制备方法对催化剂15%Mn/CePO4低温脱硝活性的影响
由图1可以看出,在低温区(150~350) ℃,水热合成法制备的催化剂优于溶剂热法和共沉淀法。
2.2 焙烧温度
在NO含量1 000×10-6、NH3含量1 000×10-6、反应温度(150~350) ℃和空速20 000 h-1条件下,不同焙烧温度对催化剂15%Mn/CePO4低温脱硝活性的影响如图2所示。

图2 不同焙烧温度对催化剂15%Mn/CePO4低温脱硝活性的影响
由图2可以看出,焙烧温度对催化剂15%Mn/CePO4低温脱硝活能的影响不大,500 ℃活性最佳,表明400 ℃以上催化剂已经完成晶型转变。因此,选择低温焙烧温度500 ℃为宜。
2.3 水热合成温度
在NO含量1 000×10-6、NH3含量1 000×10-6、反应温度(150~350) ℃和空速20 000 h-1条件下,不同水热合成温度对催化剂15%Mn/CePO4低温脱硝活性的影响如图3所示。

图3 不同水热合成温度对催化剂15%Mn/CePO4低温脱硝活性的影响
由图3可以看出,水热合成温度150 ℃的催化剂催化效果较好,达90%。因此,反应温度(150~350) ℃时,选择水热反应温度150 ℃为宜。
2.4 O2浓度
在NO含量1 000×10-6、NH3含量1 000×10-6、反应温度300 ℃和空速20 000 h-1条件下,原料气O2浓度对催化剂15%Mn/CePO4低温脱硝活性的影响如图4所示。
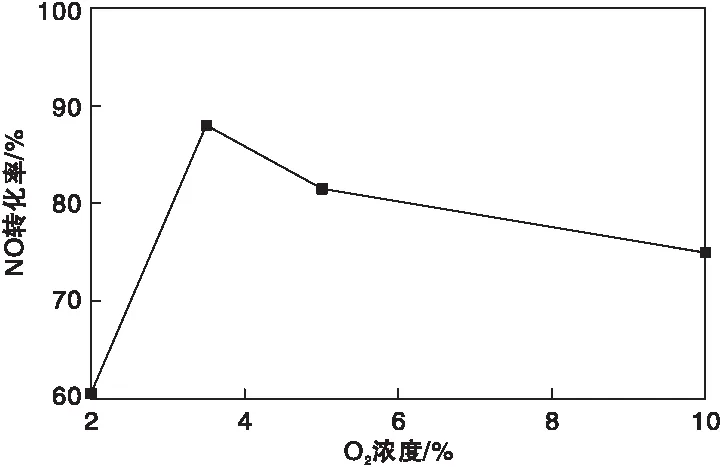
图4 原料气O2浓度对催化剂15%Mn/CePO4低温脱硝活性的影响
由图4可以看出,催化剂15%Mn/CePO4的低温NO转化率受O2浓度的影响较小,O2浓度为3.5%时,具有较高的NO转化率。
2.5 NO含量
在V(NH3)∶V(NO)=1.0、O2浓度3.5%、反应温度300 ℃和空速20 000 h-1条件下,原料气NO含量对催化剂15%Mn/CePO4低温脱硝活性的影响如图5所示。

图5 原料气NO含量对催化剂15%Mn/CePO4低温脱硝活性的影响
由图5可以看出,原料气NO含量对催化剂15%Mn/CePO4低温NO转化率影响较大,当NO含量为780×10-6时,催化剂15%Mn/CePO4具有最高的NO转化率,约93%。
2.6 V(NH3)∶V(NO)
在O2浓度3.5%、反应温度300 ℃和空速20 000 h-1条件下,原料气V(NH3)∶V(NO)对催化剂15%Mn/CePO4低温脱硝活性的影响如图6所示。

图6 原料气V(NH3)∶V(NO)对催化剂15%Mn/CePO4低温脱硝活性的影响
由图6可以看出,原料气V(NH3)∶V(NO)对催化剂15%Mn/CePO4低温脱硝活性影响较大,当V(NH3)∶V(NO)<0.8时,可能由于表面吸附的NH3物种数量不足,无法和吸附的NOx充分反应,活性较低。当V(NH3)∶V(NO)=0.8时,转化率最高。当V(NH3)∶V(NO)>1.2时,NH3可能和NO发生竞争吸附,降低了催化剂活性。
2.7 CePO4和15%Mn/CePO4催化活性测试
在NO含量1 000×10-6、NH3含量1 000×10-6、O2浓度3.5%、反应温度(150~350) ℃和空速20 000 h-1条件下, CePO4和15%Mn/CePO4催化剂的活性测试如图7所示。

图7 CePO4和15%Mn/CePO4催化剂的活性测试
由图7可以看出,在低温测试温度下,15%Mn/CePO4催化剂活性明显优于CePO4的催化活性。15%Mn/CePO4在250 ℃催化活性超过90%。
2.8 BET
CePO4和15%Mn/CePO4催化剂的比表面积及孔容如表1所示。

表1 CePO4和15%Mn/CePO4催化剂的比表面积及孔容
由表1可以看出,掺杂元素Mn的催化剂,比表面积及孔容均有提高,这有利于提高反应气体在催化剂内的接触面积和反应速率,比表面积越大,越有利于催化剂的低温脱硝活性。
2.9 XRD
CePO4和15%Mn/CePO4催化剂的XRD图如图8所示。由图8可以看出,CePO4的结构与pdf卡片库中的六方型结构CePO4(PDF 04-0632)相对应,衍射峰较窄,而15%Mn/CePO4催化剂的衍射峰发生宽化,表明具有更小的晶粒度,衍射峰相对于CePO4催化剂向小角度发生偏移,表明较大离子半径的掺杂进入了CePO4催化剂,取代了Ce。同时复合金属催化剂出现了新的XRD衍射峰,如23.1°、32.9°、55.2°和65.8°,这些衍射峰与pdf卡片库中的(PDF 41-1442)Mn2O3结构相对应,表明一部分Mn2O3分散在CePO4载体表面。

图8 CePO4和15%Mn/CePO4催化剂的XRD图
2.10 NH3-TPD
在 SCR 反应中,催化剂表面酸性点位的多少直接决定 NH3在表面的吸附及参与化学反应的能力。CePO4、15%Mn/CePO4催化剂的NH3-TPD曲线如图9所示。

图9 CePO4、15%Mn/CePO4催化剂的NH3-TPD曲线
由图9可以看出,CePO4和15%Mn/CePO4催化剂在(100~250) ℃有一个大的脱附峰和一个小的脱附峰,表明该峰对应催化剂弱酸位吸附的NH3是吸附在 L酸性位上。由图9还可以看出,催化剂15%Mn/CePO4有较大的脱附峰面积,催化剂表面酸性主要依靠弱酸吸附,且弱酸性越弱,低温脱硝效果越好。
3 结 论
以价格低廉的铈和锰为活性组分,采用水热合成法制备催化剂CePO4和15%Mn/CePO4,考察合成方法、焙烧温度、水热合成温度、O2浓度、NO含量及V(NH3)∶V(NO)对催化剂15%Mn/CePO4低温脱硝活性的影响,得到最佳工艺条件:合成方法为水热合成法,焙烧温度500 ℃,水热合成温度150 ℃,O2浓度3.5%,NO含量780×10-6,V(NH3)∶V(NO)=0.8。

