香草醛调控蜡质玉米淀粉-壳聚糖交联薄膜的结构和性能
张旭鑫,张书艳,李琳,朱杰*,赵雷
(1.华南农业大学食品学院,广东广州 510642)(2.东莞理工学院食品营养健康与智能化加工研究中心,中国轻工业健康食品开发与营养调控重点实验室,化学工程与能源技术学院,广东东莞 523808)
保鲜是保障食品质量与安全的重要途经之一,与传统的物理、化学等保鲜方法相比,活性包装(active packaging)的使用可达到改善食品感官特性,具有延长货架期、增强抗菌和提高抗氧化性能的作用[1,2]。活性包装即在包装材料或包装空隙处加入特殊组分,如包装材料中添加精油(essential oil),精油是一类纯天然、无毒无害的食品添加剂,具有抗菌、杀虫及抗氧化活性,因此,精油广泛应用于活性包装中[3,4]。此外,由于精油提取工艺简单、绿色、安全、高效、原料易得等优势,逐渐成为一种新型的食品保鲜技术,如葡萄精油、姜黄精油、丁香精油及柠檬精油等的应用[5-7]。
活性包装材料中最常见的石油基聚合物具有不可生物降解的劣势[8]。因此,近些年来,可降解生物基活性包装材料如淀粉、纤维素、蛋白质、壳聚糖等生物基包装材料逐渐引起人们的关注[3,9-11]。有研究表明,米淀粉与鱼蛋白不同比例共混并加入牛至精油后,共混体系的溶解性、水蒸气渗透率均下降,可用于防止水果和蔬菜的褐变[12]。此外,壳聚糖基薄膜中加入迷迭香精油后,薄膜的溶解性和吸水率分别下降了25%和85%,薄膜的紫外透过率提高,抗菌活性也增强[13]。壳聚糖中含有亲水性的羟基、羧基和氨基,是自然界中唯一的天然碱性多糖[14]。在活性包装材料中,壳聚糖与淀粉交联可改善壳聚糖基薄膜性能差和抗菌性不明显等缺点[15]。此外,在木薯淀粉与壳聚糖交联体系中加入植物精油和石榴提取物,并对番茄进行涂抹处理时,番茄的水分损失和可溶性固形物损失均下降[16]。当在淀粉与壳聚糖形成薄膜中加入迷迭香精油后薄膜的水蒸气透过率、溶解性、吸水性下降,拉伸强度上升,且可降低黄曲霉毒素的产生[17]。
高支链玉米淀粉在中国产量丰富,价格低廉、应用广泛,目前精油在淀粉-壳聚糖交联体系中的作用研究中,对高支链玉米淀粉的研究不足。本研究以高支链蜡质玉米淀粉(waxy)为主要原料,制备蜡质玉米淀粉-壳聚糖薄膜,并研究香草醛对蜡质玉米淀粉-壳聚糖交联薄膜结构和性能的影响,为进一步拓宽玉米淀粉/壳聚糖在活性食品包装中的应用提供参考。
1 材料与方法
1.1 材料与试剂
蜡质玉米淀粉(waxy,直链淀粉含量为0.67%±0.07%[15]),秦皇岛骊华淀粉股份有限公司;壳聚糖(chitosan,粘度:100~200 mPa·s)、香草醛(vanillin),分析纯,上海麦克林生化科技有限公司;冰醋酸(CH3COOH)、聚乙二醇(Polyethylene glycol,average Mn=4000,简称PEG),分析纯,上海阿拉丁生化科技股份有限公司。
1.2 主要仪器与设备
KLJX-8型均相反应器,郑州长征仪器制造有限公司;RWD100搅拌器,上海沪析实业有限公司;POWEREACH接触角测量仪,上海中晨数字技术设备有限公司;EM-30 PLUS+扫描电子显微镜,韩国COXEM(库塞姆)公司;DX-27mini X-射线衍射仪,辽宁丹东浩元仪器有限公司;Spectrum Two傅立叶红外光谱仪,美国PE公司;TGA 8000热重分析仪,美国PE公司。
1.3 方法
1.3.1 蜡质玉米淀粉与壳聚糖交联薄膜的制备
称取蜡质玉米淀粉(waxy)0、0.60、1.00、1.40、2.00 g置于100 mL高压反应釜的聚四氟乙烯内胆中并加入20 mL去离子水,然后将反应釜置于均相反应器中,反应温度为100 ℃,转速为15 r/min,时长2 min,使淀粉充分糊化后倒入锥形瓶中。分别称取壳聚糖2.00、1.40、1.00、0.60、0 g,用40 mL(1%,V/V)乙酸溶液溶解后倒入糊化淀粉中,淀粉与壳聚糖的质量比为2:0、1.4:0.6、1:1、0.6:1.4、0:2(为更直观地表现淀粉与壳聚糖质量比,故用10:0、7:3、5:5、3:7、0:10来表示)。后用电动搅拌器进行搅拌,转速为300 r/min,10 min后再加入0.12 g(4%,m/m)的交联剂聚乙二醇(PEG),搅拌40 min,使淀粉与壳聚糖充分混合交联。完成后把混合体系于0.1~0.5 MPa真空下抽滤脱气0.5 h,然后将溶液倒入直径d为200 mm的培养皿中,置于45 ℃烘箱中恒温24 h,烘干后将所制备的交联薄膜置于干燥器中储存。
1.3.2 添加香草醛交联薄膜的制备
将1.3.1步骤中淀粉-壳聚糖混合溶液加入交联剂PEG后,继续搅拌35 min,加入0.02 g(1%,m/m)的香草醛,继续搅拌20 min,充分混合并把混合体系于0.1~0.5 MPa真空下抽滤脱气0.5 h,后倒入直径d为200 mm的培养皿中,置于45 ℃烘箱中恒温24 h,烘干后置于干燥器中储存。
1.3.3 傅里叶红外光谱分析
将样品置于装有ATR附件的傅里叶红外光谱仪上,压头旋紧后使薄膜样品与晶体表面紧密接触,以空气作为背景,扫描范围400~4000 cm-1,扫描次数为16次,选同张薄膜表面不测试点扫描三次取平均值。
1.3.4 X-射线衍射分析
剪取样品尺寸为2×2 cm2,平铺于样品盘上的凹槽内,置于X-射线衍射仪的载物台上,采用Cu-Kα射线源(λ=0.1542 nm),测试电流及电压分别为40 mA和40 kV。测量角度2θ=5 °~50 °,步长0.02 °,扫描速度0.1 °/s。
1.3.5 扫描电子显微镜观察
剪取0.5 cm×0.5 cm大小的薄膜至于液氮中进行自然脆断,用胶带将样品断面朝上固定在样品台上,真空喷金30 s,电压20 kV,后置于扫描电子显微镜中进行拍摄具有代表性的照片。
1.3.6 水接触角分析
在室温条件下,将交联薄膜置于测量仪上进行表面接触角的测试(与平板接触的面朝上),本实验采用静态滴定法,以接触平板的薄膜表面为测定面,测定蒸馏水液滴与薄膜样品接触时刻的水接触角。
1.3.7 热失重分析
称取样品约5 mg,置于样品盘中。设置升温程序:30~600 ℃,升温速率为10 ℃/min,吹扫气体为氮气(N2),流速为20 mL/min。将TG曲线进行一阶求导得到DTG曲线,并利用软件标示热失重速率曲线的Peak温度。
1.3.8 数据处理
waxy淀粉-壳聚糖交联薄膜接触角和峰值温度均进行3次平行测定,所得实验数据均利用SPSS 22.0统计分析软件进行方差分析(p<0.05)。
2 结果与讨论
2.1 分子结构表征
图1为衰减全反射(ATR)模式下,不同质量比下,添加精油前后waxy玉米淀粉与壳聚糖交联薄膜的红外光谱图。前期研究表明,淀粉分子在3300 cm-1附近形成-OH的伸缩振动峰,在1010 cm-1附近形成C-O-C键的对称伸缩振动峰;壳聚糖分子在3408 cm-1和1081 cm-1处形成-OH和C-O键的伸缩振动,在1554 cm-1处形成壳聚糖分子中-N-H的变形振动(deformation vibration)[18,19]。
由图1a观察可知,未加香草醛时,淀粉自交联薄膜在3288.25 cm-1(10:0)形成-OH伸缩振动峰,淀粉-壳聚糖交联薄膜在3270.56 cm-1(5:5)和1015.26 cm-1(5:5)附近均形成-OH和葡萄糖环C-O-C键的伸缩振动峰。随着壳聚糖添加量的增加,-OH伸缩振动峰波数由3288.5 cm-1(10:0)降至3280.27 cm-1(0:10);壳聚糖分子中-N-H变形振动峰波数由1561.12 cm-1(7:3)下降至1551.46 cm-1(0:10)。有研究表明,相对稳定作用力的形成促使红外光谱的波数减小[20]。因此,上述结果淀粉与壳聚糖间的氢键作用强于淀粉自交联作用。
加入香草醛后,交联体系对应特征基团的红外光谱如图1b所示。由图可知,体系中-OH伸缩振动、-N-H变形振动的变化均与未加精油的交联薄膜相似,-OH伸缩振动峰的波数由3292.17 cm-1(10:0)降至3258.27 cm-1(0:10);-N-H变形振动峰波数由1552.35 cm-1(7:3)降至1541.46 cm-1(0:10)。由此可知,加入香草醛后,香草醛分子中-CHO与壳聚糖-NH3+相互作用形成-C=N键,香草醛与waxy玉米淀粉形成新的氢键作用,弱化了淀粉与壳聚糖间的氢键作用。
2.2 结晶结构表征
图2为添加香草醛前(图3a)后(图3b)waxy玉米淀粉-壳聚糖交联薄膜的X-射线衍射图谱。淀粉在经过糊化作用处理后,淀粉分子中晶态和非晶态结构中的氢键作用均被破坏,促使淀粉的结晶结构消失,同时,壳聚糖分子在2θ=10.80 °和2θ=19.90 °附近有明显的衍射峰[21,22]。由图2a可知,不同质量比下,waxy玉米淀粉-壳聚糖交联薄膜体系均呈宽泛的弥散峰,即交联薄膜内部形成无定形结构。由图2b可知,加入精油后,不同质量比条件下淀粉-壳聚糖交联薄膜的衍射图谱仍呈现宽泛的衍射峰,表明香草醛的加入并不改变交联薄膜体系的无定形结构。而当waxy淀粉/壳聚糖自交联时,分别在2θ=15.34 °和15.56 °处形成较弱衍射峰,对应香草醛2θ=13.16 °处的强衍射峰(未在图中标明),表明在淀粉/壳聚糖自交联薄膜体系中,空间位阻或自交联作用导致香草醛中的-CHO未能充分参与反应;而当薄膜体系中存在淀粉、壳聚糖与香草醛三种组分时,三者间的相互作用维持了薄膜内部的无定形结构。
2.3 断面形貌分析
由图3a可知,waxy玉米淀粉/壳聚糖自交联薄膜的断面均形成不同程度的规则孔洞结构。淀粉与壳聚糖交联后,薄膜断面的平整度均不同程度的上升,形成褶皱或颗粒状突起结构。由图3b可知,加入香草醛后,随着壳聚糖添加量的增加,waxy玉米淀粉-壳聚糖交联薄膜的颗粒度降低、平整度增大,形成均匀的断面形貌。
壳聚糖的氨基质子在酸的作用下形成-NH3+,淀粉分子中的有序结构经过糊化作用后被破坏,淀粉分子中的-OH与壳聚糖分子中的-NH3+反应并形成新的氢键,增强淀粉与壳聚糖之间的相容性,断面的平整度增大[23]。当淀粉添加量较多时,高支链淀粉的空间位阻抑制其与壳聚糖交联,导致交联薄膜断面的粗糙度较大。加入香草醛后,香草醛分子中的-CHO与壳聚糖分子中的-NH3+作用形成新的-C=N键,减弱淀粉与壳聚糖的氢键作用,同时,碳氮双键的形成促使交联薄膜的断面平整度随壳聚糖添加量的增加而增大。
2.4 水接触角分析
图4a和4b为不同质量比,添加香草醛前后交联薄膜WCA值的变化情况,表1为WCA值的汇总。前期实验结果可知,淀粉自交联薄膜的成膜性差,无法测定其水接触角[15]。由表可知,未加香草醛时,随着壳聚糖添加量的增大,交联薄膜的接触角呈下降趋势,WCA值由82.88 °(7:3)下降至75.37 °(0:10)。加入香草醛后,随着壳聚糖添加量的增加,WCA值先下降后上升。同时,当淀粉/壳聚糖质量比相同时,淀粉添加量较高时,添加香草醛的交联薄膜WCA值较未添加香草醛时低;淀粉添加量较高时则相反。
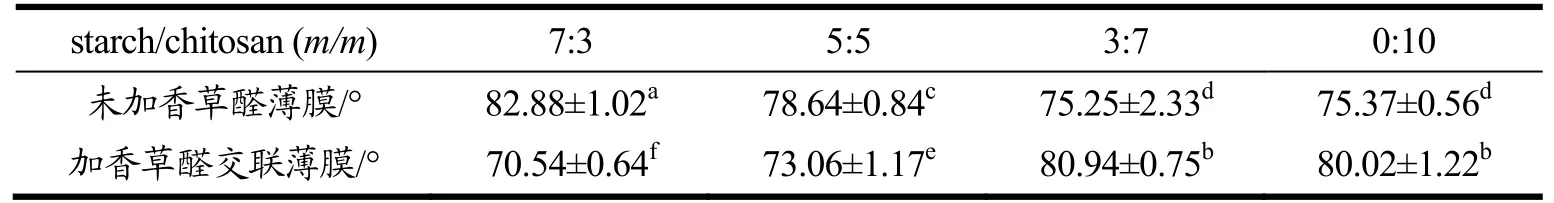
表1 不同质量比添加香草醛前后waxy玉米淀粉-壳聚糖交联薄膜的水接触角Table 1 Water contact angles of waxy corn starch-chitosan crosslinking film by different mass ratios with (without) vanillin addition
在交联体系中加入香草醛后,壳聚糖分子中-NH3+与香草醛分子中-CHO形成碳氮双键[24];同时,香草醛分子与淀粉分子形成氢键作用。壳聚糖添加量较小(7:3、5:5)时,由于waxy高支链淀粉的空间位阻作用,促使香草醛中的-CHO优先与壳聚糖分子中-NH3+作用;此外,淀粉、壳聚糖大分子间的交联受到抑制,促使体系中自由-OH增加,薄膜的亲水性增大。壳聚糖添加量较大(3:7、0:10)时,小分子香草醛分子与壳聚糖、淀粉分子相互作用,壳聚糖分子自交联,促使薄膜中的亲水性减小。
2.5 热性质分析
图5a和5b为不同质量比,淀粉-壳聚糖交联薄膜加入香草醛前后的热失重曲线(实线)及失重速率曲线(虚线)。实验可知,香草醛在195.49 ℃有明显的失重峰(未在图中标明)。由图可知,交联薄膜主要呈现出两个热损失阶段:第一阶段(<180 ℃)为水分蒸发;第二阶段(>180 ℃)为淀粉/壳聚糖分子的裂解和解聚,由于二者分子解聚温度相近,在图中表现为混合失重峰,由于香草醛添加量较少(1%),热失重曲线中并未呈现明显的香草醛热损失峰。
未加香草醛时,由图5(a)和表2可知,淀粉/壳聚糖自交联时,淀粉/壳聚糖裂解温度为336.23 ℃(10:0)和310.83 ℃(0:10),淀粉-壳聚糖交联薄膜中大分子裂解温度均低于淀粉/壳聚糖自交联薄膜;且随着壳聚糖添加量的增加,交联薄膜中大分子的裂解温度呈逐渐下降趋势。加入香草醛后,随着壳聚糖添加量的增加,薄膜中大分子裂解温度也降低,且都低于淀粉/壳聚糖自交联薄膜;同时,交联薄膜中大分子的裂解温度均低于未加香草醛的薄膜。
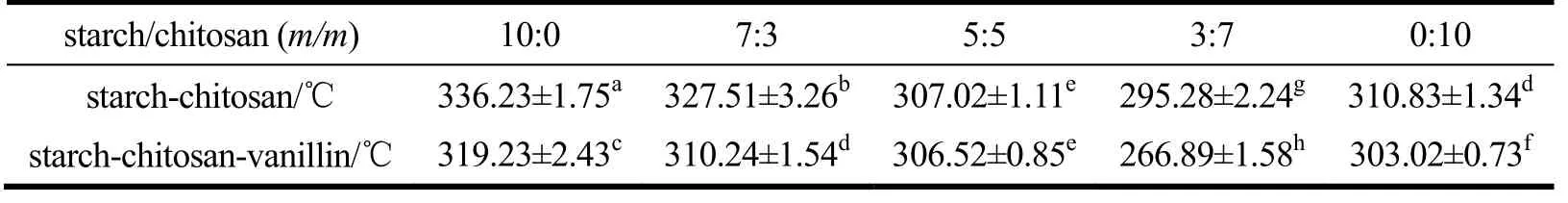
表2 不同质量比waxy玉米淀粉-壳聚糖交联薄膜添加香草醛前后分子裂解峰值温度Table 2 Peak temperatures of molecular decomposition for waxy cornstarch-chitosan crosslinking films by different mass ratios before(a) and after (b) vanillin addition
前期研究表明,淀粉与壳聚糖交联后,薄膜形成更多的无定形结构,导致解聚温度降低[15]。在淀粉/壳聚糖自交联薄膜中,氢键作用的形成促使交联薄膜中大分子的解聚温度高于淀粉-壳聚糖交联的薄膜。而加入香草醛后,香草醛的热分解破坏了香草醛与壳聚糖间的碳氮双键,同时减弱了香草醛与淀粉间的氢键作用,促使淀粉/壳聚糖的解聚温度下降。
3 结论
waxy玉米淀粉与壳聚糖交联过程的实质是淀粉分子内氢键、壳聚糖分子内氢键及淀粉-壳聚糖分子间氢键作用力的形成。在交联体系中添加香草醛后,香草醛、淀粉与壳聚糖间产生竞争作用,一方面香草醛分子中-CHO与壳聚糖分子中-NH3+作用形成-C=N键;另一方面,香草醛分子-OH与淀粉分子-OH形成新的氢键。-C=N键和新氢键的形成抑制了淀粉分子内氢键作用、淀粉-壳聚糖分子间氢键及壳聚糖分子内氢键作用。且随着壳聚糖添加量的增加,薄膜体系中形成更多的-C=N键,促使大分子间作用力减弱,自由羟基增多,薄膜的亲水性增强,-N-H键伸缩振动峰波数降低,淀粉/壳聚糖分子的解聚温度下降。以上实验结果可为淀粉和壳聚糖在新型包装材料中的应用提供实验数据和理论基础。

