苁蓉连翘合剂质量标准研究*
刘 娟,韩文均,范 伟,时扣荣,张春燕,辛蓓玮,顾伟鹰,朱建勇
(上海中医药大学附属第七人民医院,上海 200137)
苁蓉连翘合剂处方源于上海市名老中医叶景华教授的经验方,由肉苁蓉、连翘、菟丝子、续断、巴戟天、佛手6 味中药组方,已在我院临床应用20 余年[1],多用于治疗早泄,尤其对早泄型射精功能障碍具有良好疗效[2]。方中肉苁蓉为君药,其味甘咸,性温,质润,既能补肾阳、又能益精血,补而不峻、补中有通,《神农本草经》谓其“养五脏,强阴,益精气”;连翘为臣药,其性凉味苦,清心降火;菟丝子、续断、巴戟天为佐使药,可补肝肾、强筋骨;佛手具有疏肝理气、条畅气机功效。该方疗效确切,安全稳定,已获得发明专利授权[3],为了扩大其临床应用范围,拟开发成院内制剂及中药复方制剂。为控制苁蓉连翘合剂质量,本研究中采用薄层色谱(TLC)法对合剂中的肉苁蓉、连翘、佛手进行TLC 鉴别,采用高效液相色谱法测定君药肉苁蓉中松果菊苷的含量,为苁蓉连翘合剂的质量控制提供客观的评价方法。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 1260 型高效液相色谱仪(美国Agilent 公司);CP225D 型电子天平(北京赛多利斯仪器系统有限公司);DL720 - A 型超声波清洗仪(上海之信仪器有限公司);SHZ - D(Ⅲ)型循环水式真空泵(郑州博科设备有限公司);RV-10型旋转蒸发仪(德国IKA公司);BD-Ⅱ型多功能紫外分析仪(北京启航博达科技有限公司);HWS28 型电热恒温水浴锅(上海一恒科学实验有限公司);DNG-9140A型电热恒温干燥箱(上海精宏实验设备有限公司)。
1.2 试药
苁蓉连翘合剂(医院中心实验室,批号分别为20180601,20180602,20180603);连翘苷对照品(批号为111670 - 201706,含量为95.1%),松果菊苷对照品(批号为110821-201615,含量为97.2%),柚皮苷对照品(批号为110722-201714,含量为96.2%),均购于中国食品药品检定研究院;聚酰胺薄层板(浙江省台州市路桥四甲生化塑料厂);硅胶G薄层板(山东省烟台江友硅胶开发有限公司);甲醇为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 TLC 鉴别
肉苁蓉[4]:取样品5 mL,加水稀释至25 mL,加入石油醚(30~60 ℃),萃取2 次(20,20 mL),弃去石油醚液,剩余溶液再用水饱和正丁醇振摇提取3 次(30,15,15 mL)、合并正丁醇液,蒸干,残渣加甲醇使溶解并定容至5 mL,作为供试品溶液;按苁蓉连翘合剂处方及工艺,制备缺肉苁蓉的阴性样品,按供试品溶液制备方法制成阴性对照品溶液;取松果菊苷对照品适量,加甲醇制成质量浓度为1 mg/mL 的对照品溶液。按2020 年版《中国药典(四部)》通则0502 TLC 法,吸取上述溶液各5 μL,分别点于同一聚酰胺薄层板上,以甲醇- 醋酸-水(2∶1∶7,V/V/V)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的荧光斑点,斑点清晰,阴性对照无干扰。详见图1 A。
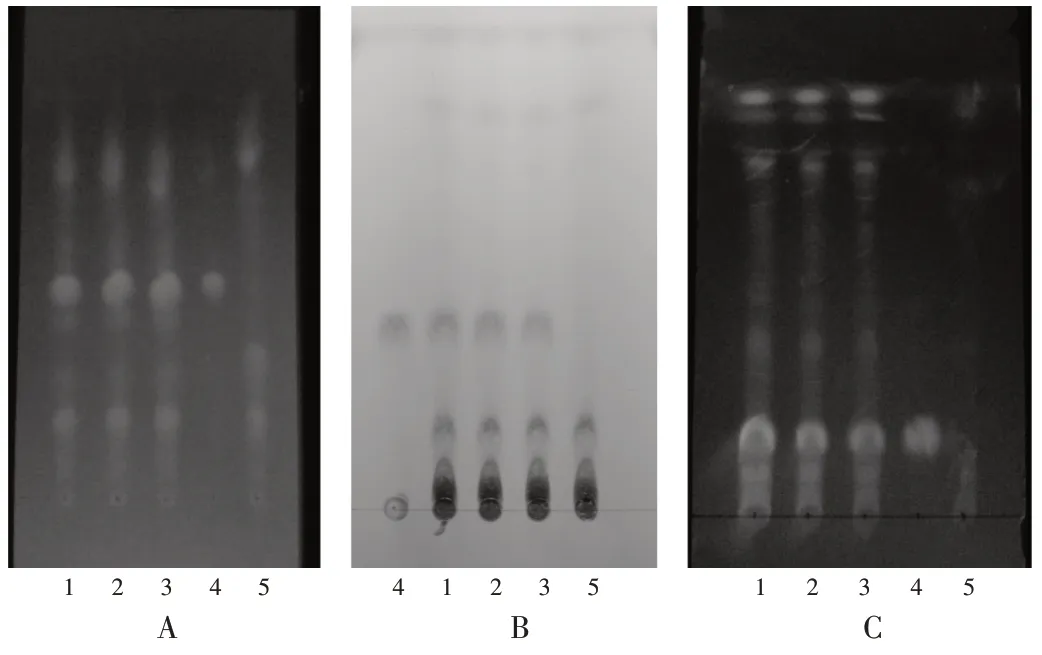
1-3. 供试品溶液(批号分别为20180601,20180602,20180603)4. 对照品溶液 5. 阴性对照品溶液A. 肉苁蓉 B. 连翘 C. 佛手图1 薄层色谱图1-3.Test solution(the batch numbers were 20180601,20180602,20180603)4.Reference solution 5.Negative reference solutionA.Cistanches Herba B.Forsythiae Fructus C.Citri Sarcodactylis FructusFig.1 TLC chromatograms
连翘[5]:取样品5 mL,加水至25 mL,超声(功率600 W,频率40 kHz,下同)处理10 min,用水饱和正丁醇振摇提取3 次(30,15,15 mL)、合并正丁醇液,蒸干,残渣加甲醇使溶解并定容至5 mL,作为供试品溶液;按苁蓉连翘合剂处方及工艺,制备缺连翘的阴性样品,按供试品溶液制备方法制成阴性对照品溶液;取连翘苷对照品,加50%甲醇制成质量浓度为1 mg/mL的对照品溶液。按2020年版《中国药典(四部)》通则0502 TLC法,吸取上述溶液各5 μL,分别点于同一硅胶G薄层板上,以二氯甲烷-甲醇(8∶1,V/V)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的斑点,阴性对照无干扰。详见图1 B。
佛手[6]:取样品5 mL,加水至25 mL,超声处理10 min,用氯仿萃取2 次(20,20 mL),弃去氯仿液,剩余溶液再用水饱和正丁醇振摇提取3 次(30,15,15 mL)、合并正丁醇液,蒸干,残渣加甲醇使溶解并定容至5 mL,作为供试品溶液;按苁蓉连翘合剂处方及工艺,制备缺佛手的阴性样品,按供试品溶液制备方法制成阴性对照品溶液;取柚皮苷对照品,加甲醇制成质量浓度为1 mg/mL的对照品溶液。按2020 年版《中国药典(四部)》通则0502 TLC 法,吸取上述3 批供试品溶液各10 μL、对照品溶液与阴性对照品溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(13∶6∶2,V/V/V)下层液为展开剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,在105 ℃加热约5 min,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的荧光斑点,阴性对照无干扰。详见图1 C。
2.2 含量测定
2.2.1 色谱条件[7]
色谱柱:Agilent Zorbax Eclipse XDB-C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇(A)-0.1%甲酸溶液(B),梯度洗脱(0~10 min 时80%A→60%A,10~15 min时60%A→50%A,15~20 min 时50%A→80%A;流速:1.0 mL/min;检测波长:330 nm;柱温:30 ℃。
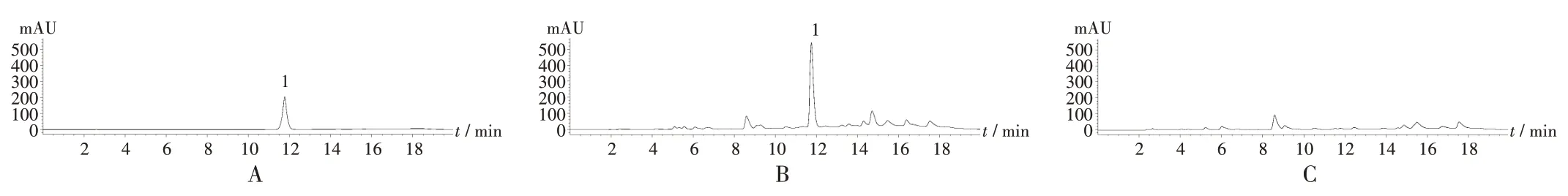
1. 松果菊苷A. 对照品溶液 B. 供试品溶液 C. 阴性对照品溶液图2 高效液相色谱图1.EchinacosideA.Reference solution B.Test solution C.Negative reference solutionFig.2 HPLC chromatograms
2.2.2 溶液制备
取松果菊苷对照品适量,60 ℃减压干燥4 h,加50%甲醇制成质量浓度为1 mg/ mL 的对照品溶液。取样品5 mL,加水稀释至25 mL,超声处理30 min,放冷,摇匀,经微孔滤膜(0.45 μm)滤过,取续滤液,即得供试品溶液。按苁蓉连翘合剂处方及工艺,制备缺肉苁蓉的阴性样品,按供试品溶液制备方法制成阴性对照品溶液。
2.2.3 方法学考察
系统适用性及专属性试验:取供试品溶液5 μL、对照品溶液与阴性对照品溶液各10 μL,按2.2.1 项下色谱条件进样测定。结果理论板数按松果菊苷峰计大于3 000,基线分离良好;阴性对照品溶液在与对照品溶液色谱保留时间相同处无干扰峰,表明专属性良好。详见图2。
线性关系考察:分别取2.2.2项下对照品溶液1.0,2.5,5.0,10.0,15.0,20.0 μL,按2.2.1 项下色谱条件进样测定,并记录峰面积。以松果菊苷进样量(X,μg)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y=296.9X+32.92(r=0.999 9)。结果表明,松果菊苷进样量在1.0~20.0 μg范围内与峰面积线性关系良好。
精密度试验:取2.2.2 项下对照品溶液适量,按2.2.1 项下色谱条件重复进样测定6 次。结果松果菊苷峰面积的RSD为1.02%(n=6),表明仪器精密度良好。
稳定性试验:取供试品溶液适量,分别于室温下放置0,2,4,6,8 h时按2.2.1项下色谱条件进样测定,记录峰面积。结果松果菊苷峰面积的RSD为0.31%(n=5),表明供试品溶液在室温放置8 h内稳定。
重复性试验:精密量取同一批(批号为20180601)样品,共6份,按2.2.2项下方法平行制备6份供试品溶液,再按2.2.1 项下色谱条件进样测定,记录峰面积并计算松果菊苷的含量。结果松果菊苷的平均含量为17.45 mg/mL,RSD为0.97%(n= 6),表明方法重复性良好。
加样回收试验:取已知含量(17.45 mg/mL)的样品(批号为20180601)适量,共9份,分别加入低、中、高质量浓度的松果菊苷对照品各适量,再按2.2.1项下色谱条件进样测定,记录峰面积,并计算加样回收率。结果见表1。
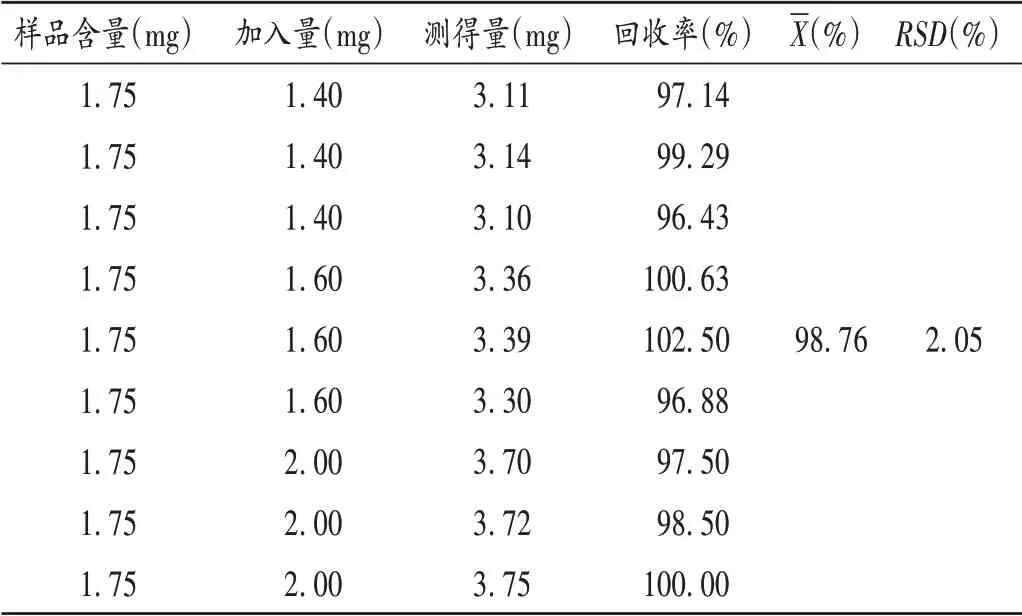
表1 加样回收试验结果(n =9)Tab.1 Results of the recovery test(n=9)
2.2.4 样品含量测定
取3 批样品各适量,分别按2.2.2 项下方法制备供试品溶液,并按2.2.1 项下色谱条件进样测定样品含量。结果3批样品中松果菊苷含量分别为17.59,17.40,17.23 mg/mL,平均含量为17.41 mg/mL。
3 讨论
本研究中参照2020 年版《中国药典(一部)》,采用TLC法对肉苁蓉、连翘、佛手进行定性鉴别[8],并在供试品处理过程中,结合所含成分极性的差异采取差异化处理,肉苁蓉中松果菊苷极性较大,故先采用极性小的石油醚进行脱脂去除干扰,再以水饱和正丁醇萃取,从而有效富集松果菊苷。鉴别佛手中柚皮苷时,考虑其为苷类物质,极性较大,先采用二氯甲烷萃取,去除脂溶性成分,再利用水饱和正丁醇萃取出柚皮苷,所得TLC图斑点清晰,且阴性对照无干扰。
本研究中松果菊苷的含量测定方法主要参考2020年版《中国药典(一部)》肉苁蓉的含量测定方法[8],由于该合剂中松果菊苷含量较高,故样品直接以水稀释,然后滤过,进样测定[9]。另外,梯度洗脱时间设定为20 min,保留时间相差较大,理论板数大于3 000,峰形佳且分离度好,基线较稳定,组分间互不干扰,操作方法简易且高效,结果可靠。
综上所述,本研究中建立的方法简便易行,灵敏度高且重复性好,可用于苁蓉连翘合剂的质量控制。

