安徽某市B河水体多环芳烃含量特征及生态风险评价
蒋少杰,冯松宝,罗贤胜
(1.安徽省地质环境监测总站,安徽合肥 230001;2.宿州学院资源与土木工程学院,安徽宿州 234000)
0 引言
多 环 芳 烃(polycyclic aromatic hydrocarbons,PAHs)20世纪70年代就已经被国际癌症研究中心(IARC)列为致癌物[1]。多环芳烃是一种持久性有机污染物(POPs)[2],能够长时间存在于环境中,并持久性地对人体造成严重影响,对生物体有遗传毒性[3~4]。多环芳烃具有三致作用(致癌、致畸、致突变)和内分泌干扰作用[5]。樊晶光[6]对多环芳烃诱导的致癌作用与免疫毒性进行了研究。近年来研究发现,多环芳烃能够在暴露的空气中,受紫外线影响产生光致毒效应,使PAHs光化学氧化成为直接致突变物[7]。如孙红文[8]对于多环芳烃的光致毒效应进行了研究,匡少平[9]对多环芳烃的光致毒效应和致癌机理方面做了研究,唐治炜[10]建立了固相萃取-气相色谱/质谱联用测定河水中16种多环芳烃的分析方法。
城市中流动的河流,一般都是工业废物排放的最佳场地。多环芳烃在城市的河流中主要来源有:生活污水的排放,工厂化石燃料的不完全燃烧和石化产品产生的有机污染物,市内交通的气体排放等[11],使得多环芳烃在环境中富集含量越来越高。多年来,安徽省地质环境监测总站等单位,对淮北平原包括某市区域地下水环境做了大量研究工作,而对于地表水环境关注不够以致于研究较少。因此,为了弥补相对不足,安徽省地质环境监测总站和宿州学院资源与土木工程学院联合对地表水环境中的多环芳烃问题尝试开展相关研究,基于此,对安徽省某市B河水体中多环芳烃含量进行了检测并对其生态风险进行了分析评价。
1 研究区概况
安徽某市B河是经过某市区的一条主要河流,北起A河,南至某市外环南路,全长10.5km,途经某市三角洲生态公园、某市市区、电厂、医院、某市郊区。沿某市B河两岸,建有B河景观带,是提供人们生活、休闲、娱乐的场所。同时在B河闸上游两侧以往有某县木材加工厂、老农药厂等分布。现如今,某市经开区化工园区就分布在B河闸以下西侧。另外,某市城区北关火电厂就位于B河和A河叉口之间(紧靠B河),京沪铁路货场位于B河闸西侧,长年堆积、运输大量煤炭。
2 调查评价方法
2.1 样品采集方法
2.1.1 采样布局
本次采样主体物质为水体,根据水流分散发育的规律,结合水系长度、水系异常等可能的衰减速度,适当选择采样密度,保持采样点分布的均匀性。结合实地情况及采样困难程度,本次采样依据河道走向、宽度等情况进行等距采样(即网格布点法)。
2.1.2 样品采集
使用液体采样器沿B河岸边,约每千米标记一个点,每个点采取B河水体水样1L。在某市内共采集10个点,分别命名为TH-2-1—TH-2-10。采样点分布如图1所示。
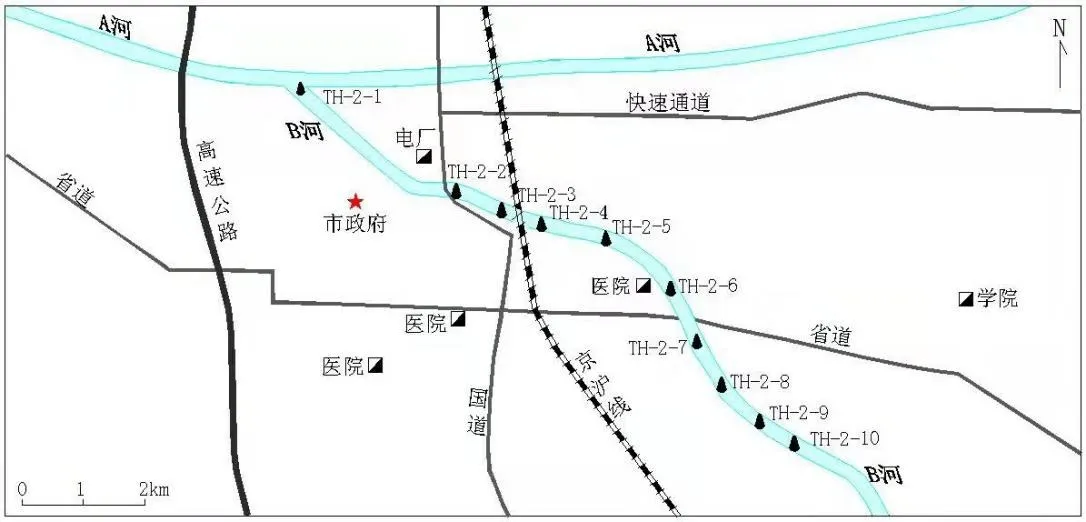
图1 安徽省某市B河水体采样点分布图Figure 1.Distribution of sampling spots along the river B in a city of Anhui Province
2.2 样品分析测试
2.2.1 样品制备
仪器:液体采样器,抽滤装置,SPEColumnC18固相萃取柱(500mg/6mL,美国),固相萃取装置(SPE-12A),无油真空泵(PS-10),氮吹仪(NDK200-1),液体自动进样器(AI1310,美国赛默飞世尔科技有限公司),气相色谱-质谱联用仪(ISQQD,TRACE1300,美国赛默飞世尔科技有限公司)。
试剂:多环芳烃标准溶液,二氯甲烷(优级纯),甲醇(色谱纯),正己烷(色谱纯),甲苯(色谱纯),去离子水(实验室自制)。
预处理步骤如下:
(1)抽滤。将样品先用抽滤装置抽滤,再用容量瓶定容至1L(滤膜0.45μm)。
(2)活化。使用二氯甲烷(5mL)、甲醇(5mL)、去离子水(5mL)依次加入C18小柱进行活化(活化过程中不能抽干柱床,流速为2mL/min)。
(3)上柱。在水样中加入55mL甲醇,混合均匀后,倒入C18小柱中,控制流速为5mL/min。待混合水样全部流经柱床后,将固相萃取装置真空度开到最大,使其水分全部流出柱床。
(4)洗脱。用10mL正己烷(也可用二氯甲烷代替)分三次加入完全抽干后的C18小柱进行洗脱,流速为2mL/min,收集洗脱液。
(5)浓缩。收集后的洗脱液使用氮吹仪进行浓缩至1mL,然后再用正己烷(或二氯甲烷)进行定容至5mL容量瓶中。混合均匀后,待测。
2.2.2 分析测试
色谱条件:TG-5MS石英毛细管色谱柱(30m×0.25mm×0.25μm);载气为氦气(纯度≥99.999%);采用恒流模式,不分流进样,进样体积为1μL;流速1.2mL/min。升温程序:初始温度40℃,保持2min,再以5℃/min升温至290℃,保持4min。
质谱条件:传输线温度为280℃;离子源为EI源,温度为300℃;扫描模式为SIMScan;溶剂延迟5min。
2.2.3 测试质量控制
根据美国国家环保局(USEPA)的标准对实验进行了质量控制与保证。对平行样、空白样及基质加标样的每个样品使用内标法对其回收率进行了检测,结果显示回收率在78.53%~119.64%。实验数据结果进行了回收率校正处理。
3 特征分析和来源解析及生态评价
3.1 含量
本次对于某市B河水采集了10个样品,经气相色谱-质谱联用仪定性、定量分析后,检测结果见表1。
本次对于某市B河水共采取了10个样品,对于单体PAHs而言,水相中萘的含量最高。萘最高含量达到了20.76050ng/g,最低含量为18.65145ng/g,平均含量为19.55960ng/g。B河水中PAHs第二含量高的是苊,最高含量为16.59420ng/g,最低含量为16.51040ng/g,平均含量为16.55187ng/g。从表1测试数据结果显示,除了萘、苊的含量高达16.51040ng/g及以上,其他的PAHs含量均在5.19060ng/g及以下。除了二氢苊、苯并[a]芘、茚苯并[1,2,3-c,d]芘的含量未检测出外,苯并[k]荧蒽的含量为最低,即为1.73800ng/g。
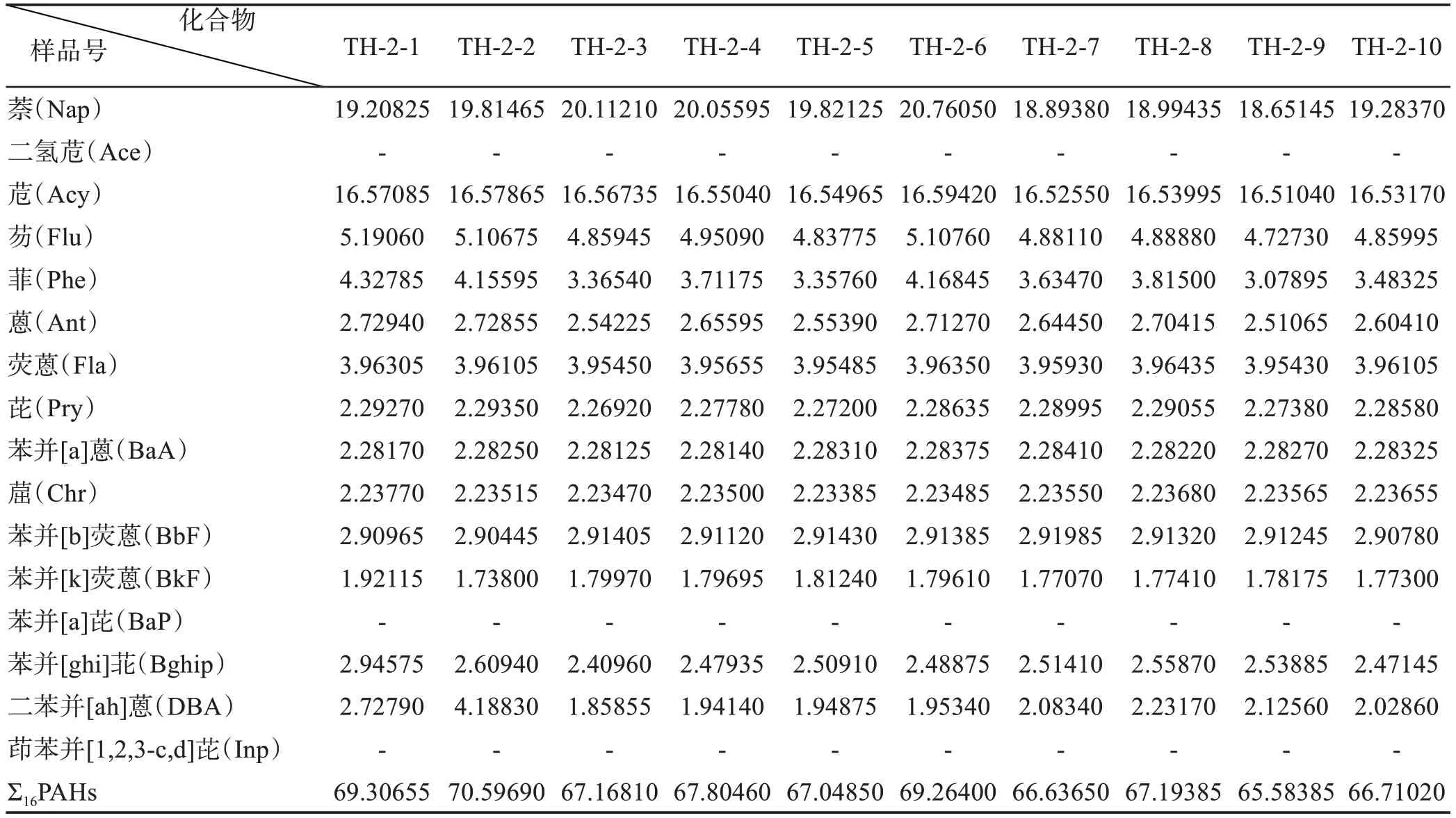
表1 某市B河水样中PAHs的含量(单位:ng/g)Table 1.The content of PAHs in water samples from the river B of a city(unit:ng/g)
3.2 某市B河水中PAHs来源解析
对于水中PAHs来源解析一般使用特征比值法(MOR),即用PAHs的同分异构体比值来判断PAHs的来源,如根据Fla/(Fla+Pyr)、BaA/(BaA+Chr)比值进行判断。判断PAHs来源的方法见表2。
根据特征比值法,用PAHs的同分异构体比值(即Fla/(Fla+Pyr)、BaA/(BaA+Chr)的比值)求得表3数据。根据表3数据可知,Fla/(Fla+Pyr)比值的最大值为0.63539,最小值为0.63331,平均值为0.63425;结合表2的特征值判断方法可知,Fla/(Fla+Pyr)的比值均大于0.5,所以某市B河水中PAHs的来源为煤炭、木材等生物质燃烧源。根据表3数据可知,BaA/(BaA+Chr)比值的最大值为0.50545,最小值为0.50487,平均值为0.50520;结合表2的特征值判断方法可知,BaA/(BaA+Chr)的比值均大于0.35,所以某市B河水中PAHs的来源为燃烧源。

表2 特征比值法分析PAHs来源的方法(据徐红,2018修改)Table 2.Analysis of the sources of PAHs using characteristic ratio method(modified,after Xu Hong,2018)
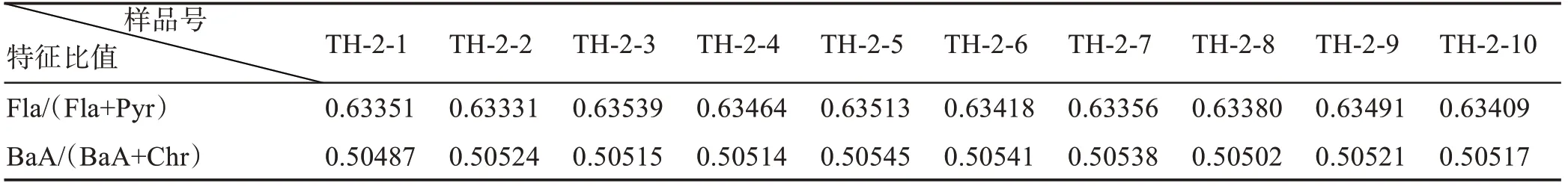
表3 某市B河水中PAHs的特征比值Table 3.Characteristic ratios of PAHs in the river B of a city
根据上述源分析结果及表1中16PAHs数据可知,样品号为TH-2-2的区域采集的水样中检测出的PAHs含量最高,结合钟岩的云南曲靖某煤化工基地及周边土壤中多环芳烃的检测研究[12]与当地实际情况可知,该点附近有常年以燃煤为主的燃煤发电厂,该点可能受到燃煤电厂的影响。TH-2-6的含量明显高于周边的TH-2-5与TH-2-7的含量;该点位于B河桥附近,由于B河桥位于S303省道上,是通往某市市区的一条主要干道,该点含量可能受机动车影响比较大。
3.3 某市B河水中多环芳烃的生态风险评价
3.3.1 利用风险熵值法对B河水体中PAHs进行生态风险评价
采用多数学者使用的风险熵值法对某市B河水中的多环芳烃进行生态风险评价。Cao[13]成功地将风险熵值法运用于水体中多环芳烃的生态风险评价,即用各个PAHs的浓度与其对应的PAHs毒性当量因子(toxic equivalency factor,TEF)的比值得出风险熵值(RQ)。公式为:

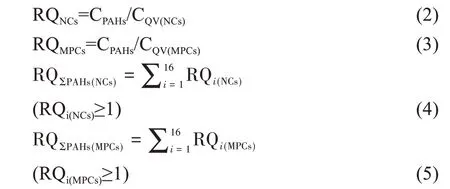
(1)—(5)式中:RQ表示风险熵值,RQNCs表示低风险熵值(NCs),RQMPCs表示高风险熵值(MPCs),CPAHs表示各个PAHs的浓度,CQV表示PAHs风险标准值,CQV(NCs)表示PAHs低风险浓度值,CQV(MPCs)表示PAHs高风险浓度值,RQΣPAHs(NCs)表示总的PAHs低风险熵值,RQΣPAHs(MPCs)表示总的PAHs高风险熵值[14]。
当RQNCs<1时,说明该区域PAHs属于低污染程度;当RQNCs>1且RQMPCs<1时,说明该区域PAHs属于中等污染程度;当RQNCs>1且RQMPCs>1时,说明该区域PAHs属于严重污染程度[6]。按照上述公式得出表4数据。根据数据可知:单体PAHs处于中等污染程度,具有一定的生态风险。
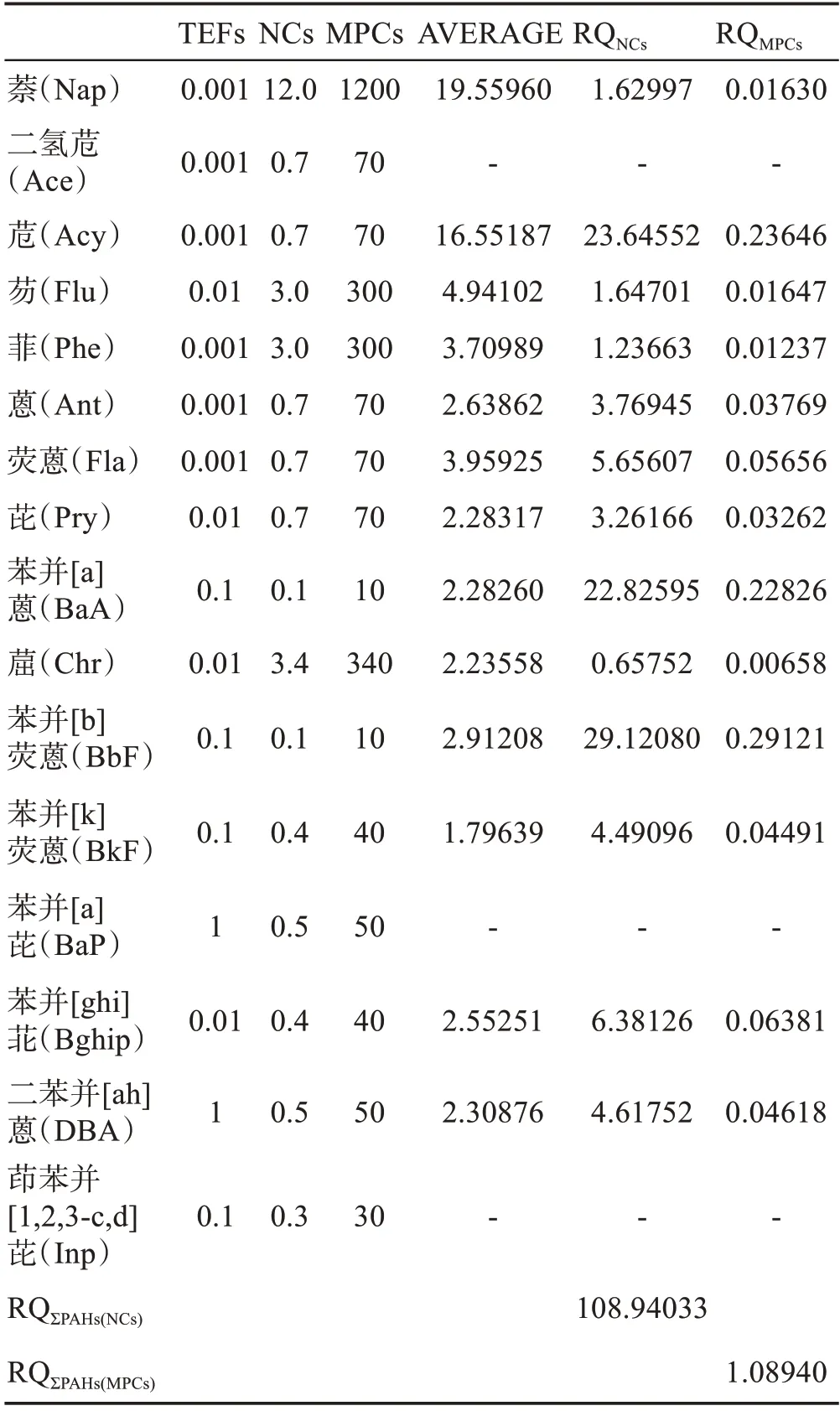
表4 某市B河水体中PAHs的风险熵值Table 4.RQs of PAHs in water of the river B of a city
3.3.2 利用累积毒性等效剂量对B河水体中PAHs进行致癌风险评价
累积毒性等效剂量(total toxic benzo[a]pyrene,TEQ)是指:将BaP对人体的危害当作1,即将BaP的毒性等效因子(the toxic equivalency factors,TEF)设定为1,其他的PAHs对人体的危害性与BaP比较,得出相对应的毒性等效因子(表5),用各PAHs的浓度与其对应的毒性当量因子相乘,所得乘积求和,即为累积毒性等效剂量[15]。其公式为:
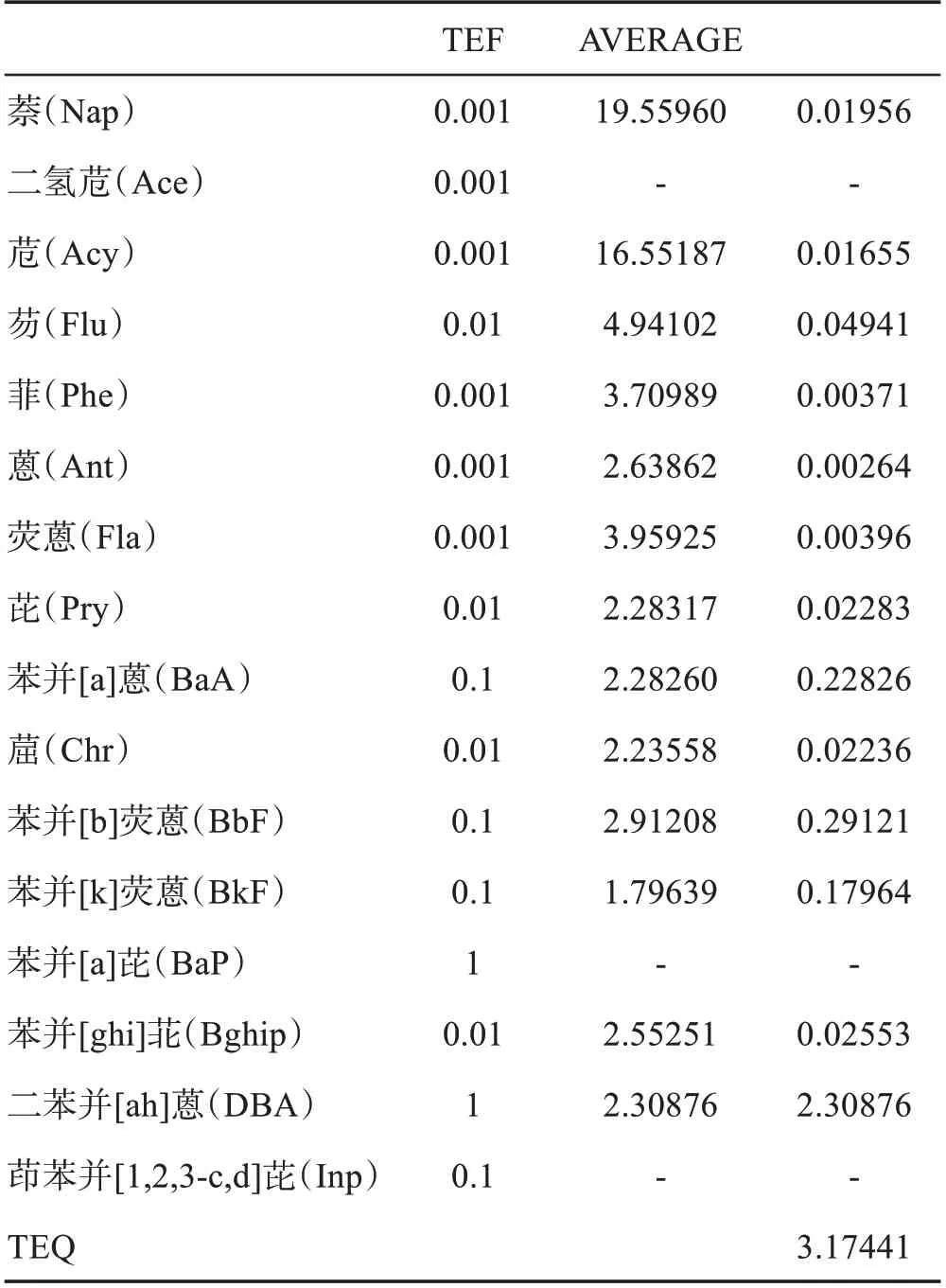
表5 PAHs的毒性当量因子及毒性等效剂量(单位:ng/g)Table 5.The toxic equivalency factors and toxic equivalency quantity of PAHs(unit:ng/g)

(6)式中:TEQ表示PAHs的毒性等效BaP毒性的累积毒性等效剂量;CPAHs为各个PAHs的浓度;TEF为各个PAHs的毒性等效因子。
通过上述(6)式计算出的某市B河水体中多环芳烃的毒性等效剂量为3.17441ng/g。我国环保局发布的《中华人民共和国地表水环境质量标准》(GB3838—2002)规定BaP≤2.8×10-3ng/g,根据该标准与研究结果其累积毒性等效剂量为3.17441ng/g。对比判断可知,某市市区B河水体中多环芳烃具有一定的致癌风险。
4 结论与建议
4.1 结论
(1)安徽省某市B河水体中多环芳烃含量中萘含量和苊含量较其他含量尤为突出,其中萘的含量最高,最高为20.76050ng/g;苯并[k]荧蒽的含量最低,最低为1.73800ng/g;致癌性最强的苯并[a]芘含量未检出。
(2)安徽某市B河水体中多环芳烃的主要来源是以煤炭、木材等生物质为主的燃烧源。
(3)安徽某市B河水体中单体多环芳烃属于中等污染程度,具有一定的生态风险;B河水中多环芳烃含量根据累积毒性等效剂量计算为3.17441ng/g,具有一定的致癌风险。
4.2 建议
(1)对周边排放较高多环芳烃污染的工厂进行限制排放或进行尾气处理后排放。
(2)植物具有一定的吸收多环芳烃污染的作用,对于污染较为严重地区周边多种植植物。

