孤立性肺结节良恶性预测模型的系统评价*
李梦乾,张晓梅,胡家蕊,车丽坤,李瑞,于小林
100029 北京,北京中医药大学 研究生院(李梦乾、胡家蕊、车丽坤、李瑞、于小林);100078 北京,北京中医药大学东方医院 呼吸科(张晓梅)
肺结节是指肺内单独出现的或者多发性的,直径不超过3 cm的圆形或类圆形异常密度影,边界或清晰或模糊,发生孤立性肺结节(solitary pulmonary nodules,SPN)原因诸多,目前发病机制尚未明确,肺部原发肿瘤、结核感染、肺部转移瘤、错构瘤、炎性假瘤、腺瘤样改变等均可引起SPN[1]。近年,随着低剂量CT技术的普及,人工智能阅片技术的应用,人们健康体检意识的增强,肺结节人群检出率越来越高,研究显示健康体检人群中肺结节的检出率可达20.65%~26.8%[2-3],约1/5~1/4,也就是说健康体检人群中,平均每4~5个人中就有一个肺结节患者。
肺癌是我国发病率和死亡率均最高的恶性肿瘤[4],恶性肺结节病理类型多为肺癌,有研究表明阳性肺结节中有11.66%肺癌可疑率[5],因此肺结节的良恶性预测尤为重要,及早识别恶性肺结节并及时干预治疗可防止肺癌发生,近年来有关肺结节恶性概率预测的数学模型层出不穷,本文通过查阅文献对现有的SPN良恶性预测模型进行系统评价,寻找肺结节恶性风险的独立危险因素及独立保护因素,以期为今后肺结节良恶性预测模型的建立及肺结节良、恶性的评估提供参考。
1 资料方法
1.1 文献检索
使用计算机检索CNKI、VIP、Wanfang和Pubmed、Embase、Web of Science数据库,对关于SPN良恶性预测模型进行全面检索,检索的时间为自建库至2021年2月9日,中文检索词为“孤立性肺结节”“预测模型”,英文数据库检索主题词为“solitary pulmonary nodule”“prediction model”。
1.2 纳入、排除标准
纳入标准:1)国内外公开发表的有关SPN的良恶性预测模型的研究;2)研究类型为回顾性研究或前瞻性研究;3)研究对象为病理诊断的SPN患者或病理诊断结合随访的SPN患者,包含良性和恶性SPN患者;4)原始数据提供OR值和95%CI;5)文献资料完整,包含模型公式、预测因子、建模病例数、良恶性分布、性别分布、AUC值、灵敏度、特异度等。排除标准:1)摘要、综述、信件、专利、会议/学位论文、基于系统评价/元分析建立模型或非临床研究;2)资料不全、未建模/模型公式缺失或重复、借助现有经典模型进行比较或验证、研究质量差的文献;3)预测因子≤2个及风险因素赋值描述不清者;4)建模样本量≤100例;5)语言为非中文、英文类文献。
1.3 文献的筛选和资料提取
由2名研究者对文献进行筛选和资料提取,共同核对,若出现意见分歧,则与第3位研究者进行商讨决定。资料提取的内容包括:篇名、第一作者、研究起止时间、研究地区、纳入结节直径、建模样本量、恶良性病例数、性别、预测因子、模型公式、AUC、灵敏度、特异度、阳性预测值、阴性预测值等。
1.4 名称统一规范化
对模型中包含的独立预测因素进行名称规范化统一,如最大径、结节最大直径、结节直径、病变直径、结节面积等统一为直径;血管集束、血管牵拉、血管征、三维血管穿透征等统一为血管集束征;磨玻璃结节、磨玻璃成分、含磨玻璃成分、混合磨玻璃等统一为磨玻璃成分;恶性肿瘤史、既往肿瘤史、肿瘤既往史、肿瘤病史等统一为肿瘤史;肿瘤家族史、家族恶性肿瘤史、家族癌症史等统一为肿瘤家族史等。
1.5 统计分析
采用Excel软件提取数据,并对数据进行统计处理,查找SPN恶性风险的独立危险因素及独立保护因素,并对独立危险因素和独立保护因素进行频次统计,按频次高低依次排序,查找出现2次及以上的独立相关因素进行展示分析。
1.6 文献质量评估
借助临床预测模型偏倚风险评估工具CHARMS清单[6]对最终纳入的文献进行方法学及质量评价,从数据来源、参与者、预测结局、筛选因子、样本量、缺失数据、模型建立、模型性能、模型评价、结果解释、讨论等11个方面对模型进行评价。纳入文献的质量评价由两名研究者共同完成,遇到意见分歧时,则同第三名研究者共同商讨裁决。
2 结 果
2.1 文献检索结果
共检索出文献574篇,其中CNKI(114篇)、VIP(29篇)、Wanfang(90篇)和Pubmed(163篇)、Em-base(85篇)、Web of science(93篇),通过阅读题目、摘要和全文,剔除重复及不符合要求文献,最终纳入文献27篇[7-33],包含27个建模公式,文献筛选流程如图1。
2.2 独立危险因素情况
对模型中出现的独立危险因素进行汇总,并统计频次,筛选出现2次及以上的独立危险因素共22种,累计出现频次共138次,分别为:1)年龄;2)直径;3)分叶征;4)毛刺征;5)胸膜牵拉征;6)血管集束征;7)细胞角蛋白19(Cyfra21-1);8)肿瘤家族史;9)边界不清;10)空泡征;11)磨玻璃成分;12)吸烟史;13)肿瘤史;14)癌胚抗原(carcinoembryonic antigen,CEA);15)18F-FDG摄取;16)SUVmax;17)边界清楚;18)空气支气管征;19)女性;20)神经元特异性烯醇化酶(neuron-specific enolase,NSE);21)男性;22)上叶。出现次数≥2次的危险因素情况如表1。
2.3 独立保护因素情况
对模型公式中出现的独立保护因素进行汇总,并统计排序,独立保护因素共13种分别为a)钙化;b)边界清楚;c)边缘光滑;d)有症状;e)中性粒细胞淋巴细胞比值;f)非上肺;g)形状规则;h)戒烟;i)CEA;j)密度值(heat unit,HU);k)混合磨玻璃;l)实性;m)卫星灶,其中出现2次及以上的独立保护因素依次是:钙化、边界清楚、边缘光滑。分布情况如表2。
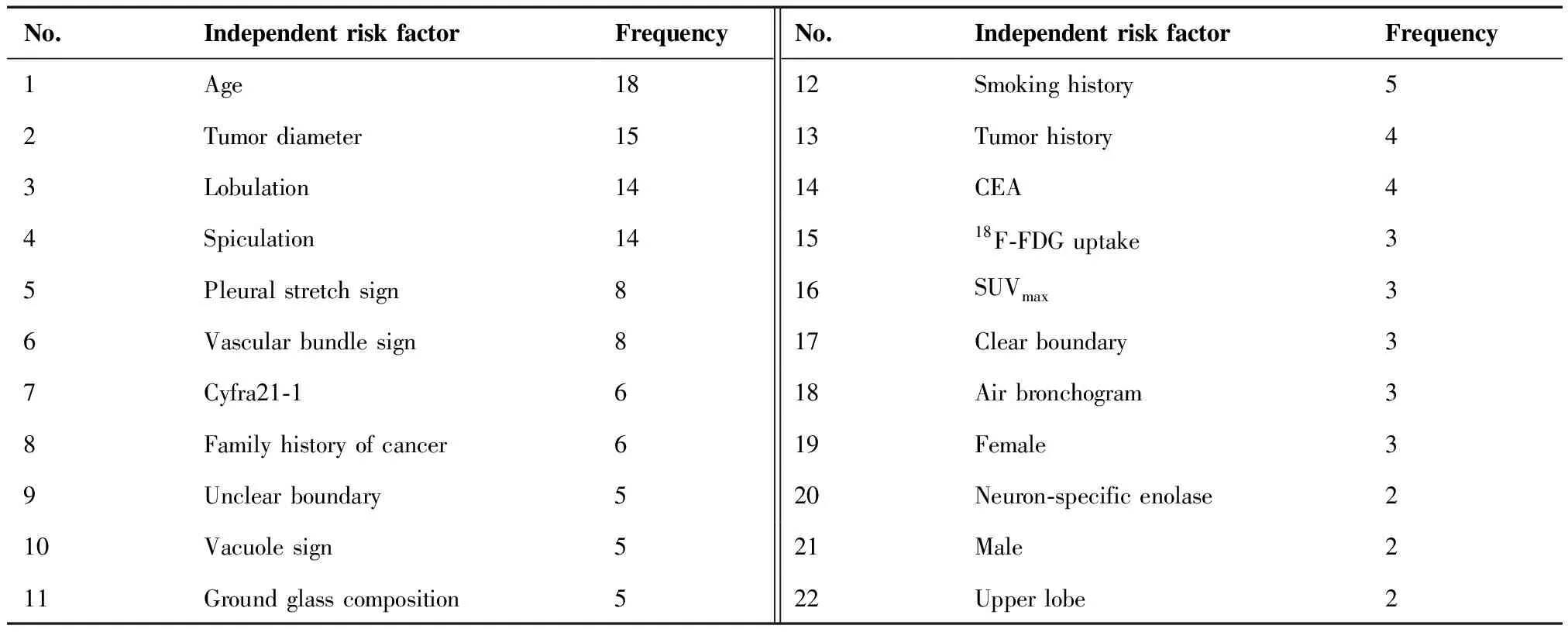
表1 出现次数≥2次的独立危险因素
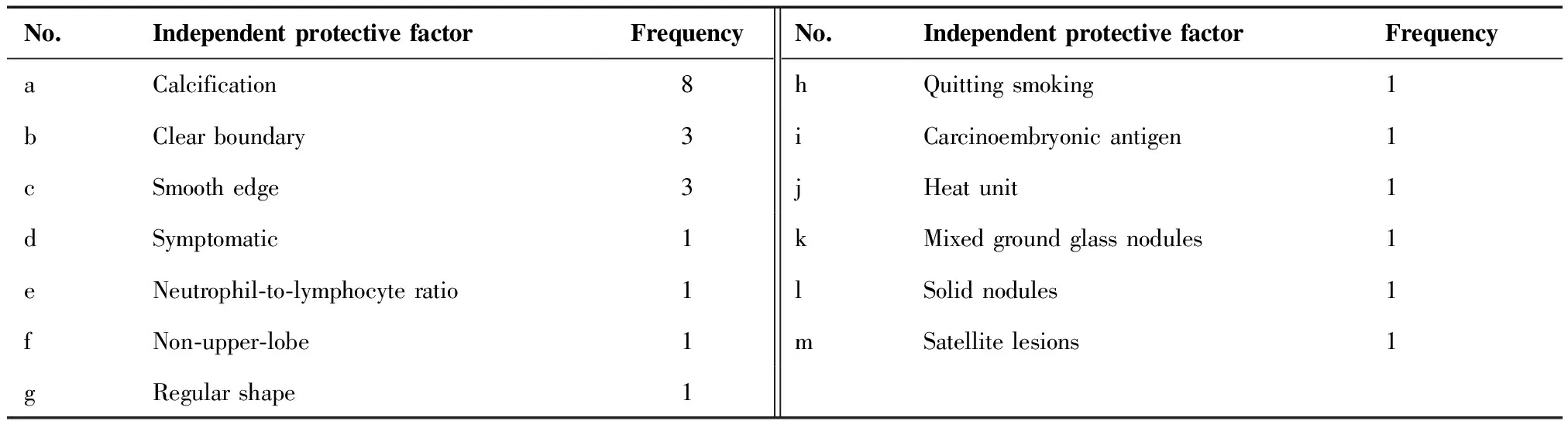
表2 独立保护因素分布情况
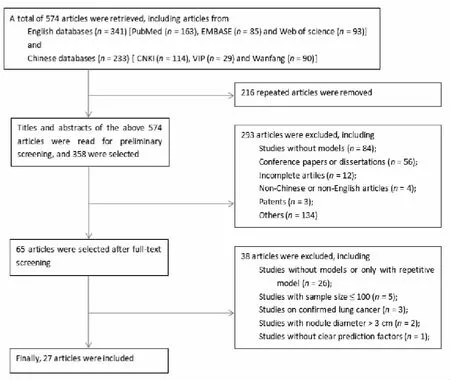
图1 文献筛选流程图
2.4 模型特征情况
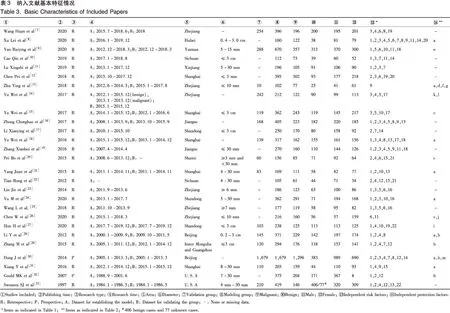
最终纳入27篇文献,近五年发表的文献有18篇;27项研究中,25项回顾性研究,2项前瞻性研究;5项研究进行了外部模型验证,8项研究进行了内部模型验证,2项研究进行了验证(内外部不详);纳入文献中3项研究是多中心研究,22项研究为单中心研究,2项研究的研究中心不详。纳入文献基本特征情况见表3,模型预测效能情况见表4。
2.5 纳入研究的偏倚风险评价
本研究纳入的研究借助临床预测模型偏倚风险评估工具CHARMS清单进行评价,结果显示纳入研究整体偏倚风险低,方法学和质量评价较好,评价结果情况见表5。


3 讨 论
随着人群健康体检意识的增强及胸部CT技术的普及,肺结节成为一种新兴的肺部疾患,人群检出率较高,恶性SPN的病理类型多为肺癌,及早的识别恶性肺结节并及早采取干预措施对于肺癌的防治意义重大,近年来SPN预测模型层出不穷,成为国内外研究和讨论的热点,尽管各大指南关于SPN已有相应的随访策略,肺结节预测模型则能更好的量化其恶性风险概率,本文通过文献回顾对国内外SPN良恶性预测模型进行系统分析,查找肺结节恶性风险的独立危险因素,并对模型预测效能进行分析,发现预测模型的整体性能较好,预测模型的验证有待探讨,希望本研究能为SPN良恶性的判定及预测模型的建立完善提供参考。
3.1 独立危险因素分析
研究结果显示,胸部CT表现出的结节直径、分叶征、毛刺征、胸膜牵拉征、血管集束征、边界不清、空泡征、磨玻璃成分、边界清楚、空气支气管征、上叶位置是恶性SPN的独立危险因素,钙化、边界清楚、边缘光滑是其独立保护因素。大多数预测模型中结节的直径与恶性概率密切相关,结节直径越大,恶性风险越高,结节直径小于5 mm的恶性率低于1%,直径5~10 mm的恶性率增至6%~28%,直径超过20 mm的恶性率高达64%~82%[34]。分叶的形成与癌细胞小叶内增殖速度相关,以深分叶多见;毛刺征的病理基础为肿瘤引起的结缔组织快速增生或肿瘤细胞快速侵犯局部淋巴管;胸膜牵拉征的形成与靠近胸膜的恶性结节恶性增生时纤维组织牵拉胸膜相关,通常此类结节离胸膜较近;空泡征与肿瘤破坏肺支架和支气管扭曲有关,多见于鳞腺癌、细支气管肺泡癌、腺癌;血管集束现象与肿瘤细胞产生血管因子,引起原有血管增粗或诱发新生血管向肿瘤供血等有关[35]。空气支气管征的形成病理基础为沿肺泡和细支气管表面生长的肿瘤侵袭管腔所致,良恶性结节均可见到,恶性结节多见于淋巴瘤和细支气管肺泡癌。
本研究的磨玻璃成分多为密度不均的混合磨玻璃结节,张晓辉等[19]将密度不均作为恶性肺结节的影像表现建立的预测模型曲线下面积达0.901,Chen等[26]将混合磨玻璃(mixed ground-glass nodule,mGGN)作为独立危险因素建立的模型曲线下面积达0.744,且与良性结节相比恶性结节mGGN出现的概率更高。混合磨玻璃结节是三类结节中恶性度最高的结节,ACCP指南、亚洲指南和中国专家共识均认为直径<8 mm的混合磨玻璃结节应至少3个月、12个月、24个月复查,一旦发现结节增大或者实性成分增多均建议手术切除[36],此外,实性结节中一旦出现空泡或磨玻璃样成分,也提示结节有向混合磨玻璃转化的恶性倾向,需要引起重视。边界不清或边缘模糊多为恶性肺结节的影像学征象,而边界清楚和边界光滑多提示良性结节,本研究纳入喻微等[14]的研究将边界清楚作为独立危险因素,多考虑纳入的良性患者里非特异性炎性结节比例偏高,而此类结节的边界是模糊的。将上叶位置作为恶性SPN的独立危险因素,最早见于梅奥诊所的Mayo模型,后期研究认为恶性肺结节可出现在任何肺叶位置,上叶已经不作为独立危险因素纳入模型。18F-PDG摄取常分为5个等级[20]:0级表示无摄取(摄取程度与周围肺组织相当);1级表示摄取高于肺组织但低于纵膈;2级表示与纵膈吸收接近;3级表示高于纵膈但低于肝脏;4级表示摄取明显高于肝脏)摄取等级越高,摄取等级越高表明病灶代谢越高,3项研究[20,22,31]将18F-PDG摄取作为独立危险因素,根据其摄取程度等级赋值,也有3项研究[23-25]将最大摄取量SUVmax作为独立危险因素建模,认为肺结节的恶性程度与最大摄取量相关,这与指南建议的考虑恶性的肺结节行PET-CT检查或病理活检的观点一致,PET-CT可用于良恶性肺结节的辅助鉴别诊断。
传统特征中高龄、吸烟、肿瘤史、肿瘤史家族、Cyfra21-1、CEA、NSE、男性、女性作为恶性SPN的独立危险因素。多项研究认为随着年龄增长,恶性SPN发生的风险增高,尤其是40岁以后,主要考虑与人体衰老机体免疫力下降、线粒体功能低下有关,基因更容易发生突变或异常表达,研究表明[37]川芎嗪联合顺铂可调节PI3K/AKT/mTOR通路,改善线粒体功能,抑制肺癌A549细胞增殖;而肿瘤史和肿瘤史家族史则更从基因遗传学家角度增加了其恶变的概率。男性、吸烟作为独立危险因素与我国2015年肿瘤普查结果肺癌男女比例3∶1相符合,且吸烟是肺鳞癌的明确诱因。近年来不吸烟的女性肺腺癌发病率逐渐升高,考虑女性更容易处于焦虑抑郁状态,从情志方面影响结节发生恶变,且有研究表明[38]女性血浆对尼古丁清除能力较差,导致吸烟史,促进其鳞癌的发生,还有研究显示[39]EGFR 在女性患者中的突变频率高于男性,促使非小细胞肺癌的发生,因此将女性作为恶性SPN的独立危险因素。Cyfra21-1、NSE、CEA均为肿瘤标志物,其中Cyfra21-1作为非小细胞肺癌的免疫标记物,6项研究[8,10,11,17,29-30]将Cyfra21-1作为独立危险因素建立模型曲线下面积均在0.789以上,显示包含血清肿瘤标志物的模型具备良好的预测性能,NSE作为小细胞肺癌的特异性肿瘤标志物,对于小细胞肺癌的预测和诊断具备一定特异性,CEA虽不能作为某种恶性肿瘤的特异性指标,但是确是一种广谱肿瘤标志物,对于恶性肺结节的预测可以提高预测准确度,李笑莹等[17]结合血清肿瘤标志物建立的预测模型,预测模型的AUC为0.734±0.033、灵敏度为63.5%、特异度为71.2%,与指南推荐的Mayo模型比较差异无统计学意义,值得引荐。
3.2 模型建立、评价及效能情况分析
本研究纳入的27篇文献,建模时均采用Logistic回归,而Logistic回归是常用的建模方法,27个模型[7-33]计算恶性概率时均根据回归系数权重对预测因子进行赋值,且24个模型[7-22,25-31,33]均得出了最佳截断值,各研究模型可以针对性的预测恶性SPN发生的风险比例。模型预测效能常用曲线下面积AUC值表示,AUC值介于0~1间,越接近1表明预测效能越好,本研究纳入的27个模型整体预测效能好,建模组AUC值均在0.70以上,进行验证的模型[7,9,13-16,18,20,21,27-31,33]验证组AUC值均在0.80以上,表明模型在验证时依旧具备较好的预测效能。
本研究有15个模型[7,9,13-16,18,20-21,27-31,33]在模型建立后进行了验证,其中5个模型[7,13-15,18]进行了外部验证,其AUC值在0.859~0.978,准确度在83.5%~85.4%,灵敏度在81.8%~90.8%,特异度在78.79%~100%,表明模型在外部使用时可能具备较好的预测效能;8个模型[9,16,21,27-28,30-31,33]进行了内部验证,AUC值在81.6%~84.5%,准确度在81.6%~84.5%,敏感度在64.8%~94.7%,特异度在70%~86.3%,表明预测模型具备较好的内部适用性,但是进行外部推广仍待商榷;2个模型[20,29]进行了验证,但验证组来源信息不详,虽然验证组AUC值均在0.85以上,但是其可信度和适用性存疑;其余12个模型[8,10,11-12,17,19,22-26,32]未进行验证,因此其内外部推广使用情况仍待进一步深入研究确定。虽然纳入的研究中一半模型进行了验证,但多为内部验证,验证集多随机抽自前期纳入的病例或同一家研究中心获得的病例,因此研究中心具备单一性,研究人群具备一定限制性,而进行外部验证的模型,多为单一外部验证或受验证组病例的限制,因此预测模型的整体推广问题仍待商讨和进一步研究。
纳入研究中有14个模型[9-11,16-17,20,22,24,26-27,29-30,32-33]进行了评估检验,其中11个模型[10-11,17,20,22,26-27,29-30,32-33]进行了Hosmer-Lemeshow检验表明模型具有较好的拟合优度;3个模型[9,27,33]进行了校正曲线评价表明模型的预测效果好;1个模型[24]进行了K-ford交叉验证表明模型的准确度良好;5个模型[26-27,29-30,33]进行了多项检验评价,表明模型的质量和价值较高,可供临床参考使用。本研究纳入的文献借助CHARMS清单进行评价,纳入研究整体偏倚风险低,方法学和质量评价较好,研究结果具有一定参考价值。
3.3 研究的局限性分析
本研究纳入的模型多为影像学定性结合传统定量模型,此外,国内外已广泛开展人工智能、影像组学相关研究模型,包括人工智能新模型,如人工神经网络、支持向量机、随机森林、卷积神经网络、深度神经网络等模型[40],此类模型将定性的影像学图像转化为可采集、高保真的数据资料进行深度挖掘,且图像分割的速度和效率均较手动分割得以提升,在SPN的良恶性鉴别及有无侵袭性鉴别上具有较为显著的优势,但本研究考虑到此类新兴领域模型问世时间有限,目前仍处于研究开发阶段,且不同的研究机构及扫描仪器,不同的研究方法及算法,具备不同的参数和评分标准,难以统一,对于放射科医生也有较高的交叉学科要求,相比之下传统模型相对简单适用,因此纳入的研究模型多为传统模型,具备一定局限性。但研究者相信随着人工智能模型的不断发展完善,今后将有较好的应用前景。且本研究经过严格的纳、排后最终纳入文献27篇数量有限,文献筛选时语言设置为中、英文存在一定选择偏倚,实为本研究的局限与不足之处。
4 总 结
本研究对现有的肺结节良恶性预测模型进行系统评价,查找出了肺结节恶性风险的独立危险因素,包括影像特征:直径、分叶征、毛刺征、胸膜牵拉征、血管集束征、边界不清、空泡征、磨玻璃成分、18F-FDG摄取、SUVmax、边界清楚、空气支气管征、上叶等;传统特征:年龄、肿瘤家族史、吸烟史、肿瘤史、女性、男性、血清肿瘤标志物(Cyfra21-1、CEA、NSE)等。而钙化、边界清楚、边界光滑则是其保护因素。通过对模型的效能进行分析,发现纳入模型整体具备较好的预测效能,并由半数以上模型进行了内部或外部验证,显示出良好的适用性。筛选出的独立危险因素和预测模型可帮助临床医护人员鉴别良、恶性肺结节,但是模型的大范围外推使用待商讨,且模型中包含的预测因素数目有限,未来需开展进一步深入研究来完善模型并对模型进行外部验证。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。

