超声引导下竖脊肌平面阻滞对老年患者经皮穿刺椎体后凸成形术中疼痛和满意度的影响
宋铖 蒋宗明 王宏伟 宋胜文 易声华 陈念平 沈琴 方向明
老年患者骨质疏松后易出现椎体压缩性骨折(vertebral compression fractures,VCF),会造成椎体进行性后凸,严重者脊髓受压造成肢体感觉、运动障碍;同时疼痛时限制性体位会增加褥疮、肺炎、下肢静脉栓塞和肺栓塞的风险[1]。手术是治疗椎体压缩性骨折的有效方式,可以恢复椎体高度,缓解患者疼痛,改善患者生活质量[2]。其中球囊扩张椎体后凸成形术(percutaneous kyphoplasty,PKP)缓解疼痛效果最好,是最常用的手术方式[3]。局部麻醉是目前临床上PKP手术最常用的镇痛方案,但在球囊扩张及骨水泥注入等操作节点时疼痛明显[4],有时需中断手术操作来缓解患者疼痛。疼痛会引起心率和血压骤然上升,增加老年患者发生心血管不良事件的风险,降低依从性。超声引导下竖脊肌平面阻滞(erector spinae plane block,ESPB)理论上能多节段镇痛,但目前临床上对于ESPB的麻醉效果仍存在一定的争议。因此,本文探讨超声引导下竖脊肌平面阻滞对PKP术中疼痛控制、血流动力学变化和患者满意度的影响。
1 资料与方法
1.1 临床资料 选取2019年12月至2021年7月本院行PKP手术患者100例,纳入标准:因骨质疏松压缩性骨折拟择期行PKP手术患者,年龄65~85岁,ASA分级 I~III级。排除标准:局麻药过敏史;阿片类药物使用禁忌;穿刺部位感染;穿刺部位严重畸形;认知功能障碍无法配合;精神异常;严重凝血功能障碍。因手术方式改变剔除1例,患者主动退出2例,术后失访4例,最终纳入93例。采用随机数字表法分为ESPB组(E组)和对照组(C组)。两组患者一般资料比较差异无统计学意义见表1。本项目经绍兴文理学院附属医院及绍兴市人民医院医学伦理委员会批准,所有患者均签署知情同意书。
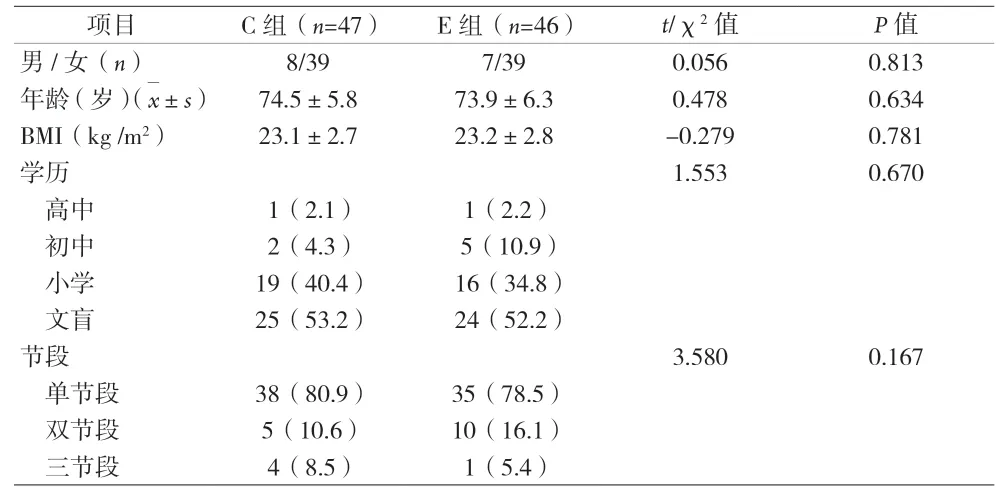
表1 两组患者一般资料比较
1.2 方法 患者入室后开放上肢静脉通路,常规心电监护,面罩吸氧4 L/min。E组患者B超引导下竖脊肌平面阻滞。采用超声低频凸阵探头定位穿刺点,旁矢状位进行探查,腰段穿刺首先确定骶骨及第五腰椎横突,然后往头端移动探头位置依次确定各腰椎横突位置,以明确目标椎体横突的位置。胸段穿刺先确定十二肋,从胸十二横突依次向头端确定各椎体横突位置。单节段穿刺点为责任椎体,多节段穿刺点为各伤椎中点。确定位置后作相应的标记,消毒铺巾,旁矢状位探查确定目标椎体横突的最外侧缘作为穿刺点。B超引导下20 G穿刺针头向尾平面内进针的方式至椎体横突,回抽无血无气后注入0.375%罗哌卡因20 mL。对侧进行同样的操作,针刺法测出手术节段皮肤痛觉减退后行手术操作。C组患者由外科医师常规局部浸润阻滞后行手术操作。术中患者VAS评分>3分使用酮咯酸15 mg单次静推止痛,如疼痛未缓解或VAS评分>6分则使用芬太尼静推止痛,首次剂量0.4 μg/kg,后续追加剂量0.2 μg/kg,追加间隔不<5 min,密切关注患者呼吸,如呼吸频率<8次/min,则停止使用阿片类药物并采取开放气道等措施。
1.3 观察指标 记录患者术前(T0)、穿刺时(T1)、球囊扩张时(T2)、骨水泥注入即刻(T3)、手术结束出室前(T4)心率、血压和VAS,多节段手术患者取各节段操作时各数据均值每例患者术后3 h、术后6 h、术后12 h、术后24 h和术后48 h VAS评分。评价患者对手术的满意度及再次接受类似手术的意愿。
1.4 统计学方法 采用SPSS 24.0 统计软件。符合正态分布计量资料以(±s)表示,组间比较采用独立样本t检验,非正态分布计量资料组间比较采用秩和检验,计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者术中HR、MAP和VAS比较 见表2。
表2 两组患者术中HR、MAP和VAS比较(±s)

表2 两组患者术中HR、MAP和VAS比较(±s)
注:与C组比较,*P<0.01
?
2.2 两组术后各时间点VAS评分 见表3。
表3 两组患者术后各时间点VAS评分(±s)

表3 两组患者术后各时间点VAS评分(±s)
注:与C组比较,*P<0.01
?
2.4 两组患者芬太尼使用率、满意度及再次手术意愿比较 见表4。

表4 两组患者芬太尼使用率、满意度及再次手术意愿比较
3 讨论
PKP手术时减轻或消除疼痛的方法有局部浸润阻滞、连续硬膜外阻滞和全身麻醉等。硬膜外阻滞能提供良好的镇痛[5],但骨质增生和韧带钙化等因素会降低穿刺成功率,增加脊髓损伤、硬膜外血肿和神经损伤等发生的风险。全身麻醉时患者耐受性好,术后疼痛缓解率更高,但增加住院时间和费用,同时增加术中神经损伤风险,因此临床应用受到一定限制[6]。目前临床上最常使用的是局部浸润阻滞,患者术中疼痛控制不佳。
单纯局部浸润阻滞不能提供良好的术中镇痛的主要原因:①椎体及其周围组织神经支配复杂,受脊神经后支、窦椎神经、交感神经等共同支配;②皮肤及肌肉疼痛由脊神经后支传导,支配椎体骨膜及椎体内部的神经是窦椎神经,属于脊神经的一个分支,在脊神经分出前支和后支前分出,通过椎间孔后返回椎管内,分布于椎体内、骨膜、韧带及关节囊等部位,该神经还借白交通支及灰交通支与交感神经链相沟通,椎体疼痛来源于相应节段的神经及远节段的背根神经节[7]。因此,单点阻滞不能提供良好的镇痛。
ESPB对脊神经后支多节段的阻滞及其潜在的椎旁/硬膜外扩散的特点为PKP的术中镇痛提供新的思路[8]。ESPB最早由FORERO等[9]提出并成功用于两例胸部神经病理性疼痛的治疗。SINGH等[10]证实T10水平的ESPB可以降低腰椎手术患者术后疼痛评分,减少阿片类药物的消耗。不同平面ESPB时药液可通过筋膜向前扩散至椎旁间隙甚至硬膜外隙,并影响上下多个节段[11-12]。YANG等[13]研究认为在胸段ESPB时药液是通过渗透作用通过肋横突上韧带等结构进入椎旁间隙从而发挥作用。而腰段ESPB类似于腰方肌后侧阻滞,也是药液在筋膜间扩散直至椎旁间隙或发挥作用[14]。理论上局麻药液注射在竖脊肌平面后可前向渗透进入椎旁和硬膜外间隙从而阻滞窦椎神经及背根神经节,而对脊神经后支的阻滞则依靠药液在竖脊肌平面内的头尾方向扩散,达到上下多个节段的阻滞,从而达到完善的术中镇痛。
本资料中,患者手术节段皮肤痛觉减退,术中疼痛评分下降,围术期血流动力学更稳定,但在穿刺导管进入椎体、球囊扩张、骨水泥注入三个手术操作节点无法达到完全无痛的理想麻醉状态,有41.3%患者需辅助阿片类药物镇痛,这表明在部分患者中,单次ESPB能阻滞脊神经后支,但并无足够的局麻药液进入同节段及相邻节段的椎旁间隙或者硬膜外隙,从而造成阻滞不全,ESPB前向扩散的稳定性需更多的临床试验来证实。该结果与部分尸体染色解剖研究相吻合。在相关研究中并未发现染料向前扩散至椎间孔附近,脊神经前支未被较好的染色,染料更多是集中在肋横突关节后,ESPB浸润染色仅是脊神经的后支[15]。在术后镇痛上,E组患者术后12 h内疼痛评分更低,这与部分研究结果一致,有研究使用0.25%罗哌卡因30 mL,在术后18 h内能提供良好的镇痛[16]。
综上所述,ESPB对减轻老年患者PKP术中疼痛有一定作用,但难以达到完全无痛的麻醉效果,对术后12 h内急性疼痛控制良好,能减轻围术期循环波动,减少术中阿片类镇痛药物消耗量,提高患者满意度,同时ESPB操作简单,并发症少,对老年患者PKP围术期镇痛具有一定的临床应用价值。

