不同血糖控制水平的化脓性肝脓肿患者临床特点和预后分析
张健 沈振华 吴小昌
化脓性肝脓肿(Pyogenic liver abscess,PLA)是发生在肝实质的严重炎症疾病,近年来发病率和病死率逐渐升高。PLA患者合并高危因素、潜在疾病、严重并发症和预后较差时,住院30 d内死亡率约10%。PLA患者中约35.3%伴糖尿病(DM)[1]。目前关于化脓性肝脓肿合并糖尿病患者的临床特点已有部分临床研究,但针对不同血糖控制水平患者的临床特征、并发症及预后相关研究较少。本文探讨不同血糖控制水平的化脓性肝脓肿患者的临床特点和预后因素。
1 资料与方法
1.1 临床资料 选取2014年1月至2019年12月本院PLA合并糖尿病患者116例。PLA诊断标准:①临床表现,如发热、寒战、腹胀、腹痛;②血液和脓肿的病因学检查;③通过肝脏腹部超声(US)、计算机断层扫描(CT)判断肝脏脓腔的影像学证据。纳入标准:①诊断符合PLA合并糖尿病;②年龄≥18岁;③DM患者符合2型糖尿病诊断标准。排除标准:①非糖尿病性相关的化脓性肝脓肿,如阿米巴、结核性肝脓肿、长期使用糖皮质激素等;②严重脏器功能障碍,如心功能不全、肝肾功能不全、慢性阻塞性肺病、脑血管病等。③未完成6个月随访或病史资料不全的患者。
1.2 方法 收集患者基本信息(年龄、性别、基础疾病等)、临床表现(发热、腹痛等)、肝脓肿情况、主要并发症和预后等临床资料。根据HbA1c不同水平进行分组:A组为HbA1c≤7%,B组为7%<HbA1c≤9%,C组为HbA1c>9.0%[2]。PLA合并糖尿病患者根据细菌培养情况均予以头孢类药物为主(三代头孢如头孢哌酮钠舒巴坦钠)必要时联合抗厌氧菌抗菌治疗,根据脓肿情况行B超或CT引导下穿刺置管引流并冲洗。出院6个月内随访,分析不同血糖控制水平患者短期临床并发症和预后情况。比较三组患者临床基线资料、临床特征、并发症和短期预后等指标。根据不同血糖控制水平,将痊愈和好转视为有效。
1.3 统计学方法 采用SPSS 20.0统计软件。计量资料以(±s)表示,多组间比较用单因素方差分析,组间两两比较采用q检验;计数资料以n(%)表示,采用χ2检验。采用Logistic回归分析糖尿病患者伴化脓性肝脓肿影响预后的单因素和多因素。P<0.05为差异具有统计学意义。
2 结果
2.1 三组患者的基线资料比较 见表1。

表1 三组患者的基线资料比较
2.2 三组患者临床特征分析 见表2。
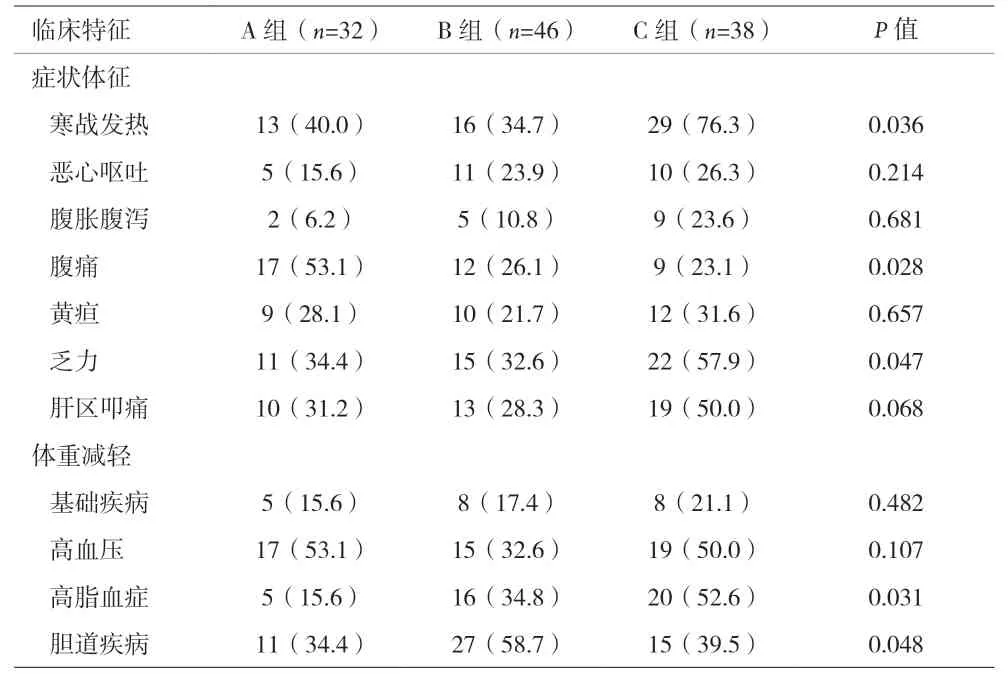
表2 肝脓肿合并糖尿病患者的临床特征[n(%)]
2.3 三组患者并发症比较。见表3。
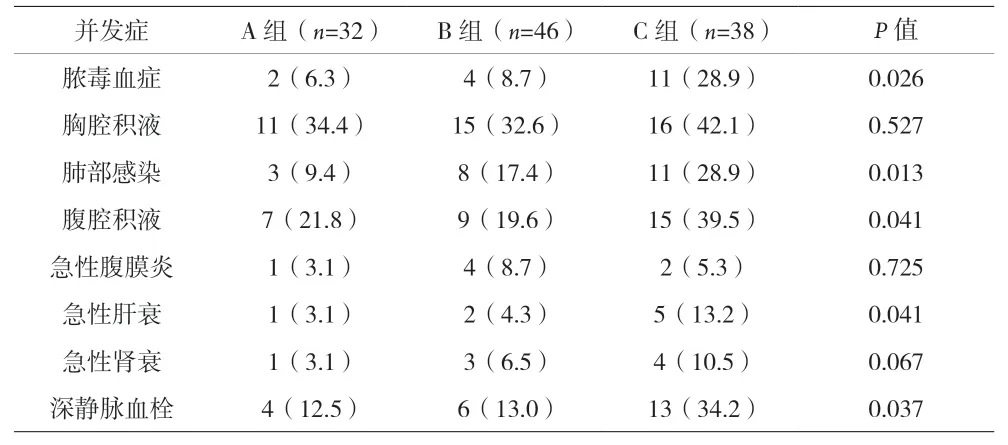
表3 三组患者并发症比较[n(%)]
2.4 血糖控制水平与化脓性肝脓肿预后因素的相关性分析 单因素Logistic回归分析显示,年龄>60岁、BMI≥24、白蛋白<35 g/L、脓肿直径>8 cm和HbA1c>7%为影响患者预后危险因素(P<0.05)。多因素回归分析显示,BMI高[OR 2.339(1.471~4.277),P<0.01]、白蛋白低[OR 3.277(1.681~5.273),P<0.05]、HbA1c>7%[OR 2.511(2.046~5.771),P<0.05]是肝脓肿预后独立危险因素。
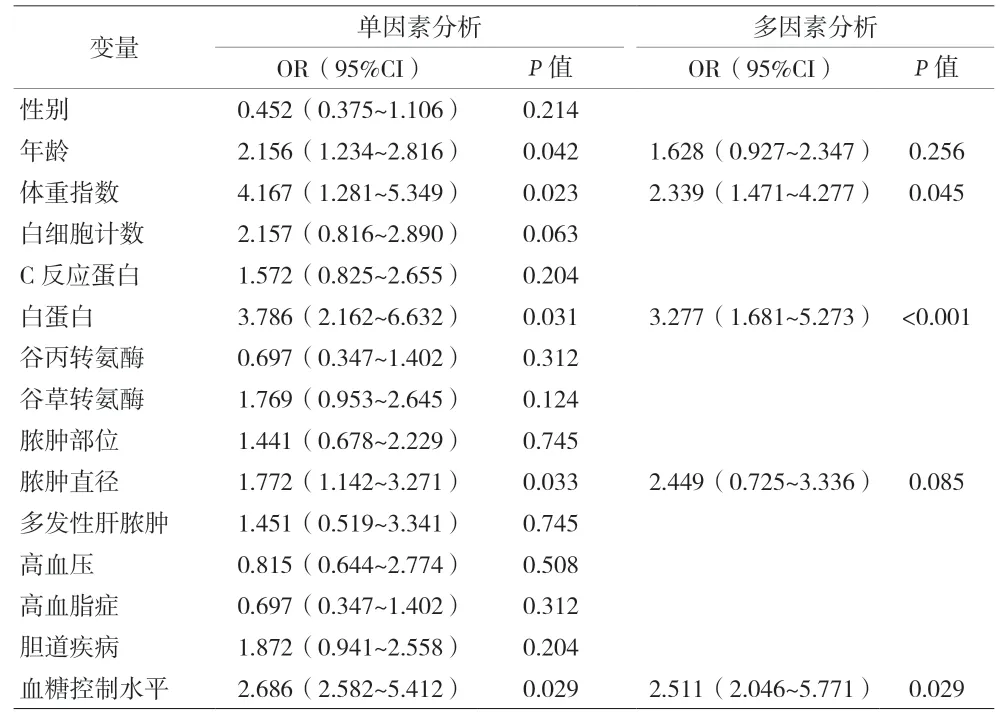
表4 肝脓肿合并糖尿病患者预后单因素和多因素分析
3 讨论
糖尿病是化脓性肝脓肿形成高危因素之一,占肝脓肿发病率的28.3%~64.2%[3-5]。糖尿病患者因长期高糖状态,可抑制白细胞黏附、吞噬及杀菌能力,降低免疫力,另外糖尿病患者血管内膜易破坏并发血管病变,加之血流变慢,从而阻碍白细胞移动,促使糖尿病患者易发肝脓肿[6-8]。糖尿病患者感染常较严重,易并发感染性休克和多器官功能障碍[9]。国内外研究报道[10-11],糖尿病合并肝脓肿患者的主要致病菌为肺炎克雷伯杆菌,目前已取代大肠埃希菌,且比在非糖尿病患者中更易常见,病原学检出率达74.2%[12]。肺炎克雷伯菌属革兰阴性杆菌,为条件致病菌,定植于肠道和呼吸道的正常菌群。因肝脏有单核-巨噬细胞系统吞噬作用,故原发性肺炎克雷伯杆菌化脓性感染难易发生,研究认为这可能因糖尿病患者的血管内膜病理性改变使其易经血源性播散,经过门静脉、肝动脉或胆道直接进入肝脏。
有研究发现糖尿病患者肝脓肿感染途径通常为隐源性,其机制尚不明确[13]。胆道原为肝脓肿最常见的感染途径之一,同时相关研究报道发现糖尿病与非糖尿病合并肝脓肿中经胆道途径感染有明显差异[14]。在胆道各种疾患如急性胆囊炎、急性胆管炎和梗阻性黄疸时,胆道黏膜屏障功能受到损害,肺炎克雷伯菌就可逆行进入胆管即细菌易位,造成胆道系统感染。
关于肝脓肿治疗方面,抗感染治疗是首选且对多数抗生素敏感[15]。随着现代影像技术发展,经皮肝脓肿穿刺引流已经为主要治疗方式[16]。早期诊断、抗生素的合理应用、强化血糖控制及时肝穿刺或手术可降低患者的病死率。本资料中,肝脓肿伴糖尿病患者常见症状体征有寒战发热、腹痛腹泻、乏力和肝区疼痛等,与以往研究大致一致[17],但血糖控制不佳患者,寒战发热、乏力症状更明显。提示临床医师在接诊患者时,发现有上述症状者密切关注腹部情况,必要时行腹部的影像学检查。JIA等[18]研究认为,患者年龄>65岁,有基础疾病,临床表现可能不典型,需引起临床注意。血糖控制差患者脂代谢紊乱致血脂更高、肝功能异常更明显,提示在治疗肝脓肿关注血脂的变化,必要时降血脂治疗。在并发症方面,随着HbAlc水平升高,患者并发肺部感染的发生率逐渐上升,但其机制尚不明确,还需进一步论证,最新个案曾报道肺炎克雷伯杆菌导致的肝脓肿并发脓毒性转移性肺栓子,形成肺脓肿[19],张露铭等[20]研究发现血糖控制欠佳可增加肺脓肿破溃致脓胸风险。
HbAlc是反映三个月平均血糖控制的指标,其水平的高低与糖尿病并发症密切关联,故HbAlc为影响肝脓肿预后的重要因素之一[21]。若患者血糖控制差(HbA1c≥9.9%),较易发展为脓毒症等全身多病灶脓肿,严重者致败血症、死亡[22-23]。本资料也显示,血糖控制差(HbA1c>9.0%)患者其脓毒血症发生率较高,且肺部感染的发生率随血糖水平的升高而增加,提示在治疗肝脓肿时关注患者肺部病情变化。血糖控制差的患者,深静脉血栓发生率较高,目前研究较少见,可能与血流中炎症介质释放,导致血小板的异常聚集,血流缓慢和高凝状态,均会导致血栓的形成,尤其以下肢血栓形成为主,应引起临床重视,争取早预防。另有研究显示,脓肿直径>10 cm是细菌性肝脓肿合并败血症的独立危险因素[24]。本资料显示,年龄、体重指数、白蛋白水平、脓肿直径和糖化血红蛋白水平为影响预后独立危险因素。进一步多因素分析,体重指数、白蛋白和糖化血红蛋白水平是患者预后独立危险因素,提示在体重指数高即肥胖患者、白蛋白水平低和糖化血红蛋白高越患者预后较差。相对于血糖控制不佳肝脓肿患者,血糖控制好患者的平均住院日更短,并发症较少,短期临床预后较好。

