帕金森病患者ApoA⁃1水平与UPDRS评分、MMSE评分及脑白质微结构改变的关系
史靖 胡军 罗开亮 贾绍环 沈鹤 胡泽凯 刘欣昊 刘婷
帕金森病(Parkinson Disease,PD)多发于老年群体,属神经系统退行疾病,主要以黑质多巴胺能神经元退行引发,具体原因尚未研究透彻,进展较缓[1]。根据最新流行病学调查显示,PD 患者多为60 岁以上群体,50 岁之前发病较少,且男性发病率稍高于女性[2]。以运动状态为基准可将PD 临床表征分为运动类、非运动类。运动类患者有运动障碍、肌肉僵硬等表现,非运动类则表现为睡眠情况及认知出现异常。其中,认知障碍作为PD 典型表现主要反应在学习能力、极易、注意力等方面,发生率约为25%~55%[3⁃4]。PD 早期表现出认知障碍、情绪等病症不明显,具备一定的隐匿性[5]。再者,由于不同个体发病特点、发病严重程度均有不同,导致早期PD 诊断较为困难。门诊评估PD 多以脑脊液检查、影像学或其他辅助检查为主[6⁃7]。价格较为昂贵,且特异度一般。载脂蛋白A⁃1(Apolipoprotein A⁃1,ApoA⁃1)有抗炎、抗氧化作用,有研究表明该指标与PD 发生、发展有紧密联系[8]。本研究探讨ApoA⁃1 水平与统一帕金森氏病评分量表(Unified Parkinson's Disease Rat⁃ing Scale,UPDRS)评分、简易精神状态检查量表(Mini⁃mental State Examination,MMSE)评分及脑白质区域部分各向异性值(fractional anisotropy,FA 值)的关系。报告如下。
1 资料与方法
1.1 一般资料
将上海交通大学医院附属仁济医院宝山分院康复科2020年6月至2021年10月收治的83 例PD 患者作为研究对象,其中男性43 例、女性40例,平均年龄(70.59±4.87)岁,平均病程(5.50±2.11)年,平均受教育年限(7.50±1.39)年。纳入标准:①中国帕金森病的诊断标准(2016 版)[9];②临床资料完整;;④无严重的心、肝、肾功能异常。排除标准:①合并凝血功能异常;②合并既往脑部疾病史;③合并确诊前认知功能异常;④合并精神疾病、无法交流患者。另选取健康检查的40 例患者为对照组,其中男性20 例、女性20 例,平均年龄(70.06±5.19)岁,平均受教育年限(7.66±1.42)年。两组患者的一般资料差异无统计学意义(P>0.05)。所有入试者家属均签署知情同意书。本实验经医院伦理委员会批准。
1.2 方法
①抽取所有患者清晨空腹周静脉血4 mL,3 000 r/min 离心15 min(r=13.5 cm)后取上层血清,在低温环境下保存待测,采用ELISA 法检测ApoA⁃1 水平,迈瑞BS⁃2000M 全自动生化分析仪,试剂盒购自上海沪峥生物科技有限公司。②UPDRS量表[10]:内容包括:总评分、第Ⅰ部分(精神、行为和情感)、第Ⅱ部分(日常生活能力)、第Ⅲ部分(运动功能分值),分数越低表示患者生存质量越优。③MMSE 量表[11]:包括:定向力、注意力、计算力、记忆力、命名、复述、三项理解指令、反应、书写和复制,总分30 分,用时5~10 min,MMSE ≥26 分为认知功能正常,<26 分有认知功能障碍。④脑白质微结构变化:通过磁共振弥散张量成像检测患者脑白质微结构改变的情况,仪器为联影3.0T 超导型磁共振uMR780,进行扫描检查。参数为:采集34 层,层厚4.0 mm,间距0 mm,相位FOV 230 mm,读出FOV 250 mm,TR 5865 ms,TE 80.2 ms,空间分辨率1.95×1.95×4.00 mm3。使用联合神经分析软件工作站对患者颞叶、顶叶、额叶、枕叶、前扣带束、后扣带束、胼胝体压部、胼胝体膝部、中脑锥体束、内囊锥体束、上纵束等脑白质区域部分FA 值进行检测。
1.3 统计学处理
采用SPSS 22.0 统计软件进行数据分析,计量资料用(±s)表示,行t检验,采用Person 相关性分析PD 患者ApoA⁃1 水平与UPDRS 评分、MMSE 评分及脑白质不同区域FA 值的关系,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者ApoA⁃1 水平、UPDRS 及MMSE 量表评分比较
PD 组患者ApoA⁃1 水平及MMSE 量表评分显著低于对照组,UPDRS 量表评分显著高于对照组,差异均有统计学意义(P<0.05)。见表1。
表1 两组患者ApoA⁃1 水平、UPDRS 及MMSE 量表评分比较结果(±s)Table 1 Comparison of ApoA⁃1 levels,UPDRS and MMSE scale scores between 2 groups(±s)
组别PD 组对照组t 值P 值n 83 40 ApoA⁃1(g/L)0.89±0.08 1.12±0.10 14.20 0.000 UPDRS 评分(分)16.88±1.79 2.40±1.41 44.85 0.000 MMSE 评分(分)21.70±1.85 27.48±1.43 17.36 0.000
2.2 两组患者脑白质不同区域FA 值比较
PD 组患者脑白质不同区域FA 值均低于对照组患者,差异均有统计学意义(P<0.05)。见表2。
表2 两组患者脑白质不同区域FA 值比较结果(±s)Table 2 Comparison of FA values in different areas of white matter between the two groups(±s)
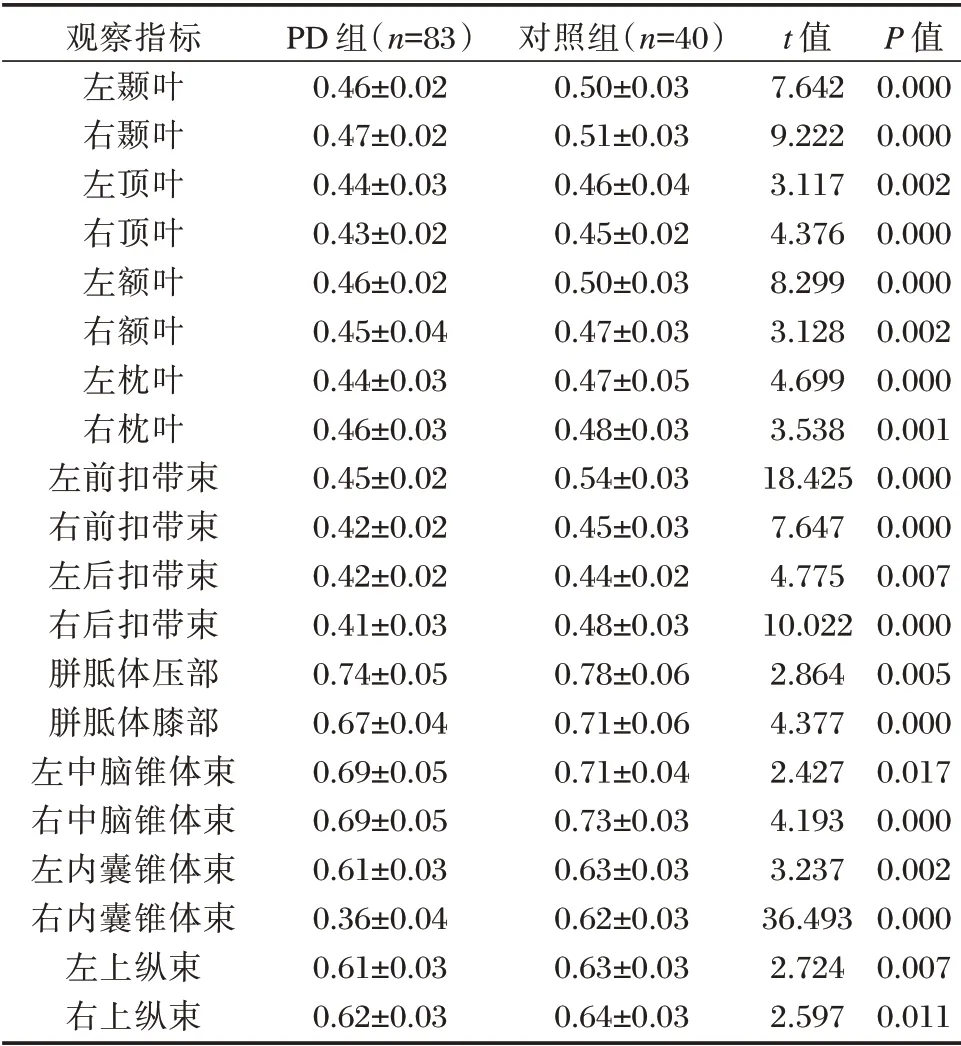
表2 两组患者脑白质不同区域FA 值比较结果(±s)Table 2 Comparison of FA values in different areas of white matter between the two groups(±s)
观察指标左颞叶右颞叶左顶叶右顶叶左额叶右额叶左枕叶右枕叶左前扣带束右前扣带束左后扣带束右后扣带束胼胝体压部胼胝体膝部左中脑锥体束右中脑锥体束左内囊锥体束右内囊锥体束左上纵束右上纵束PD 组(n=83)0.46±0.02 0.47±0.02 0.44±0.03 0.43±0.02 0.46±0.02 0.45±0.04 0.44±0.03 0.46±0.03 0.45±0.02 0.42±0.02 0.42±0.02 0.41±0.03 0.74±0.05 0.67±0.04 0.69±0.05 0.69±0.05 0.61±0.03 0.36±0.04 0.61±0.03 0.62±0.03对照组(n=40)0.50±0.03 0.51±0.03 0.46±0.04 0.45±0.02 0.50±0.03 0.47±0.03 0.47±0.05 0.48±0.03 0.54±0.03 0.45±0.03 0.44±0.02 0.48±0.03 0.78±0.06 0.71±0.06 0.71±0.04 0.73±0.03 0.63±0.03 0.62±0.03 0.63±0.03 0.64±0.03 t 值7.642 9.222 3.117 4.376 8.299 3.128 4.699 3.538 18.425 7.647 4.775 10.022 2.864 4.377 2.427 4.193 3.237 36.493 2.724 2.597 P 值0.000 0.000 0.002 0.000 0.000 0.002 0.000 0.001 0.000 0.000 0.007 0.000 0.005 0.000 0.017 0.000 0.002 0.000 0.007 0.011
2.3 PD 患者ApoA⁃1 水平与UPDRS、MMSE 量表评分及脑白质不同区域FA 值的相关性分析
PD 患者ApoA⁃1 水平与UPDRS、MMSE 量表评分及脑白质不同区域FA 值均呈现显著正相关(P<0.05)。见表3。
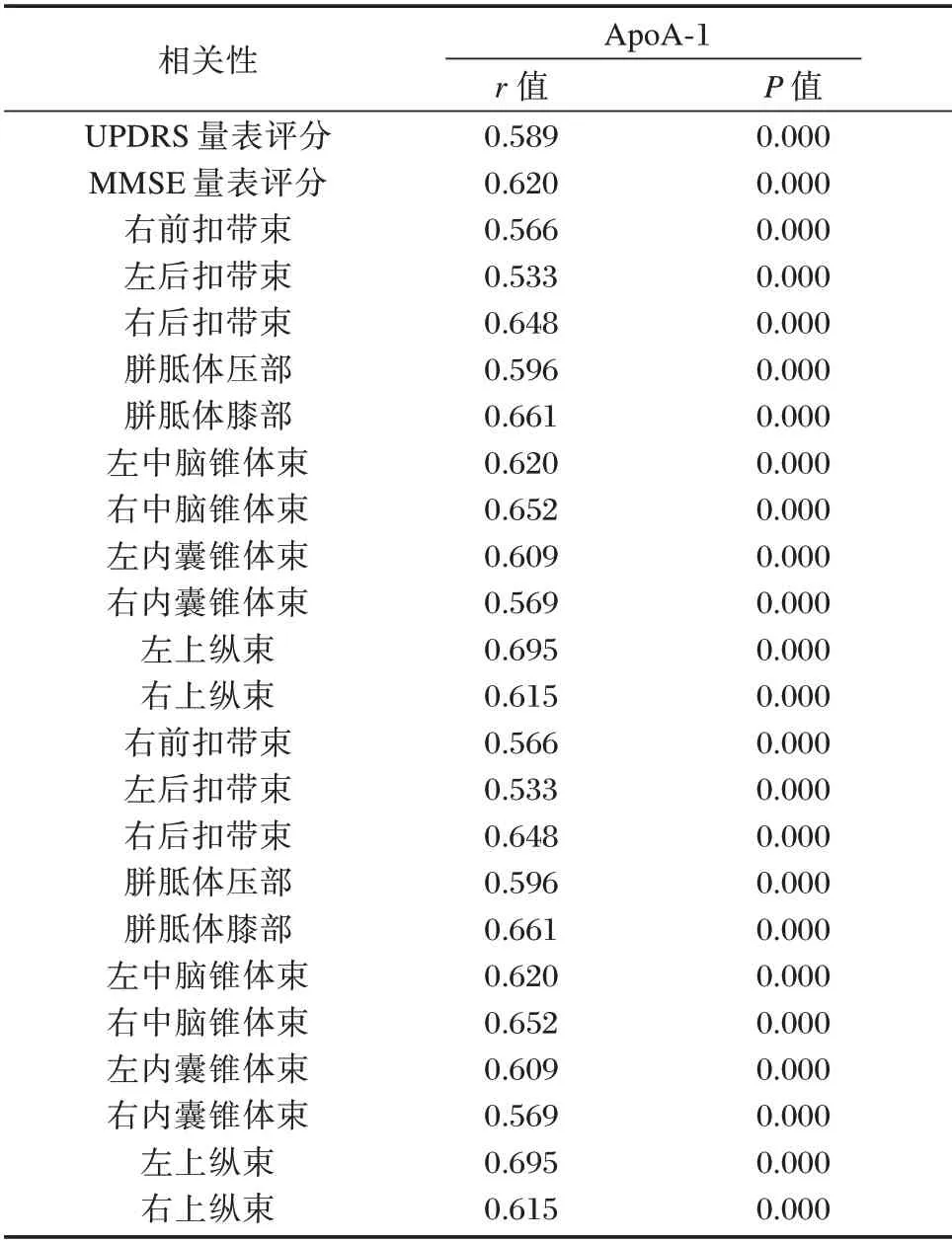
表3 PD 患者ApoA⁃1 水平与UPDRS、MMSE 量表评分及脑白质不同区域FA 值的相关性分析结果Table 3 Correlation analysis results of ApoA⁃1 levels in PD patients with UPDRS,MMSE scale scores and FA values in different areas of white matter
3 讨论
研究表明,神经系统疾病已成为导致人们发生残疾的主要疾病类型,PD 的增长速度在神经疾病中位列前位,其增长速度已经高于阿尔茨海默氏病,是影响当代人身心健康的重要疾病[12]。研究表明,到2040年,全球PD 患者预计将超过千万人,且PD 造成的全球负担正不断的增加,据研究表明,随着人口老龄化及工业化的进展,这种负担增加的趋势正由西方转向东方,尤其是中国。PD 的早期症状并不显著,进展缓慢,表现为一定程度的单侧肢体活动异常,逐渐累及另一侧肢体运动障碍[13]。认知障碍是PD患者主要的非运动症状,部分患者早期识别认知障碍较困难,导致临床难以发觉,在确诊时往往已进展到一定程度,耽误最佳治疗时期。认知功能损伤与多个因子及因素相关,血脂、脑白质结构的变化均可引起患者的认知障碍[14],故对其进行探究是关键。
本研究结果,提示PD 患者表现为ApoA⁃1 水平的下降,生活水平降低与认知功能的损伤,随着ApoA⁃1 的降低,患者的认知功能障碍越严重、生活质量越差,究其原因在于:ApoA⁃1 是高密度脂蛋白的重要成分,能够维持人体内胆固醇的稳定,有效清除部分胆固醇并抑制周围组织的脂质堆积,发挥抗氧化及防止炎症反应的作用,常用于心血管疾病中预测动脉粥样硬化的发生[15]。在本研究中,ApoA⁃1 水平在PD 患者中表现为降低,且随着水平的下降患者的疾病进展严重。UPDRS 评分代表PD 患者症状的严重程度,常与患者智力变化相关;MMSE 量表表示患者认知功能障碍情况,当ApoA⁃1 水平降低的同时,MMSE 水平下降,UP⁃DRS 评分上升,预示着ApoA⁃1 水平是影响PD 患者认知功能的重要因素,患者的认知功能障碍程度越高,其体内的ApoA⁃1 水平越低。除此之外,PD 患者脑白质各FA 水平均显著低于对照组,且ApoA⁃1 水平与脑白质不同区域FA 值均表现出相关性显著,这可能是因为:PD 患者多存在脑白质病变情况,改病变与认知功能损伤密切相关,多由脑白质区域与日常活动相关的环路纤维联系阻碍而引起,因神经环路的连接水平降低而导致功能障碍生成,表现为认知障碍。磁共振技术是监测PD 患者疾病进展的重要辅助手段,而弥散张量成像能够有效分析患者脑白质体积的减少及微结构的变化。本研究中,PD 患者颞叶、顶叶、额叶、枕叶、前扣带束、后扣带束、胼胝体压部、胼胝体膝部、中脑锥体束、内囊锥体束、上纵束等区域的FA 值均低于对照组,FA 水平与患者嗅皮层、边缘系统等通路发生损伤有关,故FA 水平的降低代表患者脑部的损伤处于进展中,表明PD 患者脑白质微结构的变化程度剧烈,提示损伤程度严重,各FA 值均与ApoA⁃1 相关性显著,提示脑白质微结构的变化与认知障碍相关,在认知功能损伤中起到重要影响。
综上所述,ApoA⁃1 水平下降预示着PD 患者的病情严峻,ApoA⁃1 的变化与患者认知功能障碍及脑白质病变的关系密切,临床可以通过对ApoA⁃1进行监测,预测患者疾病进展及判断患者的认知障碍程度。但本研究存在一些不足之处,例如只是单中心的回顾性分析,且为回顾性分析,缺乏一些实验的设计性与前瞻性,在今后的研究中将会进一步改进,使研究结果更具有说服力。

