培美曲塞、顺铂联合125I粒子植入治疗晚期非小细胞肺癌患者临床效果观察
李澜欣
河南科技大学第一附属医院肿瘤放疗科,洛阳市 471000
在我国,非小细胞肺癌(NSCLC)患者占所有肺癌患者的80%以上[1]。NSCLC患者早期无典型症状,多数患者在中晚期出现症状后才被确诊,此时无法通过手术根治,患者的生活质量受到严重影响。铂类药物联合培美曲塞化疗能够较好地控制NSCLC患者病情,但对已发生转移患者的治疗效果并不理想,且毒副作用较大[2-4]。125I是一种放射性同位素,经皮穿刺术将125I粒子植入NSCLC患者肿瘤组织内,由其所发出的射线能杀灭肿瘤细胞而发挥治疗作用;125I联合培美曲塞和铂类药物化疗可以防止肿瘤复发与转移,从而有效弥补化疗的不足[5-6]。晚期NSCLC患者无法进行手术治疗,培美曲塞、铂类联合125I粒子植入治疗可作为较好的治疗方案,可有效抑制病灶的生长与肿瘤细胞的扩散,减轻患者的痛苦[7-8]。为探讨培美曲塞、顺铂联合125I粒子植入治疗NSCLC患者的临床疗效,本研究选取68例患者进行了治疗观察,现将结果报告如下。
1 资料与方法
1.1 一般资料 选取2018年7月至2019年7月在我院接受治疗的68例晚期NSCLC患者作为研究对象。纳入标准:(1)符合《中国原发性肺癌诊疗规范(2015年版)》中晚期NSCLC诊断标准[9];(2)近3个月未使用其他抗肿瘤药物治疗;(3)凝血功能正常;(4)患者及其家属均了解本研究基本情况,签署治疗研究知情同意书。排除标准:(1)感染发热患者;(2)合并其他恶性肿瘤患者;(3)合并免疫系统疾病患者;(4)预计生存期不足半年的患者。采用随机数字法将入选患者分为观察组和对照组各34例。对照组患者男18例、女16例;年龄35~68岁,平均(41.46±4.73)岁;病程4~35个月,平均(15.22±3.52)个月;肿瘤直径0.99~6.23 cm,平均(4.38±1.14)cm;肿瘤分期Ⅲb期21例、Ⅳ期13例。观察组患者男20例、女14例;年龄37~66岁,平均(42.01土4.52)岁;病程3~36个月,平均(19.59±3.17)个月;肿瘤直径0.97~6.40 cm,,平均(4.27±1.22)cm;肿瘤分期Ⅲb期19例、Ⅳ期15例。两组患者的性别、年龄、病程等一般资料比较,差异无统计学意义(P<0.05)。本研究经我院医学伦理委员会审核批准。
1.2 方法
1.2.1 基础治疗 化疗前给予两组患者防止呕吐及补充电解质治疗。化疗前2周,口服叶酸(北京斯利安药业有限公司)治疗,0.4 mg/次,1次/d;肌肉注射维生素B12(遂成药业股份有限公司),1 mg/次,2次/d。化疗前1天、化疗治疗当天及化疗第2天,口服地塞米松片(广东南国药业有限公司)治疗,9 mg/次,1次/d。
1.2.2 对照组 化疗第1天,静脉滴注培美曲塞(齐鲁制药有限公司,生产批号:061191102200),500 mg/m2,10~15 min内滴注完成;化疗第1~3天,静脉滴注顺铂(齐鲁制药有限公司,生产批号:6M025A89),25 mg/m2,1次/d。
1.2.3 观察组 接受培美曲塞、顺铂联合125I粒子(北京智博高科生物技术公司,生产批号:ZBS-1602-10-20)植入治疗。培美曲塞、顺铂化疗方案同对照组,可在125I粒子植入治疗前后1个月进行。125I粒子植入前,通过放射治疗计划系统模拟实施放射治疗确定治疗计划,在超声引导下确定穿刺点。术前应用透皮贴剂预防和缓解患者术中以及术后疼痛。术前采用64排螺旋CT(西门子)行胸部检查,层厚设定为5 mm,将CT扫描图像传输至治疗计划系统(TPS,HGGR-2000,珠海和佳),勾画靶区,确定剂量为90~110 Gy、粒子活度为0.5~0.8 mCi(北京智博高科生物技术有限公司,北京)、粒子间距为0.5~1.0 cm、针道间距约为1 cm,评估穿刺路径及安全性,制定治疗方案。再次进行CT扫描定位选取穿刺点,使用18 G的PTB针从进针点穿刺至肿瘤底部,穿过肿瘤中心距边缘0.5 cm;退出内芯,确认无血液从外针芯内流出,开始植入。各穿刺点间隔1 cm,对特殊部位进行补种,确保125I粒子布满整个瘤体。完成植入术后按压穿刺点10~20 min。
1.3 观察指标
1.3.1 治疗前、治疗3个月后,取患者清晨空腹静血,使用酶联免疫吸附测定法[10]检测血清细胞角蛋白19片段(CYFRA 21-1)和神经元特异性烯醇化酶(NSE)水平。
1.3.2 治疗3个月后,根据实体肿瘤的疗效评价标准(RECIST1.1)[11]评估两组患者的临床疗效。完全缓解(CR)指非淋巴结病变完全消融;部分缓解(PR)指肿瘤负荷减少≥30%;疾病稳定(SD)指肿瘤负荷未发生显著变化;疾病进展(PD)指肿瘤负荷增加≥20%。治疗总有效率=(CR例数+ PR例数)/总例数×100%
1.3.3 治疗3个月后,采用生活质量综合评定问卷-74(GQOL-74)[12]评估两组患者的生活质量。问卷包括躯体、心理、社会及物质生活4个维度,总分为20~100分,评分越高表示患者的生活质量越好。
1.4 统计学处理 采用SPSS 23.0统计学软件分析数据,计量资料用x±s表示,组间比较采用独立样本t检验,组内治疗前后比较采用配对t检验;计数资料以%表示,比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者治疗前后的血清CYFRA 21-1和NSE水平比较 治疗前,两组患者的CYFRA 21-1、NSE水平比较,差异无统计学意义(P>0.05);治疗3个月后,两组患者的CYFRA 21-1、NSE水平均明显下降,观察组患者的水平显著低于对照组,差异有统计学意义(P<0.05)。见表1。
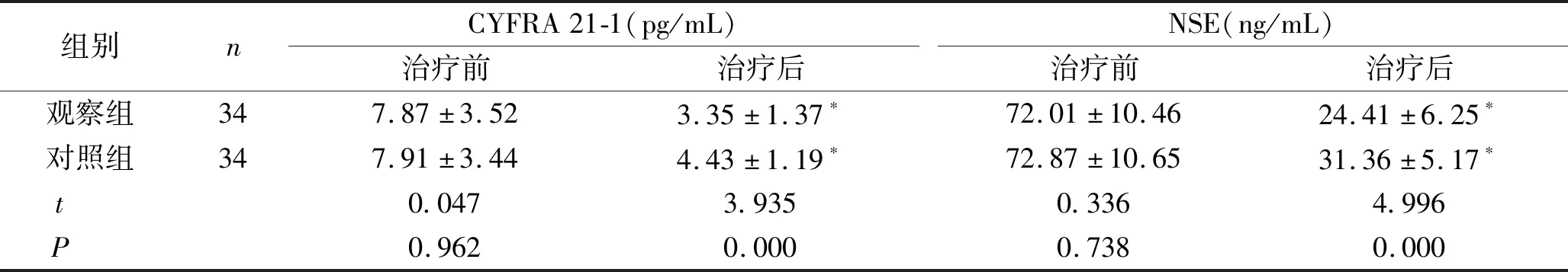
表1 两组患者治疗前后的血清CYFRA 21-1和NSE水平比较 (n,x±s)
2.2 两组患者的临床疗效比较 治疗3个月,观察组患者的治疗总有效率(82.35%)明显高于对照组(55.88%),差异有统计学意义(P<0.05)。见表2。

表2 两组患者的临床疗效比较 [n(%)]
2.3 两组患者治疗前后的生活质量评分比较 治疗前,两组患者GQOL-74中的躯体功能、心理功能、社会功能及物质生活评分比较,差异无统计学意义(P>0.05);治疗3个月后,两组患者的躯体功能、心理功能、社会功能及物质生活评分均明显增高,观察组患者的评分显著高于对照组,差异有统计学意义(P<0.05)。见表3。
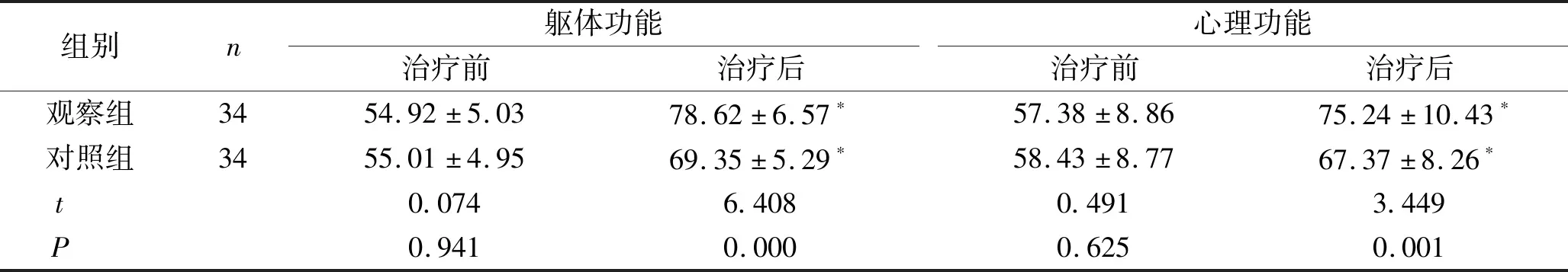
表3 两组患者治疗前后的生活质量评分比较 (n,x±s)
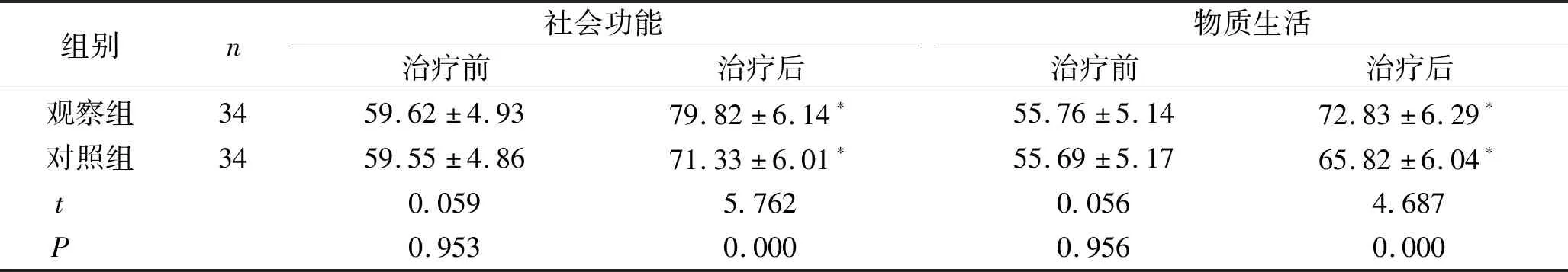
续表3
3 讨 论
125I粒子植入治疗为目前治疗实体肿瘤的一种新型放射治疗方法,具有创伤小、放射性元素用量少、可持续照射等特点,能将无法手术切除或切除不干净的肿瘤组织(细胞)通过持续的射线照射灭活,对多种实体肿瘤均有较好的控制和杀灭作用,可弥补外科手术治疗以及化疗的缺陷。
NSE为一种酸性蛋白酶,其含量与肿瘤细胞的增殖周期成正比,可用于反映NSCLC治疗的情况。125I粒子可干扰癌细胞的增殖活动,联合药物治疗能够使细胞内的NSE释放减少。CYFRA 21-1常被用作诊断NSCLC的标志物,机体某些部位发生癌变时其水平也会升高。在本研究中,对照组患者接受培美曲塞、顺铂方案化疗,观察组患者接受培美曲塞、顺铂方案化疗联合125I粒子植入放疗。结果显示,治疗3个月后,观察组患者的CYFRA 21-1和NSE水平均显著低于对照组,提示培美曲塞、顺铂联合125I粒子植入治疗能够显著降低晚期NSCLC患者的血清肿瘤标志物及酸性蛋白酶水平,与茹玉航等[13]报道的结果相似。本研究结果显示,治疗3个月,观察组患者的临床疗效高于对照组,提示培美曲塞、顺铂联合125I粒子植入治疗NSCLC患者能获得较好近期疗效[14]。培美曲塞可抑制胸苷酸等物质的生成,而植入的125I粒子在患者体内衰变过程中可持续释放出低频、低剂量的伽马射线使肿瘤细胞的DNA链断裂,从而影响肿瘤细胞的裂变与增殖。由于125I粒子辐射半径小,故对患者肿瘤周围正常组织的影响甚微,与常规的化疗联用还可以增加肿瘤细胞对药物的敏感性,加快肿瘤病灶消除,提高治疗效果。本研究结果显示,治疗后两组患者GQOL-74中的躯体功能、心理功能、社会功能及物质生活评分均明显增高,观察组患者的评分显著高于对照组,提示125I粒子植入联合化疗治疗,可明显改善NSCLC患者的病情及身体机能,提高患者的生活质量,与孙俊凯等[15]报道的结果相似。125I粒子治疗能在保留人体正常器官生理功能的情况下,不采用手术治疗也同样可以达到缩小肿瘤病灶、抑制肿瘤生长的效果,减轻患者的痛感;培美曲塞与铂类药物可与肿瘤细胞的DNA、核苷形成结合物,抑制DNA的复制,抑制病情进展,提高患者的生活质量。
化疗作为非小细胞肺癌患者的主要治疗方案,但不能完全地杀死肿瘤细胞,且存在一定副作用;外科手术切除肿瘤组织可能存在术后复发以及并发症多发的情况。培美曲塞、铂类化疗联合125I粒子植入治疗晚期NSCLC患者能弥补化疗及手术治疗的不足,近期疗效良好,能明显提高患者的生理功能和生活质量,值得推广应用。

