基于网络药理学的葛根降糖机制研究
舒建中 李颖慧 蒲雨晴 刘庆灵 张 娟 甘玉立 谢永芳▲
1.重庆市中医院脑病科,重庆 400021;2.重庆邮电大学生物信息学院,重庆 400065
葛根为多年生草质藤本植物[1],内含有葛根素、大豆黄酮苷等丰富的黄酮类化合物,还有蛋白质氨基酸、糖和人体必需的铁、钙、铜、硒等矿物质,药用价值极高[2]。本研究利用网络药理学,期望从成分-靶点-通路进行整体预测,并阐明葛根在体内的作用机制,选取葛根基本成分,结合靶点功能以及通路对蛋白质相互作用(protein-protein interaction,PPI)网络进行聚类,探讨相关显著的作用模块及每个模块的关键基因,并期望构建PPI 网络以及基因本体(gene ontology,GO)功能、京都基因和基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路分析,旨在分析其靶点以及信号通路,对葛根成分小分子及其作用靶点的结合潜力进行探究,以明确其与靶点的结合潜力,为最终构建“化合物-靶点-信号通路”网络奠定基础。本研究预期通过对葛根化学成分的网络药理学分析寻找葛根发挥作用的关键成分、靶点及作用通路,探讨其多靶点多通路协同作用机制,期望能为葛根的开发应用奠定基础。
1 方法
1.1 化合物成分及靶点分析
中药系统药理学数据库与分析平台(pharmacology database and analysis platform of traditional Chinese medicine system,TCMSP)数据库收集中草药的组分和分子结构、关键ADME(吸收、分布、代谢和排泄)参数、成分作用靶点等关键信息[3]。通过TCMSP 数据库,查询葛根主要成分,并筛选出口服生物利用度(oral bioavailability,OB)>30、类药性(drug-likeness,DL)>0.18 的小分子,研究其作用方式。获得小分子的Chem ID,在Pubchem 数据库中找到其对应smile 序列,若无对应靶点信息的成分,利用MOE 软件,使用swiss target prediction 网站获得其成分靶点信息[4]。
1.2 构建PPI 网络及化合物-靶点-信号通路网络
使用STRING 在线软件进行PPI 网络的构建与分析,以预测靶点之间的相互作用,并通过metascape获得靶点的相关富集通路和功能注释,并对靶点进行聚类并筛选关键靶点,通过cytoscape 对所得信息进行整理构建化合物-靶点-信号通路网络。
1.3 关键靶点及分子对接验证
对获得的关键靶点进行验证,利用MOE 软件进行分子对接,通过其结合能力从空间结构匹配和能量匹配来验证其结合机制。观察pose 数量、pose 之间的最佳得分以及偏离原配体程度(root-mean-square deviation,RMSD)值[3-4]。
根据经验使用PDB(protein data bank)数据库搜索含有小分子配体,且配体结构更接近对接药物的小分子结构,选择口袋和共晶配体完整的结构和分辨率高的晶体结构[5-6]。
2 结果
2.1 化合物成分及靶点分析结果
通过对葛根化学成分的筛选,共获得4 种满足OB>30、DL>0.18 的小分子,它们可能是潜在的活性成分。本实验分析材料为除葛根素的四种符合筛选条件的葛根主要成分:芒柄花黄素(formononetin)、谷甾醇(β-sitosterol)、3′-甲氧基大豆苷元(3′-methoxydaidzein)、大豆苷元-4′,7-二葡萄糖苷(daidzein-4′,7-digluco side)、葛根素(puerarin)。最终获得106 个相关靶点的基因信息(gene symbol)来进行后续分析。葛根成分的部分靶点信息见表1。
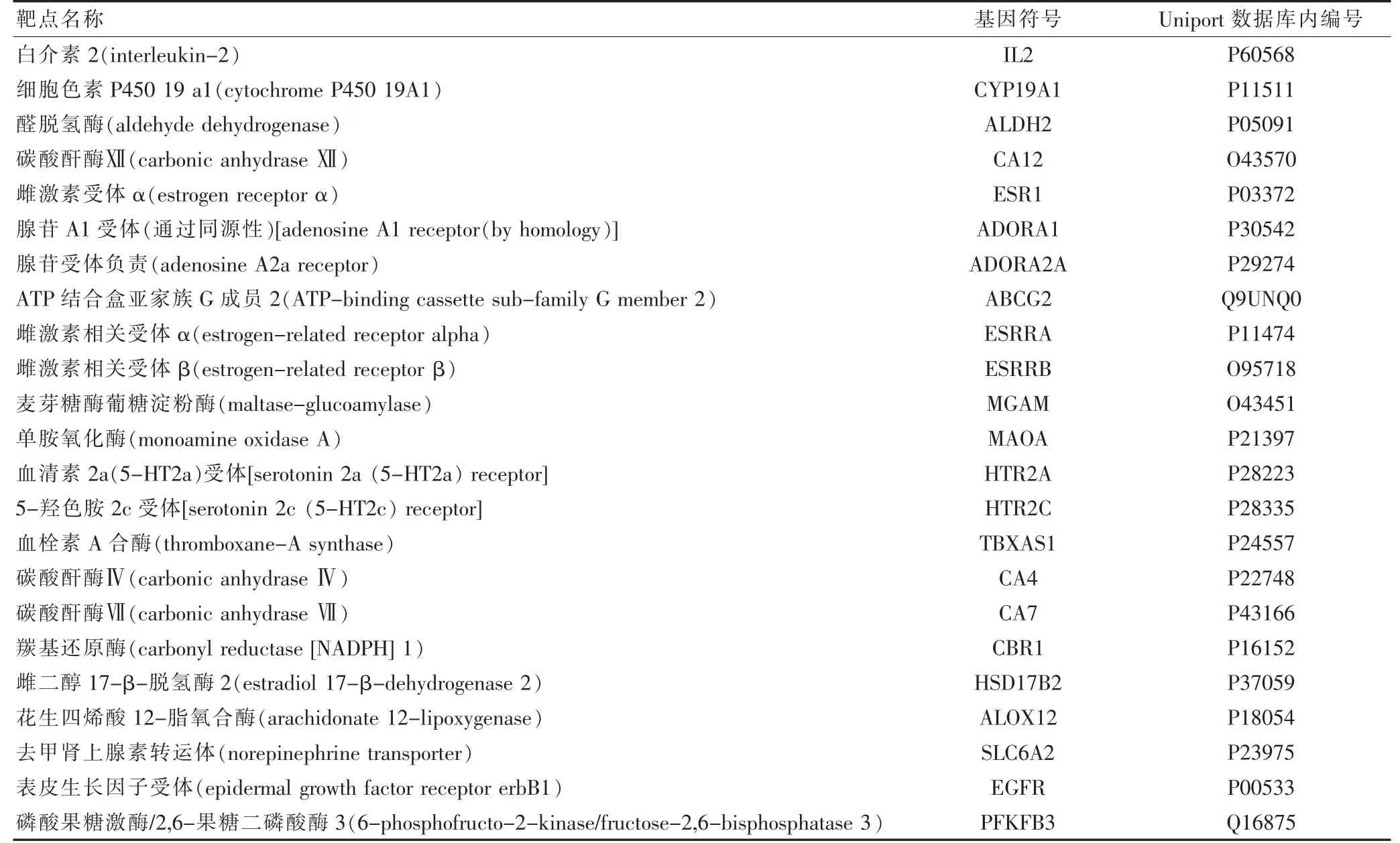
表1 葛根成分的部分靶点信息
2.2 构建PPI 网络
从STRING 网站上传葛根相关靶点构建PPI 网络关系数据,获得相关GO 分子功能118 条及细胞组分注释及KEGG 通路注释51 条。利用metascape 根据基因gene symbol 富集到的通路和生物学过程,来分群和构建PPI 网络。挑选出富集程度较高的gene,注释相关性,构建PPI 网络。图1A(封三)表示富集到的基因关联性网络;图1B(封三)为基因富集程度网络;图2A(封三)显示PPI 网络,可以观察到不同基因的作用关系;图2B(封三)显示其中主要的几个模块及其基因数量。
图1 metascape 富集结果
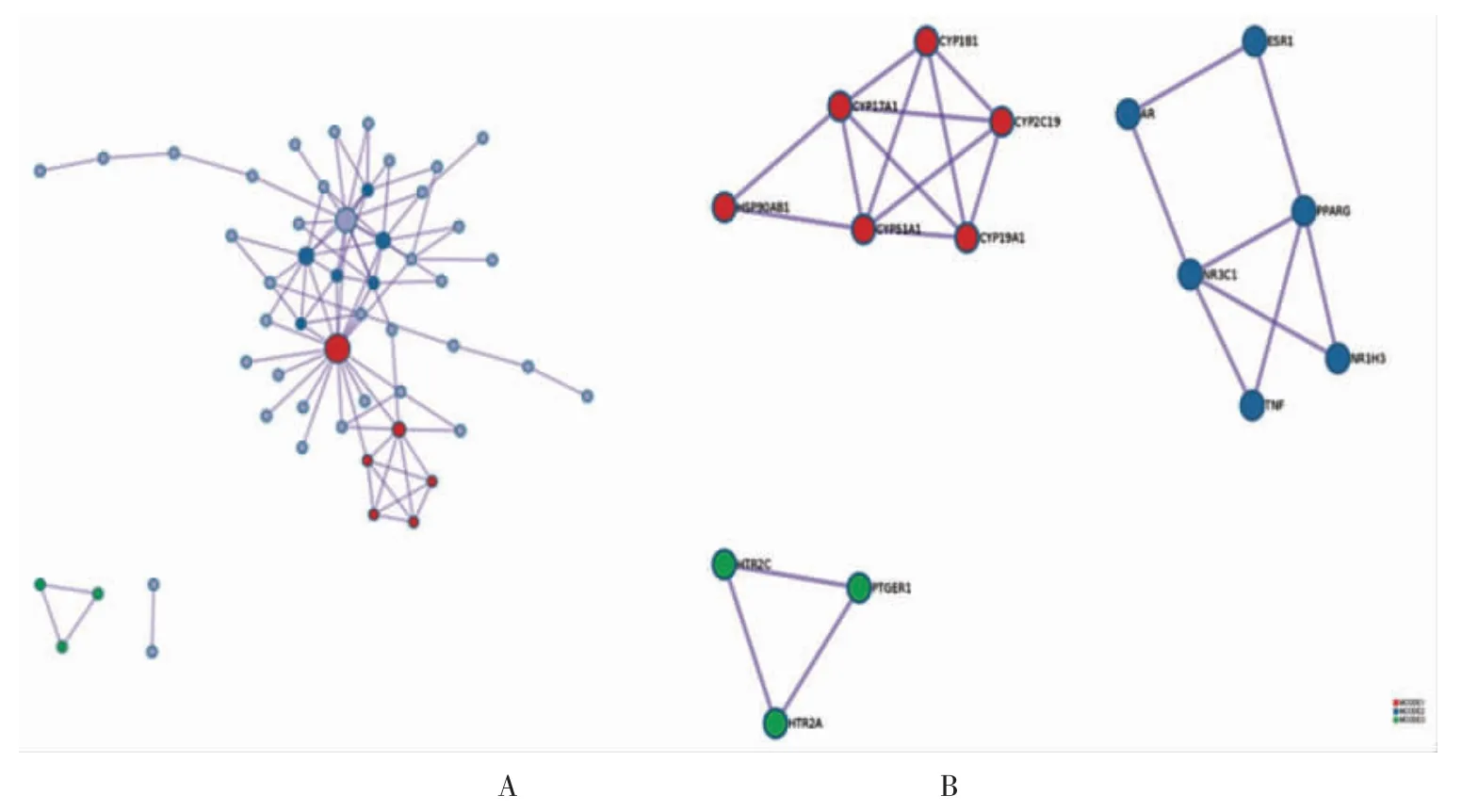
图2 PPI 网络
2.3 构建“化合物-靶点-信号通路-功能”网络
将“2.2”项中的PPI 数据与通路和生物学过程富集数据相结合,可得三类基因模块及代表基因(表2);其中模块1 包括CYP17A1、HSP90AB1、CYP19A1、CYP51A1、CYP2C19、CYP1B1;模块2 有NR3C1、PPARG、AR、TNF、NR1H3、ESR1;HTR2C、PTGER1、HTR2A 属于模块3。
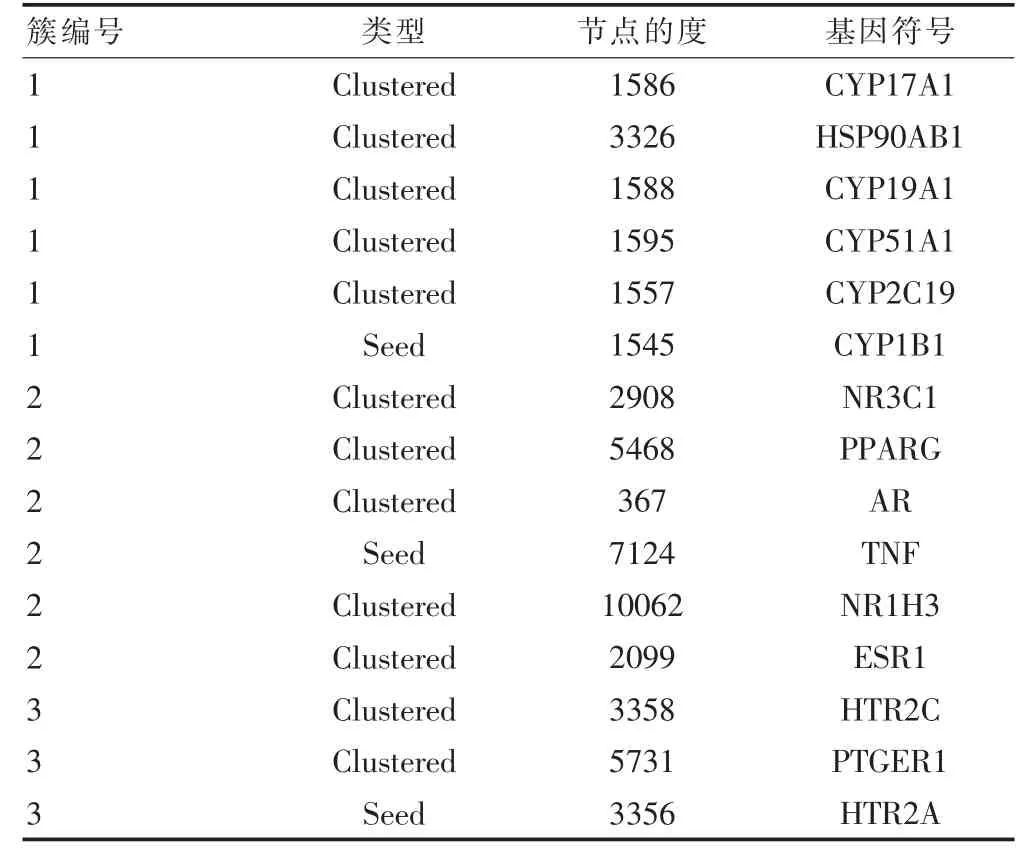
表2 各模块高分代表基因
图3(封四)绘制出了所有靶点相关的“化合物-靶点-信号通路-功能”,结果显示,网络中既存在一个分子与多个靶点蛋白的相互作用关系,也存在不同分子作用于同一个靶蛋白的现象,显示出多成分多靶点多通路特点,一定程度上也暗示葛根可能在多种疾病上均可发挥作用。

图3 “化合物-靶点-信号通路-功能”关系图
2.4 关键靶点及分子对接验证
选取每组打分最高的基因靶点CYP17A1、NR3C1、HTR2C,进行分子对接验证。在PDB 数据库中查找符合条件的PDB 结构,即靶点蛋白的三维结构,得到CYP17A1(P05093)的靶点蛋白,其PDB ID为5IRQ,对应结合的药物小分子为β-谷甾醇;NR3C1(P04150)在PDB 数据库中查找得到的对应靶点蛋白的PDB ID 为4UDD,对应小分子为β-谷甾醇;在PDB 数据库中查找到得到HTR2C(P28335)的对应靶点蛋白的PDB ID 为6BQH,对应小分子为芒柄花黄素和3′-甲氧基大豆黄素。运行MOE 软件,分别进行分子对接,对接打分结果见表3,对接图见图4(封三)。其中S值表示一系列的小分子与蛋白质的对接pose 中的得分最佳的,通常S 值越负,对接情况越好;由于PDB 结构中下载的蛋白质结构中含有小配体,因此,可以通过药物小分子与原配体的叠合能力来预测小分子与靶点蛋白的结合能力,而配体与小分子的叠合能力由RMSD值来衡量,其中RMSD值越小,表示该小分子与靶点蛋白具有良好的结合潜力。表3 结果显示,β-谷甾醇与ID 为4UDD 的靶点蛋白结合能力以及与原配体的叠合能力较好。

表3 各对接情况打分表
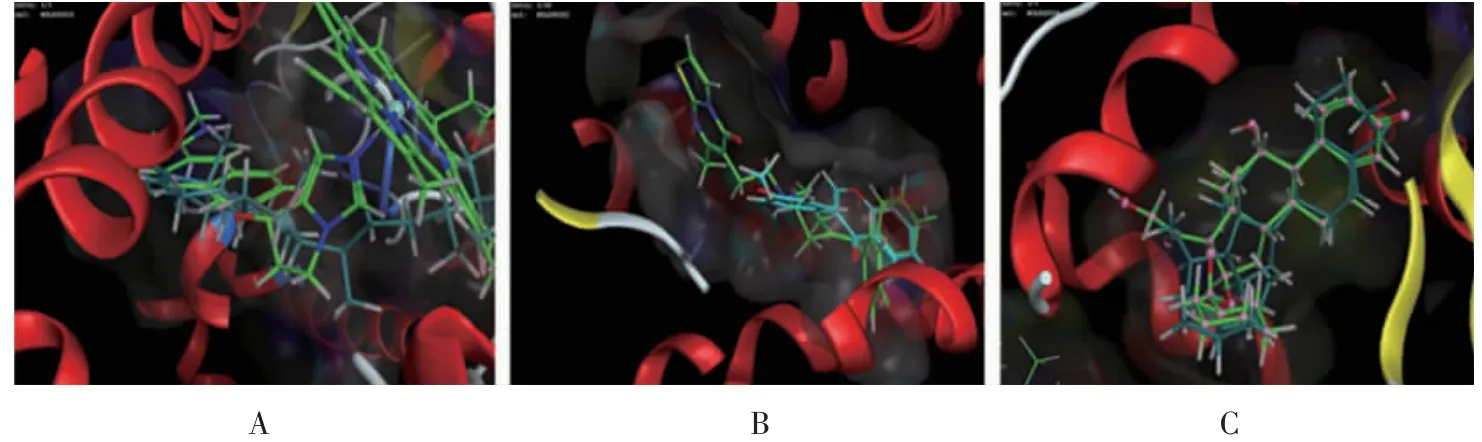
图4 靶点与药物分子对接
3 讨论
3.1 三个模块的降糖作用分析
目前一般认为糖尿病发病机制与胰岛素分泌和/或胰岛素作用缺陷有关[7-8],有研究表明,含葛根的汤剂配合西医常规治疗对2 型糖尿病(type 2 diabetes mellitus,T2DM)湿热证患者血糖有明显改善作用[9]。模块1 包括CYP17A1(1.141432)、HSP90AB1、CYP19A1(1.141419)、CYP51A1、CYP2C19、CYP1B1,该模块五个基因主要富集到类固醇代谢途径[9]。类固醇激素及其受体主要参与真核基因表达的调节,并影响靶组织中的细胞增殖和分化。其中CYP1B1,细胞色素P450 1B1。细胞色素P450 是一组血红素硫醇单加氧酶[10]。在肝微粒体中,该酶参与还原型烟酰胺腺嘌呤二核苷酸磷酸(reduced nicotinamide adenine dinucleotide phosphate,NADPH)依赖性电子转运途径[11-12]。它会氧化类固醇、脂肪酸、类维生素A 等。模块2 包括NR3C1、PPARG、AR、TNF、NR1H3、ESR1 主要功能富集在类固醇激素反应以及类固醇介导的信号通路。PPARG 是过氧化物酶体增殖物激活受体γ;结合过氧化物酶体增殖物(如降血脂药和脂肪酸)的核受体。一旦被配体激活,核受体就会与DNA 特异的PPAR 反应元件结合并调节其靶基因(如酰基辅酶A 氧化酶)的转录,控制了脂肪酸的过氧化物酶体β-氧化途径,是脂肪细胞分化和葡萄糖稳态的关键调节器[13-14]。ARF6 充当组织特异性脂肪细胞P2(adipocyte P2,aP2)增强子的关键调节剂[15]。PTGER1 是前列腺素E2(prostaglandin E2,PGE2)受体EP1 亚型,该受体的活性由激活磷脂酰肌醇钙第二信使系统的G(q)蛋白介导,可能是肾脏功能的重要调节剂,涉及各种组织中对PGE2的平滑肌收缩反应,分析与肠胃蠕动消化调节有关。模块三包括HTR2C、PTGER1、HTR2A 主要功能富集在钙信号通路以及磷脂酰肌醇生物合成过程。
3.2 相关基因与降糖途径分析
CYP17A1 是细胞色素P450 家族17 亚家族A 成员,可催化17-α-羟基化和17,20-裂合酶反应,对于雄激素和糖皮质激素的产生都是必不可少的。有实验证明,肝脏CYP17A1 在糖异生中的作用是通过其下游产物17-OHP 激活糖皮质激素受体转录活性,使糖异生的关键酶基因的转录上调,从而促进了糖异生的过程[16-17]。皮质醇是主要的内源性糖皮质激素,它影响多种生理功能,例如脂质和葡萄糖代谢,代谢稳态和对压力的适应性。皮质醇的生产主要受促性腺激素中促肾上腺皮质激素(adrenocorticotrophic hormone,ACTH)的调节。ACTH 对皮质醇合成的刺激作用取决于cAMP 依赖性信号传导,但也涉及膜去极化和胞浆Ca2+增加。cAMP 和Ca2+各自诱导StAR 的表达,刺激线粒体内胆固醇的转移,以及从胆固醇到皮质醇的途径中的类固醇生成酶(例如CHE、CYP17A1、CYP11B1)[16]。
NR3C1 是糖皮质激素受体,具有转录抑制活性。NR3C1 是应激反应系统的关键组成部分。糖皮质激素对糖代谢具有干扰作用,与胰岛素的降糖有拮抗作用,是胰岛素反调节激素,糖皮质激素过多可能会导致继发性糖尿病[17-18]。有研究表明,糖皮质激素可以应用到某种糖尿病患者的临床治疗中,可以有效控制炎症反应、减少血糖波动[19-20]。
HTR2C 是G 蛋白偶联的5-羟色胺受体,有研究表明,基因HTR2C 与高血糖、神经系统疾病以及免疫代谢等方面有关[21]。
综上所述,通过构建葛根多成分-靶点-信号通路,并对靶点基因功能和代谢通路进行分析,借助网络药理学的思路解释葛根降血糖的可能作用机制。文中预测的靶点与已知的药理作用相吻合,说明靶点预测的准确性,获得其主要靶点有三个,分别为CYP17A1、NR3C1 和HTR2C,揭示了葛根作用的多成分、多靶点、整合调节作用特点。

