超声引导下微波消融术用于甲状腺良性结节对甲状腺功能及结节体积水平的影响分析
商百良
(辽宁省盘锦市中心医院普外科,辽宁 盘锦 124000)
甲状腺良性结节指甲状腺腺瘤、炎症性结节、肿瘤性结节及结节性甲状腺肿等疾病,一般良性结节不会影响甲状腺功能,部分患者颈部肿大,导致声音嘶哑,甚至影响正常呼吸[1]。临床予甲状腺激素抑制剂、放射、手术等治疗方法,除手术外,其他方式疗程较长,临床应用受限[2]。手术切除甲状腺结节创伤较大,影响患者术后恢复。经皮穿刺微波消融术是微创手术方式,微波消融针可直插病变组织内部,经热、冷刺激,使病灶内部蛋白质发生凝固和坏死,从而达到治疗作用[3]。本研究旨在分析超声引导下微波消融术治疗甲状腺良性结节对患者甲状腺功能、结节体积水平产生的影响,现报道如下。
1 资料与方法
1.1 临床资料 选取本院2018年3月至2020年3月收治的120例甲状腺良性结节患者作为研究对象,随机分为观察组与对照组,每组60例。对照组男22例,女38例;平均年龄(45.5±4.2)岁;结节数78枚,囊性结节12枚,实性结节45枚,囊实混合结节21枚;结节体积1.2~10.3 cm3,平均体积(5.17±3.64)cm3。观察组男23例,女37例;平均年龄(44.8±4.3)岁;结节数79枚,囊性结节13枚,实性结节46枚,囊实混合结节20枚;结节体积1.2~10.2 cm3,平均体积(5.16±3.64)cm3。两组临床资料比较差异无统计学意义,具有可比性。所有患者均对本研究知情同意并自愿签署知情同意书。本研究已通过本院伦理委员会审核批准。
纳入标准:经彩超确诊为甲状腺结节;甲状腺功能正常;免疫抗体正常;甲状腺直径0.45~4.2 cm。排除标准:甲状腺恶性肿瘤者;甲状腺亢进者;凝血功能障碍者;严重脏器衰竭者。
1.2 方法 对照组给予腹腔镜切除术,术前气管插管全麻,仰卧位,颈部稍伸,垫高肩部,充分暴露手术视野。经由胸乳入路,切口10 mm,分别于双侧乳晕取两个5 mm操作孔,将30 ml 0.9%氯化钠溶液与2滴肾上腺素混合,通过注射器注于胸前壁操作区皮下深筋膜。剥离至皮下深筋膜层,置管后建立CO2气腹,维持气腹压力0.8 kPa,置10 mm腹腔镜,经镜下操作,使用电凝钩分离下皮疏松结缔组织。超声刀切开颈白线,游离甲状腺,保持甲状旁腺组织的完整,切除病灶,经观察孔取出,最后缝合处理。
观察组于超声引导下行微波消融术治疗,仰卧位,垫高肩部,稍后屈,微仰头部,保持颈部过伸状态,充分暴露颈部。显示颈前区,超声检查后确定结节病灶位置、范围。术中监测心率、血压及血氧饱和度等指标,开放静脉通路。消毒、铺巾后,经超声引导,对肘静脉团注造影剂,经超声观察结节、周围血流灌注的变化。注射2%利多卡因局麻,范围包括皮肤至甲状腺外包膜穿刺通路,避免温度过高产生不适感。经超声观察结节前、结节后、上下左右各路径情况,选择液体隔离带法穿刺,取30~40 ml 0.9%NaCl注射液分离甲状腺后包膜、食管间隙,分离周围甲状腺与后包膜、喉返神经等区域,尤其是结节邻近颈动脉、喉返神经等结构,形成5 mm液体隔离带,保护周边组织神经。术中避开大神经、血管,选择合适进针方向及位置。进针路径遵循从远至近、从深至浅的原则。经颈外侧朝内侧穿刺,颈中线外侧穿刺外下象限结节,消融时需注意穿刺路径。插入微波消融针,微波功率25~30 W,消融时间1 min。结节过多可采用多次进针方式进行消融治疗;结节过大需进行多面、多点消融方式治疗;囊实性结节可使用注射器抽吸囊液,也可使用聚桂醇硬化剂冲洗囊腔,再使用微波消融针消除其他成分和囊壁。气化回声覆盖结节后,注入造影剂,观察结节消融状态,如造影剂显影,需再次对此区域进行消融治疗,至无造影剂显影为标准,手术结束。
1.3 观察指标 术后6个月,采用全自动免疫分析仪检测两组血清游离三碘甲状腺原氨酸(FT3)、游离甲状腺素(FT4)和促甲状腺激素(TSH)水平;通过彩超观察并记录结节体积水平。采用视觉模拟疼痛评分法(VAS)评价两组术后8、24、48 h疼痛情况,0分表示无疼痛感,1~3分表示疼痛轻,4~6分表示中度疼痛,7~9分表示疼痛严重,10分表示疼痛剧烈不能忍受。比较两组术后甲状旁腺损伤、甲状腺结节破裂发生率。
1.4 统计学方法 采用SPSS 19.0统计学软件分析数据,计量资料以“±s”表示,采用t检验,计数资料以[n(%)]表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组术后甲状腺功能、结节体积比较 观察组FT3、FT4水平均低于对照组,FSH水平高于对照组,结节体积小于对照组,差异均有统计学意义(P<0.05),见表1。
表1 两组术后甲状腺功能、结节体积水平比较(±s)Table1 Comparison of postoperativethyroid function and nodule volumebetween the two groups(±s)
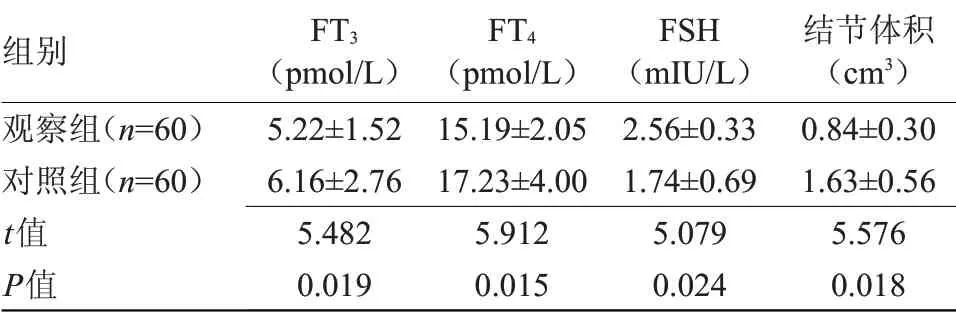
表1 两组术后甲状腺功能、结节体积水平比较(±s)Table1 Comparison of postoperativethyroid function and nodule volumebetween the two groups(±s)
注:FT3,游离三碘甲状腺原氨酸;FT4,游离甲状腺素;TSH,促甲状腺激素
组别观察组(n=60)对照组(n=60)t值P值FT3(pmol/L)5.22±1.52 6.16±2.76 5.482 0.019 FT4(pmol/L)15.19±2.05 17.23±4.00 5.912 0.015 FSH(mIU/L)2.56±0.33 1.74±0.69 5.079 0.024结节体积(cm3)0.84±0.30 1.63±0.56 5.576 0.018
2.2 两组术后疼痛评分比较 术后8、24、48 h,观察组VAS评分均低于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组术后疼痛评分比较(±s,分)Table2 Comparison of postoperative pain scoresbetween the two groups(±s,scores)
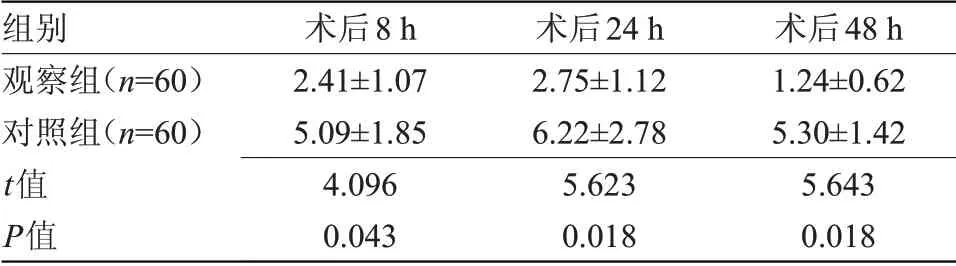
表2 两组术后疼痛评分比较(±s,分)Table2 Comparison of postoperative pain scoresbetween the two groups(±s,scores)
组别观察组(n=60)对照组(n=60)t值P值术后8 h 2.41±1.07 5.09±1.85 4.096 0.043术后24 h 2.75±1.12 6.22±2.78 5.623 0.018术后48 h 1.24±0.62 5.30±1.42 5.643 0.018
2.3 两组术后并发症发生率比较 观察组术后发生甲状旁腺损伤1例,并发症发生率为1.7%(1/60);对照组术后发生甲状旁腺损伤1例,甲状腺结节破裂2例,术后并发症发生率为5%(3/60),两组比较差异无统计学意义(χ2=1.035,P=0.309)。
3 讨论
多数结节性甲状腺肿是在单纯弥漫性甲状腺肿基础上,由于病情反复进展,上皮细胞过度增生,病情恶变进展为恶性肿瘤。甲状腺受损后,影响正常生活,破坏内环境。为避免甲状腺结节恶化,感觉受损,多实施手术切除治疗。传统开放手术切口较大,易损伤喉返神经,影响颈部美观和预后[4-6]。与腹腔镜手术效果相比,微波消融术实施后,不影响患者甲状腺功能,注射氯化钠注射液后,可形成隔离带,保护甲状腺正常功能,避免功能受阻。微波消融时剖开结节周围的血管、神经和气管等外侧组织,能避免周围二次受损,减少并发症发生。消融术使用微波针灼烧结节血管,可阻断血液供应,避免术中大出血,降低手术操作难度[7]。
超声引导下微波消融术是甲状腺外科微创新型技术,经超声引导锁定甲状腺病灶,微波消融针穿刺病灶,经物理高热辅助,使病变组织脱水、凝固至变性、坏死。通过新陈代谢,由机体自行吸收,达到清除病灶的作用[8]。微波消融术以针孔微术操作,能减轻患者创面疼痛,减少瘢痕,且不会损伤甲状腺正常组织。微波消融术可确保颈部外观美观度,保证甲状腺正常功能,改善患者预后[9]。
本研究结果显示,观察组FT3、FT4水平低于对照组,FSH水平高于对照组,结节体积小于对照组,差异均有统计学意义(P<0.05),表明超声引导下微波消融术治疗甲状腺良性结节能增强甲状腺功能,缩小结节体积。术后8、24、48 h,观察组VAS评分均低于对照组,差异有统计学意义(P<0.05)。两组并发症发生率比较差异无统计学意义,提示超声引导下微波消融术定位精准,能减小患者受伤创面面积,减轻患者疼痛感,减少并发症发生。与余庆林[10]研究结果一致。需注意的是,微波消融术操作时,需控制适宜的消融功率和时间,一旦发生过度消融,结节组织会产生严重的焦化反应,导致术后组织吸收发生障碍,吸收时间过长,影响甲状腺机体功能恢复,而消融时间不足易导致恢复期结节再次复发,需二次手术治疗。高龄患者对手术耐受能力较差,应选择适宜治疗方式,如间歇性消融治疗,分阶段完成手术,保护甲状腺组织,维持动脉血液正常供应。
综上所述,超声引导下微波消融术治疗甲状腺良性结节效果显著,可促进患者甲状腺腺体功能恢复正常状态,缓解患者疼痛感,改善预后,值得临床推广应用。

