前处理方法对测定山药中的汞和砷含量的影响
翟硕莉李志涛张秀丰
(1.衡水学院生命科学系,河北 衡水 053000;2.石家庄海关技术中心,河北 石家庄 050000)
山药为薯蓣科植物薯蓣(Dioscorea opposita Thunb.)的干燥根茎[1],因其含有丰富的多糖、氨基酸、脂肪酸、淀粉、微量元素等营养元素以及尿囊素、黄酮、甾醇类、盐酸多巴胺等功能性成分,是我国传统的药食同源的养生食材。近几年,随着人们食品安全意识的提高及对环境污染的重视,山药中重金属含量的检测受到广泛关注。汞和砷都是自然界中分布广泛的重金属元素,作为原料普遍应用于多种工业中,可能造成环境污染,进而通过各种途径进入食物链,微量的摄入在人体内具有强的蓄积性,产生远期效应或慢性疾病。无机汞主要蓄积于肾脏,造成肾脏损伤,甲基汞毒性强,能够通过血脑屏障进入大脑,造成神经损伤。无机砷的毒性大于有机砷,无机砷中三价砷毒性最大,能够阻碍细胞的呼吸和代谢。
国标以及收集的文献表明,冷原子吸收光谱法、原子荧光光谱法、电感耦合等离子体质谱法是汞和砷常用的检测方法。季澜洋[2]等以稻谷为研究对象检测汞,对比了冷原子吸收光谱法与原子荧光法,测定数据表明,二者无显著差异,冷原子的准确度、精密度和加标回收率高于原子荧光光谱法。刁春霞[3]等分析了微波消解-电感耦合等离子体质谱法测定带鱼中汞和砷等5种重金属,结果表明,实验选择的方法灵敏度高,重现性好。由于汞极其不稳定,样品的前处理必须慎重,前处理也会影响砷的检测结果,选择合适的汞和砷的前处理方法尤为重要。汞和砷常用的前处理方法有湿法消解、微波消解、干法灰化、压力罐消解法[4-7]。陈亮[8]建立了快速消解的前处理方法,石墨炉原子吸收测定大米、茶叶、奶粉中砷的检测方法。刘钰钗[9]等建立了压力罐消解法测定面粉中的汞和砷。李蓉[10]等采用微波消解同时处理香辛料,建立测定汞和砷的前处理方法。陈洪浪[11]等汇总了2019年之前关于山药中重金属污染的相关文献,对其进行了分析表明,按照GB2762-2017[12]标准比较,山药中的汞和砷均已超标,因此建立健全山药中汞和砷的前处理方法和测定方法很有必要。本文采用检测技术成熟的原子荧光法检测山药中汞和砷,选择实验室常用的湿法消解和微波消解,研究不同前处理方法对检测结果的影响。比较2种前处理方法对测定结果的影响,以期获得较高准确度和精确度的汞和砷测定方法。
1 材料与方法
1.1 材料
小白嘴山药(购于菜市场)。
1.2 仪器与试剂
SH220F石墨炉消解仪、AFS3100原子荧光光度计、EHD-24控温赶酸器、微波消解仪、汞空心阴极灯、砷空心阴极灯。
汞标准储备液(1000mg·L-1,国家有色金属及电子材料分析测试中心)、砷标准储备液(1000mg·L-1,国家有色金属及电子材料分析测试中心)、硝酸、高氯酸、硫酸、过氧化氢、重铬酸钾、硼氢化钾、氢氧化钾、硫脲、抗坏血酸。
硫脲加抗坏血酸的混合溶液配制:10g硫脲,加80mL水,加热溶解,冷却后,加入10g抗坏血酸,定容至100mL,现用现配。
1.3 实验方法
1.3.1 标准溶液的配制
1.3.1.1 50μg·L-1汞标准溶液
0.5g·L-1重铬酸钾的硝酸溶液稀释汞标准储备液(1000mg·L-1),现用现配。
1.3.1.2 1mg·L-1砷标准溶液硝酸溶液(2+98)稀释砷标准储备液(1000mg·L-1),现用现配。
1.3.2 样品处理
将山药清洗、去皮、烘干、研磨,过60目筛,备用。
1.3.3 湿法消解
参考GB5009.11-2014[2]和GB5009.17-2014[3]。选择不同的混酸和消解温度取2g山药粉,加入一定体积的混酸,混酸分别选择硝酸、硝酸加高氯酸、硝酸加过氧化氢、硝酸加高氯酸加+硫酸,放置过夜,第2天于石墨炉消解仪消解,若消解至1mL时仍有未分解物或者颜色较深,冷却后补加硝酸直至消解完全,降低温度至100℃赶酸至白烟散完,备用。同时做试剂空白实验。
汞测定前,将上述消解液转入25mL容量瓶中,用水洗涤消解管3次,合并洗涤液,定容,待测;砷测定前,将上述消解液转入25mL容量瓶中,用水洗涤消解管3次,合并洗涤液,加入硫脲加抗坏血酸溶液2mL,定容,放置30min,待测。
1.3.4 微波消解
取0.5g山药粉于微波消解管中,加入一定量的硝酸和过氧化氢,按照微波消解的步骤消解山药粉,消解完成后80℃加热至棕色气体消失,冷却后将消解液加入25mL容量瓶中,用水洗涤消解管3次,合并洗涤液,备用。同时做试剂空白实验。
汞测定前,将上述消解液用水定容至25mL,待测;砷测定前,将上述消解液加入硫脲加抗坏血酸溶液2mL,定容,放置30min,待测。
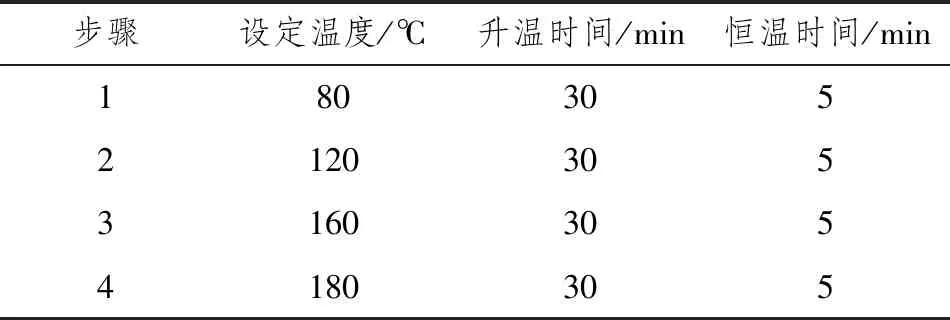
表1 微波消解升温程序
1.3.5 原子荧光光度计的工作条件[2,3]
1.3.5.1 汞测定仪器条件
负高压:240V;汞空心阴极灯电流:30mA;载气:氩气;载气流速:500mL·min-1;屏蔽气流速:800mL·L-1;测量方法:荧光强度;读数方式:峰面积。试样进入原子荧光光谱仪,以5%盐酸为载流,5g·L-1硼氢化钾和氢氧化钾还原汞成原子态,由载气带入原子化仪中,氩气火焰将其形成基态原子,在汞阴极灯发射光的激发下产生原子荧光。
1.3.5.2 砷测定仪器条件
负高压:260V;砷空心阴极灯电流:50mA;载气:氩气;载气流速:50mL·min-1;屏蔽气流速:800mL·L-1;测量方法:荧光强度;读数方式:峰面积。试样进入原子荧光光谱仪,以盐酸为载流,10g·L-1硼氢化钾和氢氧化钾生成砷化氢气体,由载气带入原子化仪中,氩气火焰将其形成基态原子,在砷阴极灯发射光的激发下产生原子荧光,测得原子荧光强度。
2 结果与分析
2.1 标准曲线的绘制
用5%硝酸溶液将50μg·L-1汞标准溶液和1mg·L-1砷标准溶液进行稀释,配制汞和砷混标溶液,混标溶液中汞为0μg·L-1、0.2μg·L-1、0.5μg·L-1、1.0μg·L-1、1.5μg·L-1、2.0μg·L-1、2.5μg·L-1系列浓度,砷为0μg·L-1、5.0μg·L-1、10μg·L-1、20μg·L-1、30μg·L-1系列浓度。在1.3.5原子荧光光度计的工作条件下进行测得,根据测得荧光值绘制标准曲线,其对应的回归方程如下。汞:y=779.3x-3.3778,砷:y=171.92x-45.6。R值分别为0.9990和0.9992。说明汞在0~2.5μg·L-1范围内有较好的线性关系,砷在原子荧光光度计的工作条件0~30μg·L-1范围内有较好的线性关系。
2.2 湿法消解最高消解温度考察
根据1.3.3的实验步骤,对山药样品进行消解,消解体系选择GB 5009.11-2014规定的混酸体系,即20mL硝酸加4mL高氯酸加1.25mL硫酸,最高消解温度选择100℃、150℃、200℃、350℃、300℃。在该条件下消解山药样品,测得汞和砷含量如图1、图2所示。
由图1、图2可知,最高消解温度为150℃时,汞含量最大,消解温度超过150℃后,随着温度的升高,测得汞含量降低,可能是因为湿法消解过程属于半封闭,温度越高汞溢出量增加,因此汞消解的最高温度选择150℃。而砷含量随最高消解温度的升高一直在增加,200℃以上时,砷含量的增幅速度减慢,这是因为实验中选择的消解体系为硝酸、高氯酸和硫酸的混酸体系,硝酸沸点为121℃,高氯酸沸点为203℃,硫酸沸点为338℃,高氯酸和硫酸的存在可能影响元素的测定[13],因此砷测定的前处理消解温度应为350℃。所以山药样品选择湿法消解时,汞和砷不能同时消解。
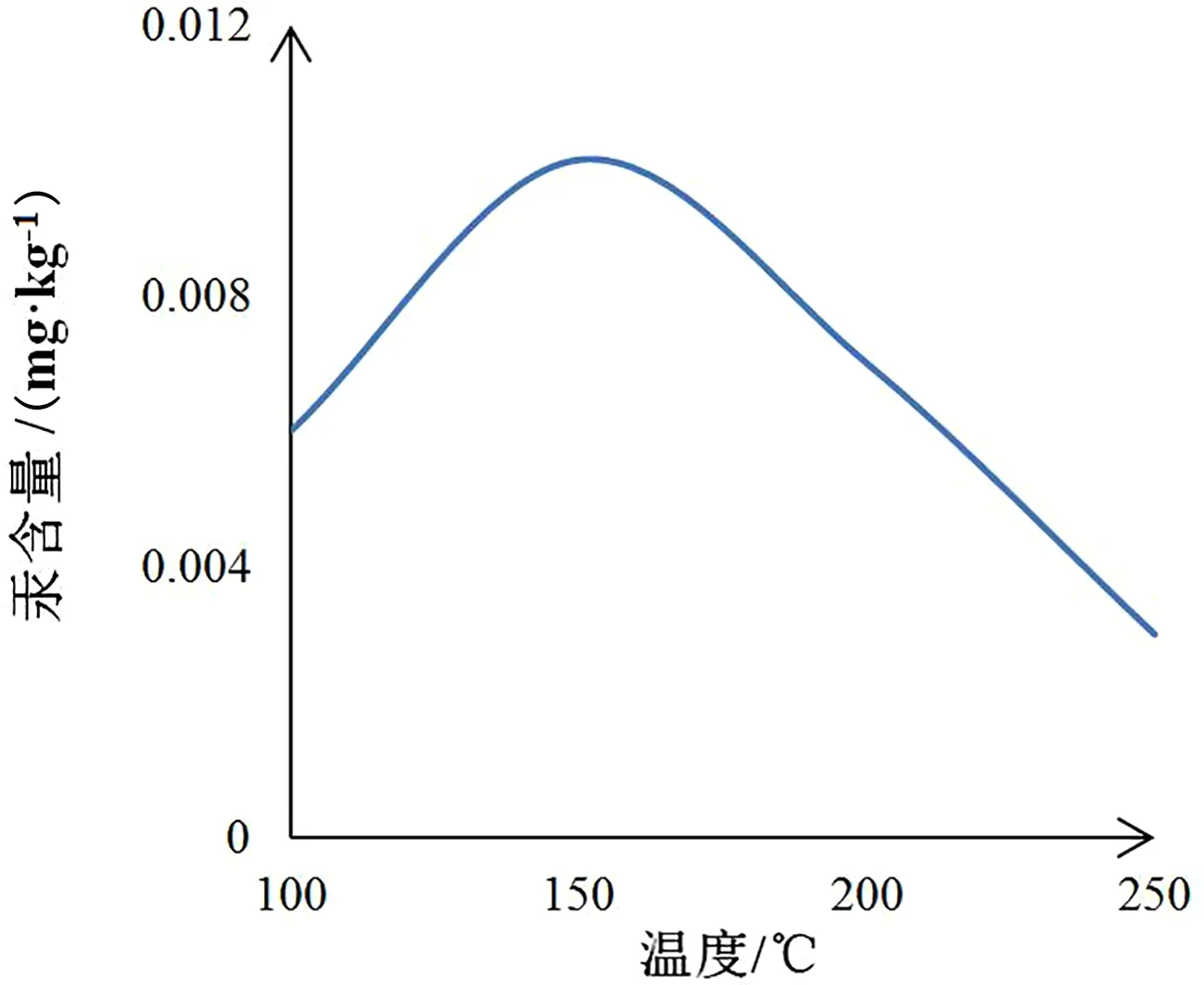
图1 湿法消解温度与汞含量关系图
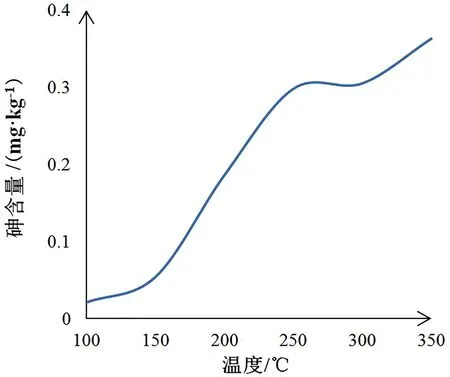
图2 湿法消解温度与砷含量关系图
2.3 微波消解最高消解温度考察
根据1.3.4的微波消解程序,山药样品中加入5mL硝酸进行消解,最高消解温度设计范围在160~200℃,其它升温条件仍按表1设置。在该条件下消解山药样品,测得汞和砷含量如图3、图4所示。
由图3、图4可以看出,随着微波消解最高温度的增加,汞和砷的含量在增加,汞含量在190℃时最高,砷含量在180℃时最高,但通过图3、图4可知,在180℃以上,汞和砷的测定值波动不大,因此实验中可选择180℃或190℃作为微波消解的最高温度。
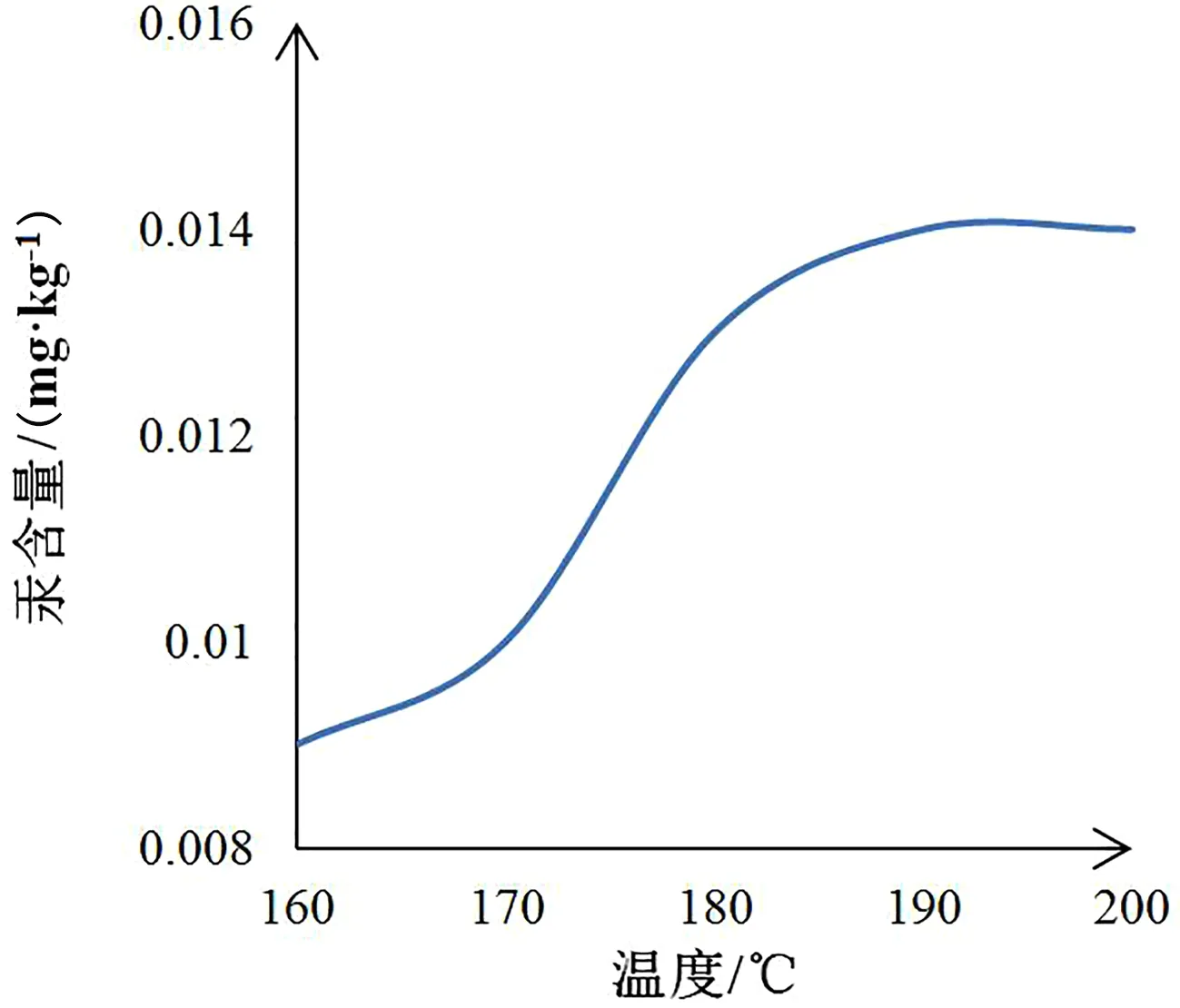
图3 微波消解温度与汞含量关系图
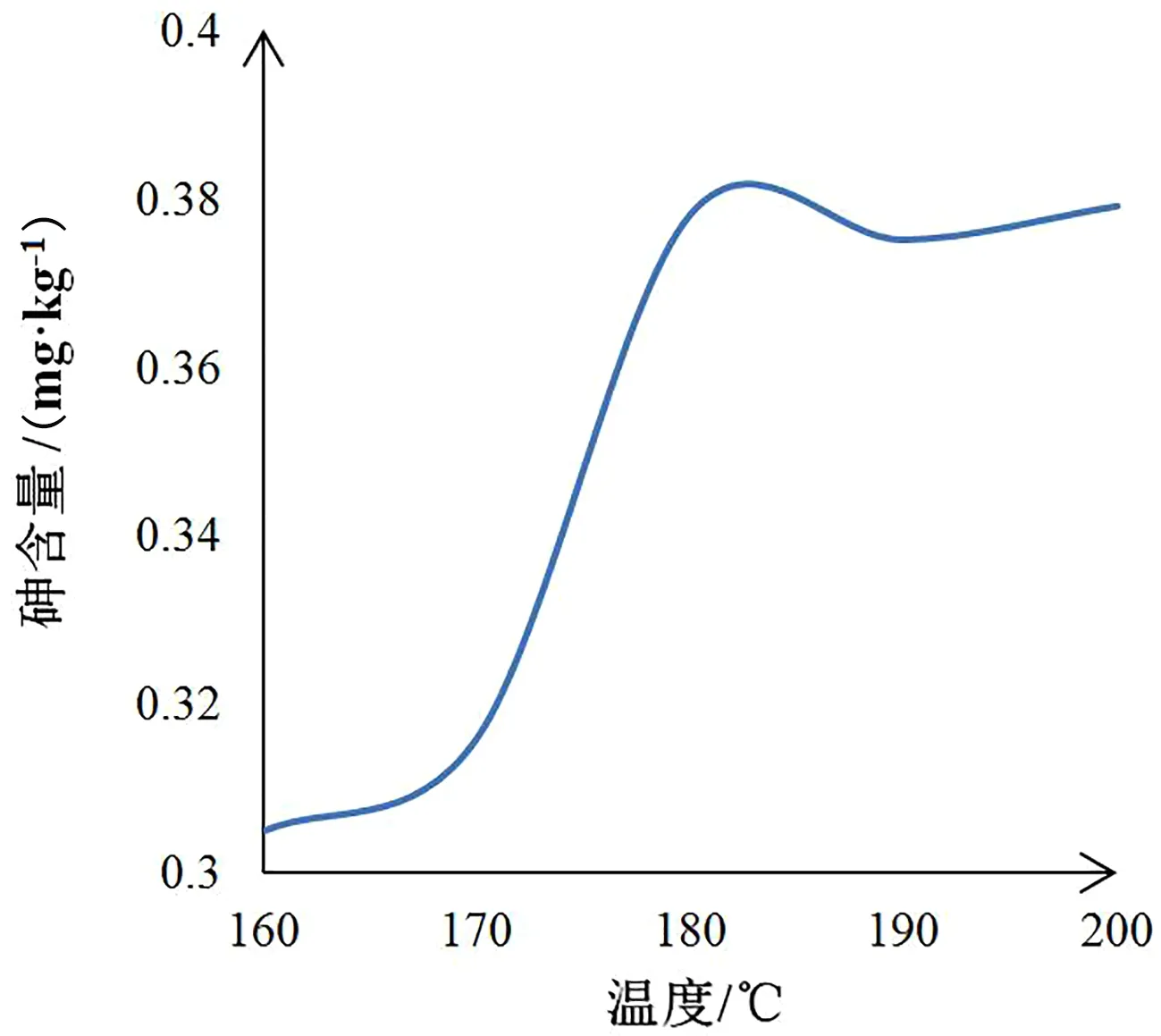
图4 微波消解温度与砷含量关系图
2.4 不同混酸体系对汞和砷含量的影响
根据2.2的实验结果,测汞的山药样品湿法消解选择150℃,测砷的山药样品湿法消解选择350℃。微波消解温度选择180℃。由表2实验结果可以看出,湿法消解测定的汞含量最高为0.010mg·kg-1,砷含量为0.363mg·kg-1,微波消解测定的湿法消解时汞含量最高为0.016mg·kg-1,砷含量为0.381mg·kg-1,可见微波消解前处理方法优于湿法消解。湿法消解处理时,混酸选择10mL硝酸加2mL高氯酸,汞含量最高;砷含量最高的混酸体系为10mL硝酸加2mL高氯酸加0.5mL硫酸。微波消解时,硝酸加过氧化氢体系测定的汞值略高,不同消解体系测定的砷含量相差不大。
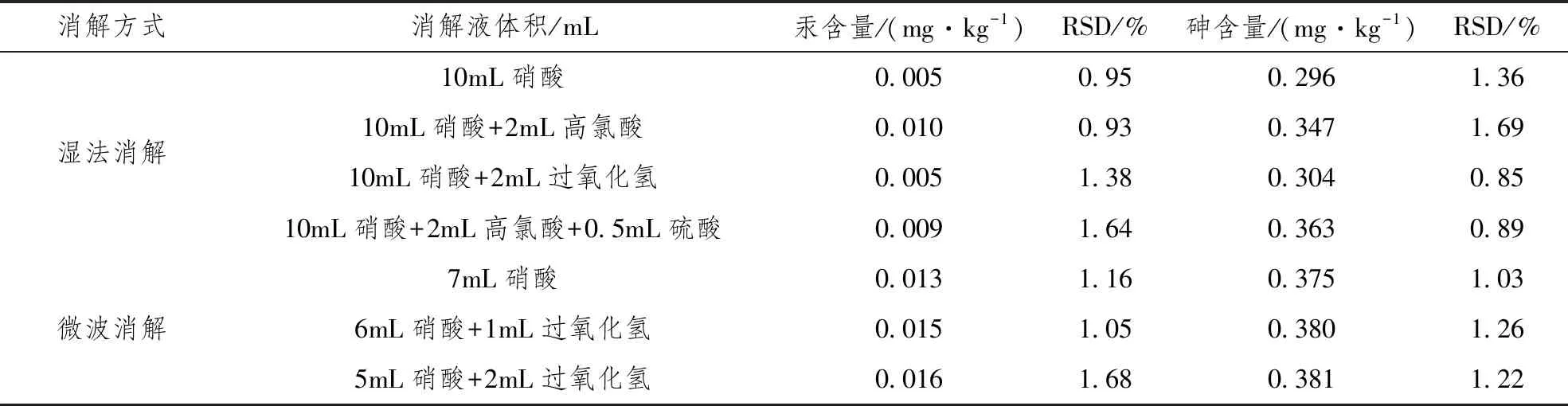
表2 不同前处理方法的汞和砷测定结果
2.5 回收率实验
将山药粉采用微波消解的方法进行前处理,消解液选择6mL硝酸加1mL过氧化氢,分别加入一定量汞、砷标准溶液进行加标回收实验,结果见表3。
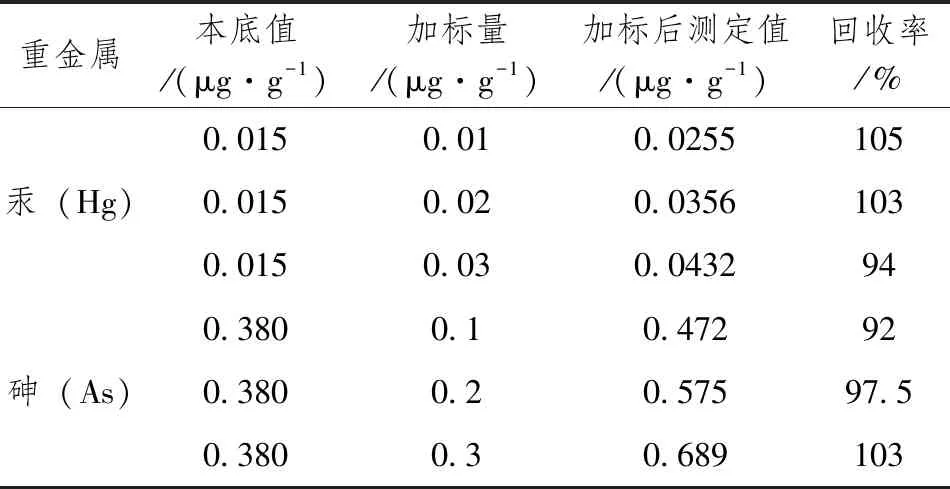
表3 汞和砷的加标回收结果
由实验结果可知,采用5mL硝酸加2mL过氧化氢进行微波消解处理,测得的汞加标回收率在94%~105%,砷加标回收率在92%~103%,说明此前处理方法可获得较好的加标回收率。
2.6 精密度实验
取汞标准溶液1.0μg·L-1,砷标准溶液10.0μg·L-1,原子荧光光谱法连续测6次,根据数值计算RSD值分别为1.05%和0.83%,表明选择的原子荧光光谱法的工作条件适用于山药中汞和砷的测定,精密度好。
根据2.4的实验结果,将山药样品在6mL硝酸加1mL过氧化氢消解体系下微波消解,连续测定6次,汞和砷的其RSD值分别为0.96%和0.72%。分别取6份山药样品在6mL硝酸加1mL过氧化氢消解体系下进行微波消解,汞和砷的其RSD值分别为1.63%和1.28%。表明在5mL硝酸加2mL过氧化氢消解体系下进行微波消解重复性好。
将山药样品在6mL硝酸加1mL过氧化氢消解体系下微波消解,原子荧光光谱法测定,消解液放置24h后,再次测定,结果显示2次所测数据相差无几,说明此消解条件下测得汞和砷的稳定性好。
3 结论
食品中汞和砷检测的前处理方法很多,通过实验可以看出,湿法消解和微波消解分别处理后,汞和砷的检测值有差别,微波消解处理检测值略高于湿法消解。分别对2种前处理方法的最高消解温度进行实验,湿法消解条件下,汞需要在较低温度下消解,而砷则需要较高的温度,因此不能同时对样品进行前处理。微波消解温度相差不大,可以同时处理样品,精密度、准确度、重复性较好,能够满足测定要求。且微波消解过程为密闭空间,危险系数低。本实验结果表明,微波消解是处理山药样品的可靠方法。

