机械取栓治疗急性前循环大血管闭塞性脑梗死患者预后的影响因素
吴建明 马斌武 吴艳蓉 杨 平 谭波飞 邵 娜
宁夏医科大学总医院,宁夏 银川 750000
急性缺血性卒中(acute ischemic stroke,AIS)占脑卒中类型的70%左右[1]。对于超早期AIS 的患者治疗极为关键,超早期治疗的主要方法为静脉溶栓和机械取栓(mechanical thrombectomy,MT)。静脉溶栓对于穿支动脉或远端血管再通率较高[2],然而对于大血管闭塞(large vessel occlusion,LVO)患者的效果较差,并发症较高[3-5]。2015 年五大MT 对于前循环AIS-LVO 的研究取得明显的临床疗效,极大改善了患者预后[6-10],目前已成为《急性缺血性卒中血管内治疗中国指南2018》最高级别推荐[11],然而部分接受MT治疗的患者仍然存在预后不良。NEUBERGER等[12]在MT 研究中的结果显示术后预后不良率为46.6%,一项来自随机对照试验的荟萃分析结果显示MT 不良预后率高达54%[13],寻找AIS-LVO患者MT术后预后不良的危险因素至关重要。本研究通过分析宁夏医科大学总医院因急性前循环AIS-LVO 而行MT 治疗患者的临床资料,探讨影响预后的因素,尽早进行临床干预。
1 对象与方法
1.1 研究对象回顾性纳入2019-07—2022-02 宁夏医科大学总医院收治的急性前循环大血管闭塞性脑梗死患者102 例,所有患者进行了机械取栓治疗。纳入标准:(1)符合《中国急性缺血性脑卒中诊治指南2018》[14]中AIS的诊断标准;(2)依据《急性缺血性卒中血管内治疗中国指南2018》[11]确诊伴急性前循环LVO 导致的AIS 患者;(3)发病至入院时间≤6 h;(4)年龄≥18 岁;(5)发病前患者改良Rankin 量表(modified Rankin scale,mRS)评分≤2 分;(6)家属签署知情同意书;排除标准:(1)术前头颅CT显示合并颅内出血;(2)发病至入院时间>6 h;(3)年龄<18岁;(4)有活动性出血或凝血功能障碍;(5)对造影剂及肝素过敏;(6)合并严重的心、肺、肝、肾等疾病;(7)临床资料不完整。
1.2 一般资料收集患者的一般资料,包括年龄、性别、原发性高血压、冠心病、糖尿病病史、吸烟、入院时美国国立卫生研究院卒中量表(National Institutes of Health stroke scale,NIHSS)评分、术前Alberta卒中项目早期CT 评分(Alberta score program early CT score,ASPECTS)、术前随机血糖水平、是否桥接治疗、发病至血管再通时间、取栓的部位和次数、侧支血管代偿情况、术中是否使用替罗非班、术后是否血流完全再通、术后是否并发颅内出血及随访情况。
1.3 手术过程对于符合静脉溶栓适应证且排除禁忌证的患者,先进行静脉溶栓再进行桥接MT 治疗。患者仰卧位,采用Seldinger 技术穿刺成功后置8F 动脉鞘,快速行全脑血管造影检查以明确病变血管及侧支代偿情况。采用同轴技术将6F Navien 导管放置在病变近心端,再将微导丝和微导管置于病变远端,造影证实远端为血管真腔,后撤出微导丝,将Solitaire AB 取栓支架置于闭塞段,回撤导管打开支架,5 min 后将6F Navien 导管、取栓支架、微导管一起取出,取栓的同时助手利用50 mL注射器连接“Y”形阀抽吸6F Navien 导管防止血栓脱落。术中若发现病变血管合并重度动脉粥样硬化型狭窄,则选择球囊扩张术及支架成形术。
1.4 评定标准根据改良脑梗死溶栓分级(modified thrombolysis in cerebral infarction,mTICI)标准[15],将mTICI 3 级作为血流完全再通的标准[16]。发病至血管再通时间定义为出现症状或末次正常时间至首次取栓后血流通畅的时间。根据美国放射介入学会评估侧支循环系统,3~4分为侧支循环良好,0~2 为级侧支循环差[17]。通过电话或门诊进行随访,第90天采用mRS评估患者术后预后情况。预后良好为mRS评分≤2分,预后不良为mRS评分>2分。
1.5 统计学分析应用SPSS 22.0 统计软件进行数据分析,符合正态分布的计量资料以均数±标准差(±s)表示,组间比较采用独立样本t 检验。非正态分布的计量资料以中位数和四分位间距[M(P25,P75)]表示,组间比较采用非参数秩和检验。计数资料以频数(%)表示,2组间比较采用χ2检验。对于单因素分析差异有统计学意义的参数行Logistic 回归分析,绘制ROC 曲线,计算曲线下面积,评价影响因素的效能,P<0.05表示差异有统计学意义。
2 结果
2.1 2 组患者临床资料比较2 组患者在年龄、性别、高血压史、冠心病史、吸烟史、术前血糖、术前是否溶栓、基线NIHSS 评分、取栓部位、术中是否使用替罗非班、症状至血管再通时间、术后血流完全再通等方面差异无统计学意义(P>0.05),而2组患者在糖尿病史、术前ASPECTS 评分、侧支循环代偿、取栓次数、术后是否并发脑出血方面差异有统计学意义(P<0.05)。见表1。
2.2 多因素Logistic 回归分析结果将表1 中有统计学差异的变量进行Logistic回归分析,结果显示侧支循代偿差和术后并发脑出血是机械取栓术后不良预后的独立危险因素(P<0.05)。见表2、图1。

表1 2组患者临床资料比较Table 1 Comparison of clinical data of the two groups
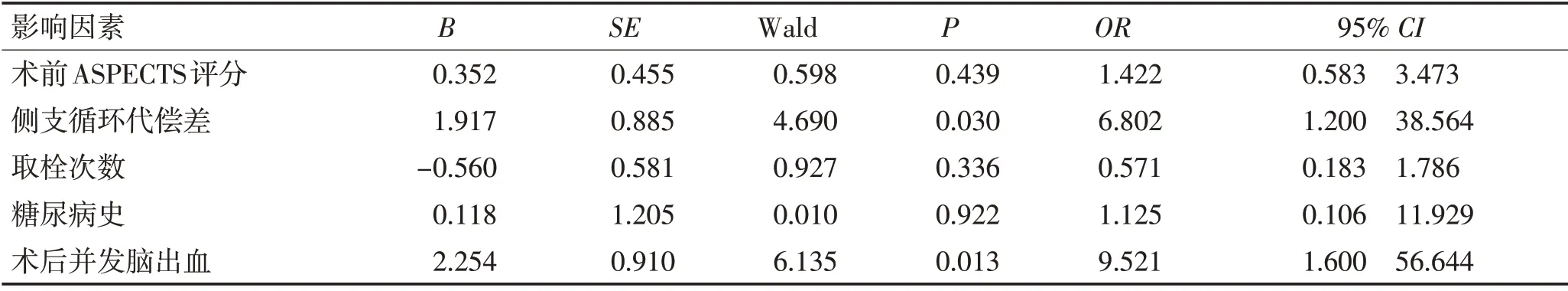
表2 多因素Logistic回归分析Table 2 Multivariate Logistic regression analysis
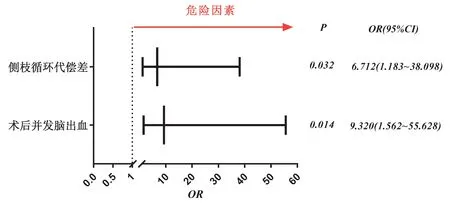
图1 多因素Logistic回归分析示意图Figure 1 Schematic diagram of multivariate Logistic regression analysis
2.3 各因素对预后的预测价值各因素AUC值比较显示侧支循环代偿(AUC=0.784,灵敏度68.0%,特异度88.9%,P<0.01)、术后是否并发脑出血(AUC=0.804,灵敏度72.0%,特异度88.9%,P<0.01)的预测价值良好。见表3、图2。
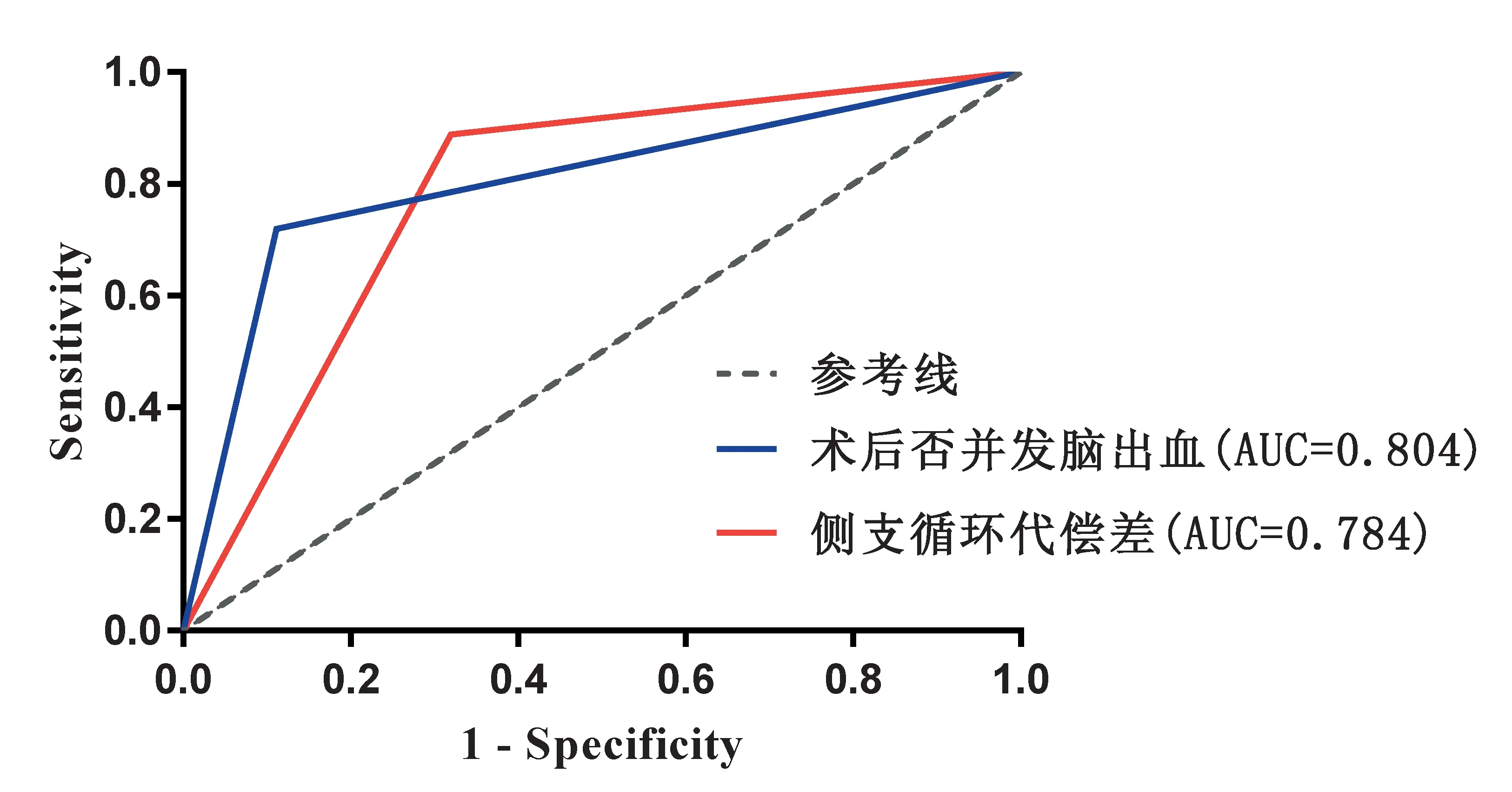
图2 各因素指标对预测预后不良的工作特征曲线Figure 2 The working characteristic curve of each factor index for predicting poor prognosis

表3 各因素对预后不良的预测价值Table 3 Predictive value of each factor for poor prognosis
3 讨论
AIS是导致死亡和永久性残疾的最常见病因[18],对于发病在6 h 内伴LVO 的AIS 患者,MT 已成为此类患者的标准治疗方法[19]。尽管MT可从根本上开通闭塞的血管,恢复脑组织的血运,但一些患者仍未能获得良好的临床结局。既往研究报道中MT术后的良好预后率为45%~54.5%[20-22]。本研究中MT治疗AIS-LVO的良好预后率为51.9%,与既往文献报道相符。积极寻找影响MT 术后预后不良的因素尤为重要。血流未完全再通、低ASPECTS 评分及高NIHSS 评分是目前已知MT 术后预后不良的独立危险因素[13,22]。本研究发现侧支循环差和术后并发脑出血也是MT 术后预后不良的独立危险因素。
侧支循环是指脑内已存在或新生的血管旁路系统,当脑内某一血管发生病变导致相应脑组织血流量降低时,脑血流可以通过侧支循环到达缺血的脑组织,良好的侧支循环可以改善缺血半暗带的血供。良好的侧支循环意味着大范围的缺血半暗带及良好的临床预后结果[23]。本研究显示侧支循环差是MT 术后预后不良的独立危险因素(OR=0.784,95%CI 0.653~0.916,P<0.01),且具有良好的预测价值。SALLUSTIO 等[24]对135 例行MT 治疗的急性前循环AIS患者进行回顾性分析,发现侧支良好的患者有更好的临床结局。RENÚ等[25]研究表明侧支循环不良是AIS-LVO患者梗死体积扩大和预后不良的有效预测因素,可能的机制是良好的侧支循环可以延长缺血半暗带转化为梗死所需的时间,减少核心梗死面积,从而改善预后。良好的侧支循环可以改善MT术后患者的临床预后,减少手术并发症。
脑出血是MT 术后致命的并发症,也是MT 术后预后不良的独立危险因素。MT 术后并发脑出血的发生率为4.4%~16%[13,26-27]。回顾性研究通过分析得出16.8%的患者在MT术后发生脑出血,且出血组的良好预后率低于未出血组[28-30],说明脑出血是MT 术后预后不良的危险因素。本研究表明术后并发脑出血是机械取栓术后的独立危险因素(OR=0.804,95% CI 0.678~0.931,P<0.01),同样具有一定的预测价值,可能的病理机制是血-脑屏障破坏、大脑自我调节能力下降导致血管破裂出血。在一项对1 122例发病8 h 内接受MT 治疗的AIS-LVO 患者进行的多中心研究中,脑出血与不良预后和更高的病死率有显著相关性[31-33],因此MT术后预防脑出血的发生尤为重要。侧支循环差、术后并发脑出血是AIS-LVO 患者MT预后不良的危险因素,应警惕并尽早予以相应的干预。

