白蛋白结合型紫杉醇联合奈达铂化疗对复发转移性宫颈癌的效果及血清CYFRA21-1、VEGF-C水平的影响
陆小玲,林华明,黄毅超,刘云军,黎昌国,黄逸生,麦大海(茂名市人民医院肿瘤科,广东茂名 525000)
宫颈癌是临床最为常见的妇科恶性肿瘤,高发年龄为35~55 岁,近年有年轻化趋势。早期患者的局部肿瘤病灶小,治疗后预后较好,5 年内生存率可达90%,而中晚期宫颈癌患者预后较差[1]。目前临床针对晚期、复发性癌症宫颈癌首选及使用最多的治疗方案为紫杉醇联合铂类药物。常用的铂类如卡铂、奈达铂等,属于第二代化疗药物,其水溶性较大,相对副作用小[2-3],因此临床接受度较高。白蛋白紫杉醇是近年新增的紫衫类化疗药物,研究显示其可提升复发、转移性中晚期癌症患者的治疗效率,较溶剂型紫杉醇更具优势[4-5]。本研究对比了白蛋白结合型紫杉醇联合奈达铂与溶剂型紫杉醇联合奈达铂治疗复发转移性宫颈癌的效果,及其对血清细胞角蛋白19 片段抗原21-1(CYFRA21-1)和血管内皮生长因子C(VEGF-C)的影响,以期为宫颈癌患者治疗方式的选择提供参考。
1 资料和方法
1.1 一般资料
选取2017年1月-2021年1月我院收治的复发转移性宫颈癌患者70 例,按入组时间分为对照组(2017年1 月-2019 年1 月)和研究组(2019 年2 月-2021 年1月),每组35 例。对照组年龄35~69 岁,平均(46.8±4.0)岁;病理类型:鳞癌26 例,腺癌9 例;复发转移部位:盆腔或腹膜后淋巴结15 例,盆腔及远处转移10例,肺部7 例,多部位远处转移3 例。研究组年龄35~71 岁,平均(47.1±3.3)岁;病理类型:鳞癌25 例,腺癌10 例;复发转移部位:盆腔或腹膜后淋巴结13 例,盆腔及远处转移11 例,肺部9 例,多部位远处转移2 例。两组患者一般资料比较差异无统计学意义(P>0.05)。纳入标准:(1)经宫颈组织病理检查、影像学检查等确诊为宫颈癌,符合相关诊断标准[6],且经影像学、妇检等提示出现转移;(2)存在可测量或评估的肿瘤灶;(3)患者及家属知情同意;(4)ECOG评分≤2分;(5)无颅内转移或神经压迫症状的椎体转移;(6)白细胞计数≥4×109/L,中性粒细胞计数≥2×109/L,血红蛋白≥100 g/L,血小板计数≥100×109/L。排除标准:(1)1个月之内使用过影响本研究的药物;(2)认知障碍或精神疾病;(3)对本研究所用药物过敏或不良反应严重者;(4)研究中途退出或失访者。
1.2 方法
两组患者均接受常规化疗前检查及胃黏膜保护治疗,给予地塞米松20 mg、西咪替丁400 mg/m2静脉推注,以及苯海拉明40 mg 肌肉注射,以预防过敏反应,若未发生过敏反应,后续化疗则无需再进行。化疗过程中密切关注患者血压、心率、呼吸,药物注射完后,给予托烷司琼5 mg 静脉推注,预防恶心、呕吐。对照组患者接受溶剂型紫杉醇(江苏奥赛康药业有限公司;规格:10 L,60 g;国药准字H20083848)联合奈达铂化疗(大连金泉宝山生物工程制药有限公司;规格:50 mg;国药准字H20051481):紫杉醇135 mg/m2混合5%葡萄糖稀释成0.3~1.2 g/L溶液,静脉滴注3 h;奈达铂80 mg/m2,采用生理盐水溶解稀释至500 mL,静脉滴注,时间≥1 h,滴完后继续滴注生理盐水1 000 mL以上。研究组患者接受白蛋白结合型紫杉醇(石药集团中诺药业有限公司;规格:100 mg;国药准字H20183044)联合奈达铂化疗:150 mg/m2白蛋白结合型紫杉醇混合100 mL 0.9%氯化钠注射液,缓慢静脉滴注,30 min滴完,奈达铂用量及方法同对照组。3周为1个疗程,每个疗程用药1次。
1.3 观察指标
比较两组患者治疗2 个疗程后的临床疗效、治疗前后血清CYFRA21-1 和VEGF-C 水平,以及治疗期间的不良反应发生情况,具体如下:(1)疗效,参考WHO 实体肿瘤近期疗效的分级标准,并结合患者检查结果进行评估。完全缓解(CR):患者病灶完全消失;部分缓解(PR):患者肿瘤病灶体积缩小≥50%;病情稳定(SD):患者肿瘤病灶体积缩小<50%;病情进展(PD):患者肿瘤病灶增大>25%,或出现新的病灶。缓解率=(CR+PR)/样本量×100%。(2)血清CYFRA21-1和VEGF-C 水平:取患者清晨空腹静脉血4 mL,置于惰性分离胶促凝管中,离心(3 000 r/min,10 min)后,取上层清液,仪器及试剂盒为美国Bio-RAD 公司,Bio-RAD550 型酶标仪及其配套试剂盒,采用酶联免疫吸附法测定患者血清VEGF 水平;采用全自动化学发光免疫分析仪与配套试剂盒(美国雅培公司,AXSYM),化学发光免疫法测定血清CYFRA21-1 水平。(3)不良反应:记录两组患者治疗期间疲倦、呕吐、腹泻等消化道反应,以及白细胞计数下降、血小板计数下降、骨髓抑制、过敏反应等不良反应发生情况。
1.4 统计学处理
采用统计学软件SPSS19.0 进行数据分析。计量资料以表示,采用独立样本t检验;计数资料以百分率(%)表示,采用χ2检验;有序分类资料采用秩和检验。P<0.05表示差异有统计学意义。
2 结果
2.1 疗效
研究组总缓解率为71.4%,高于对照组的45.7%,两组疗效比较差异有统计学意义(P<0.05),见表1。
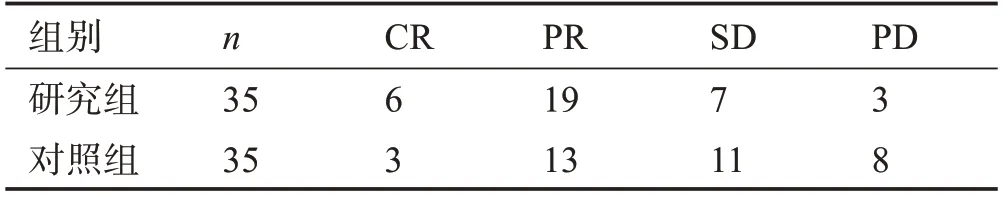
表1 两组患者疗效的比较 (例)
2.2 血清CYFRA21-1和VEGF-C水平
治疗前,两组患者血清CYFRA21-1 和VEGF-C水平比较差异无统计学意义(P>0.05)。治疗后,研究组患者的血清CYFRA21-1 和VEGF-C 水平均低于对照组(P<0.01)。见表2。
表2 两组患者治疗前后血清CYFRA21-1和VEGF-C水平的比较 (,n=35)
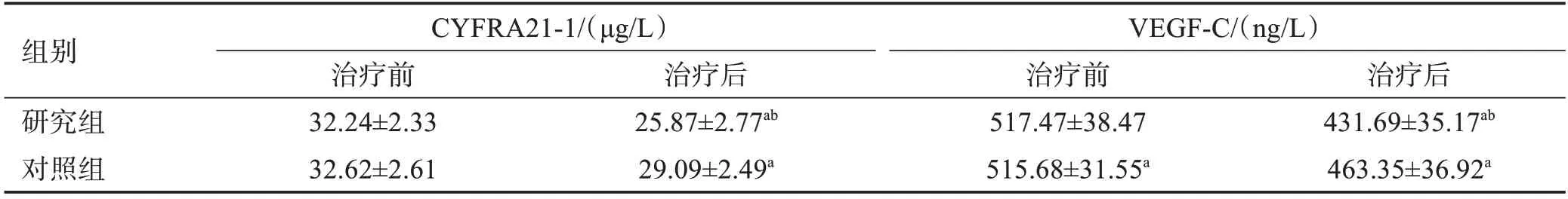
表2 两组患者治疗前后血清CYFRA21-1和VEGF-C水平的比较 (,n=35)
与同组治疗前比较:aP<0.01;与对照组治疗后比较:bP<0.01
2.3 治疗期间不良反应发生情况
研究组患者不良反应发生率显著低于对照组(P<0.05),见表3。
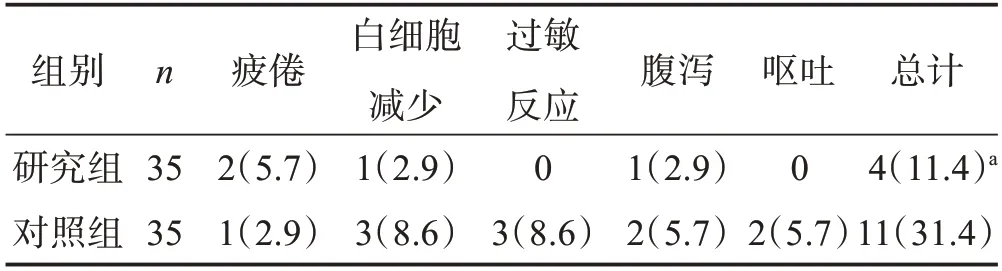
表3 两组患者治疗期间不良反应发生情况的比较 例(%)
3 讨论
众多研究显示,肿瘤标志物与病灶的大小、转移及浸润情况密切相关,部分肿瘤标志物还可作为判断癌症患者预后情况的参考及治疗效果的评价指标[7]。CYFRA21-1 能对细胞角蛋白19 片段进行定量检测,敏感反映机体细胞的分化和肿瘤发生,常作为肺鳞癌患者前瞻性的肿瘤标记物[8-10]。近年有学者发现,其在宫颈癌疾病诊断、预后预测等应用中也具有较为重要的作用[11]。肿瘤组织中新生血管的形成对肿瘤病灶的发生、发展尤为重要。VEGF 是目前研究发现的重要血管生成因子,其水平与肿瘤的生长、转移、侵袭及复发密切相关,是临床常用的肿瘤转移、代谢标志物[12-13]。本研究通过检测两组患者血清CYFRA21-1和VEGF-C 水平,以探讨两种化疗方式对复发转移性宫颈癌的应用价值。
本研究对复发转移性宫颈癌患者不同化疗方式进行比较,结果显示,采用白蛋白结合型紫杉醇联合奈达铂化疗的研究组患者治疗2 个疗程后的效果明显优于对照组。白蛋白结合型紫杉醇对复发转移性宫颈癌患者血清CYFRA21-1 和VEGF-C 水平改善效果优于溶剂型紫杉醇。其原因可能在于白蛋白结合型紫杉醇中的白蛋白通过与患者机体血管内皮细胞膜表面的gp60 特异性结合,运载的紫杉醇可高效率转运至肿瘤细胞内,快速提高药物浓度,发挥抗肿瘤效果;而溶剂型紫杉醇对肿瘤部位靶向性较弱,药物转运率较低、利用率较小,因此其临床疗效及其对血清CYFRA21-1 和VEGF-C 水平的改善作用低于白蛋白结合型紫杉醇[14-15]。既往研究显示,白蛋白结合型紫杉醇在卵巢癌[16]、乳腺癌[17]中疗效均优于溶剂型紫杉醇,本研究结果与其相似,提示临床对复发转移性宫颈癌采用白蛋白结合型紫杉醇联合奈达铂不失为优质的治疗方式,而血清CYFRA21-1 和VEGF-C 水平的监测亦可作为患者疗效判定的标准。本研究中,研究组不良反应发生率明显低于对照组,表示白蛋白结合型紫杉醇较溶剂型紫杉醇联合奈达铂的安全性更高,可能是因为紫杉醇水溶性较低,溶剂型紫杉醇常以聚乙烯蓖麻油、无水乙醇等作为助溶剂,易导致过敏反应、神经毒性等副作用;而白蛋白为疏水性物质的内源性载体,无需助溶剂就能较好的结合血管内皮细胞膜表面的受体发挥作用,从而大幅度降低了患者不良反应的发生[18]。
综上所述,白蛋白结合型紫杉醇联合奈达铂治疗复发转移性宫颈癌患者疗效确切,能够降低患者血清CYFRA21-1 和VEGF-C 水平,安全性较高,值得临床推广应用。

