石榴皮安石榴苷纯化工艺及稳定性研究
牛若惠,常占瑛,热娜·吉恩斯,高晓黎,2*(.新疆医科大学药学院,乌鲁木齐 8300;2.新疆天然药物活性组分与释药技术重点实验室,乌鲁木齐 8300)
石榴(Punica granatum
L.)是石榴科石榴属植物。石榴皮为石榴的干燥果皮。研究发现,石榴皮中富含多酚类、生物碱类、黄酮类、氨基酸和有机酸等化学物质,具有涩肠止泻、止血、驱虫等功效。石榴皮具有安全可靠、多功能、天然等优点。石榴皮多酚有很强的抗氧化活性,可用于预防和治疗多种疾病如炎症、糖尿病和心脑血管疾病等。安石榴苷(punicalagin)为石榴皮多酚的主要成分,其含量在10%左右。因其结构中含有较多羟基,也具有很强的抗氧化活性。研究表明,安石榴苷还对癌症、炎症、病毒、糖尿病等有一定的治疗效果,其可以抑制脂肪酸合成酶的活性,因此对肥胖也有一定的防治作用。此外,其还在多种慢性疾病如心血管疾病和肝脏疾病中发挥着积极的作用。目前,安石榴苷的纯化方法有柱色谱分离,如大孔吸附树脂、凝胶LH-20 色谱、MCI-gel CHP-20P、高速逆流色谱法、制备型高效液相色谱法等。膜分离技术是一种全新的高效分离、浓缩、提纯的技术,其具有效率高、运行稳定及成本低等特性,近年来在中药制药领域得到了广泛的应用。本试验拟在课题组已获得安石榴苷纯化技术专利的基础上,优化洗脱条件,并使用膜分离技术进行浓缩,进一步优化安石榴苷的纯化工艺,建立简便、高效的纯化方法,以提高安石榴苷的转移率及纯度。并对制备得到的安石榴苷精制物进行稳定性考察,为其存储提供理论依据。1 材料
1.1 试药
安石榴苷粗品(试验室自制,经HPLC 测定含量为45%);安石榴苷对照品(纯度大于98.82%,批号:MUST-20050502)、鞣花酸对照品(纯度大于 99.65%,批号:MUST-17052603)、安石榴林对照品(纯度大于99.37%,批号:MUST-16030105)(成都曼斯特生物科技有限公司);HPD500 型大孔吸附树脂(沧州宝恩吸附材料科技有限公司);95%乙醇(食用酒精);甲醇(色谱纯,美国Sigma 公司);三氟乙酸(Macklin);氢氧化钠(NaOH,天津市北联精细化学品开发有限公司);盐酸(洛阳市化学试剂厂)。
1.2 仪器
LC-20AT LC-20AB 高效液相色谱仪(日本岛津公司);AB135-S 型电子天平(瑞士梅特勒公司);PB-10 型pH 计(北京赛多利斯公司);ZXMP-AL230 恒温恒湿箱(上海智城分析仪器制造有限公司);ZS51213340 药品强光稳定性试验箱(侦翔环境试验设备);FH-UF/NF-2 型复合型纳滤浓缩装置(江苏凯米膜科技股份有限公司);R-2003 型旋转蒸发浓缩装置(巩义市予华仪器有限责任公司)。
2 方法与结果
2.1 安石榴苷HPLC 方法学验证及含量测定
2.1.1 色谱条件 根据课题组前期建立的质量标准,采用高效液相色谱法测定。色谱柱:Agilent SB-C色谱柱(4.6 mm×250 mm,5 μm);流动相为0.1%三氟乙酸(A)-甲醇(B),梯度洗脱(0 ~15 min:97%A;15 ~25 min:80%A;25 ~35 min:55%A;35 ~40 min:35%A);检测波长370 nm;流速1 mL·min;进样量10 μL;柱温30℃。
2.1.2 对照品溶液的配制 分别精密称取安石榴苷、安石榴林、鞣花酸对照品6.5、5、5 mg 于10 mL 的棕色量瓶中,加甲醇定容至刻度,混匀,配制成质量浓度分别为650、500、500 µg·mL的对照品储备液,备用(临用时稀释至所需质量浓度)。
2.1.3 供试品溶液的配制 精密称取安石榴苷精制物25 mg 于25 mL 量瓶中,加甲醇定容至刻度,混匀,即得供试品溶液,备用。
2.1.4 方法学考察 分别取空白溶剂、对照品溶液及供试品溶液按照“2.1.1”项下色谱条件进行HPLC 检测,记录峰面积,对方法的专属性、线性、精密度、重复性、稳定性及回收率进行考察。色谱图见图1,安石榴苷峰形良好,样品的保留时间与对照品的保留时间一致,溶剂不产生干扰。安石榴苷在40.625 ~650 µg·mL与峰面积具有良好的线性关系(A
=5654.6C
+7725.5,R
=0.9999)。精密度、稳定性、重复性试验的RSD
值均小于2.0%,符合方法学要求。样品的平均回收率为99.75%(n
=6),RSD
为2.8%,表明方法准确度良好。
图1 安石榴苷色谱图Fig 1 Chromatogram of punicalagin
2.1.5 样品含量测定 精密称取安石榴苷精制物25 mg 于25 mL 量瓶中,加甲醇定容至刻度,混匀,精密量取2 mL 至10 mL 量瓶,甲醇定容至刻度混匀后,用0.22 µm 微孔滤膜过滤,取续滤液10 µL,按照“2.1.1”项下色谱条件进样分析,将峰面积代入标准曲线,计算含量。
2.2 精制工艺的优化
2.2.1 上样液制备 根据课题组前期建立的纯化工艺,采用HPD500 型大孔吸附树脂进行分离纯化,取安石榴苷粗品,用水配制成安石榴苷质量浓度为1.3 mg·mL的溶液(相当于石榴皮生药浓度20.8 mg·mL),用HCl 调pH 至2,过滤,取滤液即得上样液。
2.2.2 大孔吸附树脂的预处理 取HPD500 型大孔吸附树脂适量,95%乙醇溶液浸泡24 h 进行活化,将活化后的树脂投入玻璃柱内,用95%乙醇溶液冲洗树脂,洗净至与纯化水1∶5 混合不呈白色混浊,再用纯化水洗至流出液不含酒精(用酒精计测量),放置,备用。
2.2.3 上样吸附工艺条件 取pH 值为2、安石榴苷质量浓度为1.3 mg·mL的溶液5 BV,加到已预处理好的HPD500 型树脂柱上,以2 BV·h的动态吸附速度上样,静态吸附12 h 后,开始洗脱。
2.2.4 计算公式
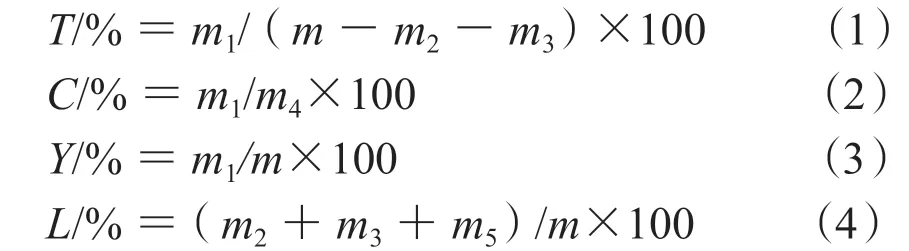
T
,安石榴苷转移率(%);C
,安石榴苷的含量(%);Y
,安石榴苷收率(%);L
,安石榴苷损失率(%);m
,上样液中安石榴苷的质量(mg);m
,洗脱液中安石榴苷的质量(mg);m
,上样液流分中安石榴苷的质量(mg);m
,除杂洗脱液中安石榴苷的质量(mg);m
,安石榴苷精制物的质量(mg);m
,剩余安石榴苷的质量(mg)。除杂率(%)是将杂质(保留时间为11.619 min 的安石榴林及保留时间在12.76 ~13.264 min 内的未知成分)的峰面积代入安石榴苷的标准曲线,计算其质量,以洗脱液中杂质的质量/上样液中杂质的质量进行计算。2.2.5 单因素考察 按“2.2.1”项下方法制备上样液,根据“2.2.3”项下方法进行上样吸附后,以4 BV·h的流速进行洗脱,分别考察除杂溶剂(水、5%乙醇、8%乙醇、10%乙醇)、除杂溶剂洗脱终点(1、2、3、4、5、6、7、8 BV)、洗脱剂中NaOH 的浓度(0%、0.001%、0.0025%、0.005%、0.01%、0.015%)、乙醇浓度(0%、5%、10%、15%、20%、25%)、 洗脱温度(20 ℃、30 ℃、40 ℃、45 ℃)、洗脱剂用量(1、2、3、4、5、6、7、8、9、10 BV)对安石榴苷含量的影响。将各洗脱液进HPLC 分析,测定安石榴苷的含量。
除杂溶剂及除杂剂洗脱终点的试验结果如表1 所示,随着洗脱剂中乙醇浓度增大,除杂率与安石榴苷的损失率均逐渐增大,在保证安石榴苷尽可能少的损失下,8%乙醇除杂率最高,因此确定使用8%乙醇作为除杂洗脱液。8%乙醇洗脱柱体积达到6 BV 时,安石榴苷的含量开始呈线性增长趋势(见图2A),为了避免损失大量的安石榴苷,确定8%乙醇洗脱终点为6 BV。
表1 除杂溶剂的影响
Tab 1 Effect of impurity removal solvents
除杂溶剂除杂率/%安石榴苷损失率/%水25.01 0.28 5%乙醇36.23 0.68 8%乙醇47.08 3.56 10%乙醇53.2315.10
氢氧化钠浓度的影响如图2B 所示,在氢氧化钠的浓度为0%~0.015%内,洗脱液中安石榴苷的含量随着NaOH 浓度的增加出现先增加后降低的趋势,在NaOH 浓度为0.01%时,洗脱液中安石榴苷的含量最高。安石榴苷呈弱酸性,在酸性条件下容易被大孔吸附树脂吸附,碱性条件有利于洗脱,因此确定洗脱剂中加入氢氧化钠的浓度为0.01%。
乙醇浓度的影响如图2C 所示,安石榴苷具有很强的极性,当以水作为洗脱剂时,洗脱液中安石榴苷的含量最高。随着乙醇浓度的增加,一些极性较小的成分会随着安石榴苷一同洗脱,含量逐渐降低。因此确定以含0.01%氢氧化钠的纯化水作为洗脱溶剂。
洗脱温度的影响如图2D 所示,在洗脱温度20 ~45℃内,洗脱液中安石榴苷的含量差异不大。考虑到安石榴苷属于多酚类物质,对热敏感,为了保证洗脱过程中安石榴苷的稳定性以及工艺的简便性,因此确定于室温条件下进行洗脱。
洗脱剂用量的影响如图2E 所示,在洗脱过程中发现,使用含0.01%NaOH 的纯化水于室温洗脱2 BV 后,树脂柱上黄色条带到达最底端,此时开始接收的洗脱液中安石榴苷含量最高,自此再洗脱3 BV 后,安石榴苷的含量开始呈下降趋势。为了得到高纯度的安石榴苷精制物,确定使用含0.01%NaOH 水洗至黄色条带到达柱底后,再收集3 BV 作为洗脱流分。
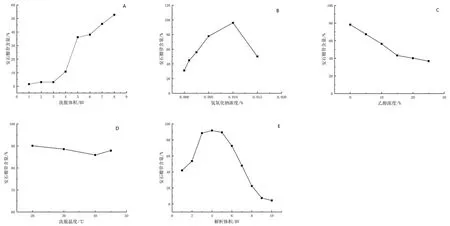
图2 除杂溶剂洗脱终点(A)、氢氧化钠浓度(B)、乙醇浓度(C)、洗脱温度(D)、洗脱剂用量(E)对安石榴苷含量的影响Fig 2 Effects of impurity removal solvent elution end point(A),sodium hydroxide concentration(B),ethanol concentration(C),elution temperature(D)and eluent dosage(E)on the content of punicalagin
2.2.6 浓缩工艺比较 根据单因素试验结果筛选的最优洗脱条件进行试验,收集安石榴苷洗脱液流分,分成2 份,分别以减压浓缩和膜分离(200 D 纳滤膜)两种方式进行浓缩。浓缩液经冷冻干燥得安石榴苷精制物,按照“2.1.5”项下方法测定精制物中安石榴苷含量。
减压浓缩和纳滤浓缩过程参数和结果如表2所示,安石榴苷对热敏感,在减压浓缩时温度需控制在45 ℃以内,但由于该工艺中洗脱剂为水,在使用减压浓缩除水时其浓缩效率仅20%,使用膜分离技术纳滤膜浓缩可在室温条件下进行,浓缩效率高,得到的精制物中安石榴苷的含量较减压浓缩的高,因此选用分子量为200 D 的纳滤膜对洗脱液进行浓缩。
表2 减压浓缩和纳滤浓缩对比结果
Tab 2 Vacuum concentration and nanofiltration concentration
浓缩方式浓缩过程参数样品量/L所用时间/h浓缩后体积/L浓缩效率/%安石榴苷的含量/%温度/℃压力/MPa减压浓缩45<-0.0810282084.14纳滤浓缩室温5 ~720157586.76
2.3 验证试验
验证试验所采用的最优洗脱工艺为:上样液静置12 h 后,先用6 BV8%乙醇溶液除杂后,再用含0.01%NaOH 的纯化水于室温条件下洗脱至黄色条带到达柱底后,开始接收3 BV 流分,流速为4 BV·h。使用分子量为200 D 的纳滤膜对安石榴苷流分进行浓缩,浓缩液冷冻干燥得安石榴苷精制物。
3 次精制试验所获安石榴苷的平均转移率为72.70%,RSD
为2.6%(n
=3);安石榴苷的平均收率为69.66%,RSD
为1.3%(n
=3);安石榴苷的平均百分含量为84.56%,RSD
为1.6%(n
=3);平均损失率为25.61%,表明精制工艺稳定可行。2.4 安石榴苷精制物中未知组分的初步鉴定
精密称取安石榴苷精制物25 mg 于25 mL 棕色量瓶中,加甲醇定容至刻度,混匀,用0.22 μm 滤膜过滤,另取“2.1.2”项下的安石榴林及鞣花酸对照品储备液各1 mL 于10 mL 量瓶中,定容混匀后,用0.22 μm 滤膜过滤,取续滤液进行分析,结果如图3 所示。通过与对照品比对,确定峰2 为安石榴林,峰10 为鞣花酸。
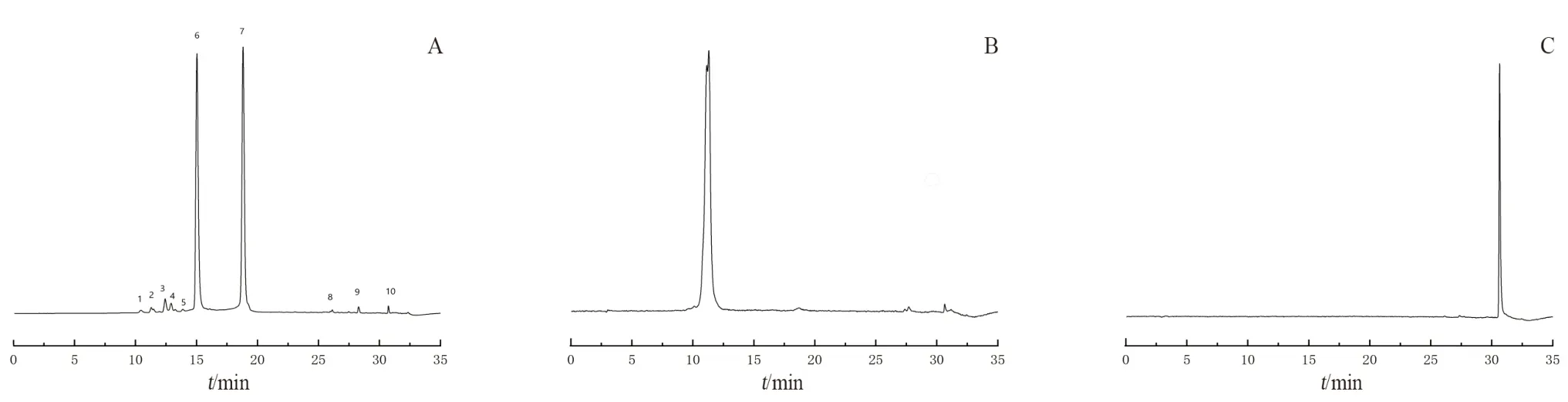
图3 安石榴苷精制物HPLC 图谱Fig 3 HPLC of punicalagin refined product
2.5 安石榴苷精制物稳定性的影响因素研究
2.5.1 高温 精密称取安石榴苷精制物适量,置于敞口的称量瓶中放在药物稳定性检查仪中(60 ℃),于0、5、10 d 取样,观察其外观性状、增减质量并测定安石榴苷的含量。并对0、5、10 d 时安石榴苷精制物中各组分进行定量分析。
安石榴苷精制物在60 ℃条件下放置5 d 后,减重4.62%,含量降低了9.0%,结果见表3。安石榴苷结构中含有多个酚羟基,高温条件加速其被氧化而降解。精制物中除安石榴苷、安石榴林及鞣花酸外,还含6 种未知成分,通过面积归一化法发现精制物在高温60 ℃条件下放置10 d,安石榴苷的含量逐渐降低,安石榴林、鞣花酸、峰1 和峰4 这4 种成分含量增加,其中,安石榴林及鞣花酸为主要的降解产物。这与文献报道一致。故安石榴苷精制物需在低温条件下保存。
表3 高温试验结果
Tab 3 High temperature test
取样时间/d外观性状质量变化 /% 含量测定 /%精制物中各组分面积占比/%峰1峰2(安石榴林)峰3峰4峰5峰6、7(安石榴苷)峰8峰9峰10(鞣花酸)总0棕黄色疏松粉末085.18±1.39 0.771.781.530.490.2893.360.290.550.95100.0 5棕黄色疏松粉末 -4.62±0.05 77.50±1.10 1.232.551.740.940.3390.350.230.592.04100.0 10棕黄色疏松粉末 -5.14±0.15 76.10±1.67 1.373.281.711.020.3588.650.290.592.69100.0
2.5.2 高湿 精密称取安石榴苷精制物适量,置于敞口的称量瓶中放在恒温恒湿箱中[相对湿度(75±5)%,25 ℃],密闭保存,于0、5、10 d取样,观察其外观性状、增减质量并测定安石榴苷的含量。
安石榴苷精制物在相对湿度(75±5)%的条件下放置5 d 吸湿增重高达13.19%,但其含量未发生明显变化,结果见表4。由于安石榴苷具有很强的吸湿性,应将安石榴苷精制物置于干燥环境中密封保存。
表4 高湿试验结果Tab 4 High humidity test
取样时间/d外观性状质量变化/%含量测定/%0棕黄色疏松粉末085.18±1.39 5棕黄色粘连粉末13.19±0.2085.40±0.92 10棕黄色粘连粉末13.00±0.2885.87±0.99
2.5.3 强光照射 精密称取安石榴苷精制物适量,置于敞口的称量瓶中于澄明度检测仪(4500±500)lx 下照射,于0、5、10 d 取样,观察其外观性状、增减质量并测定安石榴苷的含量。
安石榴苷精制物在25℃,(4500±500)lx 的强光照射下放置5 d,表层粉末出现粘连,增重2.86%,含量下降了1.7%,结果见表5,表明安石榴苷对光敏感,应注意避光贮藏。
表5 强光照射试验结果
Tab 5 Strong light exposure test
取样时间/d外观性状质量变化/%含量测定/%0棕黄色疏松粉末085.18±1.39 5棕黄色表面粘连粉末2.86±0.0583.69±0.89 10棕黄色表面粘连粉末2.92±0.0982.36±1.17
3 讨论
本试验探讨了石榴皮中安石榴苷大孔吸附树脂纯化工艺,并对其稳定性进行了研究。结果表明,用6 BV 8%乙醇进行除杂后,再用含0.01% NaOH 的纯化水在室温条件下洗脱,接收3 BV 黄色条带流分,安石榴苷总收率可达到(69.66±0.87)%,纯度由(44.77±1.77)% 提高至(84.56±0.13)%。本课题组将进一步研究鉴定安石榴苷精制物中其他的组分,为安石榴苷精制物作为原料药的应用奠定基础。安石榴苷精制物具有很强的吸湿性,其对温度最为敏感,在光照条件下不稳定。鞣花酸及安石榴林为安石榴苷主要的降解产物,对于安石榴苷的其他降解产物还需要进行深入研究,为了保证安石榴苷精制物的稳定性,应将其放置于低温、干燥密闭的容器中避光存储。
3.1 纯化工艺的优点
本文根据安石榴苷的特性对其纯化工艺中的解吸附条件进行了优化,首次采用含碱的水作为洗脱剂,大大节省了有机溶剂的使用量。本文首次将大孔吸附树脂联合膜分离技术应用于安石榴苷的纯化工艺中,大孔吸附树脂技术具有选择性强、机械强度大、吸附容量大、吸附速度快、易再生、可循环使用、成本低等优点,在天然产物分离纯化、中药制剂的纯化,有害杂质的去除等领域应用广泛。纳滤膜耗能低、成本低且可在室温条件下进行,特别适用于对热敏感的物质的分离。还可去除洗脱液中部分小分子量的物质如有机物、无机盐,实现进一步纯化。因此既可以得到高纯度的安石榴苷又能有较高的收率。在试验过程中从样品溶液的吸附到解吸附及浓缩,整个工艺过程可在24 h 内完成,工艺简单、效率较高且易于控制。并将该工艺进行了中试放大试验,工艺可行,可以用于工业化生产。
3.2 纯化工艺中的注意事项
在大孔吸附树脂纯化工艺中,洗脱剂的pH对安石榴苷的影响较大,安石榴苷为弱酸性,安石榴苷在碱性较强的条件下不稳定,应将收集的洗脱液pH 调至弱酸性,再进行浓缩。由于该工艺中所用的洗脱溶剂为水且安石榴苷对热敏感,使用传统的减压浓缩不仅效率低,而且在加热过程中容易导致安石榴苷受热降解。因此浓缩工艺在室温条件下进行较好。
综上,本试验建立的安石榴苷的纯化方法有效可行,适用于安石榴苷的工业化生产,并为安石榴苷精制物的存储提供了理论依据。

