香榧壳生物炭/g-C3N4活化过硫酸盐的光催化性能
张婷婷,许 贺*,蔡冬清,陈仕艳,王华平
香榧壳生物炭/g-C3N4活化过硫酸盐的光催化性能
张婷婷1,许 贺1*,蔡冬清1,陈仕艳2,王华平2
(1.东华大学环境科学与工程学院,上海 201620;2.东华大学材料科学与工程学院纤维材料改性国家重点实验室,上海 201620)
采用简便一步热聚合法制备高催化活性的生物炭/g-C3N4复合光催化剂,并在可见光下活化过硫酸盐 (PS) 应用于对-乙酰氨基酚 (AAP) 废水的降解研究.通过紫外-可见漫反射吸收光谱 (UV-vis DRS) 、光致发光光谱 (PL)对该复合催化剂的光学性质进行了研究.结果表明,生物炭的引入使g-C3N4的可见光吸收边界从483nm增强至553nm,并且提高了光致电子-空穴对的分离效率.扫描电子显微镜 (SEM) 、X射线衍射光谱 (XRD)、傅里叶变换红外光谱 (FT-IR) 及X射线光电子能谱 (XPS) 的表征结果显示生物炭的引入改善了g-C3N4的微结构.在反应体系中引入PS强化了AAP的去除效率,在可见光照射下其降解速率是未添加PS的8.9倍,表明该催化体系可有效活化PS产生更多高活性氧化物质.自由基捕获实验表明该催化系统可能存在·O2-、h+、·OH和·SO4-活性物种,复合材料性能的提升主要归因于生物炭作为电子受体,有效抑制了电子-空穴的复合.
可见光催化;过硫酸盐活化;生物炭;对-乙酰氨基酚
对乙酰氨基酚(AAP)是一种典型的药品及个人护理品(PPCPs),易溶于水,可生化性差[1].由于AAP的广泛应用,在各种水体中经常被检测到.通常,人体内大部分未代谢的AAP分子会通过尿液和粪便排出,然后释放到水生环境中[1-2].据报道,饮用水、地表水和生活废水中的AAP浓度分别达到了0.2,15, 180μg/L[3].研究显示,AAP及其代谢产物难以通过常规的污水处理方式降解[4],从而对生态环境和人体健康造成危害.
近年来,基于·SO4-的高级氧化技术(S-AOPs)得到了学者们的广泛关注[5-6].通常,·SO4-可通过紫外光活化、热活化、碱活化、过渡金属离子、金属氧化物以及碳基材料等活化单过硫酸盐(PMS)或过硫酸盐(PS)来生成[7-8],与PMS相比,PS具有更高的氧化还原电位以及化学稳定性而被更广泛的用于水净化领域[6,9].上述几种活化方式具有能耗高、易造成二次污染及适用范围窄等缺陷,而碳基材料因无毒、成本低、稳定性高等优点[10].其中,氮化碳(g- C3N4)材料由于带隙窄、制备工艺简单、价格低廉而被认为是一种环境友好型碳基光催化材料[11-12],且其可被可见光激发产生自由电子用以活化PS.然而,g-C3N4的可见光利用率较低、光致电子-空穴复合率较高,限制了其光催化效率[13-14].通常采用元素掺杂、调控g-C3N4的结构以及引入其他半导体构建异质结复合光催化剂等方法改善上述缺陷[15-16].
生物炭(BC)是通过废弃生物质原料在高温低氧或无氧条件下热解获得的富含芳香结构的碳质材料,其有机原料来源广泛,如农作物残基、林业废弃物、动物粪便、城市固体废弃物及污水污泥等[17].香榧果壳作为一种典型的农林副产物,内部含有丰富的纤维素、半纤维素及木质素,是制备生物炭的优质原料.有研究表明,生物炭的功能结构(如表面缺陷、含氧官能团、持久性自由基和孔隙结构)可作为催化活性位点[18],使其在一定程度上可以活化PS产生·SO4-用于污染物的降解.有研究显示[19-21],以城市污水污泥、高粱秸秆以及螺旋藻残渣为原料制备的生物炭均可有效活化PS降解有机污染物.然而目前关于生物炭用于光催化协同PS活化降解有机废水的研究较少.
因此,本研究采用香榧壳和三聚氰胺为原料,通过简便一步热聚合法制备BC/g-C3N4复合光催化材料,利用生物炭表面丰富的催化活性位点和优异的电子转移特性调控g-C3N4的微结构及光学性能,以提高复合材料的可见光响应范围和光致电子-空穴分离效率;同时,在可见光照射下,通过催化活化PS研究BC/g-C3N4体系对AAP的光催化降解性能,探究了初始AAP浓度、催化剂投加量、溶液初始pH值及PS投加量对AAP降解性能的影响.通过自由基捕获实验鉴定该反应体系中的活性物种,研究了BC/g-C3N4/PS催化体系降解AAP的反应机理,以期为碳基材料活化过硫酸盐复合光催化高级氧化技术在废水处理领域的应用提供参考.
1 材料与方法
1.1 实验试剂
三聚氰胺、对-乙酰氨基酚(AAP)、过硫酸钾(PS)、乙二胺四乙酸二钠(EDTA-2Na)、甲醇(MeOH)、对苯醌(BQ)、叔丁醇(TBA)均为分析纯,购自上海麦克林生化科技有限公司.香榧壳产自浙江诸暨一带.实验用水均为超纯水.
1.2 光催化材料的制备
通过简易一锅热聚合法制备了生物炭/石墨相氮化碳(BC/g-C3N4)复合光催化材料(记为BCCN).具体步骤如下:香榧果壳先用超纯水清洗3遍,以去除其表面杂质,烘干之后使用破碎机破碎至直径小于2mm的细小颗粒,再经筛网过滤.使用球磨法将预处理的香榧壳与三聚氰胺按照一定质量比混合均匀,然后将其转入带盖坩埚中,并置于管式炉中煅烧,煅烧条件为:以5℃/min的升温速率从室温升至550℃并保持3h,整个过程使用N2保护.将煅烧后的块状材料再经球磨法研磨至粉体状态.其中香榧果壳与三聚氰胺质量比为1:50、1:40、1:30、1:20,分别记为BCCN1、BCCN2、BCCN3和BCCN4.单一g-C3N4与BC的制备条件同上,只是不添加香榧壳或三聚氰胺.
1.3 催化剂的表征
样品的物相结构通过XRD (D/max-2550VB+/ PC型,日本Rigaku)进行表征分析,通过SEM (S- 4800型,日本Hitachi)对样品的形貌、元素分布进行表征分析,采用XPS (Escalab 250Xi,中国,赛默飞世尔科技公司)分析材料的元素组成,采用UV-Vis DRS(UV-3600,日本岛津公司)对材料的紫外-可见漫反射吸收进行分析,采用PL (FLS1000,美国,PTI)在室温条件下对样品进行光致发光测试,激发波长为380nm.
采用高效液相色谱仪(HPLC, LC-16,日本岛津公司)检测降解过程中AAP的浓度变化,使用Wondasil C18 (5μm, 150mm´4.6mm) 色谱柱进行分离.甲醇和超纯水作为流动相,体积比为25:75,检测波长为254nm.
1.4 光催化性能评估
AAP的光降解实验在一个具备循环水冷却系统的双层玻璃烧杯中进行,循环水系统保持整个光降解反应保持在25℃.采用具有420nm滤光片(过滤紫外光)的300W氙灯用作可见光光源,使用太阳能功率计测量反应溶液表面的光强度为(2000± 10)W/m2.在降解反应实验中,称取100mg催化剂投加到100mL浓度为 10mg/L的AAP溶液,溶液初始pH为7左右.在避光条件下搅拌1h,使催化剂与AAP分子充分接触并达到吸附-解吸平衡.最后在光照射之前向悬浮液中添加一定浓度的PS.光催化反应期间,在固定时间点吸取1mL反应液,经过0.22µm水系针头滤膜过滤掉催化剂,通过超高效液相色谱分析AAP浓度,降解率()可表示为:
= (0-C) /0× 100% (1)
式中代表AAP的降解率;0代表初始AAP溶液浓度;C代表时刻AAP溶液浓度.
1.5 自由基捕获实验
采用乙二胺四乙酸二钠(EDTA-2Na)、对苯醌(BQ)、甲醇(MeOH)和叔丁醇(TBA)分别作为空穴(h+)、超氧自由基(·O2-)、硫酸根自由基(·SO42-)和羟基自由基(·OH)的捕获剂.在光催化降解实验中,加入催化剂之后,再分别加入上述自由基捕获剂,搅拌1h后进行光降解,通过测定添加了不同自由基捕获剂后的AAP浓度以确定起主要作用的活性物质,本实验中BQ和EDTA-2Na的浓度均为0.5mmol/L, MeOH和TBA与PS的物质的量比均为1000:1.
1.6 AAP降解中间产物的检测
采用液相色谱-质谱联用仪(LC-MS, waters 1290,美国)检测AAP降解过程中产生的中间产物及最终产物.LC-MS检测条件:使用C18色谱柱(Waters,美国),流动相A为0.1%甲酸水溶液,流动相B为甲醇;流动相流速:0.3mL/min,进样体积4μL,ESI+模式,电压4000V,/扫描范围为50~500.
1.7 数据处理与分析
利用Excel 2016软件对降解过程中AAP的浓度进行分类整理,并编辑公式计算降解效率η;通过Origin 2019软件绘制AAP浓度随降解时间的变化趋势曲线;采用Chemdraw 18.0软件分析AAP降解中间产物结构并绘制降解路径.
2 结果与讨论
2.1 材料表征
2.1.1 扫描电子显微镜 由图1(a)和1(b)可观察到g-C3N4由表面光滑且形状不规则的大片层状物聚集而成,这是通过三聚氰胺直接热缩聚法合成g-C3N4的典型特征[22].而香榧果壳制备的生物炭呈现出形状不规则的小颗粒.由图1(c)可看出生物炭颗粒均匀分布在g-C3N4表面,减少了生物炭颗粒之间的团聚,有利于电子转移.同时由于香榧果壳与三聚氰胺的质量比仅为1:30,所以g-C3N4为主体材料且其大部分表面裸露出来,从而有利于污染物的吸附,进一步促进AAP的降解.从图1(d)~1(f) 可看出,该复合光催化剂主要由C、N以及少量的O元素组成且各元素分布均匀.

图1 g-C3N4、生物炭、BCCN3的SEM谱图以及BCCN3的元素分析谱图
(a) g-C3N4、(b) 生物炭、(c) BCCN3的SEM谱图;BCCN3的 (d) C元素、(e) N元素、(f) O元素分析谱图
2.1.2 X-射线衍射分析 如图2所示,2为12.8°和27.6°处可以观察到g-C3N4的2个较为明显的衍射峰,分别对应其在三-s-三嗪平面结构堆积的(100)晶面和共轭芳香体系堆积的(002)晶面[23],而未观察到其他杂质的衍射峰,表明所制备的样品纯度较高.在BCCN3的谱图中未发现这2个峰的明显变化,表明改性后的层状结构与g-C3N4的结构几乎相同.BCCN3的(002)晶面衍射峰较g-C3N4发生了微弱的角度偏移,这意味着通过生物炭修饰后,g-C3N4夹层状共轭芳香体系的堆积距离增加,表明该生物质的碳化发生在g-C3N4微结构的内部及表面,形成了BC/g-C3N4的复合结构[24].

图2 g-C3N4和BCCN3的X-射线衍射谱图
2.1.3 傅里叶红外光谱分析 如图3所示,从g- C3N4谱图中可看出,在 810cm-1处的吸收峰是3-s-三嗪环结构的伸缩振动而形成,位于1254~1628cm-1处的特征峰是由于C-N单键和C=N双键的典型伸缩振动所引起,而位于3000~3600cm-1附近的宽峰来自g-C3N4分子结构边缘的C-NH2和C-NH基团的拉伸振动及其表面所吸附的水分子中的-OH基团[4,25].而BCCN3的谱图可看出,其特征峰与g-C3N4相比未出现明显差异,该现象表明低剂量香榧壳的引入未对三聚氰胺的聚合过程产生影响.

图3 g-C3N4和BCCN3傅里叶变换红外光谱图
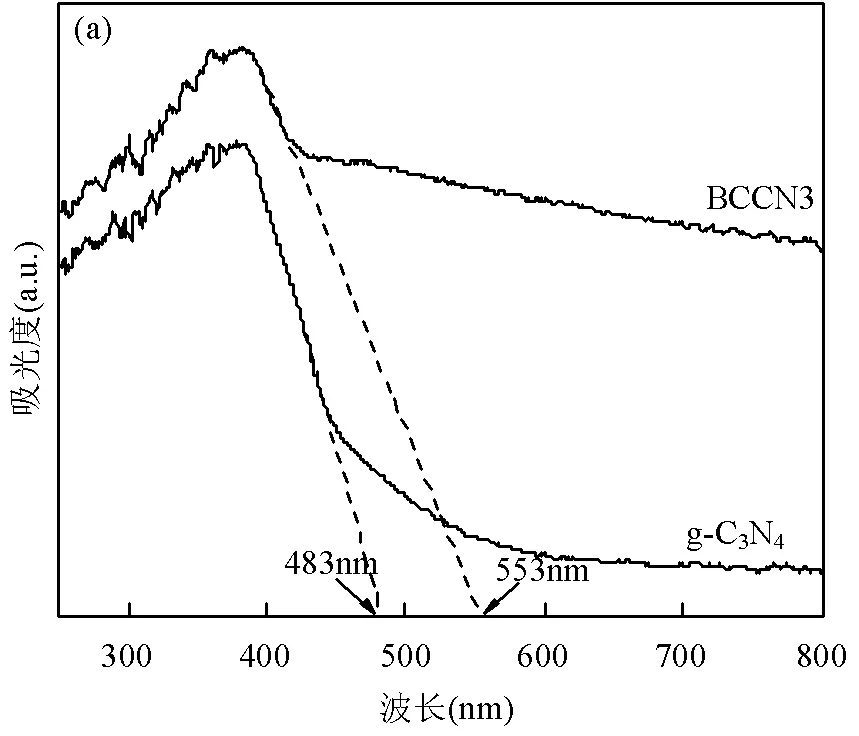
2.1.4 紫外可见漫反射吸收光谱分析 从图4(a) 可看出,与单一g-C3N4相比,引入了生物质炭的复合材料BCCN3的光吸收边界发生明显红移,吸收边界大致从483nm红移至553nm附近且出现吸收尾峰,延伸至大部分可见光区域,该现象说明BCCN3具有优异的可见光响应能力,即在相同强度的可见光照射下,BCCN3可被光子激发产生更多的电子空穴对,从而增强光催化效应.通过Tauc plot法估算光催化剂的禁带宽度[26],如图4(b)所示.计算得到g-C3N4与BCCN3的禁带宽度分别为2.71,2.53eV,由此可见在引入生物质炭之后材料的带隙能减小[27].该现象表明生物炭掺入了g-C3N4表面,并在其带隙中产生掺杂能级,从而增强了光的吸收尾峰[8].通常对半导体进行掺杂改性会导致其结构和组成发生变化,进而影响材料的电子结构和光吸收特性.
2.1.5 稳态荧光光谱分析 光致发光光谱可用以研究所制备材料的光致电子和空穴的分离效率,PL强度越高意味着电子空穴对的复合效率越高.从图5可看出,在380nm激发波长下,g-C3N4在460nm处出现了较强的发射峰,该峰值是由于g-C3N4中的n-π*电子跃迁而产生的带状PL效应[28],其能量相当于带隙能,约等于2.70eV.而BCCN3的发射峰强度远小于g-C3N4,表明在引入生物炭之后明显抑制了光致电子空穴对的复合[29].
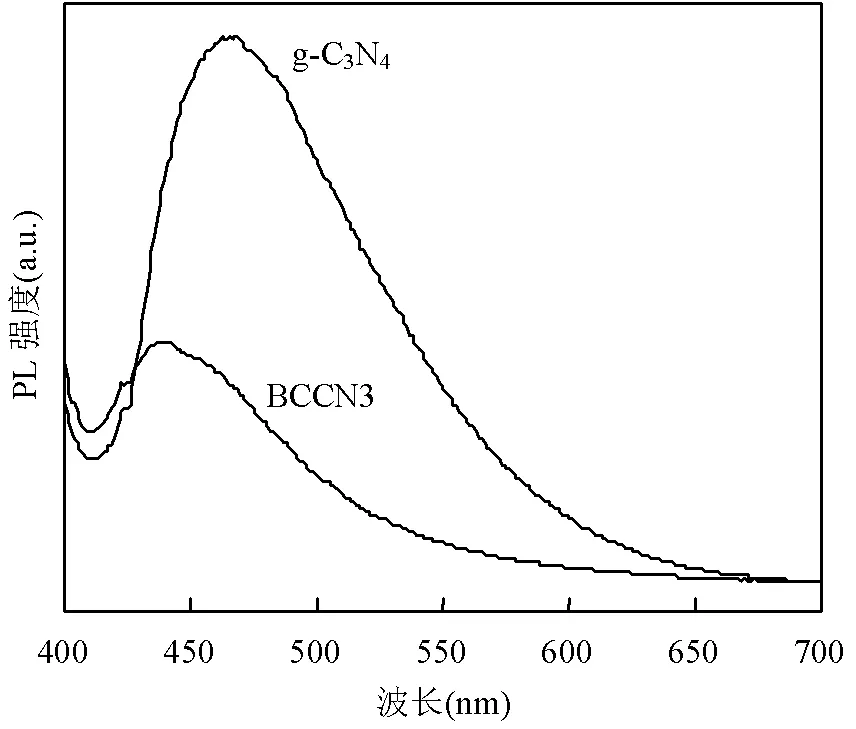
图5 g-C3N4和BCCN3稳态荧光光谱图
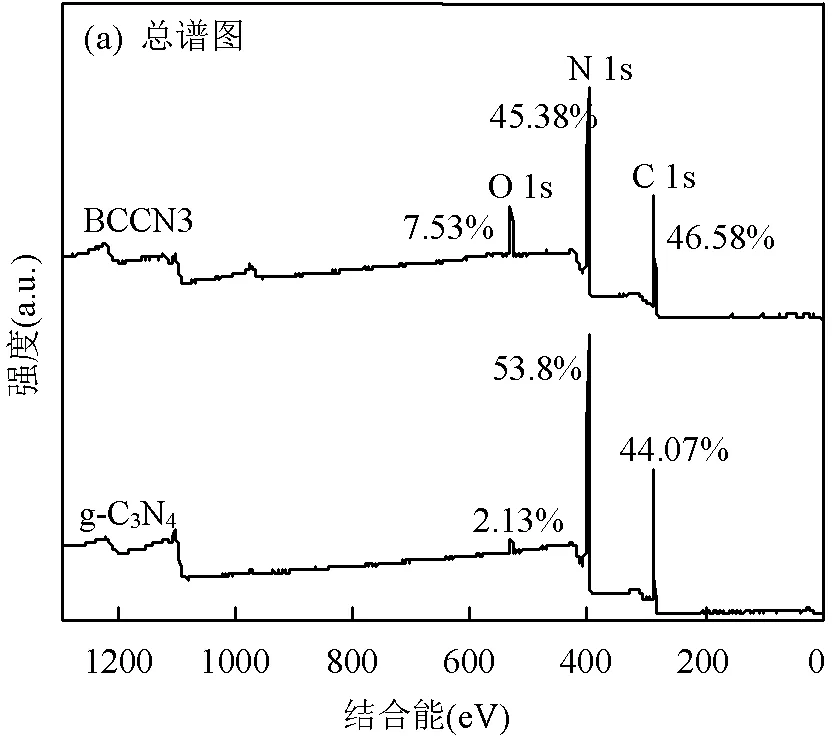
2.1.6 X-射线光电子能谱分析 由图6(a)可见,共检测到C、N、O 3种元素价态,与EDS的表征结果一致.由图6(b)可看出,在g-C3N4的谱图中,位于288.03,286.1,284.8eV的特征峰分别对应于(N)2-C= N基团的sp3杂化C、C=N基团的sp2C原子以及石墨相C-C或C=C基团[30-31].在BCCN3谱图中出现了3个与上述相似的峰,与g-C3N4相比,BCCN3中C-C或C=C特征峰位置未发生变化,而(N)2-C=N以及C=N 结合能分别增大了0.05eV和0.25eV.图6(c)可观察到,在g-C3N4的N 1s谱图中,位于400.3, 398.8,398.0eV的特征峰分别来自于N-H基团、三配位氮N-(C)3以及C-N=C基团的sp2杂化N原子[32].与g-C3N4相比,BCCN3的N-H基团特征峰增大了0.1eV,而其他两个基团的特征峰位置未发生明显变化.上述现象表明,引入生物炭未对g-C3N4的分子结构产生影响,而只影响其物相结构,表明生物炭与g-C3N4成功复合.另外,BCCN3的C 1s、N 1s的结合能与g-C3N4相比均有所增大,表明BCCN3表面的电子亲和力更大[24],更有利于吸附污染物,促进降解性能.
2.2 不同体系AAP的降解效果
由图7(a)可见,在可见光照射下, PS几乎不能降解 AAP,表明可见光不能激活 PS.g-C3N4/PS与BC/PS体系在可见光照射60min后分别仅降解了40%和55%,这是因为单一g-C3N4与BC具有较宽的带隙和较高的光致电子-空穴复合率,从而限制了该体系对AAP的降解.在BCCN/PS体系中,AAP的降解效果随着BC含量的增加呈现先增加后降低的趋势,其中BCCN3表现出最佳降解效果,在60min内AAP的去除率达99%.而随着BC含量的进一步增加,在BCCN4/PS体系中,AAP的去除率略有下降,这是因为过多的BC会和g-C3N4竞争吸收光子并为光生电子空穴对提供复合位点.在相同条件而不添加PS时,BCCN3催化体系在60min内对AAP的降解率只有36%,远低于BCCN3/PS体系,表明g-C3N4与BC的复合更有利于激活PS,从而大幅提升体系的光催化效率.
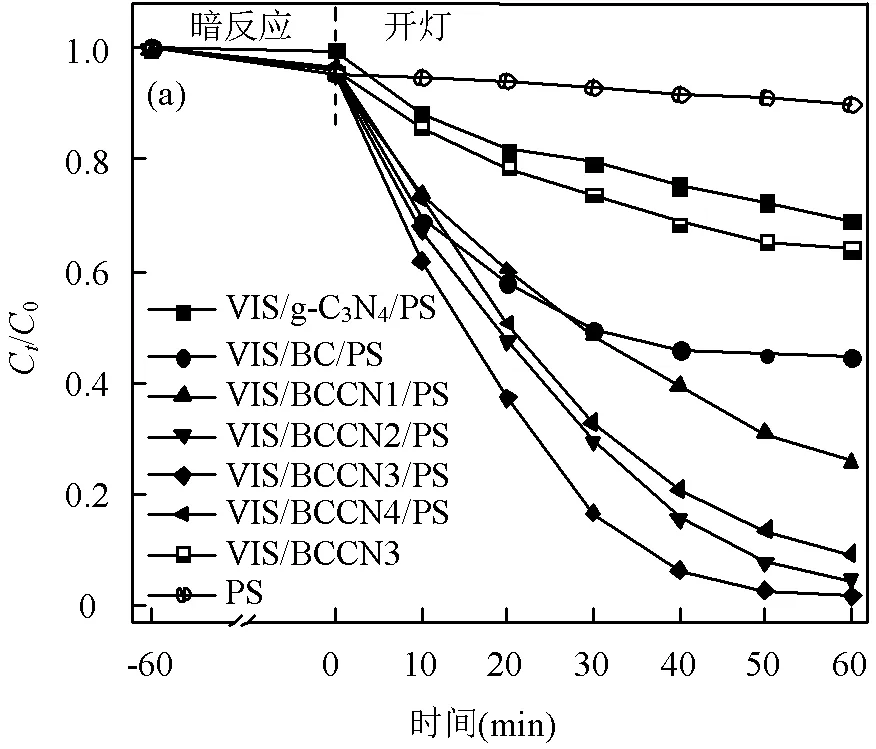
AAP浓度为10mg/L,催化剂投加量1.0g/L,初始pH=6.85,PS添加量2mmol/L,温度25℃
为了进一步量化比较不同催化体系中AAP的去除效率,使用伪一级反应速率[式(2)]比较不同体系的反应速率[33]:
ln(0/C) =(2)
式中C代表时刻反应溶液中的AAP浓度;0代表初始反应溶液中的AAP浓度;为表观反应速率常数.其拟合结果如图7(b)所示,在复合催化体系中, BCCN3/PS的降解速率最高(=0.06809min-1),分别是同等条件下g-C3N4/PS (=0.00675min-1)、BC/PS (=0.01619min-1)和BCCN3 (=0.00762min-1)的10、4.2和8.9倍.由此可见,反应体系可以高效活化PS产生有效降解污染物的自由基,从而实现AAP的高效、快速降解.
2.3 反应条件对AAP降解性能的影响

BCCN3浓度为 1.0g/L,PS添加量为2mmol/L,初始pH值为6.85,温度为25℃
2.3.1 AAP初始浓度的影响 如图8所示,当AAP浓度从5mg/L增加到20mg/L时,其降解效率从99%略微降低至94%,而相应的动力学常数从0.1174min-1降低至0.0421min-1.该现象说明当光催化剂与PS浓度保持不变时,在光催化过程中产生的活性位点和活性氧化物质的数量也保持不变.当AAP浓度较低时,BCCN3/PS催化系统产生的活性氧物质可充分的氧化AAP分子,而随着AAP浓度的增高,该催化系统产生的活性氧化物质的数量不足以降解污染物,导致降解效率和反应速率下降.另外,随着AAP浓度增加,降解中间产物增多,形成了污染物、产物与活性物种间的相互竞争关系[34],削弱了AAP与活性物种相互接触的机率,从而导致AAP的降解速率下降.
AAP浓度为10mg/L,PS添加量为2mmol/L,初始pH值为6.85,温度为25℃
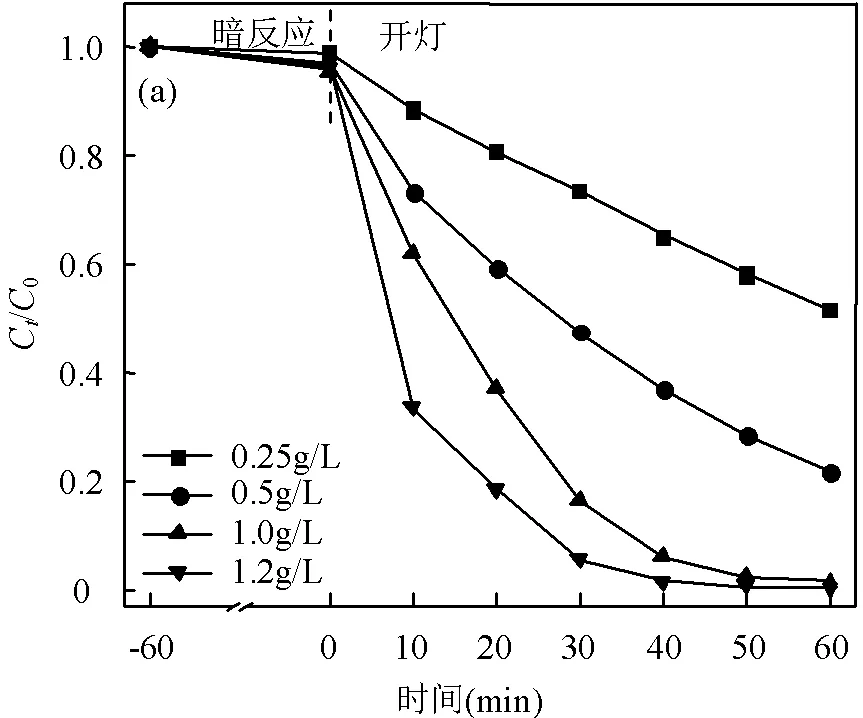
2.3.2 催化剂投加量的影响 如图9所示,随着BCCN3用量的逐步提升,光催化效率明显提升.分析其原因可能是随着催化剂用量的增加, BCCN3/ PS反应体系能够捕获更多的入射光子,从而产生大量光生电子和空穴,进一步活化PS产生更多的高活性氧化物质.但是当BCCN3的用量提升至1.2g/L时,AAP的降解速率增加的较为缓慢,其原因可归结为以下2点:一是当催化剂投加量达到饱和状态时,易发生团聚,导致光催化剂与污染物分子的有效接触面积降低,从而减少了催化活性位点;二是当催化剂投加量过高会增加溶液的浑浊度,降低光的透射率和散射率,导致光的利用率降低.因此,在高催化剂投加量条件下,为进一步提升反应速率,需在催化系统中补充更多的PS以产生更多的氧化物质.但是基于降解效率和成本的平衡性考虑,100mg 作为后续研究的最佳催化剂投加量.
AAP浓度为10mg/L,BCCN3投加量为1.0g/L,初始pH值为6.85,温度为25℃
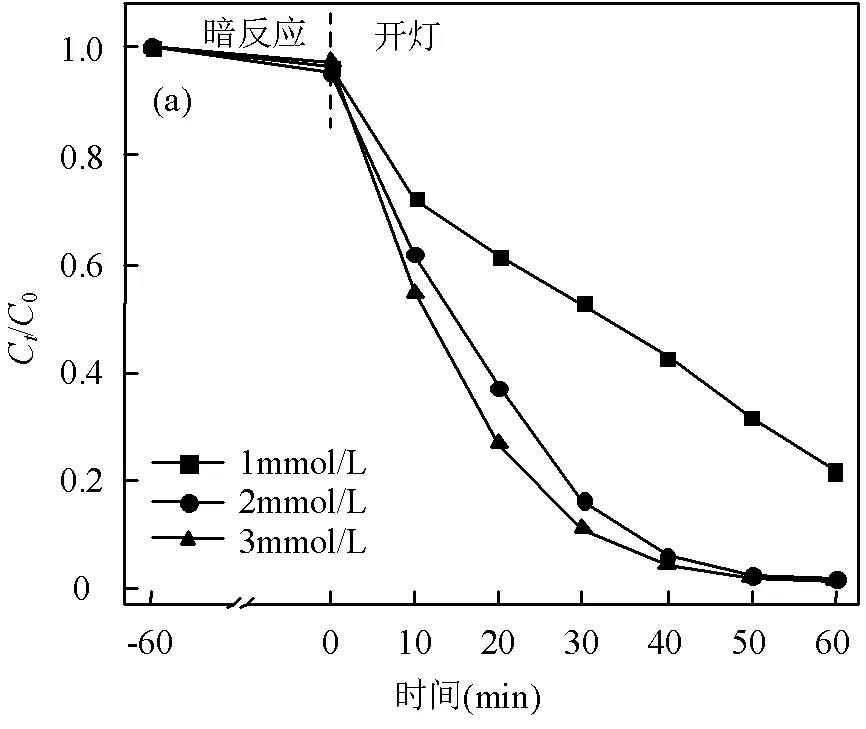
2.3.3 PS添加浓度的影响 如图10所示,随着PS添加量的增加,AAP的降解效率和反应速率都随之提高,这是由于BCCN3与可见光协同激活PS,产生了强氧化性的硫酸根自由基(·SO4-)和其他活性氧物质.当PS用量从1mmol/L增加到2mmol/L,反应速率常数从0.0230min-1提升至0.0681min-1.而当PS浓度从2mmol/L提升至3mmol/L时,反应速率从0.0681min-1略微提升至0.0747min-1.分析其原因可能是以下2点:一是在PS浓度较高时,反应体系中的催化剂用量成为限制AAP降解的主要因素,溶液中没有足够的自由电子激活PS[8],使得溶液中的部分羟基自由基(·OH)和·SO4-与PS发生反应生成活性较低的·SO5-,或者发生自由基的自结合反应,如式(3)~式(4)所示[32,35-36].二是光催化剂的光子-电子效率限制了系统中的PS的活化效率.在进一步提高PS浓度后,AAP的降解效率很难大幅提升.因此,从实用性和成本方面考虑,本研究采用2mmol/L的PS作为最优反应条件.
HSO5-+·SO4-/·OH→·SO5-+SO42-+H+/OH-(3)
SO4-+ ·SO4-→ S2O82-(4)
AAP浓度为10mg/L,BCCN3投加量为1.0g/L,PS添加量为2mmol,温度为25℃
2.3.4 初始pH值的影响 从图11(a)可看出,在酸性和中性条件下AAP的降解效率显著高于其在碱性条件下的降解效率,当pH从3增大到10时,AAP的去除效率从100%降低至50.5%,其反应速率也从0.1195min-1降低至0.0125min-1.分析其原因是由于在不同pH条件下,AAP、PS以及BCCN3具有不同的表面电子特性.其中,AAP与PS的pa值分别为9.5和9.4[37-38],如式(5)所示.表明当pH值增大到9.6时,AAP开始解离为负离子,同时PS开始以大量的HSO5-形式存在.结合图11(c)中BCCN3的Zeta电位结果来看,当pH值小于3.8时,BCCN3表面带正电荷,而此时AAP和PS带负电荷,由于库仑吸引力,使得PS与AAP分子更容易吸附在BCCN3表面,这有利于BCCN3表面产生的自由电子激活PS,从而生成·SO4-等高活性氧化物质,促进AAP分子的氧化降解.相反地,当pH值增大至10时,AAP的去除效果会因催化剂与AAP分子之间的库仑排斥力而受到抑制.此外,·SO4-还会与 OH-发生反应,生成寿命较短、氧化还原电位较低且选择性也较低的·OH,如式 (6) 所示[39].因此,当AAP溶液处于碱性条件时,溶液中过多的OH-消耗了部分·SO4-,从而降低AAP的去除率.
HSO5-→ SO52-+ H+, pK= 9.4 (5)
·SO4-+ OH-→ SO42-+ ·OH (6)
2.4 催化剂循环利用实验
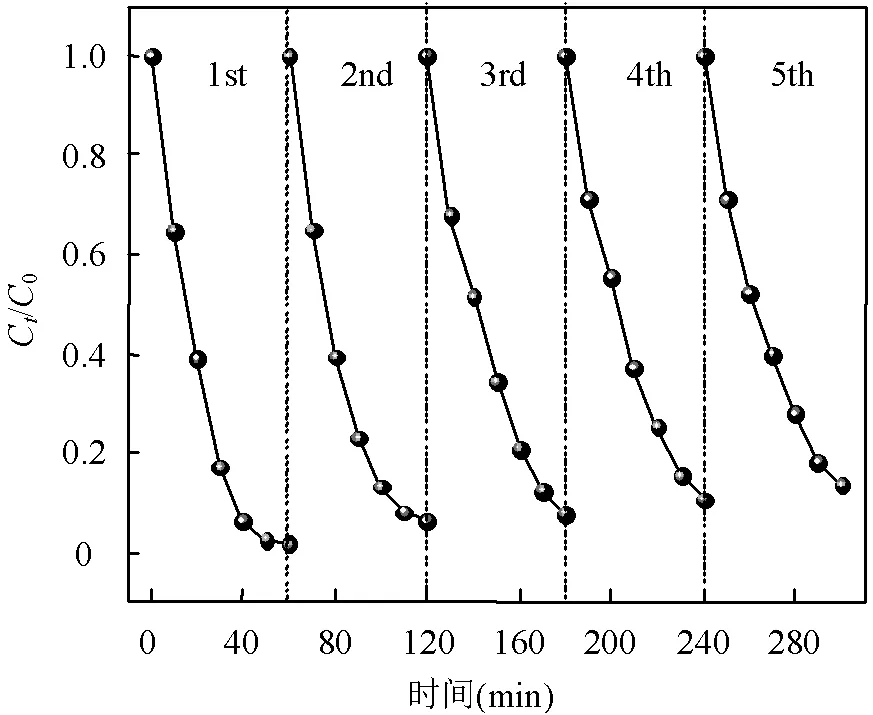
图12 BCCN3光催化剂活化PS降解AAP的循环利用实验
为检验该复合光催化剂的稳定性,通过离心收集、清洗与干燥法回收BCCN3光催化材料,并在最优反应条件下进行了5次循环实验,其结果如图12所示.BCCN3在经过5次连续循环使用之后,AAP的降解效率从99%降低至87.5%,其催化性能在可接受范围内,这意味着BCCN3复合光催化剂具有较好的可重复使用性和稳定性.
2.5 活性氧化物质的确定
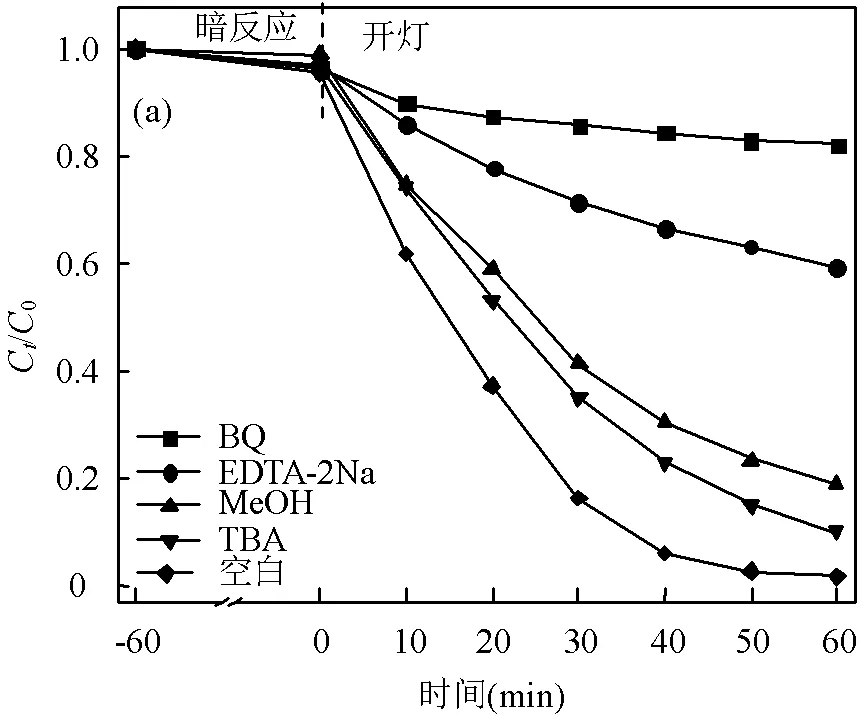
如图13所示,与空白组相比较,在加入自由基清除剂后,BCCN3/PS体系对AAP的降解效率都出现了不同程度的抑制作用.其中,BQ的抑制效果最明显,使AAP的降解效率降低至17.9%,反应速率常数也低至0.0031min-1,这是因为PS 可以与H2O反应生成·O2-,同时自由电子也可与O2发生反应生成·O2-,使得BQ的抑制效果最为明显.在EDTA-2Na的作用下,AAP的降解效率下降至40.6%,反应速率常数低至0.0088min-1,表明EDTA-2Na所产生的抑制效果仅次于BQ.而MeOH与TBA的抑制效果较为微弱,使AAP的去除效果仅分别降低至81.1%和90.2%,反应速率常数分别为0.02827,0.03656min-1.上述结果表明,在BCCN3/PS催化系统中存在·O2-、h+、·OH和·SO4-,不同活性物质均参与了AAP的氧化分解反应.
2.6 AAP降解中间产物的确定
如图14所示,检测到的中间产物有对乙酰氨基酚二聚体(产物A,荷质比为301)、对氨基酚(产物B,荷质比为110)、N-(1,4-二羟基-2,4-二烯基)乙酰胺(产物C,荷质比为169)、对苯二酚(产物D,荷质比为111)、1,2,4苯三酚(产物E,荷质比126)以及一些小分子酸(2-己烯酸,荷质比114;乙酸丙酯,荷质比103).根据其降解产物,推测了AAP的2种降解路径,其一是2个AAP分子通过二聚反应生成产物A;另一种为AAP分子中的芳香环与乙酰氨基基团受到·OH和·SO4-的攻击,生成产物B、C.产物C在·OH的作用下生成产物D,接着形成产物E,最终导致苯环开裂形成一些小分子酸,并进一步矿化形成CO2和H2O.
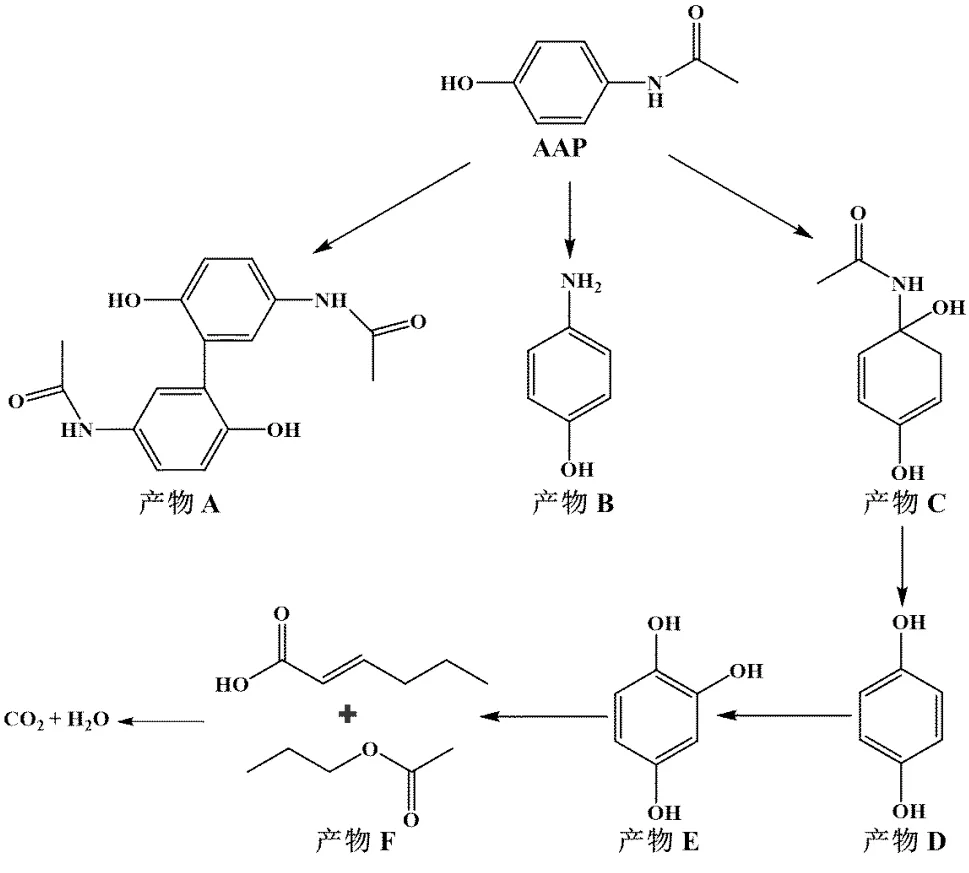
图14 AAP在BCCN3/PS体系中的降解路径
2.7 光催化降解机制
在g-C3N4的微结构中引入生物炭可改善其电子结构及可见光吸收能力,随后BCCN3在可见光照射下吸收光子能量形成电子-空穴对,由于BCCN3具有较高的电子-空穴分离效率,使得光生电子可有效激活材料表面吸附的PS,形成·SO4-和SO42-[式(7)~(8)][40],其中·SO4-可氧化H2O产成·OH [式(9)][41].另外,溶液中的自由电子可将溶解氧还原为·O2-[式(10)~(11)][32].除此之外,游离在溶液中的PS不会被光生电子所激活,但是其可与H2O直接反应生成·O2-[式(12)][8].上述几种活性氧化物质与BCCN3价带上的h+均具有强氧化性,可将AAP分子氧化为有机小分子进而矿化形成CO2和H2O [式(13)].
BCCN3 +→ h++ e-(7)
e-+ S2O82-(PS) →·SO4-+ SO42-(8)
·SO4-+ H2O → ·OH (9)
e-+ O2→ ·O2-(10)
S2O82-+ 2H2O → HO2- + SO42-+ 3H+(11)
HO2-+S2O82-→·SO4-+SO42-+H++·O2-(12)
h+/·O2-/·SO4-/·OH+AAP→CO2+H2O (13)
3 结论
3.1 采用一锅热聚合法成功合成了生物炭/g-C3N4复合光催化剂,物化和光学仪器表征结果证明生物炭成功引入到g-C3N4的微结构中,显著提高了材料的可见光吸收效率和光致电子-空穴分离效率.
3.2 在可见光照射下,BCCN3/PS反应体系在60min内对AAP的降解效率达99%,其降解速率是同等条件下BC/PS、g-C3N4/PS及BCCN3的4.2倍、10倍与8.9倍.
3.3 自由基猝灭实验显示BCCN3/PS催化系统中·O2-、h+、·OH和·SO4-均参与了AAP的氧化分解反应.
3.4 在g-C3N4的微结构中引入生物炭可改善材料的电子结构、可见光吸收能力以及光致电子-空穴对的分离效率,有效激活PS产生高活性氧化自由基,对典型PPCPs的有效去除具有潜在的应用前景.
[1] Miguel G P, Soledad G, Ismael R P, et al. Toxicity of five antibiotics and their mixtures towards photosynthetic aquatic organisms: implications for environmental risk assessment [J]. Water Research, 2013,47(6):2050-2064.
[2] Kim Y, Choi K, Jung J, et al. Aquatic toxicity of acetaminophen, carbamazepine, cimetidine, diltiazem and six major sulfonamides, and their potential ecological risks in Korea [J]. Environment International, 2007,33(3):370-375.
[3] Bueno M J M, Gomez M J, Herrera S, et al. Occurrence and persistence of organic emerging contaminants and priority pollutants in five sewage treatment plants of Spain: two years pilot survey monitoring [J]. Environment Pollution, 2012,164:267-273.
[4] Du X Y, Bai X, Xu L, et al. Visible-light activation of persulfate by TiO2/g-C3N4photocatalyst toward efficient degradation of micropollutants [J]. Chemical Engineering Journal, 2020,384:123245.
[5] Ghanbari F, Moradi M. Application of peroxymonosulfate and its activation methods for degradation of environmental organic pollutants: Review [J]. Chemical Engineering Journal, 2017,310:41- 62.
[6] Wang J L, Wang S Z. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants [J]. Chemical Engineering Journal, 2018, 334:1502-1517.
[7] Yang L, Xu L, Bai X, et al. Enhanced visible-light activation of persulfate by Ti(3+) self-doped TiO2/graphene nanocomposite for the rapid and efficient degradation of micropollutants in water [J]. Journal of Hazardous Materials, 2019,365:107-117.
[8] 雷 倩,许 路,艾 伟,等CDs-BOC复合催化剂可见光下活化过硫酸盐降解典型PPCPs [J]. 环境科学学报, 2021,42(6):2885-2895.
Lei Q, Xu L, Ai W, et al. CDs-BOC nanophotocatalyst activating persulfate under visible light for the efficient degradation of typical PPCPs [J]. Acta Scientiae Circumstantiae, 2021,42(6):2885-2895.
[9] Zhang B T, Zhang Y, Teng Y, et al. Sulfate radical and its application in decontamination technologies [J]. Critical Reviews in Environmental Science and Technology, 2014,45(16):1756-1800.
[10] Xu L, Wu C, Liu P, et al. Peroxymonosulfate activation by nitrogen- doped biochar from sawdust for the efficient degradation of organic pollutants [J]. Chemical Engineering Journal, 2019,373:238-250.
[11] Zhang S, Gu P C, Ma R, et al. Recent developments in fabrication and structure regulation of visible-light-driven g-C3N4-based photocatalysts towards water purification: A critical review [J]. Catalysis Today, 2019,335:65-77.
[12] 李冬梅,卢文聪,梁奕聪,等.Bi5O7I/g-C3N4Z型异质结的常温沉淀制备及其光催化性能研究 [J]. 中国环境科学, 2021,41(9):4120-4126.
Li D M, Lu W C, Liang Y C, et al. Room-temperature precipitation synthesis and photocatalysis of Bi5O7I/g-C3N4Z-scheme heterojunction [J]. China Environmental Science, 2021,41(9):4120- 4126.
[13] Wang X L, Yang H G. Facile fabrication of high-yield graphitic carbon nitride with a large surface area using bifunctional urea for enhanced photocatalytic performance [J]. Applied Catalysis B: Environmental, 2017,205:624-630.
[14] 刘 源,赵 华,李会鹏,等.硫氯共掺杂g-C3N4纳米片光催化降解染料 [J]. 中国环境科学, 2021,41(10):4662-4669.
Liu Y, Zhao H, Li H P, et al. Photocatalytic degradation of dyes by sulfur- and chlorine-co-doped g-C3N4nanosheets [J]. China Environmental Science, 2021,41(10):4662-4669.
[15] Ong W J, Tan L L, Ng Y H, et al. Graphitic carbon nitride (g-C3N4)-based photocatalysts for artificial photosynthesis and environmental remediation: Are we a step closer to achieving sustainability [J]. Chemical Reviews, 2016,116(12):7159-7329.
[16] Tong Z W, Yang D, Li Z, et al. Thylakoid-inspired multishell g-C3N4nanocapsules with enhanced visible-light harvesting and electron transfer properties for high-efficiency photocatalysis [J]. ACS Nano 2017,11(1):1103-1112.
[17] Al-Wabel M I, Hussain Q, Usman A R A, et al. Impact of biochar properties on soil conditions and agricultural sustainability: A review [J]. Land Degradation & Development, 2018,29(7):2124-2161.
[18] Zhou X R, Zeng Z T, Zeng G M, et al. Insight into the mechanism of persulfate activated by bone char: Unraveling the role of functional structure of biochar [J]. Chemical Engineering Journal, 2020,401: 126127.
[19] Wang S Z, Wang J L. Activation of peroxymonosulfate by sludge-derived biochar for the degradation of triclosan in water and wastewater [J]. Chemical Engineering Journal, 2019,356:350-358.
[20] 姚淑华,马锡春,李士凤.秸秆生物炭活化过硫酸盐氧化降解苯酚 [J]. 中国环境科学, 2018,38(11):4166-4172.
Yao S H, Ma X C, Li S F. Straw biochar activated persulfate oxidation and degradation of phenol [J]. China Environmental Science, 2018, 38(11):4166-4172.
[21] Ho S H, Chen Y D, Li R, et al. N-doped graphitic biochars from C-phycocyanin extracted Spirulina residue for catalytic persulfate activation toward nonradical disinfection and organic oxidation [J]. Water Research, 2019,159:77-86.
[22] Yang X L, Qian F, Zou G, et al. Facile fabrication of acidified g-C3N4/g-C3N4hybrids with enhanced photocatalysis performance under visible light irradiation [J]. Applied Catalysis B: Environmental, 2016,193:22-35.
[23] Wang S Z, Liu Y, Wang J L. Peroxymonosulfate activation by Fe- Co-O-Co doped graphite carbon nitride for degradation of sulfamethoxazole [J]. Environmental Science & Technology, 2020, 54(16):10361-10369.
[24] Wang H Z, Guo W Q, Si Q S, et al. Multipath elimination of bisphenol A over bifunctional polymeric carbon nitride/biochar hybrids in the presence of persulfate and visible light [J]. Journal of Hazardous Materials, 2021,417:126008.
[25] 高闯闯,刘海成,孟无霜,等.Ag3PO4/g-C3N4复合光催化剂的制备及其可见光催化性能[J]. 环境科学学报, 2021,42(5):2343-2352.
Gao C C, Liu H C, Meng W S, et al. Preparation of Ag3PO4/g-C3N4composite photocatalysts and their visible light photocatalytic performance [J]. Acta Scientiae Circumstantiae, 2021,42(5):2343- 2352.
[26] Javad E H, Alireza N E. Increased photocatalytic activity of Zn(II)/Cu(II) oxides and sulfides by coupling and supporting them onto clinoptilolite nanoparticles in the degradation of benzophenone aqueous solution [J]. Journal of Hazardous Materials, 2016,316: 194-203.
[27] Meng L R, Yin W H, Wang S S, et al. Photocatalytic behavior of biochar-modified carbon nitride with enriched visible-light reactivity [J]. Chemosphere, 2020,239:124713.
[28] Ong W J, Putri L K, Tan Y C, et al. Unravelling charge carrier dynamics in protonated g-C3N4interfaced with carbon nanodots as co-catalysts toward enhanced photocatalytic CO2reduction: A combined experimental and first-principles DFT study [J]. Nano Research, 2017,10(5):1673-1696.
[29] Xiao Y, Lyu H H, Yang C L, et al. Graphitic carbon nitride/biochar composite synthesized by a facile ball-milling method for the adsorption and photocatalytic degradation of enrofloxacin [J]. Journal of Environmental Science, 2021,103:93-107.
[30] Tan Y G, Shu Z, Zhou J, et al. One-step synthesis of nanostructured g-C3N4/TiO2composite for highly enhanced visible-light photocatalytic H2evolution [J]. Applied Catalysis B: Environmental, 2018,230:260-268.
[31] Lu W Y, Xu T F, Wang Y, et al. Synergistic photocatalytic properties and mechanism of g-C3N4coupled with zinc phthalocyanine catalyst under visible light irradiation [J]. Applied Catalysis B: Environmental, 2016,180:20-28.
[32] Yang L, Bai X, Shi J, et al. Quasi-full-visible-light absorption by D35-TiO2/g-C3N4for synergistic persulfate activation towards efficient photodegradation of micropollutants [J]. Applied Catalysis B: Environmental, 2019,256:117759.
[33] Xiao X, Hao R, Zuo X X, et al. Microwave-assisted synthesis of hierarchical Bi7O9I3microsheets for efficient photocatalytic degradation of bisphenol-A under visible light irradiation [J]. Chemical Engineering Journal, 2012,209:293-300.
[34] 赖树峰,梁锦芝,肖开棒,等.Ag改性石墨相氮化碳(g-C3N4)可见光辅助活化过一硫酸盐降解罗丹明B [J]. 环境科学学报, 2021,41(5): 1847-1858.
Lai S F, Liang J Z, Xiao K B, et al. Visible light assisted peroxymonosulfate activation on Ag modified graphite phase carbon nitride (g-C3N4) for Rhodamine B degradation [J]. Acta Scientiae Circumstantiae, 2021,41(5):1847-1858.
[35] Xie P C, Ma J, Liu W, et al. Removal of 2-MIB and geosmin using UV/persulfate: contributions of hydroxyl and sulfate radicals [J]. Water Research, 2015,69:223-233.
[36] Zhu K X, Wang J H, Wang Y J, et al. Visible-light-induced photocatalysis and peroxymonosulfate activation over ZnFe2O4fine nanoparticles for degradation of Orange II [J]. Catalysis Science & Technology, 2016,6(7):2296-2304.
[37] Yang L M, Yu L E, Ray M B. Degradation of paracetamol in aqueous solutions by TiO2photocatalysis [J]. Water Research, 2008,42(13): 3480-3488.
[38] Hu L M, Zhang G S, Liu M, et al. Enhanced degradation of Bisphenol A (BPA) by peroxymonosulfate with Co3O4-Bi2O3catalyst activation: Effects of pH, inorganic anions, and water matrix [J]. Chemical Engineering Journal, 2018,338:300-310.
[39] Ghauch A, Tuqan A M, Kibbi N, et al. Methylene blue discoloration by heated persulfate in aqueous solution [J]. Chemical Engineering Journal, 2012,213:259-271.
[40] Xu L, Yang L, Bai X, et al. Persulfate activation towards organic decomposition and Cr(VI) reduction achieved by a novel CQDs- TiO2−x/rGO nanocomposite [J]. Chemical Engineering Journal, 2019, 373:238-250.
[41] Liu Y, Guo H, Zhang Y, et al. Heterogeneous activation of persulfate for Rhodamine B degradation with 3D flower sphere-like BiOI/Fe3O4microspheres under visible light irradiation [J]. Separation and Purification Technology, 2018,192:88-98.
Study on photocatalytic performance of cephalotaxus shell biochar/g-C3N4activated persulfate.
ZHANG Ting-ting1, XU He1*, CAI Dong-qing1, CHEN Shi-yan2, WANG Hua-ping2
(1.College of Environmental Science and Engineering, Donghua University, Shanghai 201620, China;2.State Key Laboratory for Modification of Chemical Fibers and Polymer Materials, Donghua University, Shanghai 201620, China)., 2022,42(3):1146~1156
g-C3N4/biochar composite photocatalysts with high catalytic activity were prepared by a simple one-pot thermal polymerization method using cephalotaxus shell and melamine as raw materials, which was applied to activate peroxynitrite (PS) for the degradation of acetaminophen (AAP) wastewater under visible light. The optical properties of the composite catalyst were investigated by UV-vis diffuse reflectance absorption spectroscopy (UV-vis DRS) and photoluminescence spectroscopy (PL), which showed that the visible light absorption boundary of g-C3N4was enhanced from 483nm to 553nm and improved the separation efficiency of photogenerated electron-hole pairs due to the introduction of biochar. The results of scanning electron microscopy (SEM), X-ray diffraction spectroscopy (XRD), Fourier transform infrared spectroscopy (FT-IR) and X-ray photoelectron spectroscopy (XPS) showed that the microstructure of g-C3N4was improved by the introduction of biochar. The removal efficiency of AAP was enhanced by the introduction of persulfate into the reaction system. The results show that the degradation rate for AAP under visible light irradiation was 8.9 times higher than that without PS addition, indicating that the catalytic system can effectively activate PS to produce more highly reactive oxidants. The radical capture experiments showed the presence of ·O2-, h+, ·OH and ·SO4-reactive substances in the catalytic system. The improvement of composite material performance was attributed to the effective inhibition of electron-hole recombination by biochar as an electron acceptor.
visible-light photocatalysis;persulfate activation;biochar;acetaminophen
X703.5
A
1000-6923(2022)03-1146-11
张婷婷(1998-),女,陕西渭南人,东华大学硕士研究生,主要研究方向为光催化水处理应用.发表论文1篇.
2021-07-27
中国科学院服务项目(KFJ-STS-QYZD-199);广东省重点研发项目(2020B0202010005)
*责任作者, 副教授, hexu@dhu.edu.cn

