臭氧在中试规模污泥原位减量中的应用
孙相娟,刘宾寒,张领军,Kyohei Aketagawa,薛斌杰,任银姬,白建峰,詹 咏,陈思思,董 滨*
臭氧在中试规模污泥原位减量中的应用
孙相娟1,刘宾寒2,张领军2,Kyohei Aketagawa3,薛斌杰4,任银姬4,白建峰5,詹 咏2,陈思思1,董 滨1*
(1.同济大学环境科学与工程学院,上海 200092;2.上海理工大学环境与建筑学院,上海 200093;3.三菱电机(日本)技术研发中心,兵库县 661-8661;4.三菱电机(中国)有限公司上海分公司,上海 200336;5.上海第二工业大学WEEE研究中心,上海 201209)
为探究高、低浓度臭氧旁路处理对中试系统出水水质、污泥减量率的影响,采用两组系统(对照组:厌氧/缺氧/好氧(A/A/O),试验组:A/A/O+臭氧旁路处理)在5个工况下运行183d.结果表明,利用剂量为13mg/g MLSS (25mg/g MLVSS)臭氧处理占生物反应池容积20%的回流污泥时,系统运行性能良好;在此操作条件下,低浓度臭氧(150mg/L)和高浓度臭氧(380mg/L)处理均可使出水COD, NH4+-N, TN达到《城镇污水处理厂污染物排放标准》(GB18918-2002)的一级B标准;且与低浓度臭氧处理相比,高浓度臭氧处理出水污染物去除率下降的比例较低,即高浓度臭氧处理在对污水污染物去除方面表现出较大的优势.低浓度臭氧处理适宜SRT为25d,此时污泥有机物减少率为14.07%,剩余污泥总量减少率为8.33%;高浓度臭氧处理适宜SRT为75d,此时污泥有机物减少率为41.53%,剩余总量减少率为25.92%,即相同臭氧剂量条件下,高浓度臭氧处理的污泥减量效率明显优于低浓度臭氧.低温对高浓度臭氧处理减量率和出水水质的影响并不显著,说明A/A/O+高浓度臭氧系统的应用不受温度的大幅限制.
污泥原位减量;高浓度臭氧处理;厌氧/缺氧/好氧过程;中试
活性污泥法是目前使用最广泛的污水处理技术之一,剩余污泥是活性污泥法的副产物.截至2018年,我国县级以上城市污水处理厂污泥量已达到6765万t(含水率80%计),且每年以5%~8%的比例增长,预计2020~2025年间,我国污泥年产量将突破8000万t(含水率80%计)[1].剩余污泥的处理处置费用昂贵,约占污水处理厂总运营成本的50%~60%[2].因此,为了降低其运输和后续处理处置的费用,污泥的原位减量,即从源头最大限度地减少剩余污泥的产量,近年来得到了广泛的关注,其主要原理有溶胞-隐性生长,解偶联代谢,微生物捕食等[3-4].污泥臭氧原位减量技术,利用强氧化性的臭氧处理部分回流污泥(RAS),使微生物细胞裂解并释放胞内物质(溶胞过程);臭氧化后的RAS再回流到生物反应池内作为基质被微生物利用(隐性生长过程),以达到剩余污泥减量的目的[5].研究表明,使用剂量为30~100mg O3/g TSS的臭氧处理RAS后,污泥原位减量率可达40%~80%[5].本文前期研究也表明经臭氧旁路处理后,污水处理系统出水的COD,氨氮(NH4+-N),总氮(TN)基本不受臭氧处理的影响,或出水浓度略有上升,但仍然可以保证出水水质达到《城镇污水处理厂污染物排放标准》(GB18918-2002)的一级B标准[4,6]; Qiang等[3]利用臭氧处理实现了85%的污泥减量率,但排泥量减少使出水总磷(TP)浓度从0.1mg/L上升至2mg/L.基于以上研究现状,目前臭氧在污泥原位减量系统的研究大多停留在小试阶段,因此,其在中试系统中的效果及对出水水质的影响仍需进一步探究.
由于污泥臭氧化成本高,必须追求工艺的优化[7].臭氧剂量和污泥浓度将大幅影响臭氧对污泥的溶解效率(20%~70%),进而影响污泥的原位减量效率[4].同时,由于臭氧与底物之间的反应为两阶段或三阶段的一级动力学,因此除上述2个因素外,臭氧浓度和臭氧流速也是决定臭氧化效率的主要因素[8-9].目前,常见的臭氧发生器最大臭氧浓度均在150mg/L以内,以往研究中应用的臭氧浓度大多局限于此范围[7,10].目前,已有臭氧浓缩器可将臭氧浓度进一步提高到800mg/L以上[11].臭氧浓度增加时,由于其传质更快,气液平衡浓度更高,可形成更多的羟基自由基[12],有望提高污泥的溶解效率,提高污泥减量率,最终在相同的臭氧剂量下进一步提高系统效率.然而,鲜有研究关注臭氧浓度提升至150mg/L以上对污泥原位减量效率的影响.因此,为了对比分析相对较高(380mg/L)和较低(150mg/L)浓度的臭氧对污泥原位减量效率的影响,本文采用两组中试系统(对照组:厌氧/缺氧/好氧(A/A/O),试验组:A/A/O+臭氧处理)共运行183d,探究臭氧剂量相同,臭氧浓度由150mg/L提升至380mg/L时,臭氧旁路处理对剩余污泥减量,出水水质的影响;分析较高浓度臭氧处理系统在高,低温条件下的运行效果,旨在为较高浓度臭氧处理技术的实际工程应用提供中试验证,为臭氧原位减量技术的优化提供新方向.
1 材料和方法
1.1 试验装置
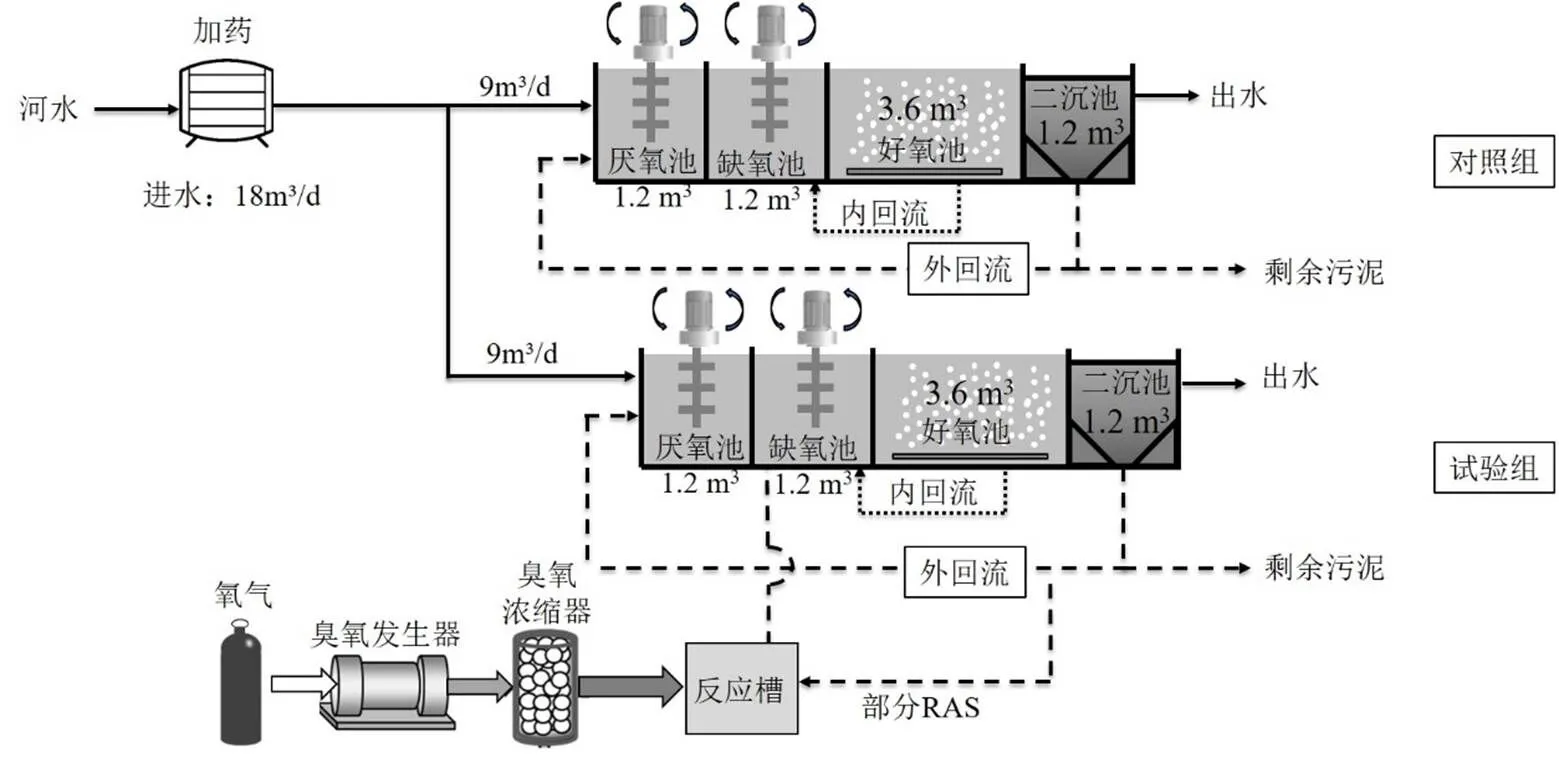
图1 臭氧原位减量中试装置运行示意
中试系统运行装置如图1所示,系统包含2组相同的A/A/O装置(厌氧池:1200L,缺氧池1200L,好氧池3600L,二沉池1200L).对照组(A/A/O)和试验组(A/A/O+臭氧处理)同时运行,对照组的RAS不进行臭氧处理,试验组的部分RAS通过臭氧处理后返回到缺氧池.A/A/O的进水水量为9.0m³/d,水力停留时间 (HRT)为16h,污泥内回流比150%,剩余污泥回流比50%.缺氧池和好氧池的溶解氧(DO)分别通过搅拌和曝气装置控制在0.4~0.5mg/L和2.0~ 2.5mg/L.
污泥臭氧化装置由臭氧发生器,臭氧浓缩器,圆柱形有机玻璃反应槽(内径20cm,高60cm)以及必要的臭氧探测器(调整臭氧剂量)组成,臭氧通过射流器与回流污泥混合,混合物进入反应槽内充分接触后通过上部的溢流管回流至缺氧池内,该系统装置由某公司提供.
1.2 试验用水
中试系统进水采用人工配水,2组系统共用一套配水储罐,将中试现场附近的河水泵入进水罐,并向罐中投加乙酸钠,葡萄糖,蔗糖和淀粉,氯化铵和磷酸二氢钾分别作为碳源,氮源和磷源,投加量分别为(mg/L):CH3COONa:100,C6H12O6:200,蔗糖:200,淀粉:200,NH4Cl:225和KH2PO4:18;投加(mg/L): CaCl2·2H2O:0.37, MgSO4·7H2O:5,MnCl2·4H2O:0.28, ZnSO4·7H2O:0.45,FeCl3:1.45,CuSO4·5H2O:0.4,CoCl2·6H2O:0.4以补充微量元素.
1.3 试验过程
中试系统接种泥来自上海某污水厂的二沉池,试验开始前在温度20~25℃,泥龄15d下培养30d,使两组生物反应池MLSS基本稳定在3000mg/L.中试系统运行分为5个阶段,分别为LI(0~12d),LII (28~ 45d),LIII(46~65d),HI(81~118d),HII(147~183d).不同工况的具体操作参数如表1所示. LI,LII和LIII均用低浓度臭氧处理(150mg/L;水温20~25℃),臭氧从臭氧发生器产生后直接由射流器通入RAS中.根据本团队薛冰等[6]的小试结果,臭氧处理的RAS量为SBR反应器总污泥量的10%时可以达到较好的出水水质和减量效果.为了在中试规模进行试验验证和进一步探究,在LI工况下,臭氧处理RAS总量为3200L (生物池污泥量的53.3%);在LII工况下,臭氧处理RAS总量为1200L (生物池污泥量的20%);LIII与LII的臭氧处理参数相同,但排泥由240L/d减少至80L/d.
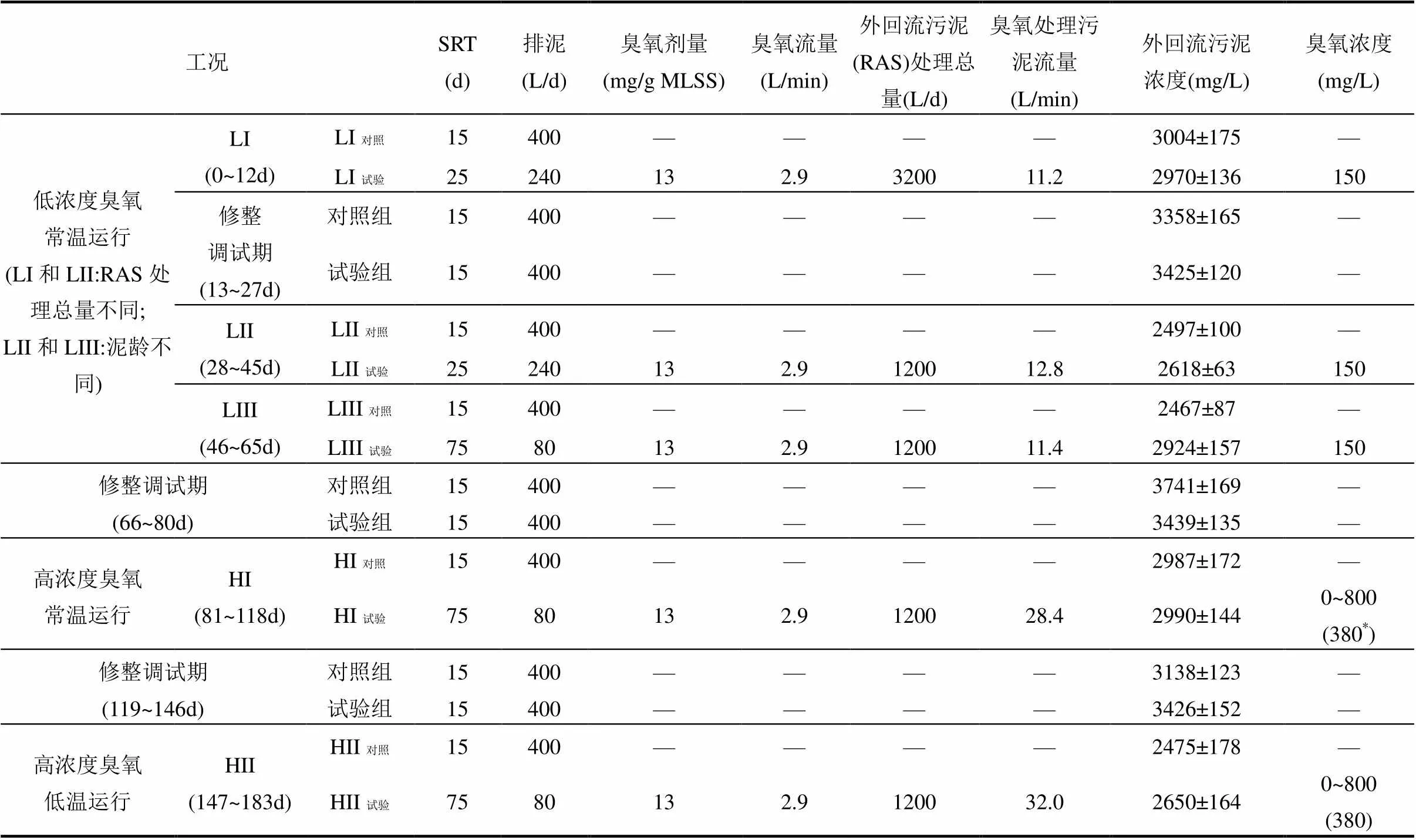
表1 中试系统运行参数设置
注:“—”表示此操作阶段没有臭氧注入;*表示平均值.实际操作过程中,一个臭氧处理循环内,臭氧在臭氧浓缩器内浓缩后进入反应槽,一般在3min时达到臭氧浓度最大值(800mg/L),稳定在最大臭氧浓度一定时间后浓度逐渐降低,直至臭氧处理停止.
HI和HII采用高浓度臭氧处理(平均浓度380mg/L),臭氧从臭氧发生器产生再由臭氧浓缩器浓缩后通入RAS中.在HI工况下,臭氧处理RAS总量为1200L (生物池污泥量的20%),排泥量为80L/d,水温为20~25℃;为了探究高浓度臭氧处理系统在低温下的运行情况,HII的水温降低至7.8~16.8℃,其他参数与HI工况相同.根据文献调研[4,6]和预实验结果,低浓度臭氧处理初始减量率设定为40%,高浓度初始减量率设定为80%,因此排泥分别由对照组的400L减少至240和80L.
1.4 分析方法
每天收集中试系统进出水和好氧池内的活性污泥样品,分别用于测定COD,NH4+-N,TN,TP,SS和MLSS,MLVSS.常规指标测定参照薛冰等[6]的方法:COD采用重铬酸钾法;TN 采用过硫酸钾氧化-紫外分光光度法;NH4+-N采用纳氏试剂分光光度法;TP 采用钼锑抗分光光度法测定 PO43--P,再换算成TP含量;进水温度采用便携式测定仪;污泥样品MLSS采用重量法;MLVSS 采用马弗炉测定.
负荷(,以COD/MLSS计)是影响有机物降解和活性污泥增长的重要因素[13],按照下式计算.
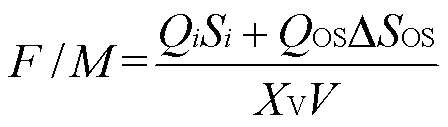
式中:Q为每日进水水量, L/d;S为每日进水COD浓度, mg/L;OS为臭氧处理的RAS量, L/d;DOS为臭氧处理后RAS增加的SCOD浓度, mg/L;V为生物反应池内的污泥浓度, mg/L;为生物反应池容积, m3.
其中,DOS按照下式计算.
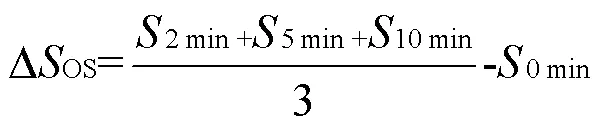
式中:0min,2min,5min,10min,分别为臭氧处理RAS 0, 2, 5, 10min时SCOD的浓度. RAS经过高浓度和低浓度臭氧处理后的DOS分别为(127±38),(195± 35)mg/L.
2 结果与讨论
2.1 不同工况下出水水质的变化
如图2和表2所示,在5个工况下,中试系统进水COD,NH4+-N,TN,TP浓度基本保持在358~361, 39.2~41.7,51~53,4.1~4.3mg/L.H I工况正值雨季,河水的SS升高,导致系统进水的SS较高.在中试系统运行的183d内,对照组出水COD,NH4+-N,TN,TP浓度均可达到《城镇污水处理厂污染物排放标准》(GB18918-2002)的一级B标准(COD:60,NH4+-N: 8,TN:20,TP:1mg/L),且对COD,NH4+-N,TN,TP去除率超过91%,91%,75%,85%,表明系统运行稳定且具有良好的有机物去除能力和脱氮除磷效能,因此对照组可以作为试验组在不同工况下运行结果的参考.
2.1.1 低浓度臭氧研究结果 在LI工况下, 臭氧每日处理的RAS为整个生物反应池容积的55.3%.此时出水COD, TN, TP的平均浓度为65, 20, 1.7mg/L,并未达到一级B标准.说明尽管臭氧剂量保持在13mg O3/g MLSS (25mg O3/g MLVSS),但臭氧处理的RAS量过多,可能导致较多的微生物细胞裂解死亡,释放的COD,TN和TP超过系统的有机负荷[3];并导致系统本身具有污染物去除能力的微生物量下降和活性降低[14], 致使出水水质超标.因此,臭氧处理的RAS量是系统能否稳定运行的关键因素,处理超过合适范围的RAS不仅会使整个系统运行崩溃,也浪费臭氧,经济性较差.
经过15d的调试,对照组和试验组的运行情况基本一致后,在低浓度臭氧处理下连续运行了另外两个工况(LII和LIII).LII在LI工况的基础上,将臭氧处理的RAS量由整个生物反应池容积的53.3%降至20%;在LII工况的基础上,将LIII试验组污泥龄延长至75d.结果发现,LII试验的去除率相对LIII试验略高(LII试验:COD 91.45%,NH4+-N 97.18%,TN 74.83%,TP 58.39%;LIII试验:COD 91.03%,NH4+-N 94.49%,TN 73.92%,TP 53.49%),且都低于相应对照组的去除率,其去除率下降百分比见表2.低浓度臭氧处理导致COD,NH4+-N,TN去除率略微下降的结果与之前的研究结果吻合[3-5].可能是由于臭氧处理导致污泥中有机氮释放,增加了进入生物反应池的NH4+-N和TN[3-4],但臭氧对生物反应池内的硝化菌群落并无明显影响[3],因此出水仍然可以达标.LII试验与LIII试验出水TP平均浓度分别为1.7和1.9mg/L,去除率下降百分比分别为31.35%和37.72%.这是由于LII试验,LIII试验的排泥量分别为240和80L,而LII对照, LIII对照的排泥量为400L,排泥量减少使磷在系统内累积,导致出水TP超标[3].
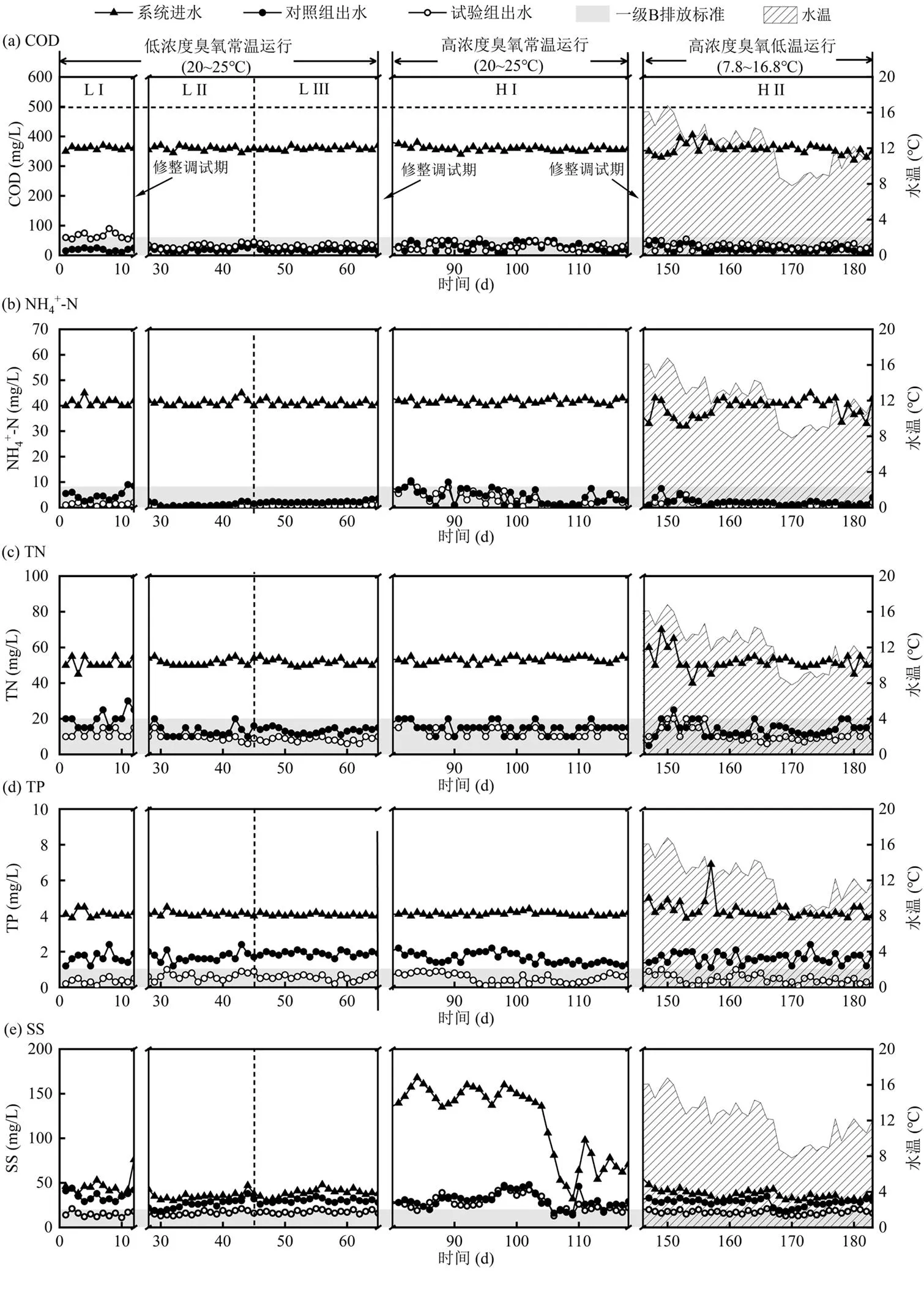
图2 不同工况下中试系统进出水 COD, NH4+-N, TN, TP, SS的浓度变化
(a) COD; (b) NH4+-N; (c) TN; (d) TP; (e)SS
2.1.2 高浓度臭氧研究结果 在系统转变为高浓度臭氧处理前,对照组和试验组在相同的条件下培养15d,基本稳定后向RAS中注入高浓度臭氧,并在HI(81~118d)工况下连续运行38d. HI试验的COD去除率与HI对照相比并无明显差异(去除率下降百分比为0.40%); NH4+-N, TN, TP的去除率下降百分比分别为2.12%, 5.71%, 30.61%,除NH4+-N去除率下降百分比略高于LII外, TN和TP的去除率下降百分比均低于LII和LIII(表2).这说明高浓度臭氧处理后系统对有机物和氮磷的去除效果比低浓度臭氧处理好,高浓度臭氧处理对整个A/A/O系统的影响更小.即水温保持在20~25℃时,同样臭氧剂量下,高浓度臭氧处理的出水水质比低浓度臭氧处理显示出较强的优势,尤其是对COD和TP的去除效果.

表2 中试系统进出水COD, NH4+-N, TN, TP, SS的浓度及去除率均值
注: “—”表示SS不进行去除率计算;去除率下降百分比(%)= (对照组去除率-试验组去除率) /对照组去除率´100%.
由于污水处理厂生化过程受低温影响较大[15-16],因此在低温下“A/A/O+臭氧处理”系统能否稳定运行也是评估该技术实际应用的关键因素.经过29d的修整调试,进入冬季后,生物反应池的水温降低至7.8~16.8℃.HII工况水温和各项水质指标的变化如图2所示.与HI相比,低温下HII试验去除率下降百分比有所增加,分别为COD:3.06%,NH4+-N: 2.30%,TN:7.96%和TP:31.53%.说明低温对高浓度臭氧处理有轻微抑制作用,可能是由于低温下生物反应池内的微生物活性较低,对臭氧处理后释放的有机物和氮磷的利用速率降低[3,15].但是出水COD, NH4+-N,TN浓度依旧可达到《城镇污水处理厂污染物排放标准》(GB18918-2002)的一级B标准(COD: 60,NH4+-N:8,TN:20,TP:1mg/L).
综上所述,低浓度臭氧处理在排泥量为240L (LII)工况下对污染物的去除能力更强,尽管排泥量为80L时减少了剩余污泥量,但其出水水质也相应变差,因此从出水水质的角度,低浓度臭氧处理更适合240L的排泥量;而高浓度臭氧处理在排泥80L时出水水质仍然可以保持相对较好的水平,且其在低温下的出水水质也可达到一级B排放标准,因此高浓度臭氧处理在对污水污染物去除方面表现出较大的优势.
然而,臭氧处理后出水的TP含量均高于一级B排放标准,这是由于臭氧处理使部分回流污泥溶解,并释放其中的有机磷和无机磷,使出水的TP浓度升高[3,17].为了降低出水TP的浓度,并有效回收磷资源,可以通过以下几种方式与高浓度臭氧处理耦合:(1)化学结晶法.在臭氧反应槽后接厌氧释磷池,未经臭氧处理的回流污泥在此利用部分碳源,聚磷菌将多聚磷酸盐分解为无机磷释放至液相,再经过“沉淀池”,“磷结晶池”将磷与Mg或Ca的结晶产物回收[17];在Tsuno等[18]的中试中,该装置的磷回收率达到75%,出水磷浓度保持在1mg/L以下.(2)吸附法. Suzuki等[19]采用ZrFe2(OH)8可吸附进水磷的85%,并回收吸附量的80%.因此,在高浓度臭氧处理使污泥减量的基础上,添加“磷回收”单元,可减少出水TP浓度,使其达到排放标准,并可回收污泥中的磷资源.
2.2 不同工况下F/M的变化

表3 中试系统不同工况的F/M
注:中试系统不同阶段BOD5/COD均为0.3.
/是影响有机物降解和活性污泥增长的重要因素[20-21],/低于0.15g BOD5/(g MLSS×d)时,COD降解速率的关系符合莫诺(Monod)方程,即/越高,COD降解速度越快[22].由于LI臭氧处理的RAS较多(3200L),/从0.180kg COD/(kg MLSS×d)上升至0.205kg COD/(kg MLSS×d),微生物降解COD的速度加快,但仍然不能将RAS增加的DOS完全降解,从而导致出水水质超标;LII工况的/变化并不明显,此时微生物的活性变化不大,未被微生物完全利用的DOS导致出水COD略有增加;LIII试验的/由0.220kg COD/(kg MLSS×d) (LIII对照)下降至0.191kg COD/(kg MLSS×d),COD降解速率变慢,因此与LII工况相比,LIII工况的出水水质相对恶化,说明与排泥80L相比,低浓度臭氧更适合排泥量为240L的工况.
HI工况下,HI试验的/由0.180kg COD/(kg MLSS×d)(HI对照)上升至0.192kg COD/(kg MLSS×d),此工况下高浓度臭氧处理后RAS的DOS浓度更高,升高的/使COD降解速率进一步加快[22],这印证了HI试验的COD去除率与HI对照基本相同的结果,并进一步说明与低浓度臭氧处理相比(LII,LIII),H I工况生物反应池的微生物降解COD的能力更强.HII试验的/与HII对照基本相同,但HII试验的出水水质却明显差于HII对照,说明低温运行影响了高浓度臭氧处理系统对COD降解速率的加强,即低温对高浓度臭氧处理系统存在抑制作用.
2.3 不同工况下的污泥减量效果
2.3.1 不同工况下MLSS和MLVSS/MLSS变化 如图3所示,在5个工况下系统内污泥的MLVSS/MLSS基本稳定在0.60~0.62之间.通常,SRT的延长会导致生物反应器MLSS升高[20].低浓度臭氧处理下,LI和LII工况对照组排泥400L,试验组排泥240L,但对照组和试验组MLSS并无明显差异,说明排泥量由400L(LI对照,LII对照)减少至240L(LI试验, LII试验)是由低浓度臭氧处理引起的.LIII工况进一步将排泥量减少至80L,其他操作参数不变,此时LIII试验的MLSS从2618mg/L逐渐上升至2924mg/L,5d后基本稳定.LIII试验中F/M下降(2.2节)和MLSS上升是延长SRT的明显特征[20],暗示了LIII比LII减少的排泥量主要由人为延长SRT得到[20],臭氧的作用并不占主导地位.而人为延长SRT时会导致出水水质恶化[23-24],韦佳敏等[20]将其延长至25d时,系统脱氮除磷受到抑制,这与本研究中LIII试验对污水中污染物去除率比LII试验低的结果相互印证.
在高浓度臭氧处理阶段,HI对照和HI试验的MLSS并无明显差异,分别为2987和2990mg/L,结合2.1,2.2节的结果,可以发现LIII延长SRT导致生物反应池内MLSS浓度升高,F/M降低,出水水质严重恶化[20]的现象并未在高浓度臭氧处理下出现,说明HI工况排泥量减少不是由人为延长SRT引起的,高浓度臭氧处理是其主要原因.HII对照和HII试验的MLSS分别为2475和2650mg/L,即低温下试验组的MLSS比对照组略有上升,赵丰等[22]也发现温度在9.5~13.7℃时,臭氧中试系统生物反应池的MLSS浓度与温度呈现负相关,这进一步说明低温是影响高浓度臭氧处理系统的污泥减量率的关键因素.
2.3.2 不同工况下中试系统的质量平衡 由于中试系统实际运行搅拌装置的限制,两组生物反应器均出现部分污泥沉积.无机物可能会在沉积污泥中累积[5],以往的减量率计算并未涉及生物反应池的沉积污泥[23,26].为了进一步得到准确的污泥减量率,根据无机物守恒原则对中试系统进行质量平衡计算(表4).结果表明,在低浓度臭氧处理阶段,LI,LII的有机物减少率和总量减少率基本相同,分别为13.82%,8.51%(LI)和14.07%,8.33%(LII),说明低浓度臭氧处理可使有机物有效降低[3,5].LIII的有机物减少率和总量减少率分别为31.02%和18.19%.由于与L II的减量率相比,L III工况增加的减量率主要由延长SRT获得,因此LII工况的减量率更能代表低浓度臭氧处理的真实效果.
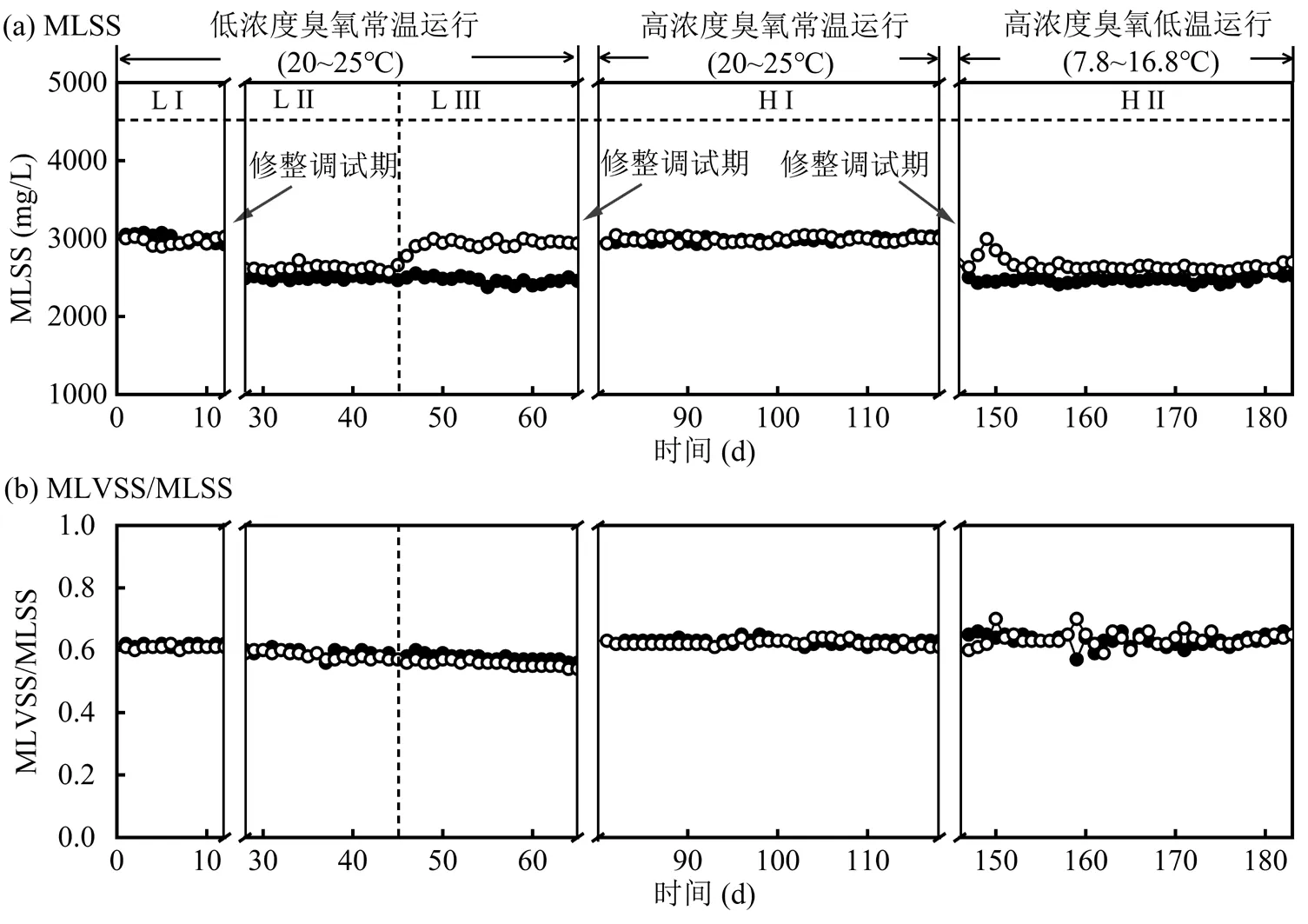
图3 中试系统5个工况生物反应池MLSS和MLVSS/MLSS变化
(a) MLSS; (b) MLVSS/MLSS

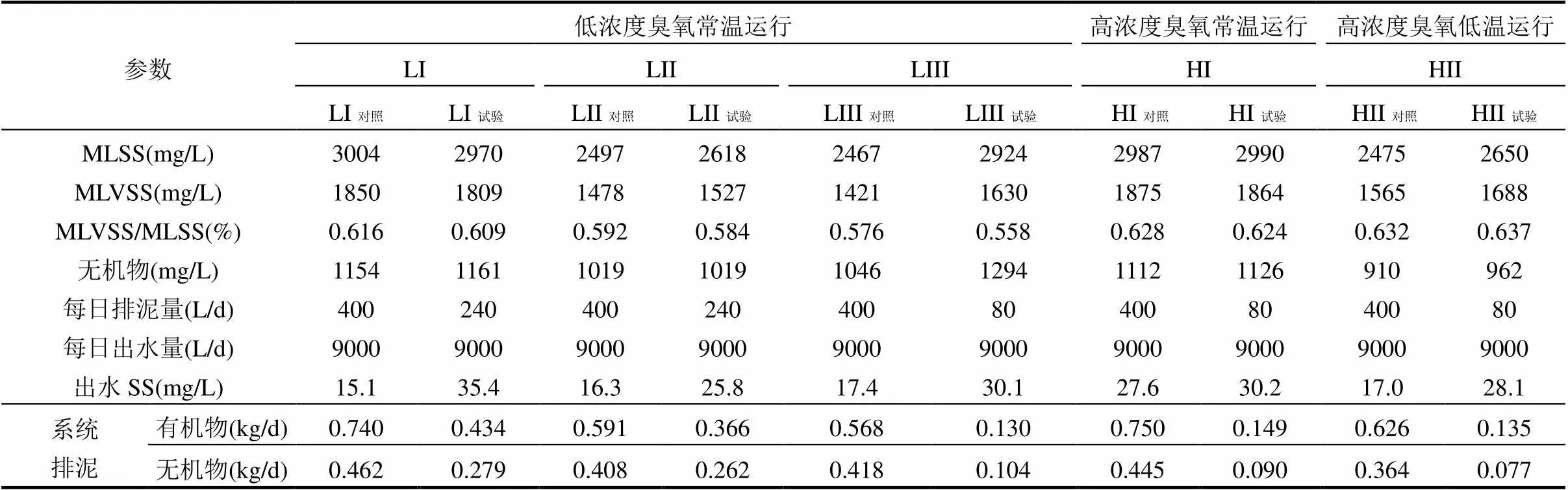
表4 不同工况下中试系统质量平衡计算

续表4
注:无机沉积物增加量=对照组无机物总排放量-试验组无机物总排放量;有机沉积物增加量=(无机沉积物增加量/(1-VS/TS))*VS/TS;剩余污泥有机物减少率=(对照组有机物总排放量-试验组有机物总排放量-有机沉积物增加量)/对照组有机物总排放量×100%;剩余污泥总量减少率=(对照组有机物总排放量+对照组无机物总排放量-试验组有机物总排放量-试验组无机物总排放量-有机沉积物增加量-无机沉积物增加量)/(对照组有机物总排放量+对照组无机物总排放量)×100%.
HI工况的有机物减少率和总量减少率分别为41.53%和25.92%,此工况下MLSS并未上升,说明高浓度处理产生的污泥减量可使该工况下的SRT自然延长至75d,因此高浓度臭氧处理在该工况下的实际减量率即为41.53%(有机物减少率)和25.92%(总量减少率).HII的有机物减少率和总量减少率分别为37.69%和23.83%,说明低温对实际减量率有轻微影响.综上所述,高浓度臭氧处理使剩余污泥相比于低浓度臭氧大幅减量,优势显著.
3 结论
3.1 利用13mg/g MLSS (25mg/g MLVSS)剂量臭氧处理占生物反应池容积20%的回流污泥时,系统运行性能良好;在此操作条件下,低浓度臭氧(150mg/L)处理和高浓度臭氧(380mg/L)处理均可使出水COD, NH4+-N, TN达到《城镇污水处理厂污染物排放标准》(GB18918-2002)的一级B标准.高浓度臭氧处理在对污水污染物去除方面表现出较大的优势;但经高,低浓度臭氧处理后,系统排泥量减少使出水的TP浓度为1.6~1.9mg/L,即P的去除是臭氧原位减量技术应用的限制因素.可以通过臭氧原位污泥减量耦合化学沉淀法或吸附法回收部分磷资源.
3.2 低浓度臭氧处理适宜的SRT为25d,此时污泥有机物减少率为14.07%,剩余污泥总量减少率为8.33%;高浓度臭氧处理适宜的SRT为75d,此时污泥有机物减少率为41.53%,剩余总量减少率为25.92%,即相同剂量条件下,高浓度臭氧处理的污泥减量效率明显优于低浓度臭氧.
3.3 低温对高浓度臭氧处理的减量率和出水水质存在影响,但影响并不显著,这说明“A/A/O+高浓度臭氧”系统的应用不受温度的大幅限制.因此,“A/A/ O+高浓度臭氧”在适用性上具备优势.
[1] 戴晓虎,李小伟,杨 婉,等.污水处理厂污泥中病毒的赋存特性及处理处置过程中暴露风险防控研究进展 [J]. 给水排水, 2020,56(3): 60-73.DOI:10.13789/j.cnki.wwe1964.2020.03.011.
Dai X H, Li X W, Yang W, et al. Virus in sewage from wastewater treatment plant: Occurrence and potential risk during sludge treatment and disposal [J]. Water & Wastewater Engineering, 2020,56(3):60-73. DOI:10.13789/j.cnki.wwe1964.2020.03.011.
[2] Campos J L, Otero L, Franco A, et al. Ozonation strategies to reduce sludge production of a seafood industry WWTP [J]. Bioresource Technology, 2009,100(3):1069-1073.
[3] Qiang Z, Wang L, Dong H, et al. Operation performance of an A/A/O process coupled with excess sludge ozonation and phosphorus recovery: A pilot-scale study [J]. Chemical Engineering Journal, 2015, 268:162-169.
[4] Semblante G U, Hai F I, Dionysiou D D, et al. Holistic sludge management through ozonation: A critical review [J]. Journal of Environmental Management, 2017,185:79-95.
[5] Chu L, Yan S, Xing X, et al. Progress and perspectives of sludge ozonation as a powerful pretreatment method for minimization of excess sludge production [J]. Water Research, 2009,43(7):1811-1822.
[6] 薛 冰,刘宾寒,韦婷婷,等.基于臭氧旁路处理的污泥原位减量技术工艺[J]. 环境科学, 2021,42(5):2402-2412.
Xue B, Liu B H, Wei T T, et al. In-situ sludge reduction technology based on ozonation [J]. Environmental Science, 2021,42(5):2402- 2412.
[7] Manterola G, Uriarte I, Sancho L. The effect of operational parameters of the process of sludge ozonation on the solubilisation of organic and nitrogenous compounds [J]. Water Research, 2008,42(12):3191-3197.
[8] Buffle M O, Schumacher J, Salhi E, et al. Measurement of the initial phase of ozone decomposition in water and wastewater by means of a continuous quench-flow system: application to disinfection and pharmaceutical oxidation [J]. Water Research, 2006,40(9):1884-1894.
[9] Nöthe T, Fahlenkamp H, Sonntag C. Ozonation of wastewater: rate of ozone consumption and hydroxyl radical yield [J]. Environmental Science & Technology, 2009,43(15):5990-5995.
[10] Park S L, Moon J D, Lee S H, et al. Effective ozone generation utilizing a meshed-plate electrode in a dielectric-barrier discharge type ozone generator [J]. Journal of Electrostatics, 2006,64(5):275- 282.
[11] Tabata Y, Okihara Y, Saitsu T, et al. Apparatus for producing high-concentration ozone gas and method of producing high- concentration ozone gas: U.S. Patent 8460435 [P]. 2013-6-11.
[12] Tizaoui C, Grima N. Kinetics of the ozone oxidation of Reactive Orange 16azo-dye in aqueous solution [J]. Chemical Engineering Journal, 2011,173(2):463-473.
[13] Wu D, Zhang Z, Yu Z, et al. Optimization of F/M ratio for stability of aerobic granular process via quantitative sludge discharge [J]. Bioresource Technology, 2018,252:150-156.
[14] Barbarroja P, Zornoza A, Aguado D, et al. A multivariate approach of changes in filamentous, nitrifying and protist communities and nitrogen removal efficiencies during ozone dosage in a full-scale wastewater treatment plant [J]. Environmental Pollution, 2019,252: 1500-1508.
[15] 茹 春,张 爽,路 晖,等.低温条件下污水处理厂的除污效果及运行调控分析[J]. 中国给水排水, 2021,37(9):1-6.
Ru C, Zhang S, Lu H, et al. Pollutants removal performance and operation regulation of urban wastewater treatment plant under low temperature condition [J]. China Water & Wastewater, 2021,37(9):1-6.
[16] 韩文杰,吴 迪,周家中,等.长三角地区MBBR泥膜复合污水厂低温季节微生物多样性分析[J]. 环境科学, 2020,41(11):5037-5049.
Han W J, Wu D, Zhou J Z, et al. Microbial diversity analysis of WWTPs based on hybrid-MBBR process in a low temperature season in the Yangtze river delta [J]. Environmental Science, 2020,41(11): 5037-5049.
[17] Saktaywin W, Tsuno H, Nagare H, at al. Advanced sewage treatment process with excess sludge reduction and phosphorus recovery [J]. Water Rwsearch, 2005,39(5):902-910.
[18] Tsuno H, Arakawa K, Kato Y, at al. Advanced sewage treatment with ozone under excess sludge reduction, disinfection and removal of EDCs [J]. Ozone-Science & Engineering, 2008,30(3):238-245.
[19] Suzuki Y, Kondo T, Nakagawa V, at al. Evaluation of sludge reduction and phosphorus recovery efficiencies in a new advanced wastewater treatment system using denitrifying polyphosphate accumulating organisms [J]. Water Science and Technology, 2006, 53(6):107-113.
[20] 韦佳敏,黄慧敏,程 诚,等.污泥龄及pH值对反硝化除磷工艺效能的影响[J]. 环境科学, 2019,40(4):1900-1905.
Wei J M, Huang H M, Cheng C, et al. Effect of sludge retention time and pH on the denitrifying Phosphorus removal process [J]. Environmental Science, 2019,40(4):1900-1905.
[21] Jafari Kang A, Yuan Q. Long-term stability and nutrient removal efficiency of aerobic granules at low organic loads [J]. Bioresource Technology, 2017,234:336-342.
[22] 赵 丰,戴兴春,黄民生,等.负荷(F/M)对A2/O工艺脱氮影响的研究[J]. 水处理技术, 2009,35(7):59-63.
Zhao F, Dai X C, Huang M S, et al. Influence of BOD5loading (F/M) on nitrogen removal in A2/O process [J]. Technology of Water Treatment, 2009,35(7):59-63.
[23] Meng X, Liu D, Yang K, et al. A full scale anaerobic–anoxic–aerobic process coupled with low-dose ozonation for performance improvement [J]. Bioresource Technology, 2013,146:240-246.
[24] Ersu C B, Ong S K, Arslankaya E, et al. Impact of solids residence time on biological nutrient removal performance of membrane bioreactor [J]. Water Research, 2010,44(10):3192-3202.
[25] Lee J W, Cha H Y, Park K Y, et al. Operational strategies for an activated sludge process in conjunction with ozone oxidation for zero excess sludge production during winter season [J]. Water Research, 2005,39(7):1199-204.
[26] Nie Y, Qiang Z, Ben W, et al. Removal of endocrine-disrupting chemicals and conventional pollutants in a continuous-operating activated sludge process integrated with ozonation for excess sludge reduction [J]. Chemosphere, 2014,105:133-138.
Studies on the application of ozone in the pilot-scale-sludge reduction system.
SUN Xiang-juan1, LIU Bin-han2, ZHANG Ling-jun2, KYOHEI Aketagawa3, XUE Bin-jie4, REN Yin-ji4, BAI Jian-feng5, ZHAN Yong2, CHEN Si-si1, DONG Bin1*
(1.College of Environmental Science and Engineering, Tongji University, Shanghai 200092, China;2.School of Environment and Architecture, University of Shanghai for Science and Technology, Shanghai 200093, China;3.Mitsubishi Electric Corporation Advanced Technology R & D Center, Amagasaki-Shi, Hyogo 661-8661, Japan;4.Mitsubishi Electric (China) CO., LTD. Shanghai Branch, Shanghai 200336, China;5.WEEE Research Centre of Shanghai Second Polytechnic University, Shanghai 201209, China)., 2022,42(3):1128~1137
The effects of partial ozonation of returned sludge via high- and low-concentration ozone on effluent quality and sludge reduction rate in a pilot-scale system were explored. The pilot-scale system of anaerobic/anoxic/oxic (A/A/O)+ozonated sludge recycle (OSR) process was operated under 5conditions for 183days. This system showed superior operation performance when 20% of the total volume of returned sludge in the A/A/O module was treated by the dosage of 13mg/g MLSS (25mg/g MLVSS) per day. Under this condition, the COD, NH4+-N and TN of effluent could reach the first-class B standard of "Discharge standard of pollutants for municipal wastewater treatment plant" (GB18918-2002) with the treatment of both low- and high-concentration ozone (150mg/L and 380mg/L, respectively). In addition, compared with the low-concentration ozone treatment, the reduction in nutrients removal rate via high-concentration ozone treatment was lower, indicating the advantage of high-concentration ozone treatment in nutrients removal. The optimal SRT for low-concentration ozone treatment was 25days, and the reduction rate of organic matters in excess sludge was 14.07%, and of total excess sludge was 8.33%. The optimal SRT for high-concentration ozone treatment was 75days, and the reduction rates of organic matters and total excess sludge were 41.53% and 25.92%, respectively. At the same ozone dosage, the sludge reduction efficiency after high-concentration ozone treatment was obviously higher than that of low-concentration one. In addition, low temperature had no significant effect on the reduction rate and effluent quality when high-concentration ozone treatment was applied. Thus, the application of the "A/A/O+OSR" system was not significantly affected by temperature. The application of high-concentration ozone in WWTPs in this study provides practical guidance for the improvement of-sludge reduction technology.
-sludge reduction;high-concentration ozone treatment;anaerobic/anoxic/oxic process;pilot-scale
X703.1
A
1000-6923(2022)03-1128-10
孙相娟(1998-),女,满族,黑龙江绥化人,同济大学硕士研究生,主要从事污水污泥处理与资源化.发表论文1篇.
2021-08-23
同济大学与三菱电机联合研究项目“污泥减量处理系统示范试验联合研究”;国家重点研发计划项目(2020YFC1908704)
*责任作者, 教授, dongbin@tongji.edu.cn

