乌药汤挥发性成分提取工艺的优化
程媛 孙吴倩 刘明松 邓亚伟 段续红 李春花

中图分类号 R282 文献标志码 A 文章编号 1001-0408(2022)06-0712-06
DOI 10.6039/j.issn.1001-0408.2022.06.11
摘 要 目的 优化经典名方乌药汤挥发性成分的提取工艺。方法 在单因素实验的基础上,以有效成分乙酸龙脑酯、香附烯酮、α-香附酮、藁本内酯、去氢木香内酯含量及挥发油提取率的综合评分为指标,以提取时间、浸泡时间、液料比为响应因素,采用Box-Behnken设计-响应面法优化乌药汤挥发性成分的提取工艺并验证。在此基础上,再对药液的提取状态进行量化。结果 最优提取工艺为液料比13 ∶ 1(mL/g),浸泡时间0.5 h,暴沸状态下提取6 h。3次验证实验的综合评分分别为0.948 7、0.948 4、0.948 6(RSD=0.02%,n=3),与预测值(0.947 9)的偏差均不超过1%。以180 ℃油浴下药液的沸腾状态作为暴沸状态。结论 所得乌药汤挥发性成分最优提取工艺稳定、可行。
关键词 乌药汤;挥发性成分;提取工艺;Box-Behnken设计-响应面法
Optimization of the extraction technology of volatile components from Wuyao decoction
CHENG Yuan1,SUN Wuqian1,LIU Mingsong1,DENG Yawei1,DUAN Xuhong1,LI Chunhua1,2,3(1. College of Pharmacy, Hebei University of Traditional Chinese Medicine, Shijiazhuang 050090, China; 2. Hebei Higher Education Institute Applied Technology Research Center on TCM Formula Preparation/Hebei Technology Innovation Center of TCM Formula Preparation, Shijiazhuang 050090, China; 3. Hebei Industrial Technology Institute for Traditional Chinese Medicine Preparation, Shijiazhuang 050033, China)
ABSTRACT OBJECTIVE To optimize the extraction technology of volatile components from Wuyao decoction. METHODS On the basis of single factor investigation, the extraction technology of volatile components from Wuyao decoction was optimized and validated by Box-Behnken design-response surface technology using the contents of bomyl acetate, cyperotundone, α-cyperone, ligustilide and dehydrocostuslactone, extraction rate of volatile oil as indexes, with extraction time, soaking time and liquid-material ratio as factors. On this basis, the extraction state of the decoction was quantified. RESULTS The optimal extraction technology was as followed: the ratio of liquid-material was 13 ∶ 1 (mL/g), soaking time was 0.5 h, and the extraction time was 6 h in the boiling state. The comprehensive scores of the three validation experiments were 0.948 7, 0.948 4 and 0.948 6 respectively (RSD=0.02%, n=3), and the deviation from the predicted value (0.947 9) was no more than 1%. The boiling state of the decoction in 180 ℃ oil bath was taken as the sudden boiling state. CONCLUSIONS The optimized extraction technology is stable and feasible.
KEYWORDS Wuyao decoction; volatile components; extraction technology; Box-Behnken design-response surface technology
经典名方乌药汤由乌药、香附、木香、当归、甘草5味药组成,主治妇人血海疼痛[1]。现代研究表明,乌药汤中的乌药、香附、木香、当归均含有挥发性成分,对全方活血疏经作用的贡献较大[2-4]。传统汤剂可保留药材中挥发性成分的疗效,但也有研究指出,乌药汤水煎液中挥发性成分的含量较低,在制备成制剂的过程中,挥发性成分不断损失,难以發挥传统汤剂的疗效[5]。因此,本课题组考虑将该类药材单独提取后将所得挥发性成分包合入药,以最大程度地保留药效。
挥发性成分的有效收集和保留对提高乌药汤疗效和推动其现代研究至关重要。目前,水蒸馏法是收集挥发性成分的常用方法,其设备简单、成本低廉,是工业上最常用的提取方法[6]。本研究在单因素实验的基础上,以有效成分乙酸龙脑酯、香附烯酮、α-香附酮、藁本内酯、去氢木香内酯含量及挥发油提取率的综合评分为指标,以提取时间、浸泡时间、液料比为因素,结合Box-Behnken设计-响应面法优化乌药汤挥发性成分的提取工艺,旨在为该方的开发利用提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器包括7890B型气相色谱仪(美国Agilent公司),SPH-300型氢气发生器、SPB-3型全自动空气源(北京中惠普分析技术研究所),LQ-A10002型电子天平(上海乐祺精密电子厂),98-1B型电子调温电热套(天津市泰斯特仪器有限公司),YP2002型电子分析天平(上海津平科学仪器有限公司),DF-101S型集热式恒温加热磁力搅拌器(巩义市予华仪器有限责任公司)等。
1.2 主要药品与试剂
乌药饮片(批号20010301)、香附饮片(批号200501)、当归饮片(批号200601c155)、木香饮片(批号20100501)、甘草饮片(批号20092201)均购自河北安国药材市场,经河北中医学院侯芳洁副教授鉴定,分别为樟科植物乌药Lindera aggregata(Sims) Kosterm.的干燥块根、莎草科植物莎草Cyperus rotundus L.的干燥根茎、伞形科植物当归Angelica sinensis(Oliv.) Diels的干燥根、菊科植物木香Aucklandia lappa Decne.的干燥根、豆科植物甘草Glycyrrhiza uralensis Fisch.的干燥根,均符合2020年版《中国药典》(一部)标准[7]。
乙酸龙脑酯对照品(批号MUST-20081605,纯度97%)购自中国科学院成都生物研究所;去氢木香内酯对照品(批号MUST-19101209,纯度≥98%)、α-香附酮对照品(批号MUST-20052102,纯度≥98%)均购自成都曼斯特生物科技有限公司;香附烯酮对照品(批号Z1705241,纯度≥98%)购自成都草源康生物科技有限公司;藁本内酯对照品(批号RFS-G01001901005,纯度≥98%)购自成都瑞芬斯生物科技有限公司;甲醇(色谱纯)购自赛默飞世尔科技(中国)有限公司;其余试剂均为分析纯或实验室常用规格,水为超纯水。
2 方法与结果
2.1 挥发油提取率的测定
按照2020年版《中国药典》(四部)通则“2204挥发油测定法(甲法)”[8]提取挥发油:按处方比例称取乌药20 g,当归、甘草、木香各10 g,香附40 g,粉碎为最粗粉,置于2 000 mL圆底烧瓶中,加入12倍量水浸泡0.5 h,加热,暴沸提取6 h后停止加热,静置30 min,精密读取乌药汤挥发油提取量,计算提取率:提取率(%)=提取量(mL)/全粉质量(g)×100%。
2.2 乙酸龙脑酯、香附烯酮、α-香附酮、藁本内酯、去氢木香内酯的含量测定
参考文献[9],采用气相色谱法测定乙酸龙脑酯、香附烯酮、α-香附酮、藁本内酯、去氢木香内酯的含量。
2.2.1 色谱条件 色谱柱为Agilent HP-5毛细管柱(30 m×0.25 mm,0.25 μm);检测器为氢火焰离子化检测器,程序升温(起始温度为60 ℃;以10 ℃/min升温至110 ℃,保持1 min;以1 ℃/min升温至132 ℃,保持5 min;以0.2 ℃/min升温至133 ℃,保持5 min;以0.2 ℃/min升温至134 ℃,保持3 min;以5 ℃/min升温至220 ℃);检测器温度为260 ℃;载气为氮气;进样口温度为250 ℃;进样量为1 μL,分流比为25 ∶ 1。
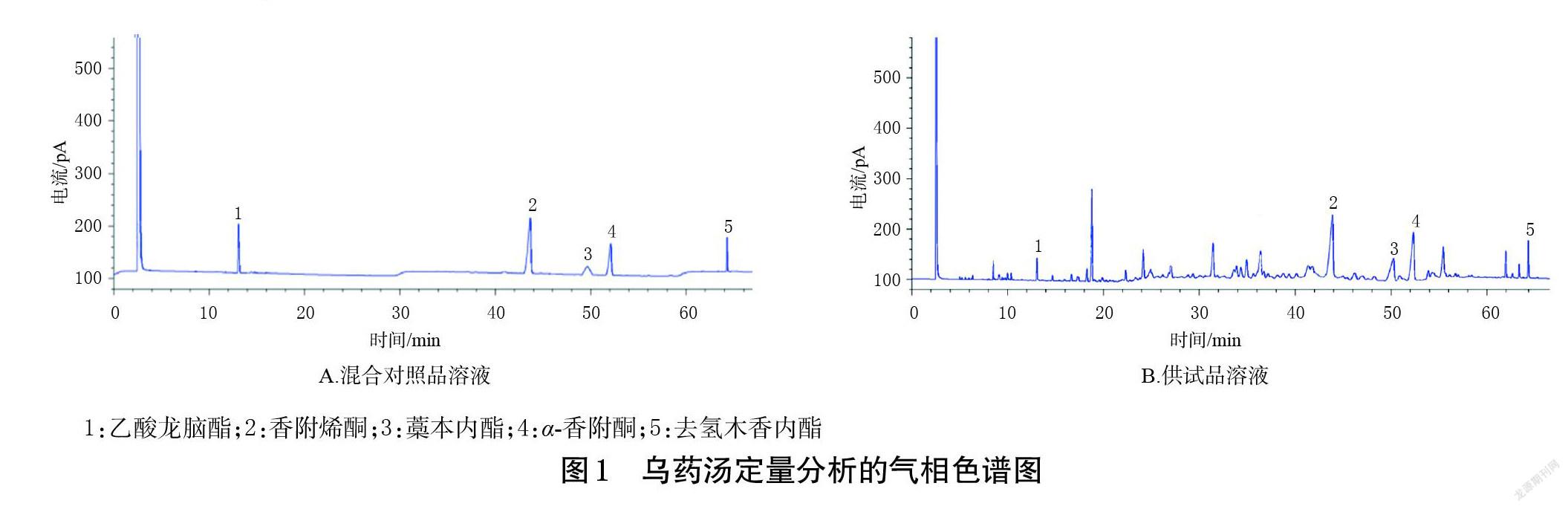
2.2.2 混合对照品溶液的制备 分别称取α-香附酮、香附烯酮、乙酸龙脑酯、去氢木香内酯、藁本内酯对照品,精密称定,用甲醇制成质量浓度分别为1.125、3.360、0.954、0.369、0.900 mg/mL的混合对照品溶液。
2.2.3 供试品溶液的制备 按照“2.1”项下方法提取挥发油,以4 000 r/min离心6 min,上清液加入适量无水硫酸钠干燥,得到不含水分的挥发油。取上述挥发油,用甲醇定容于10 mL量瓶中,精密量取2 mL置于5 mL量瓶中,再用甲醇定容,过0.22 μm微孔滤膜,即得供试品溶液。
2.2.4 系统适用性试验 取混合对照品溶液、供试品溶液和空白对照溶液(甲醇),按照“2.2.1”项下色谱条件进样测定,记录色谱图(图1)。结果显示,供试品溶液在对照品溶液的相应位置有相同的色谱峰,各色谱峰与相邻色谱峰的分离度均大于1.5,空白对照溶液对测定无干扰(图略),表明本方法系统适用性良好。
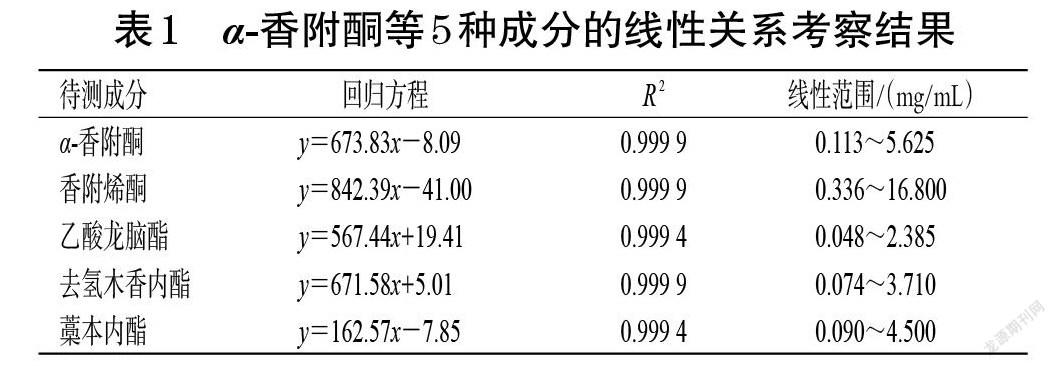
2.2.5 线性关系考察 称取α-香附酮、香附烯酮、乙酸龙脑酯、去氢木香内酯、藁本内酯对照品适量,以甲醇配制成α-香附酮质量浓度分别为5.625、2.250、1.125、0.563、0.113 mg/mL,香附烯酮质量浓度分别为16.800、6.720、3.360、1.680、0.336 mg/mL,乙酸龙脑酯质量浓度分别为2.385、0.954、0.477、0.239、0.048 mg/mL,去氢木香内酯质量浓度分别为3.710、1.484、0.742、0.371、0.074 mg/mL,藁本内酯质量浓度分别为4.500、1.800、0.900、0.450、0.090 mg/mL的系列混合对照品溶液,按照“2.2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x)为横坐标、峰面积(y)為纵坐标进行回归分析,结果见表1。由表1可见,5种待测成分在各自线性范围内均与峰面积成良好的线性关系。
2.2.6 精密度试验 取“2.2.5”项下相应质量浓度(α-香附酮1.125 mg/mL、香附烯酮3.360 mg/mL、乙酸龙脑酯0.477 mg/mL、去氢木香内酯0.742 mg/mL、藁本内酯0.900 mg/mL)的混合对照品溶液适量,按照“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。结果显示,α-香附酮、香附烯酮、乙酸龙脑酯、去氢木香内酯、藁本内酯峰面积的RSD分别为0.97%、0.65%、0.35%、0.65%、0.31%(n=6),表明仪器精密度良好。
2.2.7 稳定性试验 取供试品溶液适量,分别在室温下放置0、2、4、8、12、24 h时按照“2.2.1”项下色谱条件进样测定,记录峰面积并代入回归方程计算含量。结果显示,α-香附酮、香附烯酮、乙酸龙脑酯、去氢木香内酯、藁本内酯含量的RSD分别为0.28%、0.27%、0.54%、0.41%、0.25%(n=6),表明供试品溶液在室温下放置24 h内稳定性良好。
2.2.8 重复性试验 按照“2.2.3”项下方法制备供试品溶液6份,按照“2.2.1”项下色谱条件进样测定,记录峰面积并代入回归方程计算含量。结果显示,α-香附酮、香附烯酮、乙酸龙脑酯、去氢木香内酯、藁本内酯含量的RSD分别为0.35%、0.45%、1.38%、0.38%、0.42%(n=6),表明本方法重复性良好。
2.2.9 加样回收率考察 取已知待测成分含量的供试品溶液6份,精密加入一定量相应质量浓度(α-香附酮1.125 mg/mL、香附烯酮3.360 mg/mL、乙酸龙脑酯0.477 mg/mL、去氢木香内酯0.742 mg/mL、藁本内酯0.900 mg/mL)的混合对照品溶液,按照“2.2.3”项下方法制备供试品溶液,按照“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率。结果显示,α-香附酮、香附烯酮、乙酸龙脑酯、去氢木香内酯、藁本内酯的平均加样回收率分别为98.75%、98.21%、98.41%、98.19%、99.79%,RSD均小于3%(n=6),表明本方法准确度好。
2.3 单因素实验初步筛選挥发性成分提取工艺
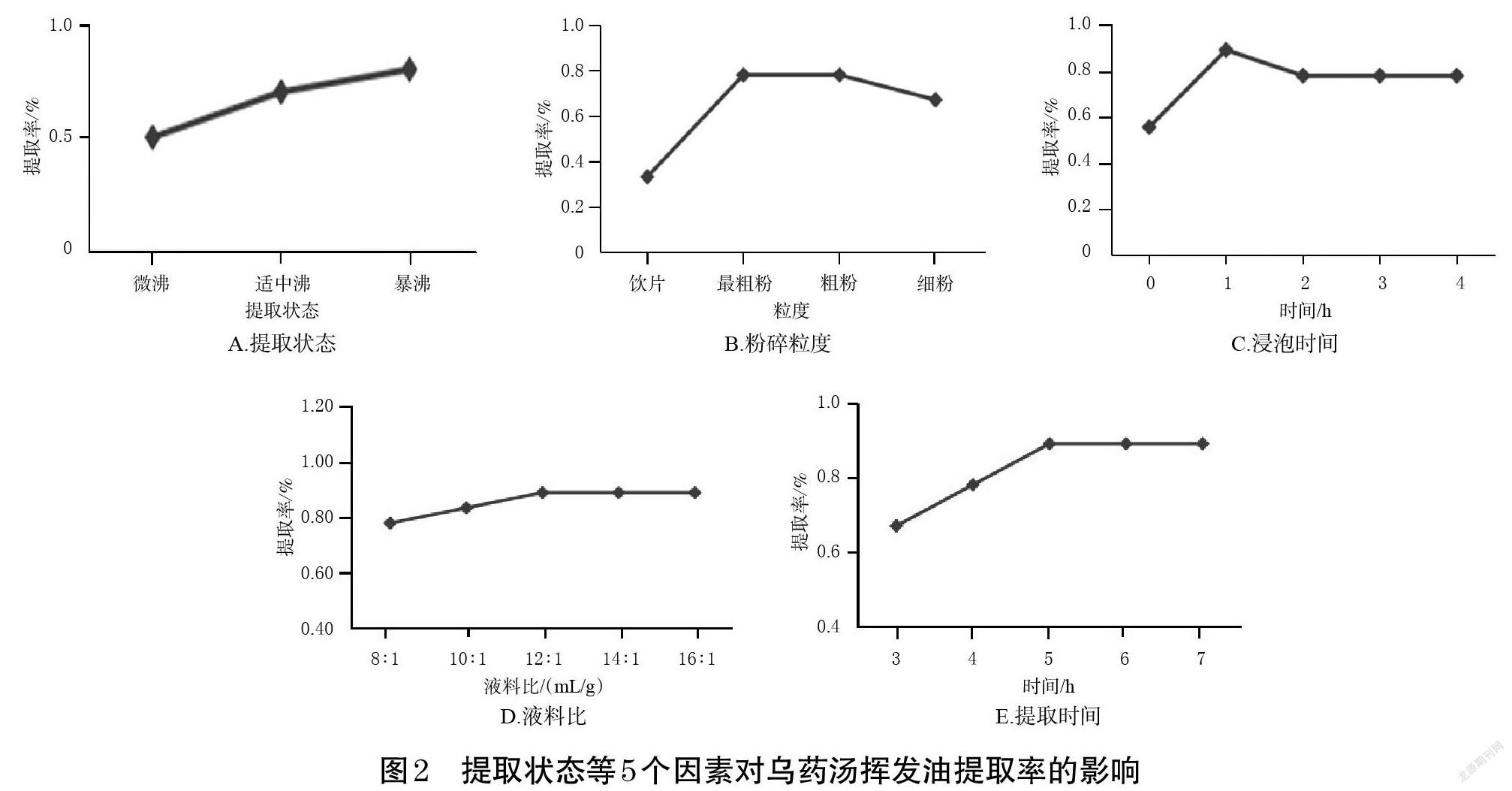
参考文献[10],本课题组通过初步筛选影响乌药汤挥发油提取率的因素发现,提取状态、粉碎粒度、浸泡时间、液料比、提取时间5个因素对乌药汤挥发油提取率的影响较大。因此,本研究以挥发油提取率为指标,以提取状态(微沸、适中沸、暴沸)、粉碎粒度(饮片、最粗粉、粗粉、细粉,参照2020年版《中国药典》(一部)“凡例”要求[7])、浸泡时间(0、1.0、2.0、3.0、4.0 h)、液料比(8 ∶ 1、10 ∶ 1、12 ∶ 1、14 ∶ 1、16 ∶ 1,mL/g)、提取时间(3、4、5、6、7 h)为因素,在固定其余4个因素的条件下进行单因素实验,结果见图2。
2.3.1 提取状态 图2A显示,在固定其他因素提取乌药汤挥发油时,火力越大,挥发油提取率越高,故选择暴沸作为提取状态。
2.3.2 粉碎粒度 图2B显示,在固定其他因素提取乌药汤挥发油时,随着粉碎粒度逐渐变小,挥发油提取率呈先升高后稳定再下降的趋势;当粒度为最粗粉时,挥发油提取率达到峰值。笔者推测,这可能是因为中药材被粉碎后,其油室受到了破坏,有利于提高提取效率,但粉碎越细药材越容易结块,且越不利于蒸馏[6]。故选择最粗粉作为粉碎粒度。
2.3.3 浸泡时间 图2C显示,在固定其他因素提取乌药汤挥发油时,随着浸泡时间延长,挥发油提取率呈先升高后下降再平稳的趋势;当浸泡时间为1.0 h时,挥发油提取率达到峰值,故选择1.0 h作为浸泡时间。
2.3.4 液料比 图2D显示,在固定其他因素提取乌药汤挥发油时,随着液料比增加,挥发油提取率呈先升高后平稳的趋势;当液料比为12 ∶ 1(mL/g)时,挥发油提取率达到峰值,故选择12 ∶ 1(mL/g)作为液料比。
2.3.5 提取时间 图2E显示,在固定其他因素提取乌药汤挥发油时,随着提取时间延长,挥发油提取率呈先增加后平稳的趋势;当提取时间为5 h时,挥发油提取率达到峰值,故选择5 h作为提取时间。
2.4 Box-Behnken设计-响应面法优化挥发性成分提取工艺
2.4.1 实验设计与结果 上述单因素实验结果提示,挥发油提取率在最粗粉、暴沸状态下均可达到峰值,结合生产实际,本研究将粉碎粒度固定为最粗粉,提取状态固定为暴沸[11]。以液料比[A/(mL/g)]、浸泡时间(B/h)、提取时间(C/h)为响应因素,以乌药汤有效成分乙酸龙脑酯、香附烯酮、α-香附酮、藁本内酯、去氢木香内酯含量及挥发油提取率为响应值,采用Design-Expert V8.0.6.1软件,运用Box-Behnken设计-响应面法设计3因素3水平17个实验点的工艺优化实验(包括12个析因实验和5个中心实验)。乌药汤挥发性成分提取工艺优化的实验设计因素与水平见表2,实验方案与结果见表3。
2.4.2 权重系数与综合评分的计算 应用信息熵法对表3中各组指标数据进行权重分析,计算权重系数(Wi)。规定在某一评价指标系统中,有m个评价对象、n个评价指标,形成的原始指标数据矩阵为X=(xij)mn(i、j分别表示矩阵的行、列);将原始评价指标矩阵(X)转化为概率矩阵(Pij),计算公式为Pij=Xij/∑Xij,再计算熵值(Hi值,Hi=-1/lnη×[∑][j=1][n]Pij×lnPij,η表示待评项目)[12-13]。结果显示,乙酸龙脑酯、香附烯酮、藁本内酯、α-香附酮、去氢木香内酯含量及挥发油提取率的Hi值分别为0.996 9、0.998 4、0.997 7、0.994 5、0.996 7、0.997 4。随后,计算各评价指标的Wi值[Wi=(1-Hi)÷[∑][i=1][m](1-Hi)][12-13]。结果显示,乙酸龙脑酯、香附烯酮、藁本内酯、α-香附酮、去氢木香内酯含量及挥发油提取率的Wi值分别为0.169 8、0.088 3、0.121 9、0.298 3、0.181 1、0.140 6。按下式计算综合评分:综合评分=(乙酸龙脑酯含量/乙酸龙脑酯含量最大值)×W1+(香附烯酮含量/香附烯酮含量最大值)×W2+(藁本内酯含量/藁本内酯最大值)×W3+(α-香附酮含量/α-香附酮含量最大值)×W4+(去氢木香内酯含量/去氢木香内酯最大值)×W5+(提取率/提取率最大值)×W6,结果见表3。
2.4.3 数据处理与分析 采用Design-Expert V8.0.6.1软件对综合评分进行多元拟合分析,得A、B、C 3个变量对综合评分的二次多项回归模型,即综合评分=0.860+7.428×10-3A-0.018B+0.13C-6.058×10-3AB-1.890×10-3AC+2.910×10-3BC-6.250×10-5A 2-5.909×10-3B 2-0.057C 2。乌药汤挥发性成分提取工艺优化的方差分析结果见表4。
表4显示,模型的P值<0.000 1,表明该实验模型真实可靠;失拟项的P值为0.219 0(>0.05),表明未知因素对实验的干扰小。由F值可知,各因素影响程度大小依次为C>B>A;由各因素单一项对应P值可知,B、C均有显著影响(P<0.05);由各因素交互项对应P值可知,各因素交互作用均无显著影响(P>0.05);由各因素二次项对应P值可知,C 2有显著影响(P<0.05);拟合方程的相关系数(R 2)为0.988 8,调整后的相关系数(R 2adj)为0.974 3,表明该模型可解释97.43%响应值的变化,模型拟合程度较好、误差较小。
本研究采用Design-Expert V8.0.6.1软件绘制各因素交互作用对综合评分影响的响应面图,结果见图3。
响应面图的陡峭程度可直接反映各因素交互作用的强弱[9]。图3显示,各因素交互作用的响应面图均不陡峭,与表5中AB、AC、BC交互作用的影响不具统计学意义的结果一致。通过求解回归模型方程得到最优提取工艺参数为:液料比12.99 ∶ 1(mL/g),浸泡时间0.62 h,提取时间6 h,综合评分的预测值为0.947 9。结合生产实际,本研究对上述提取工艺参数进行修正,得到最优提取工艺参数为:药材取最粗粉,液料比13 ∶ 1(mL/g),浸泡时间0.5 h,提取时间6 h。
2.4.4 驗证实验 按照“2.4.3”项下最优提取工艺进行3次验证实验。结果显示,综合评分分别为0.948 7、0.948 4、0.948 6(RSD=0.02%,n=3),与预测值(0.947 9)的偏差均不超过1%,表明优化的提取工艺稳定、可行。
2.5 提取状态的量化
参考文献[14],按照“2.4.3”项下最优提取工艺进行实验,采用油浴控温装置分别在120、150、170、180、190 ℃下提取乌药汤挥发性成分,每个温度条件平行操作3次,观察6 h提取过程中药液的沸腾状态,并计算提取6 h时的提取率。结果显示,在120 ℃下药液沸腾状态为微沸,平均提取率为0.56%;在150 ℃下药液沸腾状态为适中沸,平均提取率为0.72%;在170 ℃下药液沸腾状态为适中沸,平均提取率为0.78%;在180 ℃和190 ℃下药液沸腾状态为暴沸且180 ℃下的提取率更高,平均提取率为0.89%。故以180 ℃油浴下药液的沸腾状态作为暴沸状态。
3 讨论
本课题组预实验发现,乌药汤提取过程中乌药、香附、木香、当归、甘草挥发油不存在分层现象,表明处方中药材挥发油密度相近,可同时提取。本研究采用Box-Behnken设计-响应面法与熵权法相结合的方式优化了乌药汤挥发性成分的提取工艺。Box-Behnken设计-响应面法能综合考察多个提取因素的影响,具有实验次数少、精度高、预测值精准的优点;熵权法可在多指标筛选最优工艺时科学地赋予各指标相应的权重系数,以避免人为主观因素的影响[12]。利用熵权法赋予各指标的权重系数计算综合评分,再通过对综合评分进行分析,从而筛选最优工艺,所得结果较为严谨[12-13,15]。
3.1 提取状态的量化表征
外在的传热效率对挥发油提取的影响十分显著,外在的加热温度或热的传递效率会直接影响挥发油的蒸发量与蒸发速度,充分的蒸发量能保证挥发油提取完全[6]。中药传统理论多用“文火”“武火”表示,现多用“微沸”“暴沸”表示,均只能用操作者的主观经验来判断,存在主观性的弊端,因此寻找量化指标对提取状态进行表征对工艺参数的完善有重要价值。本研究利用温度对药液提取状态进行表征,结果显示,在180 ℃和190 ℃油浴下提取状态均为暴沸,但在180 ℃下提取率达到峰值,而在190 ℃下药液沸腾过于剧烈,导致药液不断涌入挥发油收集器,不利于挥发油的收集。但是仅用温度表征提取状态还不够全面,本课题组后期将考虑模拟实际大生产设备,深入研究可控参数,以达到提取状态的精准化。
3.2 指标成分的选择
在中药产品的现代化工艺开发过程中,应基于有效成分的含量及其药理活性进行综合考虑。乙酸龙脑酯具有抗炎、镇痛、调节胃肠运动、改善肝损伤的药理作用,是乌药的有效成分之一[16-18]。香附烯酮、α-香附酮存在于香附药材中,成分特有性强,且在乌药汤中的含量高[19-20]。藁本内酯是当归挥发油的主要成分,具有解痉镇痛、抗炎、缓解胃肠平滑肌痉挛的作用[21-22]。去氢木香内酯是木香的主要有效成分,且是2020年版《中国药典》(一部)规定的含量指标成分。因此,本研究选择乙酸龙脑酯、香附烯酮、α-香附酮、藁本内酯、去氢木香内酯作为评价乌药汤的指标成分,并建立了测定其含量的气相色谱法。方法学考察结果显示,所建方法符合2020年版《中国药典》(四部)的要求[8]。
综上所述,本研究确定了经典名方乌药汤挥发性成分的最优提取工艺,可为其进一步开发利用提供参考。
参考文献
[ 1 ] 国家中医药管理局.关于发布《古代经典名方目录(第一批)》的通知[EB/OL].[2021-09-21]. http://kjs.satcm.gov.cn/zhengcewenjian/2018-04-16/7107.html.
[ 2 ] 潘少斌,孔娜,李静,等.香附化学成分及药理作用研究进展[J].中国现代中药,2019,21(10):1429-1434.
[ 3 ] 陈琳,朱靖,王嵩,等.当归主要活性成分提取方法及其活性研究进展[J].上海医药,2021,42(9):71-75.
[ 4 ] 袁胜男,袁冲,毛志海,等.基于网络药理学对乌药汤治疗原发性痛经作用机制的研究[J].中国医院药学杂志,2020,40(10):1116-1121.
[ 5 ] 程媛,忻晓东,彭安堂,等.基于GC-MS指纹图谱及多成分含量测定对经典名方乌药汤物质基准质量评价研究[J].中国现代應用药学,2021,38(23):2978-2984.
[ 6 ] 伍振峰,王赛君,杨明,等.中药挥发油提取工艺与装备现状及问题分析[J].中国实验方剂学杂志,2014,20(14):224-228.
[ 7 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2020年版.北京:中国医药科技出版社,2020:57-241,ⅩⅥ .
[ 8 ] 国家药典委员会.中华人民共和国药典:四部[S]. 2020年版.北京:中国医药科技出版社,2020:233-234,480-483.
[ 9 ] 李佳佳,郑鹏,顿佳颖,等.荆芥与连翘混合挥发油提取工艺优化[J].中国药房,2019,30(6):813-817.
[10] 朱登辉,张靖柯,李孟,等. Box-Behnken设计-响应面法优化山茱萸叶总三萜提取工艺[J].中国药房,2021,32(1):46-50.
[11] 张志瑞,李喜香,李盛华,等.祛寒逐风颗粒中挥发油提取工艺和包合工艺优化[J].中国药房,2019,30(2):192- 196.
[12] 田帅,汪海涛,姜瑛,等.结合聚类分析与信息熵赋权的构件选择方法[J].计算机与数字工程,2017,45(12):2437- 2441,2551.
[13] 陈云翔,董骁雄,项华春,等.基于信息熵的群组聚类组合赋权法[J].中国管理科学,2015,23(6):142-146.
[14] 武玉,周梦鸽,文甜甜,等.基于挥发油出油量的逍遥片提取工艺优化及挥发性成分研究[J].现代中药研究与实践,2019,33(6):40-45.
[15] 郑鹏,李佳佳,顿佳颖,等.基于响应面法与信息熵法优选枳壳、醋香附总挥发性成分提取工艺[J].中国现代应用药学,2019,36(12):1522-1528.
[16] 邓桂明,向彪,肖小芹,等.基于网络药理学的乌药主要化学成分药效作用研究[J].中草药,2018,49(21):5125- 5133.
[17] 邢梦雨,田崇梅,夏道宗.乌药化学成分及药理作用研究进展[J].天然产物研究与开发,2017,29(12):2147-2151.
[18] 晏润纬,彭小梅.乌药挥发油的化学成分及药理作用[J].时珍国医国药,2014,25(11):2747-2749.
[19] 郭慧玲,骆云霞,胡律江,等.四制香附贴膏灸剂在大鼠体内的血液流变性与体外透皮特性分析[J].中国实验方剂学杂志,2017,23(11):29-33.
[20] 胡栋宝,陆卓东,伍贤学.中药香附子化学成分及药理活性研究进展[J].时珍国医国药,2017,28(2):430-432.
[21] 柳小莉,黄小英,张小飞,等.基于GC-MS成分分析结合网络药理学预测当归挥发油质量标志物(Q-Marker)[J].中草药,2021,52(9):2696-2706.
[22] 吴国泰,王瑞琼,杜丽东,等.当归挥发油药理作用研究进展[J].甘肃中医药大学学报,2018,35(4):87-92.
(收稿日期:2021-09-27 修回日期:2022-02-24)
(编辑:邹丽娟)

