转换艾考恩丙替及联合索磷布韦/维帕他韦治疗慢性丙型肝炎初治的HIV/HCV合并感染者的效果及对血脂水平的影响
党便利,康文臻,毕铭辕,李建辉,陈昭云,李姝鹏,刘 青,孙永涛,蔡卫平,康 文
1 空军军医大学第二附属医院 传染科,西安 710038;2 郑州市第六人民医院 感染科,郑州 450015; 3 广州市第八人民医院 感染科,广州 510060
HIV合并感染HCV会对患者造成持续的HCV病毒血症、更高的HCV病毒载量和更快的纤维化进展等负面影响,还会导致机体脂质和脂蛋白代谢紊乱[1-4]。抗逆转录病毒治疗(antiretroviral therap,ART)降低了由AIDS并发症引起的死亡,但HCV合并感染仍是导致HIV感染者肝病及死亡的主要原因[5-7]。有研究[8-10]表明,不同的抗病毒药物在抑制HIV或HCV病毒复制的同时对机体血脂代谢存在不同程度的改善。然而转换艾考恩丙替联合索磷布韦/维帕他韦对HIV/HCV合并感染者疗效及对血脂水平的影响尚未见报道。本研究以已接受ART并获得HIV持续抑制的、慢性丙型肝炎初治的HIV/HCV合并感染者为研究对象,分析HIV获得抑制后转换为艾考恩丙替并联合索磷布韦/维帕他韦的抗病毒疗效及对血脂水平的影响,以期为HCV初治的HIV/HCV合并感染者提供有效抗HCV治疗参考方案。
1 资料与方法
1.1 研究对象 本研究为前瞻性队列研究。选取2019年7月—2021年5月于空军军医大学第二附属医院传染科就诊并已接受ART且获得HIV持续抑制的、慢性丙型肝炎初治的HIV/HCV合并感染者。纳入标准:(1)年龄18~65岁;(2)HIV抗体确证试验阳性超过6个月,已接受抗HIV治疗且12个月内HIV RNA低于检测下限(<20 IU/mL);(3)HCV抗体阳性或HCV RNA阳性超过6个月;肝纤维化扫描(FibroScan)≤12.5 kPa。排除标准:(1)HIV、HCV急性感染期患者;(2)入选时有现症机会性感染或艾滋病相关机会性肿瘤,或入选前3个月内发生过机会性感染,入选前2周内病情仍不稳定者;(3)有下列情况之一者,ALT>10倍正常值上限(ULN),或AST>10×ULN、TBil>2×ULN、eGFR<50 mL·min-1·1.73 m-2;(4)既往使用过丙型肝炎直接抗病毒药物(direct-acting antiviral agents,DAA)者;(5)HBsAg阳性者;(6)有下列情况之一的肝硬化患者,肝组织病理诊断;FibroScan>12.5 kPa;APRI评分>2分;(7)严重精神疾病者、静脉药瘾者、有酗酒史且不能终止者(摄入酒精超过50 g/d);(8)妊娠期、哺乳期妇女。
1.2 治疗方法 纳入患者均采用转换艾考恩丙替及联合索磷布韦/维帕他韦治疗方案。(1)抗HIV治疗:原ART方案转换为口服艾考恩丙替(美国吉利德科学公司,艾维雷韦/考比司他/恩曲他滨/丙酚替诺福韦,剂量为150 mg/150 mg/200 mg/10 mg,1次/d)治疗32周,结束后患者可根据个人意愿自费继续使用艾考恩丙替抗HIV治疗,或转换为原国家免费ART方案;(2)抗HCV治疗:于转换艾考恩丙替治疗第4周联合索磷布韦/维帕他韦(美国吉利德科学公司,索磷布韦和维帕他韦的剂量分别为400、100 mg,1次/d)治疗12周,HCV治疗结束后继续随访24周(期间分别口服艾考恩丙替16周及转换为原ART方案进行抗HIV治疗)。
1.3 观察指标 分别于转换艾考恩丙替抗HIV治疗前与治疗4周及联合索磷布韦/维帕他韦抗HCV治疗第4周、12周和治疗结束后12周(PT-12W)、24周(PT-24W)检测纳入患者的体质量、BMI、HCV 基因型(Versant HCV Genotype Inno-LiPA Assay)、AFP、肝硬度值、CD4+T淋巴细胞(简称CD4细胞)数量、CD4+T/CD8+T(简称CD4/CD8)比值、肝功能相关指标(ALT、AST、TBil及Alb)、肾功能相关指标(eGFR及Cr)、血脂相关指标(HDL-C、LDL-C、TC及TG)、HCV RNA水平(Roch Ampliprep Taqman 2.0,下限为15 IU/mL)、HIV RNA水平(Roch Ampliprep Taqman 2.0,下限为20 IU/mL),并记录患者自报的药物不良反应。
1.4 统计学方法 应用GraphPad Prism 8.0和SPSS 26.0软件分析处理数据。非正态分布计量资料以M(P25~P75)表示,两组间比较采用Mann-WhitneyU检验。相关性分析采用Spearman相关性检验。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 共纳入10例HIV/HCV合并感染患者,其中男性和女性各5例,年龄46.0(42.0~49.0)岁;感染途径为输血和有偿献血;HCV RNA基因型以1b型为主(8/10),其余为2a型(2/10);AFP[2.9(2.2~4.5)ng/mL]和肝脏硬度值[6.4(5.6~10.1)kPa]均正常。所有患者转换艾考恩丙替治疗前的ART方案详见表1。
2.2 转换艾考恩丙替抗HIV治疗4周后相关指标变化 相较于抗HIV治疗基线,转换艾考恩丙替治疗4周后10例HIV/HCV合并感染者的Alb水平略有下降(Z=-2.801,P=0.003 7),HIV-1 RNA均低于检测下限,体质量、BMI、CD4细胞数量、CD4/CD8比值、肝功能相关指标(ALT、AST及TBil)、肾功能相关指标(eGFR、Cr)、血脂相关指标(HDL-C、LDL-C、TC及TG)差异均无统计学意义(P值均>0.05)(表1)。
2.3 转换艾考恩丙替联合索磷布韦/维帕他韦抗HCV治疗后外周血CD4细胞计数、CD4/CD8 比值、HCV RNA及血生化指标变化 艾考恩丙替基础上联合索磷布韦/维帕他韦抗HCV治疗后患者的HCV RNA均快速降低,在第4、12周时病毒学应答率均为100%,持续病毒学应答(SVR)12和SVR24亦均达100%,且在治疗及后续随访期间HIV RNA均低于检测下限。相较于抗HCV治疗基线,治疗12周后患者的ALT(Z=-2.732,P=0.004 8)及AST(Z=-2.501,P=0.010 7)水平均显著降低,而TC(Z=-2.797,P=0.003 9)及LDL-C(Z=-2.343,P=0.018 5)均显著升高(表1);抗HCV治疗及后续随访期间患者的TC及LDL-C水平从12周的峰值逐渐降至与基线水平相当,且TC与LDL-C呈显著正相关(r=0.87,P<0.001)(图1)。10例患者在完成全部32周艾考恩丙替抗HIV治疗后,均因经济原因自愿转换回原国家免费ART方案继续抗HIV治疗,相较于PT-12W,PT-24W时患者ALT水平在正常范围内略升高(Z=-2.804,P=0.003 5),其他指标均维持稳定(表1)。随访结束时患者AFP[2.6(1.7~3.7)ng/mL]及肝硬度值[6.7(5.5~8.0)kPa]均正常。

表1 HIV/HCV合并感染患者转换艾考恩丙替及联合索磷布韦/维帕他韦治疗后各项指标变化
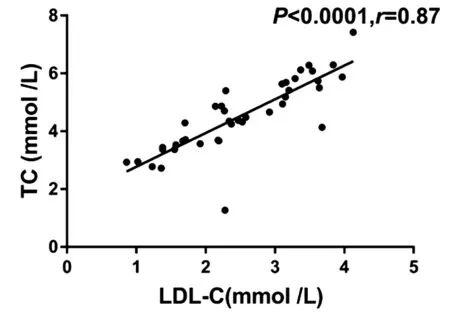
图1 转换艾考恩丙替及联合索磷布韦/维帕他韦治疗后TC与LDL-C的相关性分析
2.4 转换艾考恩丙替抗HIV治疗及联合索磷布韦/维帕他韦抗HCV治疗的不良反应 10例患者自报原ART方案不良反应主要为消化不良(n=1)、腹泻(n=1)、头晕(n=3)、恶心(n=1)、睡眠障碍(n=2);转换艾考恩丙替抗HIV治疗32周后原ART方案相关不良反应均明显减少。10例患者在转换艾考恩丙替及联合索磷布韦/维帕他韦抗HCV治疗及随访期间,出现胆囊炎1例、干咳1例、颜面浮肿1例,上述3例患者均未经处理,自行好转;另1例胆结石伴急性胆囊炎发作、酮症酸中毒,通过静滴头孢哌酮钠舒巴坦钠治愈;1例意外妊娠,自愿药流口服米非司酮和米索前列醇(剂量为150 mg和600 mg,1次/d)。上述所有不良反应经评估均与药物治疗不相关,且10例患者均未因不良反应而中断治疗及随访。
3 讨论
ART药物虽延迟了HIV/HCV合并感染者肝纤维化进展并减少了临床并发症,但机体持续的免疫激活和异常炎症反应,导致较高的发病率和死亡率[11-12]。DAA可提高SVR率并延缓HIV/HCV合并感染者的慢性丙型肝炎进展,DAA的发展彻底改变了HIV共同感染者HCV抗病毒的治疗模式[13-17]。指南[18]不再将HCV的单一和合并感染者分开治疗,唯一需要特别考虑的是HIV和HCV药物之间的相互作用(drug-drug interaction,DDI)[19]。我国免费ART方案中依非韦伦、奈维拉平等药物与多种DAA具有临床显著的DDI[20-21]。因此,本研究中将HIV/HCV合并感染者原ART方案转换为艾考恩丙替,并采用索磷布韦/维帕他韦作为DAA方案,经药物相互作用查询系统(https://www.hiv-druginteractions.org/checker或http://www.hep-druginteractions.org/)检索发现该联合治疗方案不存在潜在DDI问题[22-24]。
本研究发现,转换艾考恩丙替治疗4周及转换为原ART方案随访期间,患者的HIV RNA维持持续抑制,除Alb和ALT水平在正常范围内波动,其他指标均保持稳定,且患者报告原ART方案的抗HIV治疗相关不良事件发生情况明显改善,提示转换艾考恩丙替治疗对患者肝功能、肾功能及血脂代谢无显著影响,安全可行。
此外,本研究观察到转换艾考恩丙替并联合索磷布韦/维帕他韦抗HCV治疗后,于第4周100%获得HCV病毒学应答,且SVR12和SVR24均为100%,提示转换艾考恩丙替联合索磷布韦/维帕他韦方案在HCV基因1b型和2a型慢性丙型肝炎初治的HIV/HCV合并感染者中可迅速抑制病毒复制并获得极高的SVR;且抗HCV治疗期间,HIV/HCV合并感染者的eGFR及Cr维持稳定,ALT及AST均显著降低,提示该治疗方案可抑制HCV复制并减轻了肝脏炎症;同时患者血清TC水平及LDL-C水平在治疗12周后一过性升高,且两者呈显著正相关,提示血清LDL-C升高可能是血清TC升高的主要因素。已有研究[7,10,25]证实,不同DAA方案抗HCV治疗期间血清TC水平与LDL-C水平均显著升高,与治疗方案无关,而与HCV清除相关。DAA抗HCV治疗后,血清TC水平与LDL-C水平升高可能源于HCV的生命周期高度依赖于肝胆固醇的代谢,富含脂质的细胞微环境对HCV感染至关重要,消耗脂质的功能也随HCV病毒颗粒的清除而丧失,进而导致血液中过多的脂质[26]。但也有研究[27-28]认为,血清TC和LDL-C在治疗早期快速增加,并于治疗后逐渐减少可能依赖于治疗方案的类型。另有报道[10,25,29]发现,除HCV感染外,索磷布韦/维帕他韦本身可能具有诱导脂质代谢的药理作用。维帕他韦与雷迪帕韦均为NS5A抑制剂,分别与索磷布韦(NS5B)联合的DAA方案抗HCV治疗后,TC与LDL-C均具有相同变化趋势,推测此现象可能是NS5A抑制剂与索磷布韦产生协同作用的结果,但该治疗方案产生血脂变化的机制尚不清楚[25,30-31]。本研究还发现,患者在随访期间体质量及BMI变化较基线虽无统计学差异,但仍呈上升趋势。HCV清除后,预计患者的生活质量将得到改善,但体质量的增加可能会伴随高脂血症,需长期严格监测患者HCV清除后的血脂水平。
本研究存在一些局限性。首先,研究样本量小且入组患者HCV基因型有限(主要为1b亚型和2a亚型),100%的SVR结论不适用于其他HCV基因型患者[32-33]。其次,即使确定了索磷布韦/维帕他韦联合艾考恩丙替方案对血脂水平具有一定影响,但仍缺乏对其产生影响的其他因素(如饮食习惯和运动量等)的评估。再次,由于观察期仅限于抗HCV治疗后24周,因此无法观察到HCV清除后的长期变化(尤其是由血脂代谢紊乱引起的并发症)。最后,本研究中转换艾考恩丙替并联合索磷布韦/维帕他韦治疗方案的SVR12及SVR24均为100%,因此无法比较达到SVR12及SVR24的患者与未达到SVR12及SVR24的患者的血脂分布情况,也无法判断血脂变化与SVR是否存在相关性。
本研究证实转换艾考恩丙替治疗及与索磷布韦/维帕他韦联合避免了DDI,可作为HIV/HCV合并感染者安全且有效的抗HCV治疗方案。转换艾考恩丙替治疗期间,HIV维持持续病毒学抑制,且耐受性优于原ART方案,安全性良好。同时,艾考恩丙替联合索磷布韦/维帕他韦的治疗方案在HIV合并基因1b型和2a型初治的HCV感染者中可以实现100%的SVR并获得生化学应答。抗HCV治疗期间,血清TC和LDL-C一过性升高,可能源于HCV感染和索磷布韦/维帕他韦的药理作用。因此,需要进一步研究索磷布韦/维帕他韦对宿主脂质代谢的分子作用,进而阐明其对血清脂质谱的药理作用。
伦理学声明:本研究方案于2019年1月31日经由空军军医大学第二附属医院伦理委员会审批,批号:第K201901-07号,所纳入患者均签署知情同意书。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:党便利、康文臻负责分析数据,撰写论文;毕铭辕、李姝鹏、刘青负责实施研究;李建辉、陈昭云负责收集病例;孙永涛、蔡卫平负责行政及技术支持;康文负责获取研究经费,行政、技术支持,审阅、修改论文。

