TEE辅助下急诊TAVR抢救重度主动脉瓣狭窄合并心源性休克老年患者1例
余 凤,闫思宇,王 琼,姜春玲
(四川大学华西医院 麻醉科,四川 成都610041)
主动脉瓣狭窄(AS)是由于风湿性疾病、先天性瓣膜畸形或老年瓣膜钙化等原因所致的退行性病变,发生率随年龄的增加而增加,目前尚无有效的药物疗法。几十年来,外科行主动脉瓣置换术是治疗该病的金标椎,而近年来新兴的经导管主动脉置换术(TAVR),是对无法耐受常规开胸大手术患者的有效替代疗法。本文报道了1例急诊在经食道超声心动图(TEE)实时辅助下行TAVR手术抢救极重度主动脉瓣狭窄合并心源性休克老年患者的成功案例,以期为临床救治该类患者提供参考。
1 临床资料
患者,男,72岁,身高170 cm,体重62 kg,因“胸闷气紧1年多”入院。患者主要表现为逐渐加重胸闷、气促。既往高血压病史10余年,未规律服药。1年多前因胸闷、气紧于外院检查提示非ST段抬高型心肌梗死,症状缓解后出院。本次入院查体提示:主动脉瓣听诊区闻及5/6级收缩期喷射性杂音,心功能III级,双下肢中度水肿。辅助检查:心脏彩超检查提示全心增大,主动脉瓣狭窄(极重度),肺高压(中-重度),左室收缩及舒张功能明显减低,射血分数(EF)28%。诊断:①心瓣膜病:主动脉瓣狭窄(极重度),二、三尖瓣反流(轻-中度),肺高压(中重度),卵圆孔未闭;②窦性心律:心功能Ⅲ级;③冠心病;④高血压Ⅰ级:很高危。入院保守治疗6日病情持续恶化,出现呼吸费力,咳粉红色泡沫痰,HR 111次/分,BP降至75/33 mmHg,RR 24次/分,面罩吸氧(6 L/min)状态下SpO2仅70%-80%。实验室检查提示:脑钠肽(BNP)>35 000 pg/ml、尿素28 mmol/L、血清肌酐175.0 μmol/L、血钾6.55 mmol/L,门冬氨酸氨基转移酶 2373 IU/L、丙氨酸氨基转移酶1788 IU/L,总胆红素 131.7 μmol/L和直接胆红素 90.4 μmol/L。动脉血气提示:酸碱度 7.288,二氧化碳分压 53 mmHg,氧分压 67 mmHg(面罩吸氧6 L/min),碱剩余-6.96 mmol/L。心肌标志物:肌红蛋白152.30 ng/ml,肌钙蛋白125.0 ng/ml。患者持续心源性休克状态,遂转入心脏重症监护室(CCU),放置主动脉内球囊反搏(IABP)、并紧急行血液透析。病情仍无缓解,因此拟急诊行经心尖入路经导管主动脉瓣置换术。
患者在大剂量血管活性药物及IABP支持下进入手术间,入室HR 109 次/分,BP 80/40 mmHg,SpO2(吸氧浓度 50%)为92%。全身麻醉诱导顺利,诱导后放置TEE探头,监测显示:主动脉增宽,升主动脉明显,主动脉瓣呈二叶式畸形,瓣叶明显增厚、钙化,开放明显受限,主动脉瓣面积(Ava)为0.5 cm2,峰值主动脉瓣口流速(AV)为12.33 m/s,左心室射血分数(LVEF)显著降低27.7%,轻度二尖瓣反流和三尖瓣反流(图1A)。主动脉根部造影明确主动脉窦部形态及冠状动脉开口位置,在14Fr COOK鞘引导下置入22 mm球囊进行预扩张两次,TEE评估球囊扩张效果及瓣环结构大小后决定选择J-valve25MM瓣膜。完全释放后再次确定瓣膜位置及功能良好,再次采用球囊后扩张,TEE未见明确瓣周漏,支架展开有效瓣环径约25 mm。患者立即表现出显著的血流动力学改善,峰值AV速度从12.33 m/s下降至3.2 m/s(图1B),肾上腺素从0.3 μg/kg/min降至0.1 μg/kg/min,去甲肾上腺素从0.8 μg/kg/min降至0.3 μg/kg/min。
手术共持续120 min,在严密的麻醉监测管理下,整个过程未发生心脏骤停或恶性心律失常等不良心脏事件。术毕返回CCU继续观察,儿茶酚胺类血管活性药物逐渐减量至停止,术后两天患者BNP降至5576 pg/ml,内环境稳定,予拔出IABP。术后第四天,患者生命体征平稳,肾功能和呼吸功能逐渐改善,拔出气管导管。患者术后11天出院,无任何并发症。在术后六个月的随访中,患者的心脏功能从纽约心功能分级Ⅳ级改善到Ⅱ级。此外,超声心动图显示平均跨瓣压差和主动脉瓣面积分别为16 mmHg和1.4 cm2,在无任何正性肌力药物支持的情况下,LVEF由术前27.7%增加至50.3%(图2)。

图1 术前TEE检查结果(A),术中TEE检查结果(B)
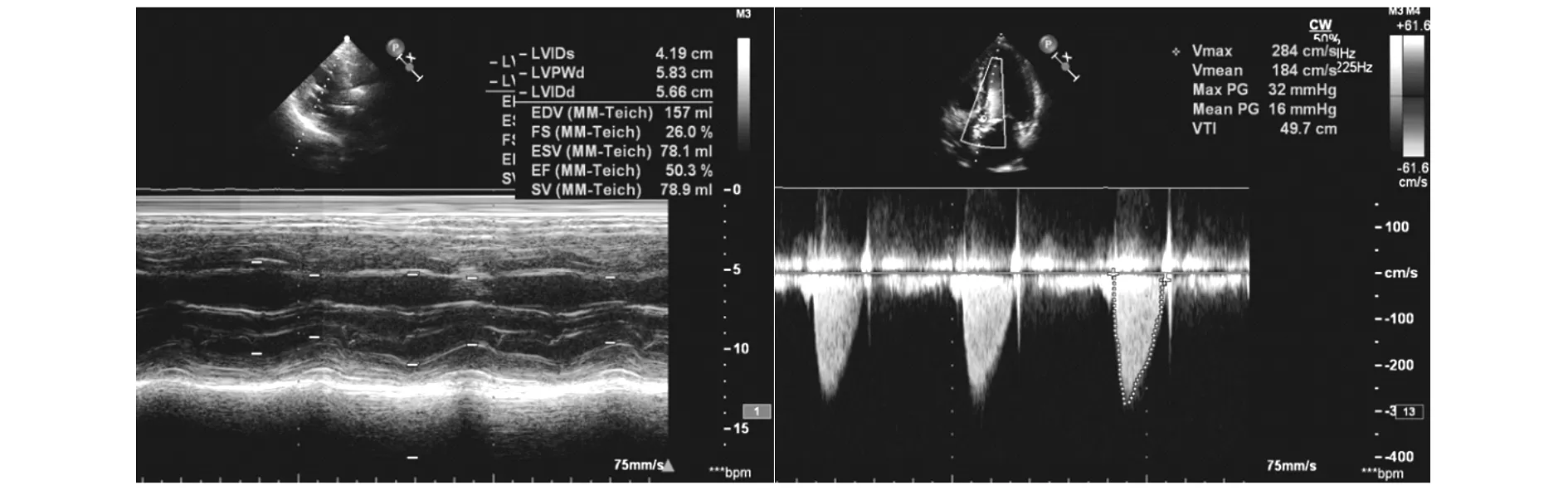
图2 术后六个月超声心动图检查结果
2 讨论
AS是老年患者中最常见的心脏瓣膜疾病之一,在75岁以上的老年患者中发病率约为12.4%,而重度AS的发病率为3.4%[1]。未经治疗的严重症状性AS预后差,1年死亡率为50%。外科瓣膜置换术(SAVR)是治疗AS的主要手段,然而并不适用于合并心力衰竭的高危重度AS患者。由于手术风险高,患者年龄较大且合并虚弱状态等,约40.5%的患者无法实施SAVR[1]。而TAVR,可通过介入方式(包括经股动脉、颈动脉、锁骨下动脉、心尖等)跨主动脉瓣植入一个生物瓣膜,有研究证明其对症状严重的主动脉狭窄患者的治疗效果优于或不劣于标准的SAVR手术[2]。TAVR首选的路径是经股动脉,而本例患者选择经心尖入路,其优势在于不仅不受血管条件的限制(如老年长期高血压的患者常合并股、髂动脉迂曲、钙化、有附壁血栓形成等),而且经心尖入路是TAVR手术中唯一的顺性入路,手术路径短、瓣膜操控性强、更精准,可显著缩短手术时间。
然而,TAVR手术多用于血流动力学稳定的择期手术患者[3]。而本例患者为极重度主动脉瓣狭窄,心功能Ⅳ级,在内科保守治疗下难以维持氧合、血流动力学稳定,已呈现心源性休克、肝肾功能急剧恶化及呼吸衰竭状态,如无有效的紧急治疗措施,患者将由于心源性休克及多器官功能衰竭无法控制而迅速死亡。对于这类预期寿命有限的极重度AS患者,主动脉瓣球囊成形术(BAV)曾是其主要的治疗方式,可迅速降低跨瓣压差,缓解患者症状,然而近年来不断有研究提出BAV的治疗缺陷,如存在术后严重主动脉瓣反流的风险,长期预后与未经治疗患者相似,甚至有研究表明[4],BAV即便是作为TAVR或SAVR的桥接治疗手段也未给患者带来任何益处,与单独行TAVR及SAVR的患者预后相似,且增加了手术费用。
主动脉瓣环尺寸的精确测量是TAVR手术成功的关键。在早期的TAVR试验中,2D TEE是评估主动脉瓣环大小的唯一手段,但是由于2D TEE测量仅能提供瓣环矢状面图像,当瓣环非圆形时常导致选择的人工瓣环径较实际小[5]。术中主动脉根部影像学的评估如多排螺旋CT(MDCT)曾被认为是主动脉瓣环测量的金标准,但是对于重症AS患者,常因为其处于急性心功能失代偿期无法平卧,而不能耐受检查。随着超声诊断技术的进步,近年发现3D TEE在测量主动脉瓣环面积、周长及左室流出道面积方面与MDCT的测量结果密切相关,并且二者对于TAVR术后瓣周漏的预测结果相似,因此提出在TAVR手术中3D TEE可作为MDCT的替代方案[6]。本例患者术前TEE提示主动脉瓣呈二叶式畸形,瓣叶钙化极严重,瓣口重度狭窄,主动脉增宽,以升主动脉为主。术中采用3D TEE对主动脉根部结构及瓣环球囊前后扩张进行充分评估,是正确选择人工瓣膜型号及成功植入的关键。此外,术中TEE实时监测还能确保球囊扩张、瓣膜释放的顺利进行,并可实时评估患者瓣膜工作状态、心脏整体舒缩功能及容量状态,进而对术中管理发挥至关重要的指导作用。此外,本例患者术前还放置了IABP作为行TAVR的桥接治疗。在IABP的支持下,术前患者循环改善,麻醉耐受性显著提高,也减少了血管活性药物的使用,为手术创造了条件。
总之,对于严重主动脉瓣狭窄合并心源性休克及多器官功能衰竭的急危重症患者,在多学科团队体系支撑及TEE技术实时辅助下,急诊行经心尖TAVR解除原发病变可能挽救患者生命,本例手术的成功一定程度上印证了这一点。然而,TAVR对这类高危患者长期预后的影响仍有待证明。

