鞣花酸pH敏感载药微球的释放规律研究
徐佳敏,蒋新元,伍佑辉,倪丹,贺靖雁
(1.中南林业科技大学 理学院,湖南 长沙 410004;2.中南林业科技大学 材料科学与工程学院,湖南 长沙 410004;3.湖南省木本生物质转化工程技术研究中心,湖南 长沙 410004)
鞣花酸(EA)是一种植物多酚类物质,存在于各种植物果实如石榴中,具有抗癌变、抗病毒等作用[1-5]。但鞣花酸水溶性差,且口服鞣花酸的半衰期短,生物利用度低[6],限制了其应用。天然高分子材料具有良好的生物可降解性、生物相容性及生物安全性,在生物医学材料尤其是药物释放方面得到广泛应用[7-8]。本文通过选择合适的方法以提高鞣花酸的分散性,以天然高分子材料为基材制备了能包覆并缓释鞣花酸的复合微球,并研究和模拟了不同pH条件下和不同介质溶液中鞣花酸复合微球包覆体系中鞣花酸的释放规律,以充分发挥其定向抗氧化、杀菌及抗癌等效果。
1 实验部分
1.1 材料与仪器
鞣花酸(纯度98%);PBS缓冲溶液,飞净生物科技有限公司;胰蛋白酶(1∶250),上海百舜生物科技有限公司;胃蛋白酶(1∶1 000),广州赛国生物;浓盐酸、戊二醛、无水氯化钙、天然高分子材料A、天然高分子材料B 均为分析纯。
TM-1810型紫外可见分光光度计;AUY120电子分析天平;JJ-1A精密电动搅拌器;PHS-25 pH计;蔡司sigma 300场发射扫描电镜。
1.2 实验方法
1.2.1 鞣花酸分散体系的制备 根据文献[9]制得鞣花酸浓度为4.0 g/L的鞣花酸分散体系,体系呈乳白色。
1.2.2 人工胃液、人工肠液的制备 取浓盐酸 234 mL 稀释至1 000 mL,得9.5%~10.5%的稀盐酸。精密吸取稀盐酸16.4 mL于1 000 mL容量瓶中,加蒸馏水约800 mL,胃蛋白酶10 g,充分摇匀后加蒸馏水定容,即得人工胃液[10]。取磷酸二氢钾6.8 g,加水500 mL使其溶解,用0.1 mol/L氢氧化钠溶液调节pH至6.8;另外称取10 g胰蛋白酶加适量水溶解,将两液混合后,加蒸馏水定容至 1 000 mL,即得人工肠液[10]。
1.2.3 鞣花酸微球的制备 精确称取适量天然高分子材料A,与25 mL鞣花酸分散体系混合,电磁搅拌器充分搅拌制得混悬液。另取醋酸与无水氯化钙搅拌溶解为一定浓度溶液。在60 ℃水浴中,用医用注射针头将天然高分子材料B混悬液缓慢滴加到氯化钙溶液中,并于600 r/min的转速下搅拌一段时间后停止加热,加100 mL与水浴温度相同的蒸馏水,冷却至室温后加戊二醛固化1 h,抽滤,水洗3遍后再抽滤,放入烘箱中烘干,即得鞣花酸复合微球,备用。
1.2.4 鞣花酸微球的形态观察 用场发射扫描电镜观察微球表面形貌。将真空干燥后的鞣花酸复合微球真空喷金,置于样品平台上观察形貌。微球在不同pH介质溶液中形态的变化采用相机拍摄(像素:3 024×3 024)。
1.2.5 鞣花酸微球的载药量和包封率的测定 称取干燥的鞣花酸复合微球于研钵中研磨成粉末,精密称取10 mg,置于100 mL蒸馏水中浸泡30 min后超声,使鞣花酸充分分散。以空白微球为参比,在398 nm处用紫外可见分光光度计测量吸光度,通过标准曲线计算鞣花酸的浓度,按下式计算微球的载药量和包封率。微球中的药物含量为m(g),微球质量为M(g),投入的药物量为M0(g)。
载药量=m/M×100%
包封率=m/M0×100%
1.2.6 鞣花酸微球的释药性能的测定 精确称取0.10 g完全烘干的微球,分别置于100 mL的pH=2.13水溶液、pH=4.02水溶液、pH=6.86水溶液(均为稀盐酸调节)和pH=4.00缓冲溶液(邻苯二甲酸氢钾)、pH=6.86缓冲溶液(混合磷酸盐)、PBS缓冲溶液(pH=7.4),及人工胃液(pH=1.70)、人工肠液(pH=6.95)中进行静态释放规律的研究,恒定温度为(37±0.5)℃。分别于0.5,1,2,4,8,15,24 h后分别取样5 mL,同时补充相同体积的释放介质。测定样品溶液的吸光度,根据不同pH下鞣花酸分散体系的标准浓度曲线,测定各时间点的鞣花酸浓度,再计算鞣花酸在各时间点的累积释放量。
2 结果与讨论
2.1 鞣花酸微球的SEM扫描图
图1为不同放大倍数的鞣花酸复合微球SEM形貌。

图1 鞣花酸微球的电镜扫描图
由图1可知,鞣花酸复合微球呈球形。表面褶皱较多,不平整,可能是微球中含有少量气泡,或者干燥时急速皱缩造成的。
2.2 微球的载药性能及在不同pH介质溶液中的释放规律
2.2.1 不同pH介质溶液中鞣花酸分散体系标准曲线的绘制 精密称取鞣花酸分散体系0.5,1.0,2.0,4.0,6.0 mL于100 mL容量瓶中,分别用相应溶液定容,摇匀。以相应的试剂为空白对照,利用紫外吸收分光光度法测量。以浓度为横坐标,吸光度为纵坐标绘制标准曲线,得到鞣花酸分散体系在不同pH介质中的回归方程,结果见表1(Y表示吸光度,C表示浓度)。表明鞣花酸分散体系在0.002~0.024 g/L浓度范围内线性关系良好。

表1 鞣花酸分散体系在不同pH介质中的回归方程
2.2.2 鞣花酸微球的载药性能 根据《中国药典》规定[10],微球、微囊与脂质体需提供载药量的数据,而分散在液体介质中的微囊、微球与脂质体应用适当方法分离后测定计算包封率,且包封率不得小于80%。本实验中,将10 mg研磨粉碎的鞣花酸微球完全溶解在100 mL蒸馏水中,利用紫外吸收分光光度计检测其吸光度,根据2.2.1节中得到的标准曲线从而计算出鞣花酸的含量,得到鞣花酸微球的载药量为14.36%,包封率为86.16%,体现了微球质量较好,制备工艺可行。
2.2.3 鞣花酸微球在不同pH介质溶液中的释放规律 实验研究了所制备的鞣花酸微球在不同pH水溶液、不同pH缓冲溶液及模拟人工胃液和人工肠液的释放规律。图2为鞣花酸微球在pH 2.13,4.02,6.86水溶液中的释放曲线。
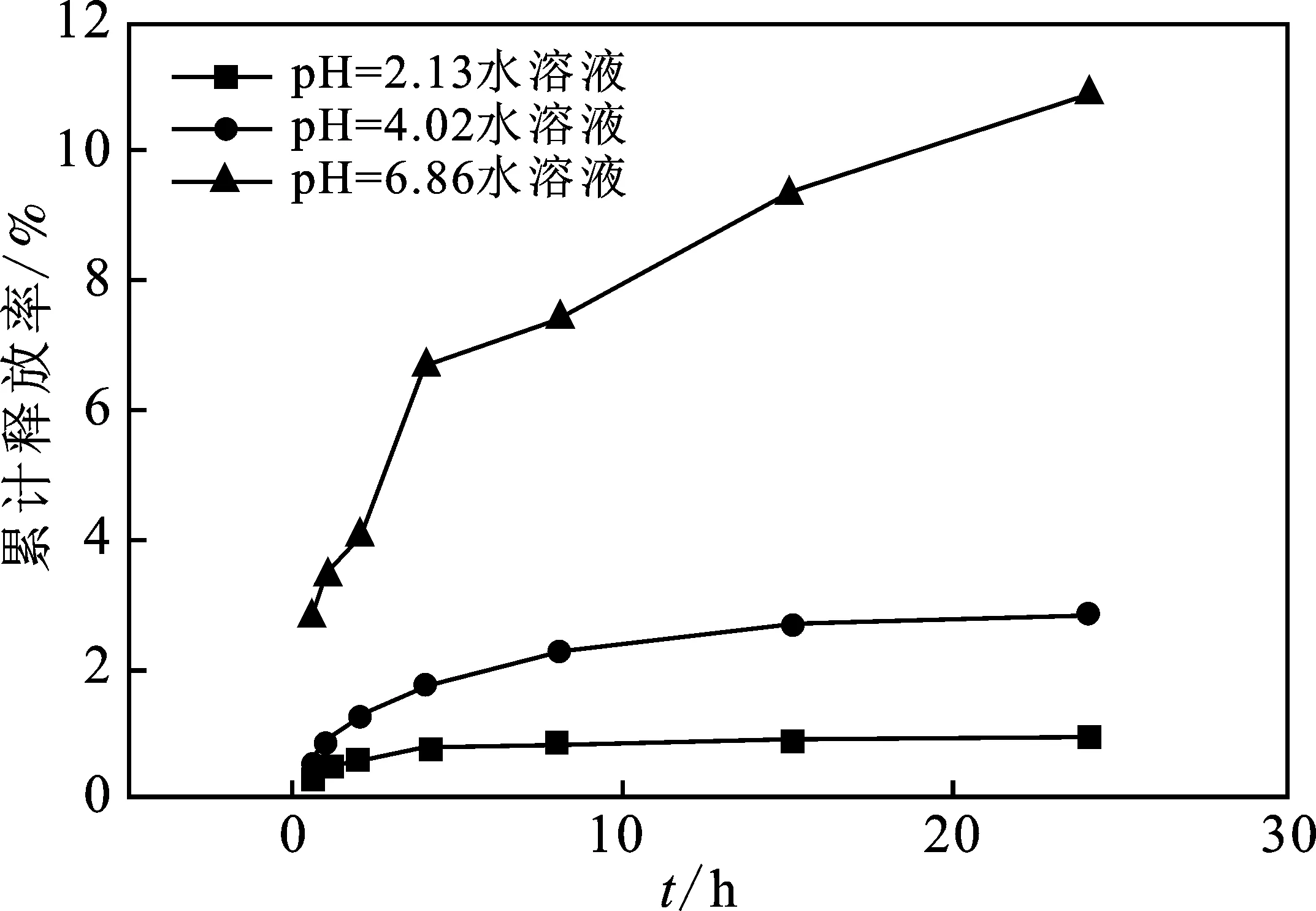
图2 鞣花酸微球在不同pH水溶液中的释放曲线
由图2可知,微球在pH=2.13和pH=4.02水溶液中释放的较为缓慢,起始0.5 h时,累计释放率分别为0.31%和0.56%,8 h时分别为0.85%和 2.14%,当释放时间达到24 h时,累计释放率分别仅为0.98%,2.67%,表明鞣花酸微球在酸性条件下累计释放率低。而微球在偏中性条件的pH=6.86 水溶液中累计释放率较酸性条件下稍高,整体趋势为先释放得快,后逐渐减慢,在0.5 h时,微球在蒸馏水中的累计释放率为2.78%,8 h时增加至7.34%,而在24 h时则达到10.79%,明显高于在pH=2.13和pH=4.02水溶液中的释放,说明微球中鞣花酸的释放率随介质溶液pH的升高而增大。
图3为鞣花酸微球在pH=4.00缓冲溶液、pH=6.86缓冲溶液和PBS缓冲溶液(pH=7.4)中的释放曲线。
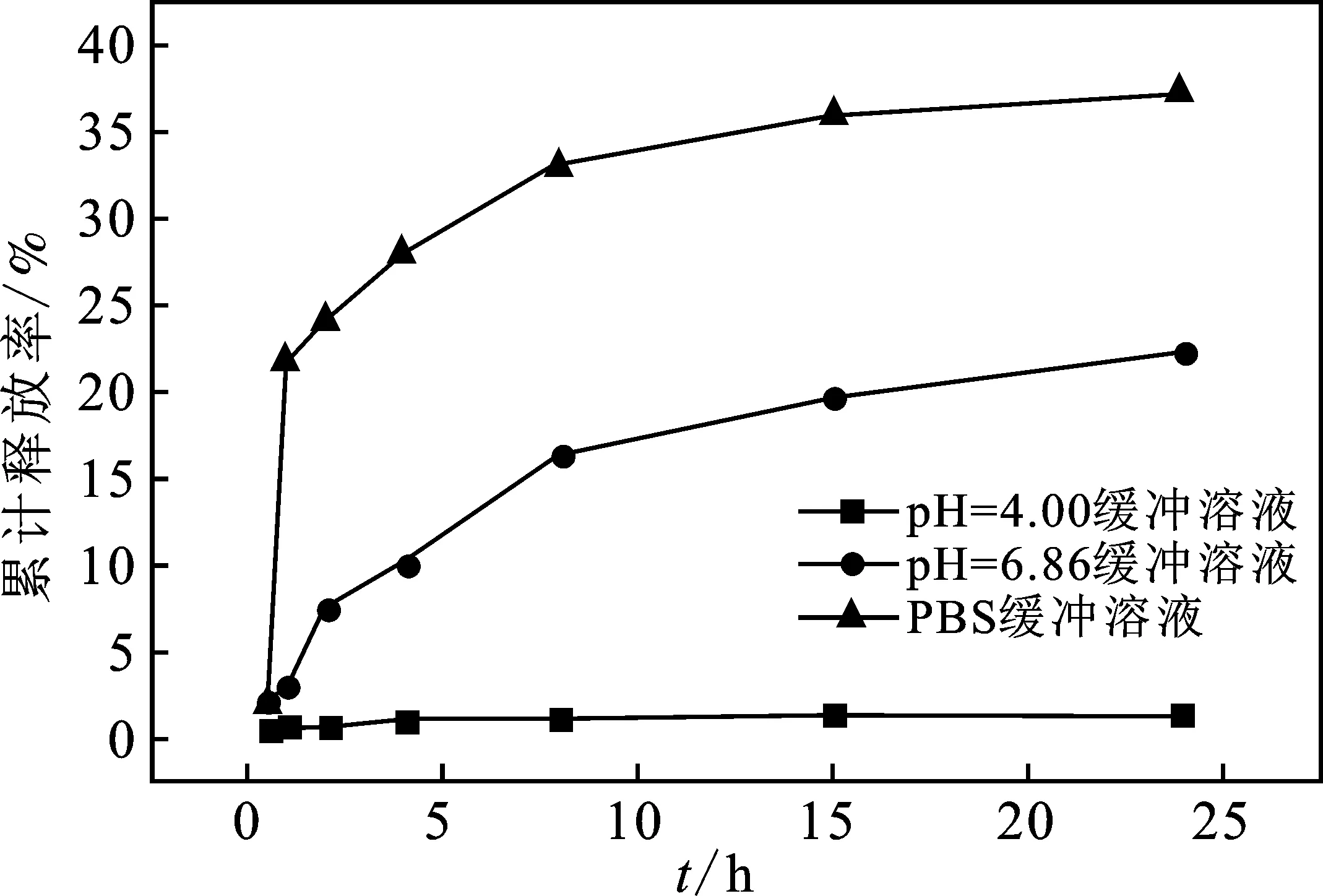
图3 鞣花酸微球在不同pH缓冲溶液中的释放曲线
由图3可知,起始0.5 h时,微球在3种缓冲溶液中的累计释放率分别为 0.59%,2.06%和1.92%,鞣花酸复合微球在pH=4.00的缓冲溶液中累计释放率较低,而微球在pH=6.86缓冲溶液中的释放稍快,0.5~1 h中微球在PBS缓冲溶液(pH=7.4)中累计释放率陡然变大,后缓慢增加,24 h 时微球在三种缓冲溶液中的累计释放率分别为1.35%,21.74%和36.73%,说明当介质溶液pH值偏中性和碱性时,微球中鞣花酸能得到一定程度的释放。
图4为鞣花酸微球在人工胃液、人工肠液中的释放曲线。
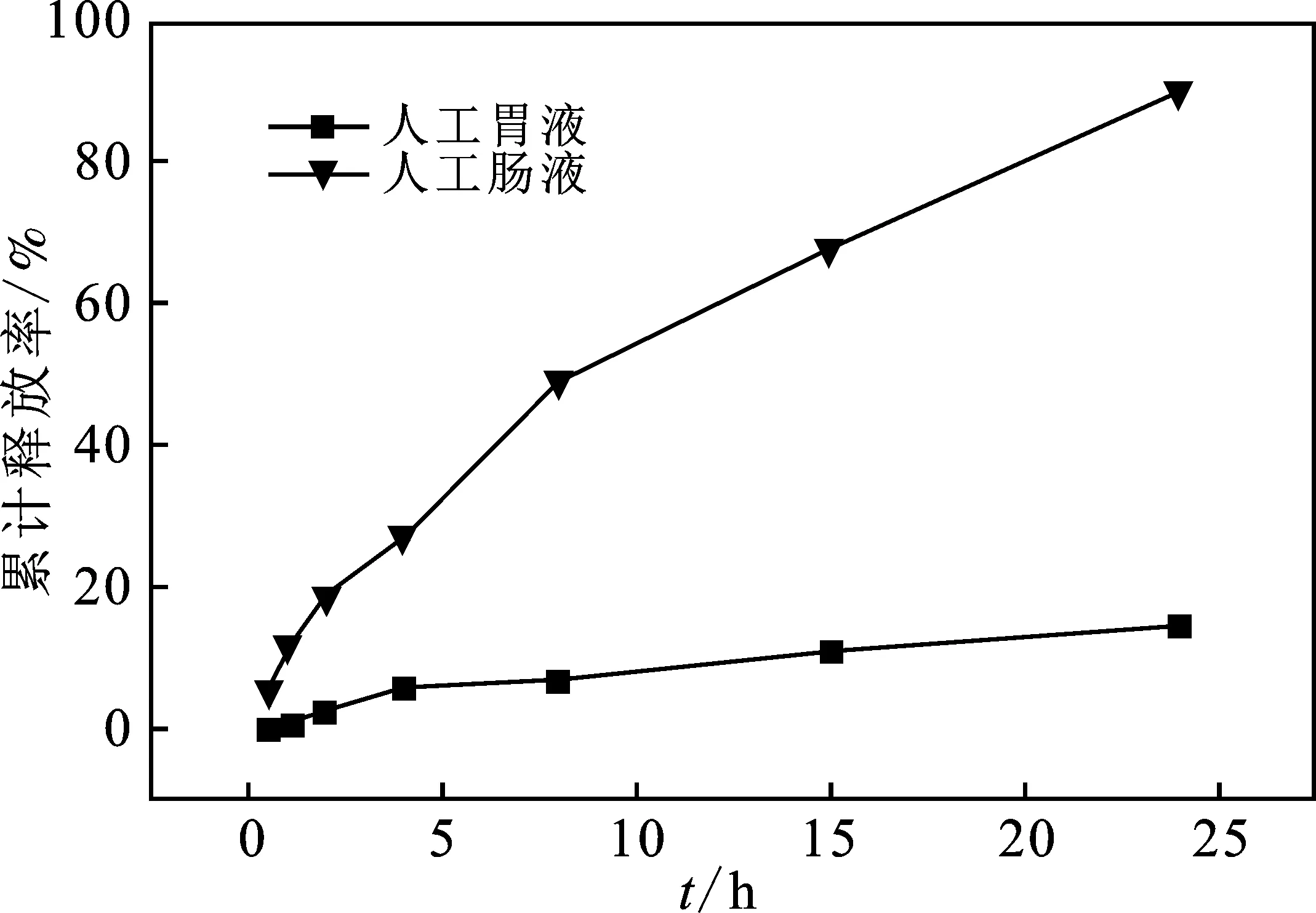
图4 鞣花酸微球在人工胃肠液中的释放曲线
由图4可知,鞣花酸微球在人工肠液中的释放远远高于在人工胃液中。起始0.5 h微球在人工胃液、人工肠液中的累计释放率分别仅为0.18%和 6.04%,8 h时微球在人工胃液和人工肠液中的累计释放率分别达到6.91%和50.18%,至24 h时在人工胃液和人工肠液中的累计释放率则分别达到13.92%和90.45%,24 h时在人工肠液中微球鞣花酸的释放远远高于在人工胃液中的释放,且差不多达到完全的释放,通过复合微球对鞣花酸的附载,可实现鞣花酸在肠液中缓慢而充分的定向释放。
2.2.4 鞣花酸微球在不同pH介质中的形态变化 图5为鞣花酸微球在部分介质中的形态变化,图中A1、B1、C1为鞣花酸微球的起始状态,图中A2、A3、B2、B3、C2、C3为鞣花酸微球分别在pH=6.86缓冲溶液、PBS缓冲溶液和人工肠液中4 h和24 h时的形态变化。

图5 鞣花酸微球在不同pH介质中的形态变化
由图5可知,鞣花酸微球在pH=6.86缓冲溶液中随时间延长体积逐渐膨胀并发生少量溶解导致鞣花酸分散体系的少量释放,24 h时溶液轻微浑浊且底部仍有大部分未完全溶解的微球;在偏碱性的PBS缓冲液中微球体积随时间的延长没有明显膨胀,但颜色逐渐变黄,且球形结构逐渐被破坏,可能是PBS缓冲液的碱性条件对微球中鞣花酸颜色的影响;鞣花酸微球在人工肠液中随着时间延长逐渐膨胀,24 h时溶液中已无微球存在,仅剩少量残渣,且溶液明显变浑浊,可能是人工肠液中的胰蛋白酶破坏了鞣花酸微球的凝胶外壳,从而使鞣花酸分散体系能得到充分的释放。
3 结论
以天然高分子材料为基材制备的鞣花酸复合微球球形度较好,对浓度为4 g/L的鞣花酸分散体系的载药量为14.36%,包封率为86.16%。鞣花酸复合微球在pH=2.13水溶液、pH=4.02水溶液和pH=6.86水溶液中24 h累计释放率分别为0.98%,2.67%和10.79%,在pH=4.00缓冲溶液、pH=6.86 缓冲溶液和PBS缓冲溶液(pH=7.4)的24 h累计释放率分别为1.35%,21.74%和36.73%,在人工胃液和人工肠液中24 h累计释放率分别为 13.92% 和90.45%。鞣花酸复合微球在较强酸性介质溶液中随时间延长形状无明显变化,在弱酸性溶液中鞣花酸微球则逐渐膨胀并发生少量溶解及释放,在偏碱性溶液中微球未发生明显膨胀,但颜色逐渐变黄,且球形结构逐渐被破坏,而鞣花酸微球在人工肠液中随时间延长逐渐膨胀,到24 h时微球基本上被完全破坏,鞣花酸分散体系几乎得到完全释放,说明该微球具有较好的pH敏感特性。

