磷酸二氢铵转化法测定重晶石中的硫酸钡含量
赵三慧 何 丹 周骏宏 马 糯 朱昌鸿
(黔南民族师范学院 磷化工重点实验室,贵州 都匀 558000)
重品石是一种以硫酸钡为主要成分的非金属矿物[1],化学性质稳定,属于不可再生资源,我国重晶石储量居世界第一,是我国出口优势矿产品之一,重晶石广泛用于石油,天然气钻探泥浆的加重剂,油漆,钡化工填料等领域。
近年来,国内外关于重晶石中硫酸钡测定方法的相关报道甚少[2-5],常沿用较为传统的重量法[6-7],但该法耗时长,不适应于时间紧的样品。虽也有一些改进方法的报道,如三酸溶矿快速重量法测定重晶石中的硫酸钡[8]。该法虽然简便、易于掌握且经济实惠,但该法避免不了干扰离子的干扰。而EDTA络合滴定法[9]缺乏合适的指示剂,文献[10]则采用高温处理试样,污染环境且分析速度较慢。
针对以上方法的不足,本文提出一种全新的样品处理及测定方法,先用磷酸二氢铵与重晶石混合,并在700 ℃灼烧,再用烧碱处理,得到的沉淀经过滤、洗涤、定容后,加入喹钼柠酮溶液,使该溶液与磷酸钡中的磷酸形成共沉淀,最后经称量此沉淀的质量进而计算出重晶石中的硫酸钡含量。
1 实验部分
1.1 主要试剂
硫酸钡、磷酸二氢铵均为分析纯,重晶石原矿(贵州都匀),喹钼柠酮溶液,NaOH溶液(100 g/L),浓度盐酸溶液(约2.67 mol/L),MgCl2溶液(0.2 mol/L),NH3-NH4Cl 缓冲溶液(pH≈9),实验用水为二次蒸馏水。
1.2 实验原理
硫酸钡与磷酸二氢铵在高温条件下钡离子与磷酸氢根结合形成偏磷酸钡,硫酸根以(NH4)2SO4形式挥发掉,经酸碱浸泡等处理将聚偏磷酸钡转化成磷酸钡沉淀后再将该沉淀溶解定容,取适量该溶液,加入50 mL喹钼柠酮溶液,通过盐酸将磷酸钡中的磷酸根离子转化为正磷酸,再通过磷酸与喹钼柠酮形成的共沉淀计算出该沉淀中偏磷酸钡的质量分数,再利用摩尔量的关系计算出重晶石中硫酸钡的含量。主要化学反应如下:
1)转化阶段:酸熔重晶石
BaSO4+2NH4H2PO4=Ba(H2PO4)2+(NH4)2SO4
磷酸钡转化 Ba(H2PO4)2+2NaOH=BaHPO4↓+Na2HPO4+2H2O
磷酸钡溶解 BaHPO4+2HCl =BaCl2+H3PO4
2)磷钼酸喹啉形成阶段:
1.3 实验步骤
1.3.1 偏磷酸钡的制备
准确称取1.00 g(精确至0.000 1 g)纯硫酸钡试样于60 mL蒸发皿中,加入2.00 g磷酸二氢铵,用约1 mm大小的小木棍搅拌均匀。将蒸发皿放于马弗炉中,使蒸发皿中样品缓慢升温至冒烟(700 ℃)煅烧2 h使硫酸钡充分反应。待冷却干燥,取出得到白色透明的玻璃状固体。
1.3.2 磷酸钡的转化
将上述制备好的试样及坩埚一起放入烧杯中,往烧杯中加入150 mL氢氧化钠溶液(100 g/L),将烧杯放于电热板上缓慢加热至溶液微沸,不断搅拌溶液,待坩埚上的玻璃体全部掉落于烧杯中后,用玻璃棒轻压掉落到烧杯内较大块的固体;取下烧杯,用蒸馏水稀释至250 mL,加入10 mL H2O2(30%),搅拌、盖上表面皿,放到电热板上继续加热至溶液无白色细小气泡产生后,趁热过滤,用水洗至滤液中无磷酸根(用MgCl2溶液检验磷酸根),往滤纸上直接滴加HCl (10%)溶解沉淀,待沉淀完全溶解后将溶液定容至500 mL容量瓶中,上述溶液除不加样品外,做样品空白。
1.3.3 总磷测定
测定前将洗净的砂芯坩埚置于250 ℃下预热,烘干且恒重待用;准确移取上述配制好的试液、空白试液各50 mL分别置于250 mL的烧杯中,每份试液取两份做平行试样,加蒸馏水至100 mL,加50 mL喹钼柠酮溶液搅拌,盖上表面皿;放于水浴锅中加热,待烧杯内溶液达到约75 ℃,取出冷却至室温,冷却时适当搅拌几次,用已恒重的坩埚过滤,过滤完成后,将坩埚及沉淀置于250 ℃的环境下烘干2 h,温度稳定开始计时,取出、放于干燥器内冷却至室温、称重。
2 分析结果计算
磷钼酸喹啉与硫酸钡关系如式(1)所示。
BaSO4~Ba(H2PO4)2~
(C9H7N)3H3(PO4·12MoO3)H2O
(1)
重晶石中硫酸钡(BaSO4)含量的质量分数W1,数值以%表示,按式(2)计算:
(2)
式中:0.104 2—将磷钼酸喹啉换算成硫酸钡的系数;
m磷钼酸喹啉—移取实验溶液的沉淀质量,g;
m空—移取空白实验溶液的沉淀质量,g;
m—试样的原始质量,g。
2.1 磷酸二氢铵的用量及不同煅烧温度对转化的影响
为了探究磷酸二氢铵和硫酸钡反应所得产物是否受配比的影响,实验选用磷钡物质的量比从1∶1至1∶2.8进行了500 ℃煅烧实验,结果见表1。
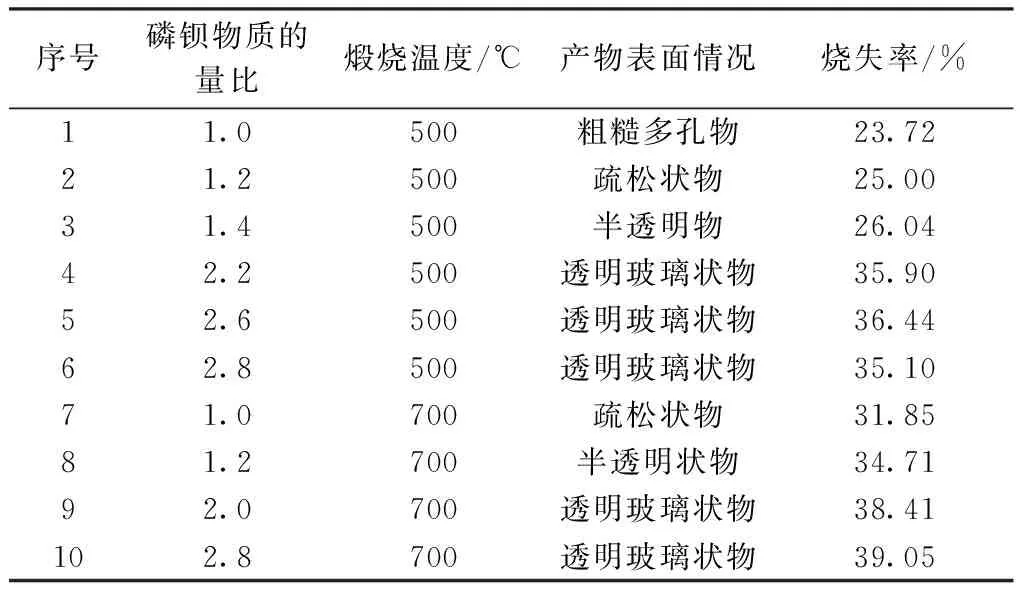
表1 不同磷酸二氢铵和硫酸钡配比的煅烧实验
为了进一步掌握硫酸钡和磷酸二氢铵混合物煅烧的转化是否完全,将煅烧产物做了X射线粉末衍射,见图1、2。从图1可以看出,煅烧出的产品随着硫酸钡和磷酸二氢铵配比的增加,500 ℃烧失率也随之增加,配比达到2.2后烧失率变化趋稳。700 ℃温度的煅烧也类似,相同配比条件下,700 ℃煅烧的烧失率高于500 ℃煅烧的情况。

图1 磷钡的不同配比在500 ℃煅烧产物的XRD图Figure 1 XRD patterns of the products calcined at 500 ℃ with different proportions of barium phosphate.
从XRD图谱可知,磷酸二氢铵和硫酸钡混合物在500 ℃煅烧,当磷钡比为1.0时,形成的偏磷酸钡物相最强峰I=1 193,但仍然存在硫酸钡衍射峰,峰强仍有116;之后,磷钡比增大到1.2时,虽然硫酸钡衍射峰强度没有减弱,但偏磷酸钡衍射峰强度不断减弱。煅烧温度升高到700 ℃情况类似,但转化效果好于500 ℃,磷钡比为2.0时,转化完全,看不到硫酸钡的衍射峰。也就是随着磷比例的增加、煅烧温度的升高,硫酸钡衍射峰渐减弱,在700 ℃磷钡比为2.0时可以确保硫酸钡转化反应完全。故选择煅烧温度为700 ℃,磷钡比为2.0进行以下实验。
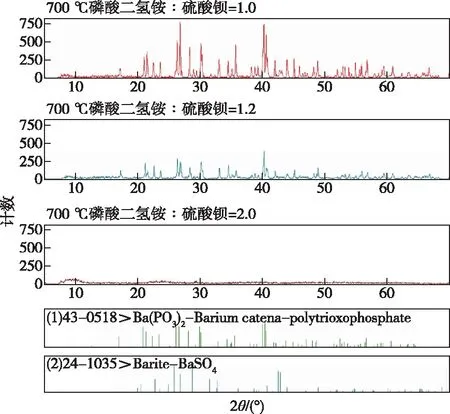
图2 磷钡的不同配比在700 ℃煅烧产物的XRD图Figure 2 XRD patterns of products calcined at 700 ℃ with different proportions of barium phosphate.
2.2 沉淀阶段取样量的确定
煅烧产物经过烧碱和双氧水处理,定容摇匀后,移取不同体积的试液与喹钼柠酮试液反应,按照实验方法进行实验,实验结果如表2所示。
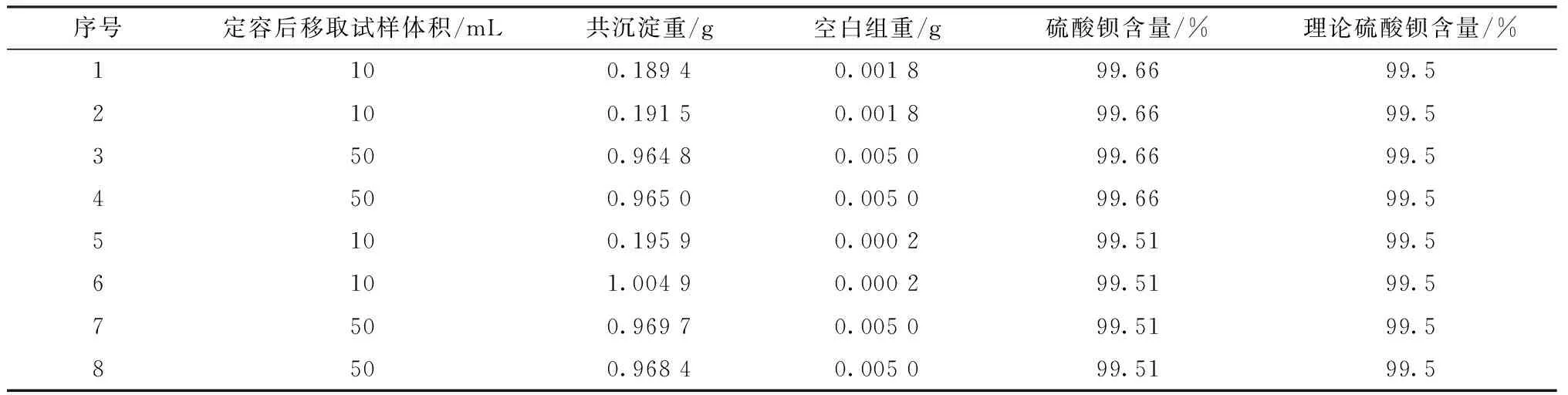
表2 取样量实验
实验表明,量取溶液的量为10 mL与50 mL时的测定结果相差不大。但取10 mL溶液进行测定得到的共沉淀较少,为避免误差的产生,实验选择取样量控制在50 mL。
2.3 氢氧化钠溶液用量的确定
实验表明,偏磷酸钡在纯水中基本不溶解,加热溶解速度很慢,基本不溶解,在酸溶液中,很难保证全部溶解,在H2O2及加热条件下,选用NaOH(100 g/L)可使溶液呈强碱性并将聚偏磷酸钡转化为磷酸钡,浓度太高,用量过大,过滤时会腐蚀滤纸且过滤时间变长;浓度太低,溶解不彻底。故实验选取氢氧化钠用量为150 mL。
2.4 样品测定
分别称取相同重量的纯硫酸钡及重晶石试样,按照实验方法进行测定,测定结果如表3所示。
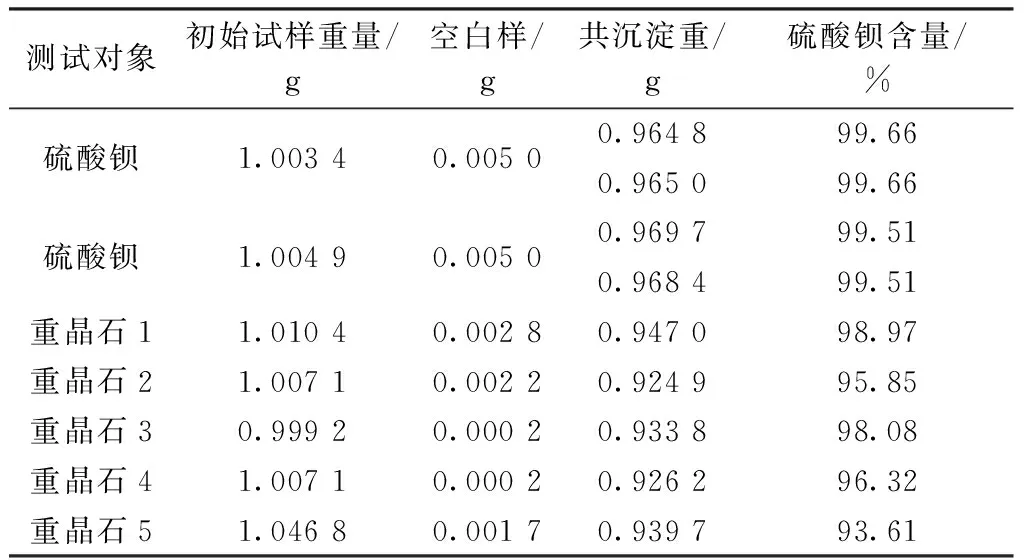
表3 纯硫酸钡及重晶石试样中硫酸钡的分析结果
实验表明,硫酸钡经熔融、碱浸泡等实验处理后,将转化成的磷酸钡通过酸溶解、定容后,取适量所定容的试液,加入适当的喹钼柠酮溶液,喹钼柠酮能够与磷酸钡形成共沉淀,可通过测定所得的共沉淀推算出重晶石中硫酸钡的量,用该方法来测定重晶石中的硫酸钡是可行的。
3 结论
1)硫酸钡与磷酸二氢铵在高温条件下会发生化学反应,硫元素组分挥发离开[以(NH4)2SO4形式]体系,剩余的钡元素与磷酸结合形成偏磷酸钡;
2)硫酸钡与磷酸二氢铵的混合物在700 ℃、磷酸二氢铵与硫酸钡的物质的量之比大于2.0的条件下,硫酸钡全部转化完全,并形成玻璃态的偏磷酸钡;
3)煅烧后的产物经过氢氧化钠、过氧化氢处理后,形成磷钡比为1∶1的磷酸氢钡形态的磷酸钡盐,再经过盐酸溶解、形成喹钼柠酮沉淀后,可以定量地依据喹钼柠酮沉淀的总磷含量间接计算出钡的含量,结果准确、方法可行。本法对测定重晶石中硫酸钡的含量提出一种新的思路和解决方案,具有实际意义。

