应用改进DDARP方法纯化天然水体样品中硫酸钡固体的效果评价
张东, 李玉红, 张鸿禹, 郝伟博, 晏文荣, 杨伟, 贾保军
(河南理工大学资源环境学院, 河南 焦作 454000)

如何去除水体硫酸钡沉淀过程中引入的硝酸盐和有机物,对于准确测定硫酸盐氧同位素值十分必要。虽然Michalski等[12]给出了校正公式来消除这些因素对硫酸盐氧同位素的影响,但并没有从根本上消除这些干扰物质。Bao(2006)[11]在实验室内采用DDARP方法处理硫酸钡固体中包裹的硝酸盐,经二次提纯后,硫酸钡沉淀中几乎没有硝酸盐,从而消除了硝酸盐对硫酸盐氧同位素的干扰,但是这一处理方法所采用的自然样品为Δ17OSO4值异常的矿石和土壤,而没有对自然水体沉淀出的硫酸钡样品处理效果进行研究,也没有针对性讨论DDARP方法对有机物干扰的处理效果。Xie等(2016)[13]对有机物干扰硫酸盐氧同位素进行了研究,选择高温烘烤硫酸钡沉淀的方式去除有机物,但是实验过程也未对真实水体样品展开研究,同时也未采用DDARP来尝试去除有机物的干扰。因此,有必要开展DDARP法对天然水体硫酸盐沉淀产生的硫酸钡固体纯化效果方面的研究,重点明确这种纯化方法对不同类型水体样品的处理效果以及硫酸盐氧同位素的干扰因素的具体影响。
鉴于此,本文采用改进的DDARP方法,对硫酸钡高纯试剂以及自然水体沉淀出的硫酸钡固体进行纯化,借助元素分析仪和稳定同位素质谱仪测定纯化前后硫酸钡固体的氧同位素值,对比分析该纯化方法对不同类型水体样品沉淀的硫酸钡固体的纯化效果及可能影响因素,拟建立自然水体样品沉淀生成的硫酸钡固体纯化程序,为准确获取水体硫酸盐氧同位素值奠定基础。
1 纯化试验方法
1.1 改进的DDARP方法
Bao(2006)[11]给出的DDARP纯化方法,实际配比是30mg硫酸钡溶于15mL DTPA溶液中,然后将二次沉淀出来的硫酸钡经过三次洗涤后,烘干备用。目前硫酸盐34S同位素测定需要约1.0mg硫酸钡,17O同位素测定需要约10mg硫酸钡即可满足要求,因此,本实验称取约20mg硫酸钡固体进行纯化,纯化后的硫酸钡固体质量可以满足后续硫和氧同位素的测定要求。
DTPA(0.05mol/L)-氢氧化钠(1mol/L)混合溶液的配制[11]:DTPA为分析纯试剂(99%,CAS编号67-43-6,阿拉丁试剂),NaOH为优级纯试剂(99.9%,CAS编号1310-73-2,阿拉丁试剂)。该混合溶液现用现配。
将称好的硫酸钡固体置于塑料离心管(聚丙烯PP材质,规格50mL,美国ThermoFisher公司)内,加入一定体积DTPA和氢氧化钠混合溶液,置于离心管振荡器(KB-5010,其林贝尔仪器公司)上振荡过夜。待硫酸钡固体溶解后,经聚醚砜滤头(PES,孔径0.22μm,直径25mm,天津津腾实验设备有限公司)过滤后,再加入5mL优级纯盐酸(36%~38%,北京化学试剂厂),置于通风橱内敞口放置约30min。加入预先酸化过的饱和氯化钡溶液(高纯氯化钡,99.99%,CAS编号10326-27-9,阿拉丁试剂)5mL,静置过夜。对离心管内溶液进行固液离心(TDL-40C离心机,上海安亭科学仪器厂)分离,转速设定为4000r/min,时间8min,再用超纯水洗涤沉淀至Cl-未检出。最后置于烘箱内于50℃烘干硫酸钡沉淀,用于下一步硫酸盐氧同位素测定。
1.2 水体样品硫酸钡沉淀纯化最佳程序的确定
选择高纯硫酸钡试剂(99.99%,CAS编号7727-43-7,阿拉丁试剂,代号A,δ18OSO4=9.0‰)、美国路易斯安那州立大学实验室硫酸钡标准物质(LSU-BaSO4,代号B,δ18OSO4=12.9‰)以及实际黄河河水硫酸钡样品(代号C,δ18OSO4=6.7‰)作为实验样品,上述样品δ18OSO4值测试过程如下1.4节所述。使用万分之一天平(Quintix224-3CN,德国赛多利斯公司)准确称取约20mg硫酸钡样品,平行置于50mL塑料离心管(聚丙烯PP材质,美国ThermoFisher公司)内,加入的DTPA-氢氧化钠混合溶液体积分别为10mL、20mL和30mL,洗涤次数设定为2次和3次。对比分析不同处理方式得到的硫酸钡氧同位素值与处理前硫酸钡氧同位素值的差异,确定最佳纯化程序。
1.3 最佳纯化方法对含硝酸盐和有机物的水体样品处理效果
根据确定的最佳纯化程序,选择6种类型自然样品,分别是洗衣粉(n=2)、地下水(n=5)、河水(n=6)、生活污水(n=3)、化学肥料(n=3)以及雨水(n=6),对上述样品预处理得到的硫酸钡固体进行纯化,对比分析水体样品纯化前后氧同位素变化趋势及差异原因。
地下水、河水、生活污水和雨水预处理过程:各取水样1L,经混合纤维滤膜(孔径0.22μm,直径50mm,天津津腾实验设备有限公司)过滤后,加入2mL优级纯浓盐酸(36%~38%,北京化学试剂厂),混合均匀后确保水体pH<2。加入5mL饱和氯化钡溶液(高纯氯化钡,99.99%,CAS编号10326-27-9,阿拉丁试剂),静置过夜。硫酸钡浑浊液经聚醚砜滤膜(PES,孔径0.22μm,直径50mm,天津津腾实验设备有限公司)过滤后置于坩埚内,在马弗炉于850℃烘干2h[8,14-16],最后得到硫酸钡固体样品。
洗衣粉和化学肥料处理过程[16-17]:各取约1g的洗衣粉和化学肥料样品,置于塑料瓶内,加入1L超纯水(电阻率18.2MΩ·cm,美国Millipore公司)混合均匀,硫酸钡的预处理方法与上述4种水样相同。
1.4 水体样品硫酸钡固体纯化前后氧同位素值(δ18OSO4)测定
水体样品纯化前后硫酸钡固体的氧同位素测定过程相同,用百万分之一天平(XPS-6,瑞士梅特勒-托利多公司)准确称取硫酸钡固体样品400±25μg,置于小号银杯(3.3mm×5mm,德国元素公司)中,赶净空气后包裹起来,置于固体自动进样器(MAS-200R,美国ThermoFisher公司)内。设置元素分析仪(Flash 2000 HT,美国ThermoFisher公司)工作条件(炉温1380℃,色谱柱温度85℃),硫酸钡固体样品经玻璃碳还原为CO气体,色谱柱分离后通过连续流样品制备专用接口(ConFloⅣ)导入稳定同位素质谱仪(MAT253)测定氧同位素组成。选择国际标准NBS127(δ18OSO4=8.6‰,VMSOW)[2,18]校准待测样品,测试精度优于±0.5‰。
2 结果与讨论
2.1 改进DDARP方法对硫酸钡高纯试剂和实际水体样品硫酸钡沉淀的纯化效果
2.1.1硫酸钡高纯试剂的纯化效果
根据前述实验设计要求,在A、B和C硫酸钡样品中分别加入10mL、20mL和30mL的DTPA-氢氧化钠混合溶液,并分别用纯水洗涤2次和3次,测定干燥后硫酸钡的氧同位素值,并与未经纯化处理的硫酸钡氧同位素值进行比较,结果如图1所示。由图1可以看出,高纯试剂硫酸钡(A和B)经不同体积DTPA-氢氧化钠混合溶液处理并洗涤后,其δ18OSO4值与原样品δ18OSO4值差异不明显,均落在原样品δ18OSO4值误差范围内,说明硫酸钡标准品A和B中的硝酸盐等杂质含量很低,处理过程对其δ18OSO4值影响不大,可以直接作为实验室标准物质使用。
2.1.2实际水体样品硫酸钡沉淀的纯化效果
实际水体样品硫酸钡固体C在纯化处理前后δ18OSO4值差异明显,处理后样品的δ18OSO4值(均值+5.9‰,n=5)普遍低于处理前δ18OSO4值(+6.7‰),说明直接从水体中沉淀的硫酸钡固体中含有较多硝酸盐等18O同位素值较高的杂质,纯化过程对样品中杂质有明显去除效果。
2.1.3改进的DDARP方法纯化程序的确定
Bao(2006)[11]选择15mL DTPA混合溶液处理30mg硫酸钡固体,据前述内容,本项目组选择20mg硫酸钡固体作为处理对象,从图1a中可以看出,对于硫酸钡高纯试剂以及实际水体硫酸钡固体,经30mL DTPA-氢氧化钠混合溶液处理后,洗涤2次和3次,二者差异性不大,稳定性好,因此选择30mL DTPA-氢氧化钠混合溶液。同时从图1b可以看出,洗涤2次后硫酸钡回收率普遍较高,可能原因是洗涤次数越多,硫酸钡被倾倒出的可能性越大,因此确定洗涤次数为2次。所以本实验对实际样品采用的纯化程序确定为:30mL DTPA-氢氧化钠混合溶液,洗涤2次。

图1 DTPA-氢氧化钠混合溶液体积和洗涤次数与δ18OSO4关系图Fig.1 Relationship between the volume of DTPA-NaOH solution and different washing times with δ18OSO4 values
2.2 改进DDARP方法对不同类型水体样品硫酸钡的纯化效果
采用上述确定的最佳纯化程序,对不同类型水体样品处理后得到的硫酸钡固体进行纯化,对比处理前后硫酸钡δ18OSO4值变化情况。如图2所示,洗衣粉样品处理前后硫酸钡的δ18OSO4值差异范围为0.3‰~1.0‰,均值0.7‰(n=2);地下水样品处理前后硫酸钡的δ18OSO4值差异范围为-0.4‰~0.5‰,均值0.2‰(n=5);河水样品处理前后硫酸钡的δ18OSO4值差异范围为0.1‰~0.5‰,均值0.3‰(n=6);污水样品处理前后硫酸钡的δ18OSO4值差异范围为-0.2‰~-0.3‰,均值-0.3‰(n=3);化学肥料样品处理前后硫酸钡的δ18OSO4值差异范围为-0.2‰~0.4‰,均值0.1‰(n=3);雨水样品处理前后硫酸钡的δ18OSO4值差异范围为0.5‰~1.9‰,均值1.4‰(n=6)。
其中,雨水样品纯化前后硫酸钡的δ18OSO4值差异最大,说明纯化过程去除了雨水样品硫酸钡沉淀中δ18O值较高的杂质,如硝酸盐[11-12]。污水样品的δ18OSO4差异值为负值,处理后硫酸钡δ18OSO4值有所增大,说明纯化过程去除了污水样品硫酸钡沉淀中δ18O值较低的杂质,如有机物[3,13]。地下水、河水和化学肥料样品处理前后硫酸钡的δ18OSO4值变化在误差允许范围内(±0.5‰),说明这三类样品中的硝酸盐和有机物等物质的含量低,对硫酸钡沉淀的干扰不大。洗衣粉处理后硫酸钡的δ18OSO4值有较大降低,说明洗衣粉处理得到的硫酸钡固体中硝酸盐含量不容忽视。

图2 不同类型天然水体样品硫酸钡固体纯化前后δ18OSO4值变化图Fig.2 Variations of δ18OSO4 value of original and treated barite in different natural water samples
2.3 影响水体样品硫酸钡的氧同位素值的潜在因素
影响水体样品硫酸钡固体的氧同位素值的潜在因素,主要包括硫酸钡沉淀过程中包裹的硝酸盐以及有机物[2-3,12-13]。Hannon等[2]以及Michalski等[12]认为硫酸钡沉淀过程中包裹的硝酸盐对硫酸盐氧同位素值(18O和17O)影响较大,当摩尔比值超过2时,硝酸盐对氧同位素值的最大贡献接近7%。本文的研究对象之一雨水样品的摩尔比值范围为0.2~1.9(图3),雨水中硝酸盐的氧同位素值(δ18O)较大(约50‰~90‰)[12],少量的硝酸盐会导致硫酸钡固体的氧同位素值增大[12],因此本研究进一步佐证了雨水中硝酸盐对雨水硫酸盐氧同位素的干扰。相比而言,地下水以及河水样品中硝酸盐对硫酸钡固体的氧同位素值影响程度则没有这么明显,其原因之一是这些样品的摩尔比值低(图3),还可能与硝酸盐的氧同位素值(约0‰~20‰)较雨水中硝酸盐的氧同位素值低有关[19-20]。

图3 不同类型天然水体样品硫酸钡固体纯化前后δ18OSO4值与样品摩尔比值关系Fig.3 Relationship between δ18OSO4 value of original and treated barite and molar ratio of in different natural water samples

2.4 改进DDARP方法对天然水体样品硫酸钡氧同位素处理效果
借助改进DDARP方法,分析不同天然水体样品(大气降水、河水、地下水、污水)纯化前后硫酸钡δ18OSO4值之间的线性关系如下:
大气降水:δ18OSO4纯化后=0.91δ18OSO4纯化前-0.30
(r2=0.95)
河水:δ18OSO4纯化后=0.99δ18OSO4纯化前-0.28
(r2=0.99)
地下水:δ18OSO4纯化后=1.02δ18OSO4纯化前-0.37
(r2=0.98)
污水:δ18OSO4纯化后=1.08δ18OSO4纯化前-0.24
(r2=0.99)
如图4所示:①除雨水外,其余样品纯化前后硫酸钡的δ18OSO4值有很好的正相关关系(落在1∶1直线附近);②雨水样品纯化前后硫酸钡的δ18OSO4值相关性稍差(r2=0.954),与雨水样品处理前硫酸钡样品中的硝酸盐影响有关。③除污水样品外,其余天然水体样品纯化前后硫酸钡的氧同位素值多数有所降低,说明该方法可以有效去除天然水体样品硫酸钡沉淀过程中包裹的硝酸盐以及有机物,对于准确测定水体溶解性硫酸盐氧同位素值(δ18O和δ17O)具有重要的现实意义。
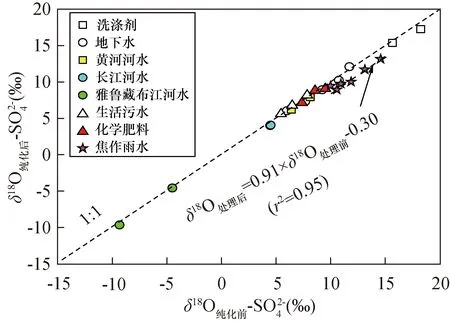
图4 不同类型天然水体样品硫酸钡固体处理前后δ18OSO4值关系图Fig.4 Relationship between δ18OSO4 of original and treated barites in different natural water samples
3 结论
本文针对天然水体样品硫酸盐处理过程中引入的硝酸盐和有机物等杂质干扰硫酸盐氧同位素测定的问题,采用改进的DDARP方法纯化硫酸钡样品,探讨最佳处理程序和潜在影响因素,主要得出以下结论:①天然水体样品硫酸钡沉淀最佳纯化程序为:20mg硫酸钡溶于30mL DTPA-氢氧化钠混合溶液中,溶解完毕,过滤后加入5mL盐酸,用超纯水洗涤重新生成的硫酸钡沉淀2次,于50℃烘箱中烘干备用。②高纯硫酸钡试剂不需要纯化,可以作为实验室硫酸盐氧同位素标准直接使用。③干扰天然水体样品硫酸盐氧同位素值的最大因素是硝酸盐和有机物,其中硝酸盐对雨水硫酸盐的氧同位素值干扰最大,经纯化后硫酸盐氧同位素值平均降低1.4‰;有机物对污水硫酸盐的氧同位素值干扰最大,经纯化后硫酸盐的氧同位素值升高约0.3‰。
研究表明,改进的DDARP方法有效减少了样品中的硝酸盐和有机物杂质对硫酸盐氧同位素测定的干扰,适用于天然水体样品硫酸盐氧同位素纯化过程。

