气相色谱法测定乙二醇生产中无机气体成分
周发海
(河南龙宇煤化工有限公司,河南 永城 476600)
乙二醇是一种重要的有机化工原料,随着我国聚酯工业的快速发展,乙二醇的需求量不断增大[1]。我国煤储量大,通过近年来的发展,煤制乙二醇已经成为我国乙二醇产能的重要组成部分。在乙二醇生产过程中需要测定其中的气体成分来指导工艺生产。现存分析方法存在切阀时间不好把控,要么导致甲烷可能偏小,要么甲烷与一氧化氮分离效果不理想等缺点,笔者通过大量实验,最终确立了最优实验条件,实现了样品气中所有组分的完全分离测定。
1 实验部分
1.1 实验仪器及配置
PANNA A91Plus气相色谱仪(常州磐诺仪器有限公司):辅助EPC模块,十通气体进样阀一个(其中配置0.5 mL定量环),六通气体切换阀一个,HN填充柱一根(2 m),毛细管色谱柱HP-MOLESIEVE一根(30 m×0.530 mm×50.0 Micron,-60~300 ℃),外置小柱箱一个(放置HN填充柱);阻尼两个(平衡管路阻力,使得切阀时系统及基线稳定);热导池检测器(TCD),磐诺增强版Version2.0.6.1色谱工作站。
载气、TCD 参比气、尾吹气,高纯氩气(体积分数99.999%以上),标准气1(体积分数,二氧化碳9.99%、氢气6.04%、一氧化氮20.27%、甲烷4.99%、一氧化碳39.29%、氮气为平衡气,大连大特气体有限公司),标准气2(体积分数,氧气20.90%、氮气为平衡气,大连大特气体有限公司)。
1.2 色谱气路
图1中载气1、载气2为高纯氩气,1—10代表十通阀的10个通道,a—f代表六通阀的6个通道。十通阀V1上的阻尼用于载气2直接放空时提供阻力,否则载气2压力无法达到设定值;六通阀V2上的阻尼的阻力基本等同于毛细管色谱柱HP-MOLESIEVE的阻力为最佳,以保证切阀时载气压力平衡,基线波动更小。
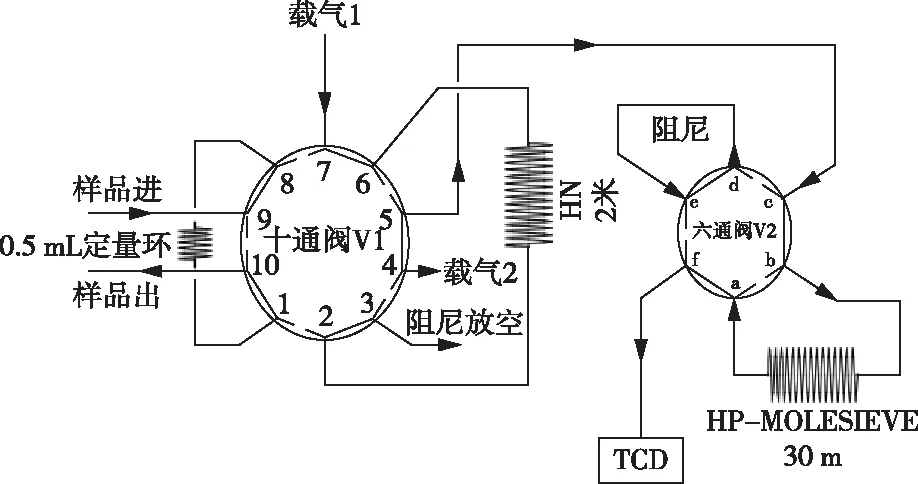
图1 色谱气路图Figure 1 Chromatographic gas path diagram.
1.3 分析过程
十通阀V1,六通阀V2起始处于图1中的实线关闭状态,利用切十通阀V1到虚线打开状态,使0.5 mL定量环中的样品气在载气1的带动下进入到填充柱HN中进行分离,待样品气中的氢气、氧气、氮气、一氧化碳、一氧化氮、甲烷流出HN填充柱进入到HP-MOLESIEVE毛细管色谱柱中且氢气未流出HP-MOLESIEVE毛细管色谱柱中,而二氧化碳未进入HP-MOLESIEVE毛细管色谱柱中时,利用切六通阀V2到虚线打开状态,使得从HN填充柱中流出的二氧化碳经过六通阀V2的阻尼进入TCD进行检测。当二氧化碳出峰完毕,利用切十通阀V1复位到实线关闭状态,将HN填充柱中二氧化碳以后的成分(如水等)反吹出来自十通阀的阻尼进行放空。然后通过切阀使V2复位到实线关闭状态,在载气2的带动下,封存在HP-MOLESIEVE毛细管色谱柱中的氢气、氧气、氮气、一氧化碳、一氧化氮、甲烷开始分离,进入TCD被检测。
2 结果与讨论
2.1 仪器操作条件确立
2.1.1 TCD检测器工作条件
TCD温度 200 ℃,参比气流速20 mL/min,尾吹气流速2 mL/min。
2.1.2 载气压力的确定
为了达到全部组分的分离检测,本仪器采用氩气为载气,并且分两路载气供气,通过辅助EPC对两路载气压力进行控制。载气1主要为HN填充柱单独及其与HP-MOLESIEVE毛细管色谱柱串联时供气,压力设置可以稍微高一些,载气2主要为HP-MOLESIEVE毛细管色谱柱单独时供气,经过大量的实验,最终确立载气1压力为124 kPa,载气2压力为55 kPa时,切阀基线波动最小,基本可以忽略,也能满足样品气在HN填充柱中二氧化碳与其他成分分离,剩下组分能在HP-MOLESIEVE毛细管色谱柱中实现分离。
2.1.3 外置小柱箱温度确定
本仪器有一个单独的小柱箱,用于放置HN填充柱,为其单独控温,更易实现分离二氧化碳时的色谱柱温度不影响HP-MOLESIEVE毛细管色谱柱温度。样品气在HN色谱柱中的出峰顺序为氢气,氧气、氮气、一氧化碳、一氧化氮合峰,甲烷,二氧化碳。将六通阀V2切到虚线位置,让从HN填充柱出来的各组分直接进入TCD检测,测试小阀箱在不同温度下,二氧化碳与其他组分的分离情况,见表1。

表1 小柱箱不同温度下出峰情况
由表1可以看出,45~70 ℃时,甲烷,二氧化碳都能很好地单独分离出来,但是分离时间稍微长一点;80~110 ℃时,分离时间逐渐缩短,二氧化碳仍然能很好地单独分离出来,甲烷分离效果越来越差。考虑到不让二氧化碳进入HP-MOLESIEVE毛细管色谱柱,其他组分在二氧化碳未全部流出TCD之前不流出HP-MOLESIEVE毛细管色谱柱,又留给六通阀V1充分的切阀时间,故选择小阀箱温度为90 ℃,90 ℃色谱图见图2。
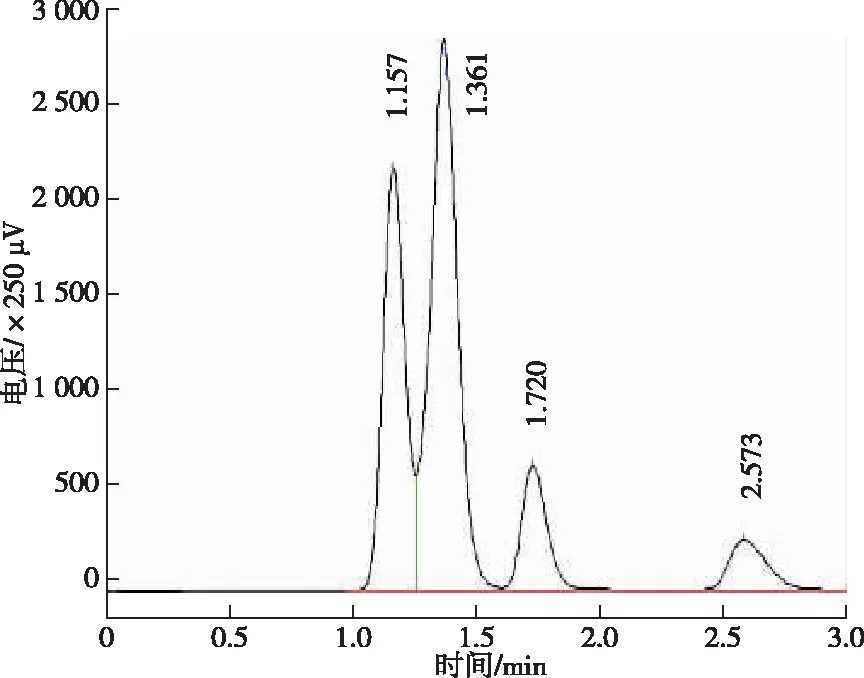
图2 小柱箱90 ℃时色谱图Figure 2 Chromatogram of the oven at 90 ℃.
2.1.4 色谱柱柱箱温度确定
本仪器色谱柱内安装有HP-MOLESIEVE毛细管色谱柱,主要用于分离氢气、氧气、氮气、一氧化氮、甲烷,通过大量实验,色谱柱箱温度初始如果高于60 ℃,一氧化氮与甲烷分离度较差,色谱柱箱温度在40~55 ℃所有组分都能实现较好的分离,但是一氧化碳严重拖尾,分析时间也比较长,效果不是很理想,为了达到分离所有组分,一氧化碳不太拖尾,且分析时间尽量短一些,最终采用程序升温的方法来实现。即初温50 ℃,保持7.5 min,以使除一氧化碳以外的所有组分分离,然后以40 ℃/min升温至120 ℃,保持1 min,保证一氧化碳快速出峰不拖尾。
2.1.5 切阀时间确定
要实现测定文中叙述的所有组分,十通阀V1、六通阀V2的切阀时间尤其重要[2]。如果切阀时间不正确将导致组分含量不准确,从分析过程中可以看出十通阀V1刚开始切到虚线打开状态,是将定量环中的样品带入HN填充柱中,此时为按色谱“开始”键后工作站开始采集数据的时间即可,为0 min,而十通阀V1复位到实线关闭状态是为了在二氧化碳出峰完毕后,将HN填充柱中二氧化碳后面不利于进入HP-MOLESIEVE毛细管色谱的水分等组分反吹出系统,其时间设置为二氧化碳刚好出峰完毕即可;六通阀V2切换到虚线打开状态时间为样品气中的氢气、氧气、氮气、一氧化碳、一氧化氮、甲烷已经进入到HP-MOLESIEVE毛细管色谱柱中且氢气未流出HP-MOLESIEVE毛细管色谱柱,而二氧化碳未进入HP-MOLESIEVE毛细管色谱柱的时间,因此受到切阀时间影响的峰为甲烷、二氧化碳和氢气,通过大量实验,得到切阀时间与甲烷、二氧化碳、氢气峰面积关系,具体见表2。
从表2中可以看出2.00 min到2.10 min六通阀V2切换到虚线打开状态都合适,为了让切阀时间与切阀前后出峰时间保留一定的时间间隔,2.05 min为最佳选择。图3为2.05 min切阀V2为打开状态的色谱图。根据二氧化碳出峰情况,也确立了十通阀V2复位到实线关闭状态的时间为3.10 min,六通阀V1复位到实线关闭状态的时间为3.30 min。但是由于每根色谱柱阻力可能有小的差别,更换色谱柱后根据实际情况适当调整十通阀V1与六通阀V2的切阀时间,十通阀V1与六通阀V2的切阀时间一定要严格把控,防止二氧化碳及水分进入毛细管色谱柱HP-MOLESIEVE,否则对其造成不可逆损害[3]。
2.2 精密度实验
按以上确定好的条件设置好气相色谱仪,等待仪器状态就绪以后,以标准气1,标准气2作为实验对象,对标准气的各组分含量进行平行测定5次,结果见表3。
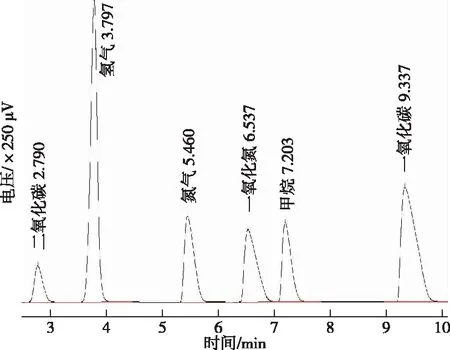
图3 2.05 min切阀V2为打开状态的色谱图Figure 3 Chromatogram of 2.05 min valve V2 in open state.

表3 精密度分析
2.3 准确度实验
在两个样品中分别加入标准样品(样品与标准气体等体积混合),做加标回收率的实验,实验结果见表4。

表4 回收率分析
由表3、4可以看出,各组分测定值都达到了较好的效果,所有组分RSD都在1%以内,加标回收率都在98.0%~101%,此分析方法分析速度快,重现性好[4]。
3 结论
经过实验探究及效果验证,最终确立了气相色谱工作条件,载气1压力为124 kPa,载气2压力为55 kPa;外置小柱箱温度为恒温90 ℃;色谱柱箱初温50 ℃,保持7.5 min,以40 ℃/min升温至120 ℃,保持1 min;十通阀V1默认状态为实线关闭状态,0 min切换为虚线打开状态,3.30 min复位到实线关闭状态,六通阀V2默认状态为实线关闭状态,2.05 min切换为虚线打开状态,3.10 min复位到实线关闭状态;TCD温度为200 ℃;参比气流速20 mL/min;尾吹气流速2 mL/min。
在此条件下,二氧化碳、氢气、氧气、氮气、一氧化氮、甲烷、二氧化碳都能实现分离度大于等于1.50,效果理想,结果准确度高,精密度好,完全能够满足乙二醇生产中无机气体成分分析需要。在不同仪器运用中根据实际情况,外挂小柱箱与色谱柱柱箱温度可微调,调整后十通阀V1与六通阀V2的切阀时间也可能需要调整。

